Совмещенный синтез и гидрооблагораживание углеводородов на кобальтовом цеолитсодержащем катализаторе
Автор: Яковенко Р.Е., Зубков И.Н., Некроенко С.В., Папета О.П.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 4 (78), 2018 года.
Бесплатный доступ
Разработан композитный Со-Al2O3/SiO2/НZSM-5 катализатор для одностадийного синтеза углеводородов топливного ряда из СО и Н2. Катализатор получен смешением и формованием порошков Со-Al2O3/SiO2 катализатора, цеолита НZSM-5 и бемита Al(O)OH?H2O. Физико-химическими методами РФА, ПЭМ, БЭТ установлен фазовый состав катализатора, размер частиц кобальта (8,2±1 нм), площадь его удельной поверхности (286 м2/г). Проведены испытания в синтезе углеводородов из СО и Н2 в непрерывном режиме в течение 60 ч при температуре 240 С, давлении 2,0 МПа, объемной скорости газа 1000 ч-1. Показано, что на синтез-газе, разбавленном на 40% азотом, возможно получать жидкие углеводороды С5+ с селективностью 69% и производительностью 81 кг/(м3?ч). Выход углеводородов С5+ составил 70 г/м3 пропущенного синтез-газа и 135 г/м3 превращённого синтез-газа. Синтетическая нефть имеет молекулярно-массовое распределение близкое к мономодальному (вероятность роста цепи составляет 0,81), на 88% состоит из бензиновой и дизельной фракций и на 12% из длинноцепочечных углеводородов С19+...
Композитный катализатор, синтез фишера-тропша, цеолит, гидрокрекинг, синтетические углеводороды
Короткий адрес: https://sciup.org/140244281
IDR: 140244281 | DOI: 10.20914/2310-1202-2018-4-304-311
Combined synthesis and hydroprocessing on a cobalt catalyst on a cobalt-containing zeolite catalyst
A composite Co-Al2O3/SiO2/HZSM-5 catalyst has been developed for one-step synthesis of fuel series hydrocarbons from CO and H2. The catalyst was obtained by mixing and forming powders with a Co-Al2O3/SiO2 catalyst, zeolite HZSM-5, and boehmite Al(O)OH?H2O. The physicochemical methods XRD, PEM, BET established the phase composition of the catalyst, the particle size of cobalt (8.2 ± 1 nm), its specific surface area (286 m2/g). Tests were carried out in the synthesis of hydrocarbons from CO and H2 for 60 hours at a temperature of 240 C, a pressure of 2.0 MPa, and a gas flow rate of 1000 h-1. It is shown that synthesis gas diluted by 40% with nitrogen can produce liquid C5+ hydrocarbons with a selectivity of 69% and a productivity of 81 kg/(m3?h). The yield of С5+ hydrocarbons was 70 g/m3 of the leaked synthesis gas and 135 g/m3 of the converted synthesis gas. Synthetic oil has a molecular mass distribution close to monomodal (the probability of chain growth is 0.81), 88% consists of gasoline and diesel fractions and 12% of long-chain C19+ hydrocarbons...
Текст научной статьи Совмещенный синтез и гидрооблагораживание углеводородов на кобальтовом цеолитсодержащем катализаторе
В настоящее время во всем мире большое количество исследований и разработок направлено на получение моторных топлив и сырья для нефтехимических производств из ненефтяного сырья (природный и попутный нефтяной газ,
уголь, торф, биомасса и др.). Актуальность этого направления обусловлена большими запасами природного газа и угля, а также наличием возобновляемых источников углерода (биомасса пищевого и непищевого происхождения).
Переработка любого углеродсодержащего сырья в углеводороды топливного и нефтехимического назначения получила название XTL технология или «нечто в жидкость». XTL включает технологии переработки газа (Gas–to–Liquids), угля (Coal–to–liquids) и биомассы (Вiоmаss–to–Liquids) [1–3]. Технология ХТL состоит из трёх стадий: 1 – превращение углеродсодержащего сырья в синтез-газ (смесь водорода и монооксида углерода); 2 – получение углеводородов по методу Фишера-Тропша (ФТ); 3 – облагораживание (гидрокрекинг и/или гидроизомеризация) продуктов синтеза второй стадии процесса. Третья стадия необходима для увеличения выхода моторных фракций углеводородов и доведения их свойств до требований стандартов. В настоящее время активно ведутся исследования, направленные на объединение второй и третьей стадий процесса и получение высококачественных топлив из синтез-газа в одну стадию. Осуществить это возможно за счет применения катализаторов, включающих в себя функции синтеза ФТ и гидрооблагораживания [4–7]. В качестве катализаторов синтеза ФТ используют кобальтовые катализаторы на носителях SiО 2 , Аl 2 О 3 , ТiО 2 , основной компонент катализаторов гидрооблагораживния – цеолиты ZSM-5, HY, MOR, β и др. [8–13].
В ЮРГПУ(НПИ) разработан кобальтси-ликагелевый катализатор синтеза ФТ для селективного получения длинноцепочечных углеводородов из СО и Н 2 [14]. В работе представлены результаты создания на его основе композитного цеолитсодержащего катализатора для одностадийного синтеза углеводородов топливного ряда из СО и Н 2 .
Материалы и методы
Методика приготовления катализатора
Композитный катализатор готовили смешением порошков (фракция < 0,1 мм) Со-Аl 2 О 3 /SiО 2 катализатора синтеза ФТ, цеолита НZSМ-5 и связующего – бемита. Катализатор ФТ, содержащий 20% масс. Co и 1% масс. Аl 2 О 3 , был приготовлен в промышленных условиях на АО «Самарский завод катализаторов» по методике, описанной в работах [14, 15]. Использовали цеолит НZSМ-5 (Si/Al = 40) в H-форме производства ООО «Ишимбайский специализированный химический завод катализаторов» [16]; бемит АlООН ⋅ Н 2 O (TH 80) производства компании Sasol. Для пластификации в смесь порошков прибавляли водно-спиртовой раствор триэтиленгликоля с азотной кислотой и перемешивали до пастообразного состояния.
Цилиндрические гранулы композитного катализатора диаметром 2 мм и длиной 3 мм формовали методом экструзии, сушили 24 ч на воздухе при температуре 20–25 °С и подвергали термообработке по режиму: 80 ºС – 4 ч; 100, 120, 140 ºС – 1 ч и 400 ºС – 4 ч. Полученный композитный катализатор имеет состав (в % масс.): 35 – Со-Аl 2 О 3 /SiО 2 , 30 – НZSМ-5 и 35 – Аl 2 О 3 .
Методики исследований физико-химических и каталитических свойств катализатора
Содержание кобальта в катализаторе определяли методом рентгенофлуоресцентого анализа (РФлА) на спектрометре ARLQUANT’X (Thermo Scientific, Швейцария) при следующих условиях: среда – воздух, тефлоновая подложка, эффективная площадь облучения 48,99 мм2.
Рентгенофазовый анализ (РФА) катализаторов производили на дифрактометре Thermo Scientific АRLХ'ТRА Powder Diffractometer с монохроматизированным Cu Kα-излучением методом сканирования по точкам (шаг 0,01°, время накопления в точке 2 с) в интервале 2θ от 5 до 90°. Определение качественного фазового состава было выполнено с помощью PDF-2 в программном комплексе Crystallographica [17].
Просвечивающую электронную микроскопию (ПЭМ) катализатора осуществляли на микроскопе Tecnai G2 SрiritВiоТWIN (FEI, США) с ускоряющим напряжением 120 кВ. Образцы предварительно восстанавливали азото-водородной смесью (Н 2 10% по объему) при линейном нагреве от комнатной температуры до 500 ºС в течение 1 ч.
Удельную поверхность катализатора по методу БЭТ определяли на приборе ChemiSorb 2750 (Micromeritics, США). Предварительно образцы дегазировали в токе гелия при 200 °С для удаления влаги и других адсорбированных газов в течение 1 ч.
Синтез углеводородов осуществляли на лабораторной установке (рисунок 1) в проточном реакторе со стационарным слоем катализатора (10 см3), разбавленного кварцевой крошкой (30 см3). Катализатор предварительно восстанавливали в токе водорода в течение 1 ч при температуре 400 °С и объемной скорости газа (ОСГ) 3000 ч-1. Затем температуру снижали до 180 °С, устанавливали требуемые технологические параметры (Р = 2,0 МПа, ОСГ 1000 ч-1, Н 2 /СО = 2) и ступенчато (2,5 °С · ч-1) поднимали температуру до 240 °С.
Газообразные продукты синтеза анализировали на хроматографе «Кристалл 5000» (Хро-матэк, Россия) с детектором по теплопроводности и двумя колонками Haysep R и NаХ.
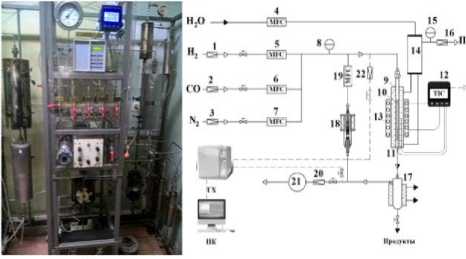
Рисунок 1. Фото и технологическая схема установки синтеза углеводородов: 1, 2, 3, 20 – регуляторы давления; 4, 5, 6, 7, 16, 19 – регуляторы расхода газа; 8,15 – манометры; 9 – реактор; 10 – термопарный чехол; 11 – термопары; 12 – регулятор температуры; 13 – печь; 14 – паросборник; 17 – сборник-сепаратор; 18 – циркуляционный насос; 21 – газовый счётчик Figure 1. Photo and flow diagram of the installation of hydrocarbon synthesis: 1, 2, 3, 20 – pressure regulators; 4, 5, 6, 7, 16, 19 – gas flow regulators; 8,15 – manometers; 9 – reactor; 10 – thermocouple housing; 11 – thermocouples; 12 – temperature regulator; 13 – reactor electrical furnace; 14 – steam chest; 17 – liquid products separator; 18 – recirculating pump; 21 – gasometer
Для цеолита наблюдаются рефлексы в области углов 2θ ≈ 7–30°. Интенсивные максимумы на рентгенограмме, характерные для структурного типа цеолита ZSM-5 [18], зафиксированы при углах: 7,92; 7,94; 13,95; 14,77; 23,08; 23.25; 23,40; 29,83; 45,20°. Исследуемый образец цеолита обладает высокой фазовой чистотой и степенью окристаллизованности. В образцах Со-Аl 2 О 3 /SiО 2 катализатора и композитного катализатора на его основе присутствует фаза оксида кобальта Со 3 О 4 в диапазоне углов 2θ ≈ 18–65°. В композитном катализаторе зафиксирована фаза цеолита ZSM-5 и нестехиометрического оксида алюминия формулой Аl 2.666 О 3.999 , имеющих кубическую структуру шпинели дефектного типа [19].
Интенсивность (Intensify), усл. ед. • - Co 3 O 4 ; ♦ - A1 2 O 3 ; о - ZSM-5 °о *
и • о / •♦ ■ • ♦
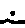
Полученные жидкие углеводороды С 5+ подвергали фракционированию, выделяя фракции углеводородов в зависимости от температуры кипения (н.к. – 180 °C, 180–330 °C, > 330 °C). Индивидуальный и групповой состав фракций устанавливали методом капиллярной газожидкостной хромато-масс-спектрометрии на газовом хроматографе Agilent GC 7890 с масс-селектив-ным детектором MSD 5975С и капиллярной колонкой HP-5МS.
Результаты и обсуждение
Рентгенограммы исходного Со-Аl 2 О 3 /SiО 2 катализатора, цеолита HZSM-5 и полученного на их основе композитного катализатора представлены на рисунке 2.
85 2θ, град. deg
Рисунок 2. Рентгенограммы цеолита ZSM-5 (1), Со-Аl 2 О 3 /SiО 2 (2) и Co-Аl 2 О 3 /SiО 2 /ZSM-5/Аl 2 О 3
катализаторов (3)
Figure 2. X-ray diffraction pattern of the ZSM-5 (1), Со-Аl 2 О 3 /SiО 2 (2) and Co-Аl 2 О 3 /SiО 2 /ZSM-5/Аl 2 О 3 catalysts (3)
Средний размер кристаллитов Со 3 О 4 (таблица 1) в исходном и композитном катализаторах был рассчитан по уравнению Шеррера [20] для наиболее интенсивной характеристической линии со значением 2θ = 36,8°.
Физико-химические свойства катализаторов
Таблица 1.
Table 1.
Physico-chemical properties of catalysts
|
Катализатор Catalyst |
с(Со), % |
S уд , м 2 /г |
Размер частиц, нм | Particle size, nm |
||
|
d(Со 3 О 4 )* |
d(Со 0 )* |
d(Со 0 )** |
|||
|
Co-Аl 2 О 3 /SiО 2 |
22,8 |
239 |
20,0 |
15,0 |
8,0 ± 1 |
|
35%Co-Аl 2 О 3 / SiО 2 + 30% ZSM-5 + 35% Аl 2 О 3 |
7,4 |
286 |
14,5 |
11,0 |
8,2 ± 1 |
* По результатам РФА, ** по результатам ПЭМ с(Со), % – концентрация кобальта в катализаторе; D – дисперсность металлического кобальта (Со 0 ); S уд , м 2 / г – площадь удельной поверхности.
* Based on the results of the RFA, ** Based on the results of FEM с(Co), % – Cobalt concentration in the catalyst; D – Dispersion of metallic cobalt (Co 0 ); S Ud , m 2 /g – Area of specific surface.
Концентрация кобальта в композитном катализаторе составляет 7,4%, площадь удельной поверхности – 286 м2/г. Размер частиц кобальта, оцененный по уравнению Шеррера для исходного и композитного катализатора, составляет соответственно 15 и 11 нм. Анализ диаграммы распределения кристаллитов кобальта по размерам для композитного катализатора, полученной с помощью ПЭМ (рисунок 3), дает средневзвешенный размер частиц кобальта в композитном катализаторе около 8,2 нм, что практически совпадает с полученным ранее значением 8 нм [14] для катализатора Co-Аl 2 О 3 /SiО 2 . Таким образом, присутствие цеолита и бемита в составе композитного катализатора не оказывает влияния на размер кристаллитов кобальта.
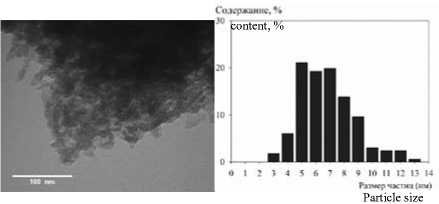
Рисунок 3. ПЭМ микрофотографии восстановленного композитного катализатора и гистограммы распределения размера частиц кобальта
Figure 3. TEM micrographs of reduced composite catalyst and histograms of cobalt particle size distribution
Активность катализатора определяли на синтез-газе (% об.: СО – 20; Н2 – 40; N2 – 40), моделирующем состав газа, получаемый при использовании на первой стадии технологии XTL в качестве окислителя воздуха вместо кислорода [21, 22]. Использование дешевого и доступного окислителя позволит сократить капитальные и эксплуатационные затраты при создании производства XTL, а присутствие в синтез-газе азота уменьшить вероятность перегрева катализатора ФТ.
Результаты каталитических испытаний представлены на рисунках 4, 5 и в таблице 2.
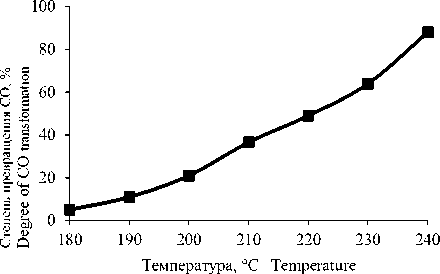
Рисунок 4. Зависимость степени превращения СО от температуры синтеза
Figure 4. Dependence of CO conversion on synthesis temperature
Испытанный образец композитного катализатора активен во всем исследованном диапазоне температуры. С ростом температуры от 180 до 240 °С наблюдается увеличение конверсии СО с 5 до 87%. В среднем увеличение температуры синтеза на 10 °С приводит к росту конверсии СО на 15%. При температуре синтеза 240 °С осуществляли синтез в течение 60 ч, усредненные каталитические характеристики за этот промежуток времени представлены в таблице 2.
Таблица 2.
Каталитические свойства композитного катализатора (Р = 2,0 МПа, ОСГ 1000 ч-1, Т = 240 °С)
Table 2.
Catalytic properties of the composite catalyst (Р = 2,0 МПа, GHSV 1000 ч-1, Т = 240 °С)
|
Конверсия Селективность (Conversion), % (Selectivity), % СО Н2 СН4 С2-С4 С5+ СО2 |
Производительность (productivity) по С5+, кг/(м3∙ч) |
|
84,0 91,1 17,3 9,4 69,1 4,1 |
81,0 |
В исследованных условиях синтеза на композитном катализаторе достигается достаточно глубокая конверсия сырья: степень превращения СО и Н2 составляет 84,0 и 91,1% соответственно. Большая на 7% степень превращения Н2 является следствием протекания реакции метанирования, на которую расходуется водорода больше, чем на образование углеводородов С5+ (соотношение Н2/СО на реакцию мета-нирования – 3, на образование углеводородов С5+ – 2). Селективность по метану составляет 17,3%, по углеводородам С2–С4 – 9,3%. Отношение селективности по метану к селективности по углеводородам С2–С4 (SСН4/SС2-С4) на исходном Co-Аl2 О3/SiО2 катализаторе в близких условиях синтеза [14] составляло 1,27. На композитном катализаторе этот показатель увеличился до 1,87 за счет роста селективности по метану. Это может указывать на то, что метан образуется не только в результате первичного синтеза углеводородов из СО и Н2, а также в результате вторичных превращений углеводородов С5+. Действительно, введение в состав катализатора цеолита ZSM-5 и Аl2О3 в качестве связующего может способствовать протеканию реакций крекинга углеводородов С5+ с образованием метана [23]. Селективность по углеводородам С5+ составляет 69,1%, по СО2 – 4,1%. Образование СО2 в условиях синтеза ФТ происходит по реакции водяного газа [24], скорость которой возрастает с увеличением температуры и парциального давления водяного пара. Достигнута производительность катализатора по углеводородам С5+ 81 кг/(м3∙ч), выход этих продуктов составил 70 г/м3 пропущенного синтез-газа и 135 г/м3 превращённого синтез-газа.
Зависимость степени превращения СО от времени синтеза представлена на рис. 5. О скорости дезактивации катализаторов судили по параметру R (%·ч-1), показывающему на сколько процентов уменьшается конверсия СО за 1 час работы катализатора. R определяли по формуле:
нк
R = CO CO
τ где XCнO – начальная степень конверсии СО, %;
X C к O – конечная степень конверсии СО, %; τ – промежуток времени от X C н O до X C к O , ч.
В целом катализатор показал закономерное снижение конверсии СО во времени [25]. Скорость дезактивации оценивали на трёх участках работа катализатора (каждые 20 ч синтеза). В первые 20 ч синтеза наблюдается наибольшая скорость дезактивации, равная 0,18%·ч-1, на втором участке скорость дезактивации несколько снижается и составляет
0,15%·ч-1. На третьем участке катализатор показал самую стабильную работу R = 0,03%·ч-1.
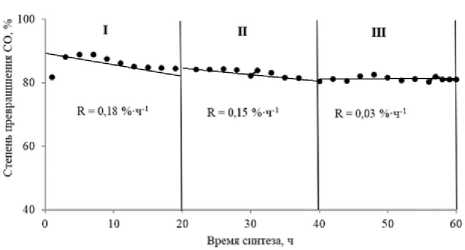
Рисунок 5. Зависимость изменения степени превращения СО от времени синтеза
Figure 5. Effect of time on stream on CO conversion
Активацию катализатора реакционной средой осуществляли в течение 24 ч путем поднятия температуры со скоростью 2,5 °С/ч от 180 до 240 °С. По-видимому, на первых двух участках продолжает происходить стабилизация катализатора под действием реакционной среды, что может приводить к изменению степени восстановления кобальта и его размеров. Скорость дезактивации композитного катализатора на третьем участке сопоставима со скоростью дезактивации коммерческого (7,5 Co – 0,19% Ru/75% ZSM-5/17%/Аl2О3) катализатора компании «Chevron» (R = 0,05% · ч-1) [26].
Состав полученных углеводородов С 5+ представлен в таблице 3.
Таблица 3.
Фракционный и групповой состав продуктов синтеза
Table 3.
Fractional and group composition of synthesis products
|
Группа углеводородов Hydrocarbon Group |
Фракционный состав углеводородов, % масс. Fractional composition of hydrocarbons |
∑ |
изо/н* |
о/п** |
|||
|
С5-С10 |
С11-С18 |
С19+ |
|||||
|
н-алканы | n-alkanes |
7,2 |
14,7 |
11,0 |
32,9 |
50,7 49,3 |
1,26 |
0,97 |
|
изо-алканы| iso-alkane н-алкены| n-alkenes |
6,0 10,1 |
10,5 1,3 |
1,3 – |
17,8 11,4 |
|||
|
разв.-алкены| r.-alkenes |
32,5 |
5,3 |
0,1 |
37,9 |
|||
|
Итого | Total |
55,8 |
31,8 |
12,4 |
100 |
|||
* Изо/н – отношение углеводородов изостроения к углеводородам нормального строения; о/п – отношение олефиновых углеводородов к парафиновым.
* Iso/n – The ratio of isobuilding hydrocarbons to normal building hydrocarbons; o/p – The ratio of oleic hydrocarbons to paraffin.
Полученные углеводороды С5+ состоят преимущественно из бензиновой и дизельной фракций, содержание которых составляет 55,8 и 31,8% соответственно. Содержание длинноцепочечных углеводородов С19+ составляет 12,4%. В продуктах синтеза присутствует значительное количество разветвленных и ненасыщенных углеводородов. Отношение количества углеводородов изомерного строения к углеводородам нормального строения (изо/н) составляет 1,26, а отношение углеводородов олефинового ряда к углеводородам парафинового ряда составляет 0,97. В бензиновой фракции углеводородов (С5-С10) отмечено высокое содержание алкенов нормального и разветвленного строения (76,3%), доля изо-алканов и н-алканов составляет 10,8 и 12,9% соответственно. По групповому составу бензиновая фракция сопоставима с бензином каталитического крекинга [27]. Можно сделать предположение, что этот бензин будет обладать высокой антидетонационной способностью, но низкой химической стабильностью вследствие большого содержания ненасыщенных углеводородов. Его возможно использовать в качестве добавки к прямогонному бензину или бензину каталитического риформинга. Дизельная фракция на 46,0% состоит из н-парафинов и на 49,7% – из углеводородов изостроения. Такое сочетание углеводородов будет способствовать высокому цетановому числу и хорошим низкотемпературным свойствам (температура помутнения, предельная температура фильтруемости). Углеводороды С19+ состоят преимущественно из н-алканов, доля которых составляет 88,7%, алкены присутствуют в следовых количествах (0,8%).
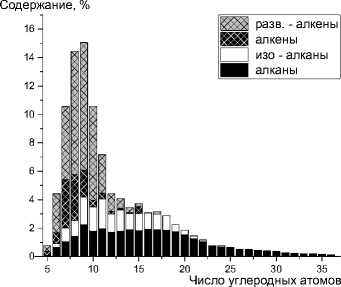
Рисунок 6. Молекулярно-массовое распределение продуктов синтеза на композитном катализаторе
Figure 6. Molecular weight distribution of synthesis products on a composite catalyst
Список литературы Совмещенный синтез и гидрооблагораживание углеводородов на кобальтовом цеолитсодержащем катализаторе
- King D.L., Klerk A. Overview of Feed-to-Liquid (XTL) Conversion//ACS Symposium Series. 2011. V. 1084. Р. 1-24 DOI: 10.1021/bk2011-1084.ch001
- Крылова А.Ю., Куликова М.В., Лапидус А.Л. Катализаторы синтеза Фишера-Тропша для процессов получения жидких топлив из различного сырья//Химия твердого топлива. 2014. № 4. С. 18-21 DOI: 10.7868/S0023117714040070
- Мордкович В.З., Синева Л.В., Кульчаковская Е.В., Асалиева Е.Ю. Четыре поколения технологии получения синтетического жидкого топлива на основе синтеза Фишера-Тропша//Катализ в промышленности. 2015. № 5. С. 23-45 DOI: 10.18412/1816-0387-2015-5-23-45
- Carvalho A., Marinova M., Batalha N., Marcilio N.R. et al. Design of nanocomposites with cobalt encapsulated in the zeolite micropores for selective synthesis of isoparaffins in Fischer-Tropsch reaction//Catalysis Science & Technology. 2017. V. 7. № 21. Р. 5019-5027 DOI: 10.1039/C7CY01945A
- Kim J., Lee S., Cho K., Na K. et al. Mesoporous MFI Zeolite Nanosponge Supporting Cobalt Nanoparticles as a Fischer-Tropsch Catalyst with High Yield of Branched Hydrocarbons in the Gasoline Range//ACS Catalysis. 2014. V. 4. Р. 3919-3927 DOI: 10.1021/cs500784v
- Sartipi S., Dijk J.E., Gascon J., Kapteijn F. Toward bifunctional catalysts for the direct conversion of syngas to gasoline range hydrocarbons: H-ZSM5 coated Co versus H-ZSM5 supported Co//Applied Catalysis A: General. 2013. V. 456. Р. 11-22
- DOI: 10.1016/j.apcata.2013.02.012
- Adeleke A.A., Liu X., Lu X., Hildebrandt M.D. Cobalt hybrid catalysts in Fischer-Tropsch synthesis//Reviews in Chemical Engineering. 2018
- DOI: 10.1515/revce2018-0012
- Valero-Romero M.J., Sartipi S., Sun X., Rodriguez-Mirasol J. et al. Carbon/H-ZSM5 composites as supports for bifunctional Fischer-Tropsch synthesis catalysts//Catal. Sci. Technol. 2016. V. 6. P. 2633-2646
- DOI: 10.1039/C5CY01942G
- Yao M., Yao N., Liu B., Li S. et al. Effect of SiO2/Al2 O3 ratio on the activities of CoRu/ZSM5 Fischer-Tropsch synthesis catalysts//Catal. Sci. Technol. 2015. V. 5. Р. 2821-2828
- DOI: 10.1039/C5CY00017C
- Nakanishia M., Uddina A., Katoa Y., Nishina Y. et al. Effects of preparation method on the properties of cobalt supported-zeolite catalysts for Fischer-Tropsch synthesis//Catal. Sci. Technol. 2015. V. 5. Р. 1847-1853
- DOI: 10.1016/j.cattod.2017.01.017
- Kang J., Wang X., Peng X., Yang Y. et al. Mesoporous Zeolite Y-Supported Co Nanoparticles as Efficient Fischer-Tropsch Catalysts for Selective Synthesis of Diesel Fuel//Ind. Eng. Chem. Res. 2016. V. 55. № 51. Р. 13008-13019
- DOI: 10.1021/acs.iecr.6b03810
- Nakanishi M., Uddina Md. A., Kato Y., Nishina Y. et al. Effects of preparation method on the properties of cobalt supported ?-zeolite catalysts for Fischer-Tropsch synthesis//Catalysis Today. 2017. V. 291. P. 124-132. doi. 10.1016/j.cattod.2017.01.017.
- Kruse N., Machoke A.G., Schwieger W., Gottel R. Nanostructured Encapsulated Catalysts for Combination of Fischer-Tropsch Synthesis and Hydroprocessing//ChemCatChem. 2015. V. 7. Р. 1018-1022
- DOI: 10.1002/cctc.201403004
- Savost’yanov A.P., Yakovenko R.E., Sulima S.I., Bakun V.G. et al. The impact of Al2 O3 promoter on an efficiency of C5+ hydrocarbonsformation over Co/SiO2 catalysts via Fischer-Tropsch synthesis//Catalysis Today. 2017. V. 279. Р. 107-114
- DOI: 10.1016/j.cattod.2016.02.037
- Нарочный ГБ., Савостьянов А.П., Яковенко Р.Е., Бакун В.Г Опыт реализации технологии кобальтового катализатора синтеза углеводородов из СО и Н2//Катализ в промышленности. 2016. № 1. С. 37-42
- DOI: 10.18412/1816-0387-2016-1-37-42
- Шавалеев Д.А., Травкина О.С., Алехина И.Е., Эрштейн А.С. и др. Синтез и исследование физико-химических свойств каталитической системы на основе цеолита ZSM5//Вестник Башкирского университета. 2015. Т. 20. № 1. С. 58-65.
- PDF2. The powder diffraction file TM. International Center for Diffraction Data (ICDD), PDF2 Release 2012. URL: www.icdd.com.
- Collection of Simulated XRD Powder Patterns for Zeolites; Ed. Treacy M.M.J., Higgins J.B. Elsevier, 2001. 586 p.
- Wilson S.J. The Dehydration of Boehmite ?-AIOOH, ?-Al2 O3//Journal of Solid State Chemistry. 1979. V. 30. P. 241-255
- DOI: 10.1016/0022-4596(79)90106-3
- Young R.A. The Rietveld Method. Oxford University Press, 1995. 308 р.
- Zhu T., Flytzani-Stephanopoulos M. Catalytic partial oxidation of methane to synthesis gas over Ni-CeO2//Applied Catalysis A: General. 2001. V. 208. P. 403-417
- DOI: 10.1016/S0926-860X(00)00728-6
- Al-Sayari S.A. Recent Developments in the Partial Oxidation of Methane to Syngas//The Open Catalysis Journal. 2013. V. 6. P. 17-28
- DOI: 10.2174/1876214X20130729001
- Zhu C., Bollas G.M. Gasoline Selective Fischer-Tropsch Synthesis in Structured Bifunctional Catalysts//Applied Catalysis B: Environmental. 2018. V. 235. P. 92-102
- DOI: 10.1016/j.apcatb.2018.04.063
- Khodakov A.Y., Chu W., Fongarland P. Advances in the Development of Novel Cobalt Fischer-Tropsch Catalysts for Synthesis of Long-Chain Hydrocarbons and Clean Fuels//Chem. Rev. 2007. V. 107. P. 1692-1744
- DOI: 10.1021/cr050972v
- Zhou W., Chen J., Fang K., Sun Y.H. The deactivation of Co/SiO2 catalyst for Fischer-Tropsch synthesis at different ratios of H2 to CO//Fuel Processing Technology. 2006. V. 87. Р. 609-616
- DOI: 10.1016/j.fuproc.2006.01.008
- Kibby C., Jothimurugesan K., Das T., Lacheen H.S. et al. Chevron’s gas conversion catalysis-hybrid catalysts for wax-free Fischer-Tropsch synthesis//Catalysis Today. 2013 V. 215. P.131-141
- DOI: 10.1016/j.cattod.2013.03.009
- Нурмухаметова Э.Р., Ахметов А.Ф., Рахматуллин А.Р. Исследование бензина каталити-ческого крекинга//Нефтегазовое дело: электронный научный журнал. 2014. № 2. С. 181-193.


