Современные подходы к минимально инвазивной хирургии аортального клапана
Автор: Комаров Р.Н., Огнев Олег Олегович, Исмаилбаев А.М., Чернявский С.В., Дзюндзя А.Н., Ленковец М.В.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Обзоры
Статья в выпуске: 3 т.26, 2022 года.
Бесплатный доступ
За последние 30 лет минимально инвазивная кардиохирургия из единичных демонстраций операций доступом через торакотомию и различных вариантов частичных стернотомий превратилась в использование мини-доступов «на потоке», а также выполнение полностью торакоскопических и роботизированных операций. В хирургию аортального клапана минимально инвазивные технологии внедрены наиболее широко. Цель данного обзора - описание современных подходов к минимально инвазивной хирургии аортального клапана, включая критерии отбора пациентов, эволюцию и описание основных операционных доступов. Стратегия поиска включила анализ международных баз данных PubMed, Scopus, Embase, Web of Science. Поиск осуществляли по ключевым словам minimally invasive surgery of aortic valve, alternative surgical approaches in aortic valve surgery, minimally invasive autologous pericardium neocuspidization. Отбор пациентов для минимально инвазивных аортальных вмешательств должен учитывать как анатомические особенности средостения и корня аорты, так и коморбидность пациента и сопутствующую кардиальную патологию. К минимально инвазивным доступам в хирургии аортального клапана относят торакотомии, частичные стернотомии и методики эндоскопической хирургии. Особый интерес представляет минимально инвазивная неокуспидизация клапана аутологичным перикардом. Используют частичные стернотомии наиболее рутинно в хирургии аортального клапана, а накопленные результаты позволяют провести крупные метаанализы для сравнения эффективности и безопасности с классическим стернотомным доступом. В минимально инвазивной аутоперикардиальной неокуспидизации и эндоскопических вмешательствах на аортальном клапане требуется дальнейшее накопление хирургического опыта и клинического материала.
Аортальный клапан, аутоперикардиальная неокуспидизация, минимально инвазивная хирургия, торакотомия, частичная стернотомия
Короткий адрес: https://sciup.org/142235608
IDR: 142235608 | DOI: 10.21688/1681-3472-2022-3-31-40
State-of-the-art surgical approaches in minimally invasive aortic valve surgery
Over the past 30 years, minimally invasive cardiac surgery has progressed from single case reports of operations via thoracotomy and various procedures of partial sternotomy to routine use of mini-accesses as well as fully thoracoscopic and robotic techniques. It is aortic valve surgery that implemented minimally invasive technologies most widely. The objective of this systematic review is to present state-of-the-art approaches to minimally invasive aortic valve surgery including patient selection criteria as well as evolution and state-of-the-art of the main surgical approaches. The search strategy covered international databases, such as PubMed, Scopus, Embase, and Web of Science. We used following queries: 'minimally invasive surgery of the aortic valve', 'alternative surgical approaches in aortic valve surgery', 'minimally invasive autologous pericardium neocuspidization'. Selection of patients for minimally invasive aortic interventions should consider both the anatomy of the mediastinum and the aortic root as well as cardiac and other comorbidities. Minimally invasive approaches in aortic valve surgery include thoracotomy, partial sternotomy, and endoscopic techniques. Of particular interest is minimally invasive neocuspidization with autologous pericardium. Partial sternotomies are the most routinely used approaches in aortic valve surgery. Their cumulative outcomes allow to compare their efficacy and safety with those of classic sternotomy access within large meta-analyses. Minimally invasive autopericardial neocuspidization and endoscopic interventions on the aortic valve require further surgical experience and clinical outcomes.
Текст обзорной статьи Современные подходы к минимально инвазивной хирургии аортального клапана
Цитировать: Комаров Р.Н., Огнев О.О., Исмаилбаев А.М., Чернявский С.В., Дзюндзя А.Н., Ленковец М.В. Современные подходы к минимально инвазивной хирургии аортального клапана. Патология кровообращения и кардиохирургия. 2022;26(3):31-40. https://
Р.Н. Комаров, О.О. Огнев, А.М. Исмаилбаев, С.В. Чернявский, А.Н. Дзюндзя, М.В. Ленковец,
За последние 30 лет минимально инвазивная кардиохирургия превратилась из единичных демонстраций операций доступом через торакотомию и различных вариантов частичных стернотомий в использование мини-доступов «на потоке», а также выполнение полностью торакоскопических и роботизированных операций. Мини-инвазивная хирургия позволяет снизить травматичность операции, длительность пребывания в стационаре, выраженность болевого синдрома, а также обеспечить более быструю реабилитацию и лучший косметический эффект по сравнению со стандартным кардиохирургическим доступом — полной стернотомией [1; 2]. В хирургию аортального клапана (АК) минимально инвазивные технологии внедрены наиболее широко.
Цель обзора — описание современных подходов к минимально инвазивной хирургии аортального клапана, включая критерии отбора пациентов, эволюцию и описание основных операционных доступов.
Стратегия поиска
Провели анализ по международным базам данных PubMed, Scopus, Embase, Web of Science. Ключевые слова для поиска: minimally invasive surgery of aortic valve, alternative surgical approaches in aortic valve surgery, minimally invasive autologous pericardium neocuspidization.
Срединная стернотомия
Большинство кардиохирургических вмешательств выполняется из классической полной срединной стернотомии (рис. 1). В Германии стандартным доступом осуществляют 92 % кардиохирургических вмешательств и 98 % изолированных коронарных шунтирований [3]. Данный доступ обладает отличной визуализацией и возможностью хирургических манипуляций, но является довольно травматичным и требует длительной реабилитации и ограничений, связанных в первую очередь с заживлением грудины. Инфекционные осложнения составляют 0,5–5,0 %. Летальность при их развитии — от 7 до 80 % [4]. Также существуют группы больных с повышенным риском несостоятельности грудины, остеомиелита и инфекционных осложнений вплоть до медиастинита. К ним относятся пациенты с сахарным диабетом, высоким индексом массы тела, мультифокальным атеросклерозом,
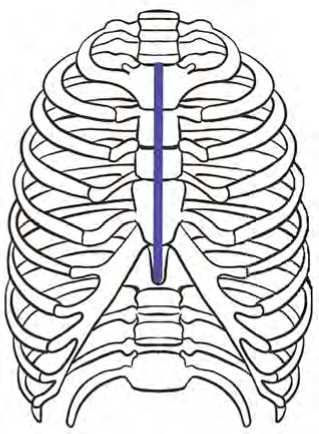
Рис. 1. Полная срединная стернотомия хронической сердечной и почечной недостаточностью, необходимостью проведения повторных вмешательств. Таким образом, раневые осложнения обладают неблагоприятным прогнозом, являются довольно трудоемкими в лечении и требуют больших финансовых затрат [5].
C. Heilmann и соавт. проанализировали 1 279 больных после кардиохирургических вмешательств c доступом через срединную стернотомию. У 76 (5,8 %) отмечали раневые осложнения с вовлечением грудины. В 43 (3,3 %) случаях дном раны являлась грудина, а у 33 пациентов (2,5 %) инфекционный процесс распространялся на средостение — медиастинит [6].
Стремление к минимизации травматичности, тенденция к fast track, снижению доступ-ассоциирован-ных осложнений, а также активное внедрение в других областях хирургии минимально инвазивного подхода, эндоскопии, развитие и внедрение эндоваскулярных методов лечения привели к разработке мини-доступов и в кардиохирургии [7].
Отбор больных для мини-доступа
У пациентов с патологией аортального клапана необходим строгий отбор на минимально инвазивные вмешательства. В некоторых ситуациях приоритет отдают стандартному доступу, например при сочетанных кардиохирургических патологиях. Отдельное внимание уделяют анатомическим особенностям, таким как глубина расположения корня аорты, длина восходящего отдела аорты, размеры и расположение камер сердца. Многие авторы оценивали не только анатомию аорты, но и ее состояние — выраженность атеросклеротического изменения стенки («фарфоровая» аорта). Первичное или повторное вмешательство — один из определяющих факторов в выборе доступа в связи с развитием спаечного процесса, который может сделать крайне трудоемким как стандартный доступ, так и мини-инвазивный.
Сниженная фракция выброса и коморбидное состояние (сахарный диабет, почечная и сердечная недостаточность) требуют от хирурга скорости с целью сокращения длительности искусственного кровообращения (ИК) и ишемии миокарда (ИМ), что может являться решающим фактором при выборе доступа в пользу классической стернотомии. Однако минимально инвазивные вмешательства выполняют опытные хирурги, что выражается отсутствием статистической разницы в продолжительности ИК и ИМ по результатам исследований. J. Lamelas и со-авт. продемонстрировали, что у пациентов старше 75 лет минимально инвазивная хирургия аортального клапана снижала летальность, и предложили сделать данный подход доступом выбора у этой группы больных [8]. В 2014 г. T.C. Nguyen и соавт. продемонстрировали преимущества минимально инвазивной хирургии аортального клапана у пациентов со сниженной фракцией выброса (< 40 %) [9].
В то же время выполнение вмешательства в ограниченном операционном поле является более трудоемким по сравнению со стандартным подходом, поэтому желание уменьшить хирургическую травму, объем кровопотери, длительность искусственной вентиляции легких и время восстановления в послеоперационном периоде с помощью мини-доступа может привести к более длительному времени ИК и ИМ при развитии осложнений, требующих конверсии, что значительно увеличивает длительность, травматичность и объем кровопотери.
Таким образом, между минимально инвазивным доступом и классической стернотомией окончательно выбирает хирург. Помимо этого, необходимо определить, какой мини-доступ больше соответствует случаю: мини-стернотомия (наиболее часто используют J-образную) или мини-торакотомия (наиболее распространенная — передняя). При операциях на АК предпочтение отдают J-образной мини-стернотомии, на митральном клапане — мини-торакотомии в связи с углом наклона операционного поля. При равных анатомических удобствах приоритет у мини-торакотомии в ситуациях с высоким риском нестабильности грудины в послеопе- рационном периоде. К этой группе относят пациентов с избыточной массой тела, остеомиелитом, сахарным диабетом или почечной недостаточностью, инфекционным процессом в области грудины. J-образную мини-стернотомию предпочтительнее использовать при невозможности однолегочной вентиляции, а также инфекции в месте торакотомии, выраженном спаечном процессе в правой плевральной полости в месте предполагаемой торакотомии в связи с высоким риском пневмоторакса в послеоперационном периоде. Уровень мини-стернотомии, необходимый для адекватной визуализации аортального клапана, зависит от типа телосложения, хронических заболеваний дыхательных путей, а также расположения сердца — вертикального или горизонтального.
Нет четких абсолютных противопоказаний к тому или иному доступу, но индивидуальные особенности больного увеличивают или уменьшают трудоемкость операции. Окончательные показания или противопоказания к выбору доступа зависят от рисков осложнений и опыта хирурга [3].
Минимально инвазивные подходы
Мини-инвазивный доступ в кардиохирургии подразумевает доступ с небольшим кожным разрезом без полной срединной стернотомии. В 1993 г. P.N. Rao и A.S. Kumar выполнили первое в мире мини-инвазивное протезирование аортального клапана доступом через правостороннюю торакотомию [10].
В 1997 г. L.H. Cohn и соавт. опубликовали работу с двумя мини-доступами для коррекции клапанных пороков. Первый — парастернальный доступ, осуществлявшийся путем пересечения нескольких реберных суставов и правой внутренней грудной артерии (рис. 2A). Второй — продольная стернотомия от яремной вырезки до 3-го межреберья и последующим изменением направления разреза к 3-му или 4-му правому межреберью (рис. 2B, C). Этот доступ в последующем получил название J-образная мини-стернотомия (или L-образная мини-стернотомия при изменении направления разреза влево) (рис. 2D, E) [11].
L.G. Svensson описал J- или L-образную министернотомию с модификацией, заключавшейся в дополнении поперечным разрезом от стернотомии до 1-го межреберья справа или слева ( ] или [ ) (рис. 2F, G) [12].
J-образная мини-стернотомия является наиболее часто используемым мини-доступом в хирургии аорты и аортального клапана. В 2018 г. E. Mikus
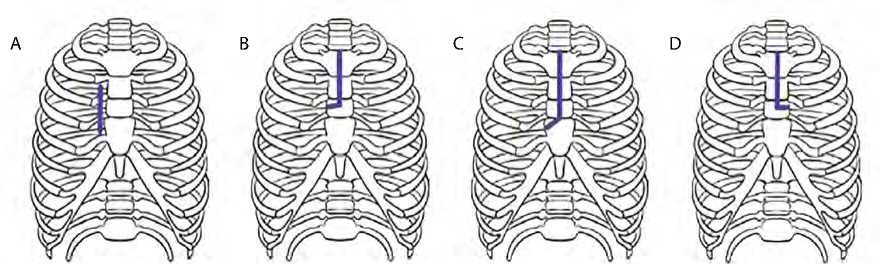
Рис. 2. Мини-доступы: парастернальный доступ (A); J-образная мини-стернотомия по 3-му межреберью (B);
J-образная мини-стернотомия по 4-му межреберью (C);
L-образная мини-стернотомия по 3-му межреберью (D);
L-образная мини-стернотомия по 4-му межреберью (E);
]-образная стернотомия (F); [-образная стернотомия (G)
и соавт. опубликовали результаты сравнения пациентов после протезирования аортального клапана из мини-доступа и полной стернотомии. Госпитальная летальность в группах не различалась [13].
Y. Wu и соавт. провели анализ 80 пациентов, которым выполнили вмешательства на восходящем отделе и дуге аорты из J-образной мини-стернотомии и классическим доступом. Мини-стернотомия увеличивала длительность ИМ (160 ± 38 и 135 ± 36 мин), но снижала длительность искусственной вентиляции легких (22 и 45 ч), пребывания в отделении реанимации (4,6 ± 2,7 и 7,9 ± 3,7 дня), госпитализации (8,2 ± 3,8 и 21,4 ± 11,9 дня, p = 0,001). В группе с мини-стернотомией значимо снижались объем гемотрансфузии (4,6 ± 3,3 и 6,7 ± 5,7 ед.), объем кровопотери (764 ± 549 и 1255 ± 745 мл). Частота послеоперационных осложнений не различалась между группами [14].
В 2017 г. B.H. Kirmani и соавт. сравнили J-образную мини-стернотомию с полной срединной: летальность была статистически незначимой. Длительность ИК также не различалась между группами, как и продолжительность ИМ. В группе с J-образной мини-стернотомией отмечали меньшие количество кровопотери и длительность пребывания в отделении реанимации [1].
J-образная мини-стернотомия обеспечивает адекватную визуализацию аортального, митрального и трикуспидального клапанов. В 2017 г.
P. Risteski и соавт. описали трехклапанную коррекцию из J-образной мини-стернотомии у 37 больных. Ранняя послеоперационная смертность составила 5 человек (13,5 %). Пятилетняя выживаемость 52 ± 10 %. Ни в одном случае не было конверсии на полную срединную стернотомию. В 4 случаях выполнили рестернотомию: по поводу кровотечения — 1 (3 %), тампонады — 3 (8 %). Длительность ИК и ИМ сопоставима с трехклапанными коррекциями через классическую стернотомию, а качество коррекции из мини-доступа соответствует оперативному вмешательству через полную срединную стернотомию [15–17].
В метаанализе K. Phan и соавт. 30-дневная летальность статистически значимо не различалась: в группе мини-стернотомии составила 33 из 2 558 больных, в группе полной стернотомии — 51 из 2 558. В длительности ИК, ИМ, количестве инсультов, повторных операций в связи с кровотечением и инфекционными осложнениями также нет статистически значимой разницы [2].
Варианты частичных стернотомий
В период развития минимально инвазивной кардиохирургии многие хирурги искали альтернативные доступы с целью избежать полной срединной стернотомии. В связи с этим разработали различные виды частичных стернотомий: H. Kasegawa и соавт.
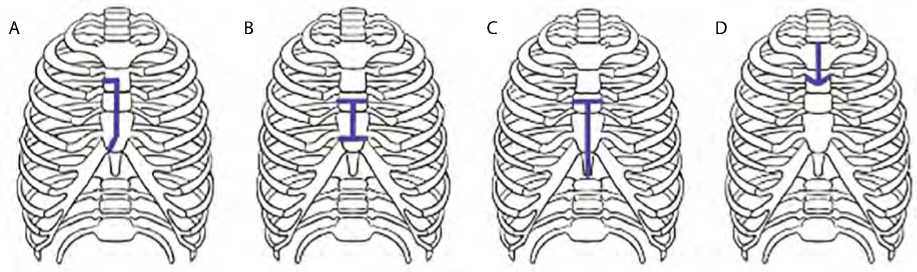
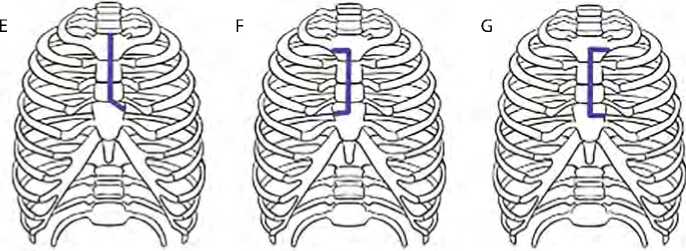
Рис. 3. Мини-стернотомии: правосторонняя частичная нижняя стернотомия (метод «открытых дверей») (A);
I-образная мини-стернотомия (B); частичная нижняя Т-образная стернотомия (C); верхняя V-образная стернотомия (D)
описали метод «открытых дверей» — правостороннюю частичную нижнюю стернотомию (рис. 3A) [18], Y.S. Chang и соавт. — I-образную мини-стернотомию (рис. 3B) [19], D.B. Doty и соавт., J.R. Fenton и J.R. Doty, C.-Y. Hsiao и соавт. — частичную нижнюю Т-образную стернотомию (рис. 3C) [20–22].
J.H. Karimov и соавт. описали одну из наименее инвазивных стернотомий — верхнюю V-образную частичную стернотомию. Выполнили данный доступ из кожного разреза 6–7 см, продольную срединную стернотомию до 2-го межреберья дополнили V-образным разрезом (рис. 3D) [23].
C.L. Burdett и соавт. провели сравнение V-образной и классической стернотомий (98 и 93 пациента соответственно). Хирургический риск в группах оценили по шкале EuroSCORE: для мини-протезирования аортального клапана — 7,15, для протезирования аортального клапана — 6,55. Средняя длительность ИК в группе мини-стернотомии на 10 мин больше, ИМ — на 6 мин. В группе с V-образной стернотомией отметили значительное снижение объема кровопотери в послеоперационном периоде 332 и 513 мл, а также объема переливаемых компонентов крови (свежезамороженная плазма и тромбоциты) 24 и 36 %. Выживаемость за период наблюдения 18 мес. статистически значимо не различалась: 99 и 97 % для мини-протезирования и протезирования соответственно. Также авторы продемонстрировали, что V-образный разрез грудины обеспечивал эффект клина, что предотвратило смещение частей грудины латерально, в отличие от других частичных стернотомий [24].
Варианты мини-торакотомий
Наилучшим способом уменьшить кровопотерю и травматичность доступа в кардиохирургии явля- ется отсутствие травмы грудины. Параллельно с различными видами мини-стернотомий разрабатывали доступы через мини-торакотомию. Классическую правостороннюю переднюю мини-торакотомию выполняли в 3-м межреберье от грудины на длину около 6–7 см (рис. 4A). В исследовании E. Mikus и соавт. длительность ИК и ИМ в группе передней торакотомии была меньше, чем при мини-стернотомии и стандартной стернотомии, а госпитальная летальность не различалась между группами [13].
В 2020 г. M.Y. Salmasi и соавт. провели систематический анализ мини-стернотомии и правой передней торакотомии у 2 926 пациентов. Группы не различались по летальности. В группе мини-стернотомий по сравнению с правой передней торакотомией снижались количество рестернотомий по поводу кровотечений, длительность ИМ, частота конверсий на полную стернотомию. Интра- и послеоперационные осложнения (фибрилляция предсердий, нарушения кровообращения головного мозга, инфекция послеоперационных ран) статистически значимо не различались между двумя группами. Длительность госпитализации была меньше в группе правой передней торакотомии. Также снижалась длительность послеоперационной искусственной вентиляции легких в группе правой передней торакотомии. Такие преимущества мини-стернотомии, как уменьшение количества рестернотомий и конверсий, объяснялись большей трудоемкостью то-ракотомного доступа в хирургии аортального клапана [25]. В метаанализе, включившем более 10 тыс. пациентов, С. Chang и соавт. продемонстрировали схожие результаты [26].
Правосторонняя переднебоковая мини-торакотомия является модификацией передней мини-торакотомии (рис. 4B). Данный доступ разработали в Японии в связи с тем, что хирурги сталкивались
Рис. 4. Мини-торакотомии: правосторонняя передняя мини-торакотомия (A); правосторонняя переднебоковая мини-торакотомия (B); правосторонняя инфрааксил-лярная мини-торакотомия (C)
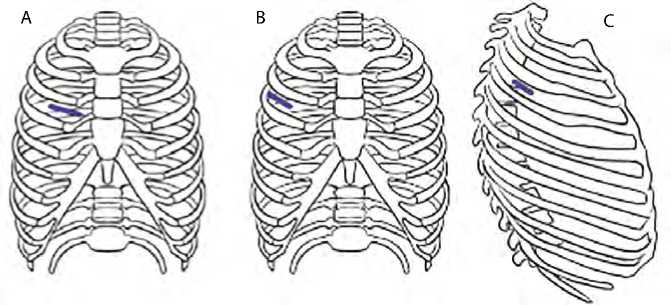
со сниженной визуализацией корня аорты, а в частности устья правой коронарной артерии при кардиоплегии. Смещение доступа латеральнее на переднебоковую поверхность позволило улучшить визуализацию корня аорты.
При сравнении стандартной передней (n = 59) и переднебоковой торакотомии (n = 21) статистически значимой разницы в длительности оперативного вмешательства не получили (247 ± 47 и 264 ± 31 мин соответственно). Длительность ИК (137 ± 32 и 155 ± 23 мин) и ИМ (93 ± 22 и 105 ± 15 мин) была достоверно больше во второй группе. Продолжительность искусственной вентиляции легких, объем перелитых компонентов крови, длительность госпитализации и эффективность оперативных вмешательств статистически значимо не различались между двумя группами. Несмотря на то что в обеих когортах осложнений, ассоциированных с правой внутренней грудной артерией, не отметили, авторы описали, что риск данного осложнения при передней торакотомии выше, чем при переднебоковом доступе [27].
S. Semsroth и соавт. сравнили переднебоковую мини-торакотомию (n = 167), J-образную мини-стернотомию (n = 315) и полную стернотомию (n = 328) и продемонстрировали, что единственным мини-инвазивным доступом в хирургии АК, который можно использовать в рутинной практике, являлась J-образная мини-стернотомия. В группе переднебокового доступа отмечали статистически значимое увеличение конверсий на срединную стернотомию — 17 (14,4 %), необходимости повторного зажима аорты — 12 (10,2 %), длительности ИК — 94 (43–231) мин и ИМ — 141 (77–456) мин, а также количества осложнений — 17 (14,4 %) [28].
Правостороннюю инфрааксиллярную мини-торакотомию (рис. 4C) чаще используют в детской хирургии, так как она имеет косметические преимущества: при развитии ребенка не происходит де- формации или асимметричного развития грудной клетки. Вертикальный разрез выполняют по передней подмышечной линии. Доступ в подмышечной области не приводит к деформации грудных мышц, а также расположен достаточно далеко от грудины и правой внутренней грудной артерии, что позволяет избегать осложнений, ассоциированных с ними. Также преимуществами данного доступа являются угол наклона АК, который близок к визуальной оси хирурга, доступ располагается вне прохождения крупных мышц, а межреберья довольно податливы при расширении операционного поля. Недостатком этого метода является глубокое расположение корня аорты: в среднем 18–20 см у мужчин и 16–18 см у женщин, что в ряде случаев требует использования эндоскопических инструментов [29].
Q. Wang и соавт. опубликовали опыт применения данного доступа у пациентов с изолированными пороками аортального и митрального клапанов, также сочетанными клапанными поражениями, коррекциями межпредсердных и межжелудочковых перегородок. Длительность ИК составила 127 ± 60 (49–193) мин, время ИМ 93 ± 25 (27–151) мин, количество отделяемого по дренажам 161,0 ± 87,9 (0–384) мл. Ни в одном случае не потребовалась конверсия на полную стернотомию. Отдаленные результаты сопоставимы с вмешательствами, выполненными из полной стернотомии [30].
M. Yamazaki и соавт. обеспечили более близкое расположение аорты и АК к хирургу путем подтягивания перикарда через дополнительные отверстия для ниток. Такая методика, названная Stonehenge technique, позволила вывести корень аорты на достаточную дистанцию, чтобы обеспечить адекватную визуализацию и возможность манипуляции стандартными инструментами [31]. При Stonehenge technique длительность ИК (125,5 ± 47,9 и 96,0 ± 14,0 мин) и ИМ (163,8 ± 55,9 и 140,0 ± 16,8 мин) была достоверно меньше, чем при аксиллярной торакотомии [32].
Мини-инвазивная аутоперикардиальная неокуспидизация
До недавнего времени неокуспидизацию, в отличие от протезирования АК, выполняли исключительно доступом через полную срединную стернотомию из-за трудоемкости забора перикарда 7 × 8 см из мини-доступа. В связи с этим к аутоперикардиальной неокуспидизации АК не применялись преимущества минимально инвазивной хирургии сердца.
В мировой литературе всего две публикации посвящены минимально инвазивной аутоперикардиальной хирургии аортального клапана. Зачастую эту процедуру проводят только через J-образную мини-стернотомию. Выполнить забор перикарда из мини-доступа возможно, но это сопряжено с рисками ятрогенного повреждения камер и сосудов сердца, диафрагмального нерва, а главное — недостаточного размера перикарда. Такие особенности зависят от размеров сердца и глубины его расположения, состояния перикарда, анатомических особенностей строения грудины. Первой работой, посвященной минимально инвазивной аутоперикардиальной неокуспидизации, являлось ретроспективное исследование Е.В. Россейкина и соавт., в котором сравнили клинические результаты операции Озаки с использованием мини-доступа (группа Ozaki Mini, n = 30) и полной стернотомии (группа Ozaki Full, n = 112). После исключения несопоставимости групп сформировали 2 когорты по 30 пациентов. Ограничением этого исследования являлось отсутствие подробного описания хирургической техники забора перикарда из мини-доступа. Вместе с тем авторы продемонстрировали сопоставимые с классической стернотомией результаты в отношении длительности искусственной вентиляции легких и 30-дневной летальности, а также меньший суммарный объем кровопотери в группе мини-доступа [33]. Уменьшить риск забора аутологичного перикарда из минимально инвазивного доступа позволяет использование торакоскопической методики. В 2018 г. D.H. Nguyen и соавт. представили ее в виде видеоотчета серии клинических случаев на 5 больных [34]. Торакоскопический забор перикарда в условиях периферического искусственного кровообращения обеспечивает лучшую визуализацию и контролируемый размер лоскута.
Полностью эндоскопическое протезирование
Создание бесшовных протезов позволило выполнять полностью эндоскопическую импланта- цию АК. В 2014 г. M. Vola и соавт. опубликовали первый в мире случай полностью эндоскопического протезирования АК. Вмешательство осуществляли при однолегочной вентиляции через 5 троакаров при периферической канюляции и эндоваскулярном пережатии аорты. Авторы использовали бесшовный биопротез, который имплантировали в позицию АК через порт 20 мм. Помимо преимуществ минимально инвазивного доступа, длительность ишемии миокарда была меньше в связи с особенностями имплантации бесшовного протеза [35].
Из-за технической трудоемкости полностью эндоскопическое протезирование АК — нераспространенная процедура, существуют лишь единичные публикации по этой теме. В 2019 г. M. Tokoro и соавт. сравнили 47 пациентов, которым выполнили протезирование АК полностью эндоскопически, и 157 больных — доступом из правой подмышечной области. Техника заключалась в выполнении правосторонней переднебоковой торакотомии 4 см и установке порта для троакара 5,5 мм в 3-е межреберье, 3-й порт установили как при торакоскопической коррекции митрального порока. Через торакотомию в грудную клетку провели 3D-камеру, специализированный аортальный зажим, а также непосредственно АК. В группе полностью эндоскопического протезирования статистически значимо уменьшалась длительность операции. Время ИК и ИМ статистически не различалось. Длительность пребывания в стационаре в послеоперационном периоде значительно меньше в группе полностью эндоскопического протезирования. Косметический эффект не различался между двумя группами. Отсутствие необходимости в использовании реберного расширителя в группе полностью эндоскопического протезирования привело к снижению интенсивности болевого синдрома. Также авторы описали преимущества использования 3D-камеры над доступом с ограниченным операционным полем, что позволило лучше визуализировать АК и провести тщательный гемостаз источников кровотечения [36].
Таким образом, из мини-доступа возможно выполнить практически весь спектр кардиохирургических вмешательств начиная с шунтирования и заканчивая операциями на дуге аорты. По безопасности и качеству операции с использованием минимально инвазивного подхода в хирургии аортального клапана сопоставимы с полной срединной стернотомией. Развитие технической составляющей и внедрение торакоскопических методик в кардиохирургию расширяют спектр операций, которые проводят минимально инвазивно.
С помощью различных мини-доступов возможно выполнить вмешательство на аортальном клапане, однако самым распространенным является J-образная мини-стернотомия. В то же время в некоторых центрах приоритет отдают другим доступам, демонстрирующим схожие результаты.
Однако необходимо понимать, улучшают ли минимально инвазивные подходы результаты лечения. Европейские и американские сообщества кардиото-ракальных хирургов поддерживают потенциальные преимущества минимально инвазивной хирургии, однако не дают конкретных рекомендаций из-за отсутствия полноценной доказательной базы. К 2019 г. в литературе представили более 14 тыс. мини-инвазивных протезирований аортального клапана [37]. Однако при проведении метаанализов исследователи столкнулись с проблемой гетерогенности групп больных, различий в хирургической технике и, самое главное, отсутствия рандомизации при сравнении мини-доступа и полной стернотомии [37]. На наш взгляд, преимущества минимально инвазивной кардиохирургии не вызывают сомнений, но требуют более полноценной статистически достоверной базы данных для формирования полноценных показаний и противопоказаний при выборе доступа.
Заключение
Отбор пациентов для минимально инвазивных аортальных вмешательств должен учитывать как анатомические особенности средостения и корня аорты, так и коморбидность пациента и сопутствующую кардиальную патологию. Минимально инвазивные доступы в хирургии аортального клапана включают как торакотомии и частичные стернотомии, так и методики эндоскопической хирургии. Особый интерес представляет минимально инвазивная неокуспидизация клапана аутологичным перикардом. Частичные стернотомии являются наиболее рутинно используемыми доступами в хирургии АК, а результаты позволяют провести крупные метаанализы для сравнения эффективности и безопасности с классическим стернотомным доступом. Минимально инвазивная аутоперикардиальная неокуспидизация и эндоскопические вмешательства на АК требуют дальнейшего накопления хирургического опыта и клинического материала.
Список литературы Современные подходы к минимально инвазивной хирургии аортального клапана
- Kirmani B.H., Jones S.G., Malaisrie S.C., Chung D.A., Williams RJ. Limited versus full sternotomy for aortic valve replacement. Cochrane Database Syst Rev. 2017;4(4):CD011793. PMID: 28394022; PMCID: PMC6478148. https://doi.org/10.1002/14651858.CD011793.pub2
- Phan K., Xie A., Di Eusanio M., Yan T.D. A meta-analysis of minimally invasive versus conventional sternotomy for aortic valve replacement. Ann Thorac Surg. 2014;98(4):1499-1511. PMID: 25064516. https://doi.orq/10.1016/i.athoracsur.2014.05.060
- Doenst T., Diab M., Sponholz C., Bauer M., Färber G. The opportunities and limitations of minimally invasive cardiac surgery. Dtsch Arztebl Int. 2017;114(46):777-784. PMID: 29229038; PMCID: PMC5730700. https://doi.org/10.3238/ arztebl.2017.0777
- Li A.E., Fishman E.K. Evaluation of complications after sternotomy using single- and multidetector CT with three-dimensional volume rendering. AJR Am J Roentgenol. 2003;181(4):1065-1070. PMID: 14500232. https://doi. org/10.2214/air.181.4.1811065
- Cecrle M., Cerny D., Sedlackova E., Mikova B., Dudkova V., Drncova E., Pokusova M., Skalsky I., Tamasova J., Halacova M. Vitamin D for prevention of sternotomy healing complications: REINFORCE-D trial. Trials. 2020;21 (1 ):1018. PMID: 33308291; PMCID: PMC7731517. https://doi.org/10.1186/ s13063-020-04920-z
- Heilmann C., Stahl R., Schneider C., Sukhodolya T., Siepe M., Olschewski M., Beyersdorf F. Wound complications after median sternotomy: a single-centre study. Interact Cardiovasc Thorac Surg. 2013;16(5):643-648. PMID: 23355648; PMCID: PMC3630417. https://doi.org/10.1093/icvts/ivs554
- Doenst T., Lamelas J. Do we have enough evidence for minimally-invasive cardiac surgery? A critical review of scientific and non-scientific information. J Cardiovasc Surg (Torino). 2017;58(4):613-623. PMID: 28580776. https://doi. org/10.23736/S0021-9509.16.09446-5
- Lamelas J., Sarria A., Santana O., Pineda A.M., Lamas G.A. Outcomes of minimally invasive valve surgery versus median sternotomy in patients age 75 years or greater. Ann Thorac Surg. 2011 ;91 (1 ):79-84. PMID: 21172490. https://doi. org/10.1016/i.athoracsur.2010.09.019
- Nguyen T.C., Thourani V.H., Pham J.Q., Zhao Y., Terwelp M.D., Balan P., Ocazionez D., Loghin C., Smalling R.W., Estrera A.L., Lamelas J. Traditional sternotomy versus minimally invasive aortic valve replacement in patients stratified by eiection fraction. Innovations (Phila). 2017;12(1):33-40. PMID: 28099179. https://doi.org/10.1097/IMI.0000000000000338
- Rao P.N., Kumar A.S. Aortic valve replacement through right thoracotomy. Tex Heart Inst J. 1993;20(4):307-308. PMID: 8298332; PMCID: PMC325118.
- Cohn L.H., Adams D.H., Couper G.S., Bichell D.P., Rosborough D.M., Sears S.P., Aranki S.F. Minimally invasive cardiac valve surgery improves patient satisfaction while reducing costs of cardiac valve replacement and repair. Ann Surg. 1997;226(4):421-426; discussion 427428. PMID: 9351710; PMCID: PMC1191053. https://doi. org/10.1097/00000658-199710000-00003
- Svensson L.G. Minimal-access "J" or "j" sternotomy for valvular, aortic, and coronary operations or reoperations. Ann Thorac Surg. 1997;64(5):1501-1503. PMID: 9386741. https:// doi.org/10.1016/S0003-4975(97)00927-2
- Mikus E., Calvi S., Campo G., Pavasini R., Paris M., Raviola E., Panzavolta M., Tripodi A., Ferrari R., Del Giglio M. Full sternotomy, hemisternotomy, and minithoracotomy for aortic valve surgery: is there a difference? Ann Thorac Surg. 2018;106(6):1782-1788. PMID: 30179623. https://doi. org/10.1016/i.athoracsur.2018.07.019
- Wu Y., Jiang W., Li D., Chen L., Ye W., Ren C., Xiao C. Surgery of ascending aorta with complex procedures for aortic dissection through upper mini-sternotomy versus conventional sternotomy. J Cardiothorac Surg. 2020;15(1):57. PMID: 32264907; PMCID: PMC7140324. https://doi.org/10.1186/ s13019-020-01095-1
- Risteski P., Monsefi N., Miskovic A., Josic T., Bala S., Salem R., Zierer A., Moritz A. Triple valve surgery through a less invasive approach: early and mid-term results. Interact Cardiovasc Thorac Surg. 2017;24(5):677-682. PMID: 28453792. https://doi. org/10.1093/icvts/ivw430
- Alsoufi B., Rao V., Borger M.A., Maganti M., Armstrong S., Feindel C.M., Scully H.E., David T.E. Short- and long-term results of triple valve surgery in the modern era. Ann Thorac Surg. 2006;81(6):2172-2177; discussion 2177-2178. PMID: 16731149. https://doi.org/10.1016/i.athoracsur.2006.01.072
- Akay T.H., Gultekin B., Ozkan S., Aslim E., Saritas B., Sezgin A., Aslamaci S. Triple-valve procedures: impact of risk factors on midterm in a rheumatic population. Ann Thorac Surg. 2006;82(5):1729-1734. PMID: 17062238. https://doi. org/10.1016/i.athoracsur.2006.05.078
- Kasegawa H., Shimokawa T., Matsushita Y., Kamata S., Ida T., Kawase M. Right-sided partial sternotomy for minimally invasive valve operation: "open door method". Ann Thorac Surg. 1998;65(2):569-570. PMID: 9485278. https://doi. org/10.1016/s0003-4975(97)01332-5
- Chang Y.S., Lin P.J., Chang C.H., Chu J.J., Tan P.P. "I" ministernotomy for aortic valve replacement. Ann Thorac Surg. 1999;68(1):40-45. PMID: 10421112. https://doi.org/10.1016/ s0003-4975(99)00314-8
- Doty D.B., DiRusso G.B., Doty J.R. Full-spectrum cardiac surgery through a minimal incision: mini-sternotomy (lower half) technique. Ann Thorac Surg. 1998;65(2):573-577. PMID: 9485280. https://doi.org/10.1016/s0003-4975(97)01368-4
- Fenton J.R., Doty J.R. Minimally invasive aortic valve replacement surgery through lower half sternotomy. J Thorac Dis. 2013;5(Suppl 6):S658-S661. PMID: 24251024; PMCID: PMC3831833. https://doi.org/10.3978/Ussn.2072-1439.2013.09.22
- Hsiao C.-Y., Ou-Yang C.-P., Huang C.-H. Less invasive cardiac surgery via partial sternotomy. J Chin Med Assoc. 2012;75(12):630-634. PMID: 23245478. https://doi. org/10.1016/i.icma.2012.09.002
- Karimov J.H., Santarelli F., Murzi M., Glauber M. A technique of an upper V-type ministernotomy in the second intercostal space. Interact Cardiovasc Thorac Surg. 2009;9(6):1021-1022. PMID: 19770135. https://doi.org/10.1510/icvts.2009.215699
- Burdett C.L., Lage I.B., Goodwin A.T., White R.W., Khan K.J., Owens W.A., Kendall S.W.H., Ferguson J.I., Dunning J., Akowuah E.F. Manubrium-limited sternotomy decreases blood loss after aortic valve replacement surgery. Interact Cardiovasc Thorac Surg. 2014;19(4):605-610. PMID: 24944150. https://doi.org/10.1093/icvts/ivu196
- Salmasi M.Y., Hamilton H., Rahman I., Chien L., Rival P., Benedetto U., Young C., Caputo M., Angelini G.D., Vohra H.A. Mini-sternotomy vs right anterior thoracotomy for aortic valve replacement. J Card Surg. 2020;35(7):1570-1582. PMID: 32652784. https://doi.org/10.1111/iocs.14607
- Chang C., Raza S., Altarabsheh S.E., Delozier S., Sharma U.M., Zia A., Khan M.S., Neudecker M., Markowitz A.H., Sabik 3rd J.F., Deo S.V. Minimally invasive approaches to surgical aortic valve replacement: a meta-analysis. Ann Thorac Surg. 2018; 106(6): 1881 -1889. PMID: 30189193. https://doi. org/10.1016/i.athoracsur.2018.07.018
- Totsugawa T., Kuinose M., Hiraoka A., Yoshitaka H., Tamura K., Sakaguchi T. Anterolateral approach for minimally invasive aortic valve replacement. Gen Thorac Cardiovasc Surg. 2014;62(5):290-295. PMID: 24293273. https://doi.org/10.1007/ s11748-013-0352-z
- Semsroth S., Matteucci Gothe R., Raith Y.R., de Brabandere K., Hanspeter E., Kilo J., Kofler M., Muller L., Ruttman-Ulmer E., Grimm M. Comparison of two minimally invasive techniques and median sternotomy in aortic valve replacement. Ann Thorac Surg. 2017;104(3):877-883. PMID: 28433220. https:// doi.org/10.1016/i.athoracsur.2017.01.095
- Ito T., Maekawa A., Hoshino S., Hayashi Y. Right infraaxillary thoracotomy for minimally invasive aortic valve replacement. Ann Thorac Surg. 2013;96(2):715-717. PMID: 23910127. https:// doi.org/10.1016/i.athoracsur.2013.03.003
- Wang Q., Ye J.-X., Ge M., Wang D.-J. Early- and long-term outcomes of cardiovascular surgery via minimal right vertical infra-axillary thoracotomy: a 15-year study of 1,126 patients. SciRep. 2018;8(1):4376. PMID: 29531314; PMCID: PMC5847571. https://doi.org/10.1038/s41598-018-22824-6
- Yamazaki M., Yoshitake A., Takahashi T., Ito T., Kimura N., Hirano A., Iida Y., Takanashi S., Shimizu H. Stonehenge technique is associated with faster aortic clamp time in group of minimally invasive aortic valve replacement via right infra-axillary thoracotomy. Gen Thorac Cardiovasc Surg. 2018;66( 12):700-706. PMID: 30117124. https://doi. org/10.1007/s11748-018-0987-x
- Ueno G., Ohno N. Aortic valve approaches in the era of minimally invasive cardiac surgery. Surg Today. 2020;50(8):815-820. PMID: 31342159. https://doi.org/10.1007/s00595-019-01848-z
- Россейкин Е.В., Кобзев Е.Е., Базылев В.В. Операция OZAKI из мини-доступа. Ангиология и сосудистая хирургия. 2019;25(3):142-148. https://doi.org/10.33529/ANGI02019319 Rosseikin E.V., Kobzev E.E., Bazylev V.V. Minimally invasive Ozaki technique. Angiology and Vascular Surgery. 2019;25(3):142-148. https://doi.org/10.33529/ANGI02019319
- Nguyen D.H., Vo A.T., Le K.M., Vu T.T., Nguyen T.T., Vu T.T., Pham C.V.T., Truong B.Q. Minimally invasive Ozaki procedure in aortic valve disease: the preliminary results. Innovations (Phila). 2018;13(5):332-337. PMID: 30394956. https://doi. org/10.1097/IMI.0000000000000556
- Vola M., Fuzellier J.F., Chavent B., Duprey A. First human totally endoscopic aortic valve replacement: an early report. J Thorac Cardiovasc Surg. 2014;147(3):1091-1093. PMID: 24290705. https://doi.org/10.1016/_i.itcvs.2013.10.010
- Tokoro M., Sawaki S., Ozeki T., Orii M., Usui A., Ito T. Totally endoscopic aortic valve replacement via an anterolateral approach using a standard prosthesis. Interact Cardiovasc Thorac Surg. 2020;30(3):424-430. PMID: 31800039. https://doi. org/10.1093/icvts/ivz287
- Jahangiri M., Hussain A., Akowuah E. Minimally invasive surgical aortic valve replacement. Heart. 2019;105(Suppl 2):s10-s15. PMID: 30846519. https://doi.org/10.1136/ heartinl-2018-313512


