Современные взгляды на проблему удаления почечного трансплантата
Автор: Лубенников А.Е., Трушкин Р.Н., Артюхина Л.Ю.
Журнал: Московский хирургический журнал @mossj
Рубрика: Обзоры литературы
Статья в выпуске: 4 (38), 2014 года.
Бесплатный доступ
Увеличение темпов трансплантации почки неизбежно влечет за собой рост количества реципиентов с нефункционирующим трансплантатом, которым возобновляется гемодиализ (ГД). У данной категории больных высокие показатели смертности и заболеваемости. Считается, что транс- плантатэктомия (ТЭ) показана либо в раннем периоде после пересадки, либо при наличии симптомов отторжения или пиелонефрита в поздние сроки. Мы провели обзор мировой литературы с целью найти ответы на следующие вопросы: влияет ли ТЭ на показатели смертности и заболеваемости, а также на результат ретрансплантации; насколько целесообразно продолжение иммуносупрессивной терапии при оставлении почки на месте; что делать с нефункционирующим трансплантатом при отсутствии симптомов; каковы показания, эффективность и безопасность эмболизации почечного трансплантата?
Трансплантатэктомия, хроническое отторжение трансплантата, иммуносупрессия, выживаемость пациентов, тест-антигеновые антитела, ретрансплантация, эмболизация нефункционирующего трансплантата
Короткий адрес: https://sciup.org/142211174
IDR: 142211174 | УДК: 616-089.843;
Текст обзорной статьи Современные взгляды на проблему удаления почечного трансплантата
Около 10% пациентов в течение первого года после пересадки почки возвращаются к гемодиализу (ГД) из-за потери функции трансплантата, в последующие годы количество таких больных составляет 3-5% [1]. Учитывая растущие темпы трансплантации почки, количество реципиентов, нуждающихся в возобновлении заместительной почечной терапии, будет увеличиваться.
Актуальность проблемы заключается в том, что уровень смертности у больных после потери функции трансплантата в 3-4 раза выше по сравнении с пациентами в листе ожидания [2]. Ojo A. и соавт. провели ретроспективное исследование летальности за 1985-1995 года у 19208 больных с трансплантатом, утратившим свою функцию. Общая смертность составила 34,5% (!) и была выше у пациентов с сахарным диабетом [3]. Инфекционные и сердечно-сосудистые осложнения являются ведущими причинами фатального исхода. Сепсис у больных с нефункционирующим транс- плантатом развивается в 5-7 раз чаще, чем у пациентов на ГД без трансплантата, при этом основная заболеваемость манифестирует в первые 3-6 месяца после возобновления ГД. Факторами риска являются: продолжение иммуносупрессивной терапии, наличие фистулы, возраст более 60 лет, сахарный диабет, сердечная недостаточность, заболевание периферических сосудов [4].
Наибольшее количество трансплантатэктомий (ТЭ) выполняется в ранние сроки после пересадки. В публикациях существуют противоречивые мнения о том, какой период после трансплантации считать ранним. В одних работах указывается срок 2 мес. [5], в других - 6 мес. [6], в третьих - 12 мес. [1, 7]. Согласно британским статистическим данным, ТЭ в течение первых 3 мес. после пересадки была произведена у 41% реципиента, в период от 3 до 12 мес. - у 23%, с 12 по 24 мес. - у 9% и только у 4% - спустя 2 года. Zerouali F. и соавт. сообщают о том, что в течение длитель- ного времени в Университетском медицинском центре г. Неймегена (Нидерланды) существовала практика консервативного лечения детей, если трансплантат утратил свою функцию через 1 мес. после пересадки. Ретроспективный анализ, включающий 63 реципиента с нефункционирующей почкой, показал, что ТЭ в течение первого месяца выполнена у 100% реципиентов, в период от 1 мес. до 1 года - у 86% и после 1 года - в 68% случаев. Эти данные заставили авторов пересмотреть хирургическую тактику в отношении нефункционирующих трансплантатов [8]. Внедрение в практику эффективных препаратов, подавляющих иммунный ответ, позволило снизило количество ТЭ за счет уменьшения количества и выраженности кризов отторжения, но на частоту ТЭ у больных после безвозвратной потери функции трансплантата это не повлияло. Так, Roberts C.S. и соавт. констатируют: до 1984 года было выполнено 70 ТЭ у 280 реципиентов, после 1984 года, с началом активного применения циклоспорина, ТЭ подвергся 61 пациент из 486 [9]. По данным различных источников, ТЭ выполняется у 4,5-84,4% реципиентов [1, 5, 7, 10, 11-13]. Такой значительный разброс обусловлен отличающимися подходами и показаниями к ТЭ, одни придерживаются тактики раннего, превентивного оперативного вмешательства, другие - выполняют ТЭ только в крайних случаях.
Наиболее частыми, общепринятыми, показаниями для ТЭ в раннем периоде (6-12 мес.) являются: сосудистые осложнения (венозный тромбоз, псевдоаневризма артериального анастомоза, окклюзия почечной артерии), криз отторжения, резистентный к медикаментозному лечению, инфекционные осложнения (сепсис, острый пиелонефрит трансплантата), первичное отсутствие функции, разрыв трансплантата. Как правило, ТЭ в раннем периоде выполняется по экстренным показаниям.
Традиционными основаниями для удаления нефункционирующего трансплантата в позднем периоде являются: лихорадка, боль в области трансплантата, увеличение и напряженность трансплантата, анемия, резистентная к терапии, часто возобновляющаяся макрогематурия, рецидивирующая мочевая инфекция, сепсис, нефропатия, обусловленная полиомавирусом, необходимость в освобождение места для последующей пересадки почки, лимфопролиферативное заболевание с вовлечением трансплантата, жизнеугрожающее кровотечение после биопсии, опухоль трансплантата, гнойно-деструктивные формы острого пиелонефрита, выраженная протеинурия.
Если в отношении пациентов с клиническими проявлениями сформировались лечебные стратегии, то вопрос о том, что делать с неработающим трансплантатом у бессимптомного больного, на сегодняшний день остается открытым. Одни авторы придерживаются мнения, что оперативное вмешательство не должно быть рутинным [14, 15], другие утверждают, что выполнение ТЭ у отдельных па- циентов (с факторами риска) в «холодном» периоде сопровождается меньшим количеством осложнений и улучшает показатели выживаемости [12, 16, 17]. Причем, последняя точка зрения в последнее время находит все больше и больше сторонников. Ayus J.C. и соавт. проанализировали данные по трансплантации почки в США с 1984 по 2004 г. За период наблюдения 10951 реципиент вернулся на ГД. ТЭ выполнена у 3451 больного, смертность у них была ниже на 32% [12]. Ранее считалось, что оставленный, никак не проявляющий себя почечный трансплантат оказывает благоприятное воздействие на организм за счет резидуальной функции (производство эритропоэтина, в некоторых случаях остаточный диурез, участие в обмене кальция и др.) [18], однако в последующих исследованиях положительное влияние не подтвердилось [17, 19].
Иммуносупрессивная терапия в низких дозах часто назначается реципиентам, вернувшихся на ГД через 612 мес. после трансплантации. В некоторых работах показано, что такой подход позволяет отсрочить или вовсе избежать ТЭ [20]. В ряде других исследованиях отмечено, что при этом повышается вероятность инфекционных и сердечно-сосудистых осложнений, ведущих к летальному исходу, создаются неблагоприятные условия для оперативного вмешательства в случае его необходимости. Поэтому некоторые авторы считают тактику продолжения приема иммунодепресантов после возобновления заместительной почечной терапии не эффективной и не безопасной [21, 22, 23]. У 30-40% больных после отмены иммуносупрессии развивается синдром хронического отторжения (graft intolerance syndrome – GIS), проявляющийся лихорадкой, гриппоподобным симптомом, гематурией, болью в области трансплантата и увеличением последнего при отсутствии признаков системной инфекции. Большинство эпизодов диагностируются в течение первого года [24]. В ряде случаев, необходимо исключить симптом Адиссона. Предикторами, указывающими на высокую вероятность GIS, являются два и более криза отторжения и прием циклоспорина в анамнезе. Madore F. и соавт. проанализировали судьбу 41 реципиента, критериями включения были: 6 и более месяцев после пересадки, начало ГД, прекращение иммуносупрессии. При наблюдении в среднем 17,8 мес. (от 6 мес. до 6,1 года) ТЭ была выполнена у 83% больных с двумя и более кризами отторжения и у 30% - без острой реакции отторжения в прошлом, у 62% - ранее принимавших циклоспорин, и у 27,3% пациентов, не леченных циклоспорином. Однако при многофакторном анализе только количество кризов отторжения явилось статистически достоверным фактором, влияющим на прогноз [25]. В другом ретроспективном исследовании констатируется, что ТЭ была необходима у 4% реципиентов, ранее принимавших азатиоприн и преднизолон, и у 21% - получавших циклоспорин [26].
У многих пациентов с нефункционирующем трансплантатом на ГД имеются признаки хронического воспалительного процесса. В лабораторных показателях выявляется гипоальбуминемия, анемия, устойчивая к терапии эритропоэтином, повышение ферритина, С-реактивного белка (СРБ), СОЭ, интерлейкина-6, причем эти изменения присутствуют и у бессимптомных больных, но в меньшей степени. В свою очередь, высокие показатели СРБ, интерлейкина-6 ассоциированы с увеличением смертности. После ТЭ отмечается улучшение этих параметров, в то же время у многих пациентов с оставленным трансплантатом на фоне гемодиализа (ГД) воспалительный процесс не редуцируется и в последствии трансформируются в клинические симптомы (лихорадка, боль в области трансплантата, потеря веса, отсутствие аппетита и др.), что требует выполнения ТЭ [17, 27]. По данным Langone A.J. и соавт., ТЭ в итоге произведена 273 реципиентам из 345 (79%) [15].
Таким образом, бессимптомные реципиенты с поздней потерей функции трансплантата, у которых имеются лабораторные изменения, характерные для системного воспалительного процесса, в анамнезе два и более криза отторжения на фоне лечения циклоспорином, продолжающие прием иммуносупрессивной терапии в низких дозах, попадают в группу риска с высокой вероятностью ТЭ. У данной категории больных целесообразно выполнение превентивного оперативного вмешательства, что позволяет снизить количество осложнений и улучшить выживаемость [16, 17].
ТЭ может выполняться по экстракапсулярному или субкапсулярному варианту. Экстракапсулярная методика более сложная и применяется, как правило, в раннем периоде после трансплантации. Преимуществами являются отсутствии полости после нефрэктомии и грубых рубцовых изменений в области подвздошных сосудов, что создает благоприятные условия для ретрансплантации. Отрицательные моменты заключаются в большей продолжительности оперативного пособия из-за необходимости тщательного гемостаза [28]. Основные недостатки субкапсулярной ТЭ -наличие полости, образованной капсулой, и грубые рубцовые изменения в забрюшинном пространстве. Ghinolfi D. и соавт. у 9 пациентов использовали сближение стенок полости, накладывая отдельные узловые швы викрилом на оставшуюся капсулу, каких-либо осложнений авторы не отметили ни в одном случае [29]. Vavallo A. и соавт. при сравнении результатов экстракапсулярной ТЭ, выполненной у 57 пациентов, и субкапсулярной ТЭ - у 32 больных, не нашли значимых отличий по критериям: кровопотеря, необходимость гемотрансфузии, количество осложнений, среднее время операции. Единственное отличие заключалось в том, что в случае субкапсулярной ТЭ длительность послеоперационного пребывания в стационаре была меньше [30].
ТЭ является процедурой с высокой заболеваемостью (17-60%) и смертностью (1,5-14%). До широкого использо- вания циклоспорина, т.е. до 1984 года, летальность составляла 7,3-38,7% [5, 8, 10-12, 16, 31-34]. Неблагоприятные исходы в основном обусловлены септическими осложнениями (сепсис, нагноение раны) и кровотечением. Реже наблюдаются повреждение кишки, мочевой свищ, травма запирательного нерва или бокового кожного нерва бедра. На результаты ТЭ оказывают влияние сроки выполнения вмешательства (в раннем или позднем периоде после трансплантации), наличие/отсутствие клинической картины, проводилась иммуносупрессивная терапия на момент операции или нет, время, прошедшее после возвращения больного на ГД [5]. Меньшее количество осложнений отмечается у пациентов в поздние сроки после пересадки, при отсутствии симптомов отторжения и признаков сепсиса [5, 17]. Наиболее крупное, ретроспективное исследование, в котором приняли участие 19707 реципиентов с нефункционирующим трансплантатом, было опубликовано в 2007 г. Johnston O. и соавт. Среди 3707 больных с ранней потерей функции почки (до 12 мес.) ТЭ была выполнена в 56% случаев и была связана с увеличением риска летального исхода. Напротив, среди 15400 пациентов с поздней дисфункцией (больше 12 мес.), почка удалена у 27%, при этом риск смерти у этих больных был ниже [1]. Сосудистые компликации (дефект подвздошной артерии, псевдоаневризма) после ТЭ развиваются у 0,9-14% больных и обуславливают плохой прогноз. Наличие сепсиса, гнойного пиелонефрита, артериита являются ключевыми факторами риска [35]. Eng M.M. и соавт. при повреждении наружной подвздошной артерии в ходе выполнения ТЭ рекомендуют воздержаться от реконструктивных операций и сразу прибегнуть к перевязке сосуда. Выполнив лигирование наружной подвздошной артерии у 7 больных, авторы ни в одном случаи не отметили выраженной ишемии нижней конечности [7]. Blohmé I. и Brynger H. из Университета г. Гетеборга в экстренных ситуациях, а именно при развитии массивного кровотечения на фоне инфицированной раны, так же отдают предпочтение перевязке общей или наружной подвздошной артерии. В своей работе, основанной на 13 больных, авторы не отметили летальных исходов или потери конечности. В раннем послеоперационном периоде признаки артериальной недостаточности присутствовали у всех пациентов, у большинства из них они разрешились в течение 3-4 нед, в трех случаях сохранялась перемежающая хромота с положительной динамикой. Через 4-10 лет после вмешательства 6 пациентов оставались живыми (летальный исход у других больных был обусловлен сердечно-сосудистыми заболеваниями и уремией) и вернулись к привычному образу жизни, однако при физической нагрузки периодически испытывали боль в конечности [36]. Развитие псевдоаневризмы после ТЭ достаточно редкое осложнение. Эндоваскулярные методы лечения с имплантацией внутрисосудистого стента являются наиболее эффективными и безопасными [37-39].
С целью снижения количества послеоперационных осложнения Zomorrodi A. и соавт. применили циторедуктивную методику субкапсулярной ТЭ. Суть операции заключается в том, что паренхима трансплантата удаляется слой за слоем до ножки, которая затем перевязывается, после нефрэктомии авторы обрабатывали полость бета-дином, капсулу и мочеточник оставляли не тронутыми, в последующие 2 мес. пациенты получали иммуносупрессивную терапию. Выполнив таким образом 25 оперативных вмешательств, авторы не отметили серьезных компликаций [31]. Улучшить результаты ТЭ позволяет предварительное выполнение эмболизации почечной артерии. По данным Neschis D.G. и соавт., кровопотеря уменьшается вдвое, длительность вмешательства на 20-30 мин., продолжительность нахождения в стационаре была ниже в 4 раза [40]. При выполнении ТЭ в связи с наличием псевдоаневризмы в области анастомоза предварительное стентирование подвздошной артерии в большинстве случаев позволяет избежать лигирования и резекции сосуда [41].
Альтернативой ТЭ является эмболизация почечного трансплантата, которая стала применяться у реципиентов с начала 90-х годов [42]. Методика привлекательна тем, что является более безопасной, чем открытое вмешательство, позволяет в значительной степени сократить койко-день, однако имеются свои ограничения. Острый пиелонефрит, острый криз отторжения, опухоль трансплантата - противопоказания для интервенционного лечения. Анализ нескольких современных работ, в общей сложности включающих 156 больных, продемонстрировал, что основным показанием для выполнения эмболизации являлся синдром хронического отторжения (GIS). Средняя эффективность (оцененная как избавление пациента от GIS-синдрома) составляла 84% при сроке наблюдения до 7 лет. Постэмболизационный симптом, обусловленный инфарктом почечного трансплантата (лихорадка, боль в области трансплантата, гематурия), развивает в среднем в 57,8% случаев, но адекватно купируется консервативно в течение первых 2-3 суток (макс. до 5 дней) [43-47]. В среднем у 16% больных после эмболизации сохраняются проявления GIS-синдрома, что требует выполнения открытого оперативного вмешательства. Предшествующая эмболизация не создает негативных условия для ТЭ. Наряду с этим, Delgado P. и соавт. не отрицают повторного выполнения эмболизации при отсутствии инфекции мочевых путей. Авторами предпринято повторное интервенционное лечение у 9 пациентов, эффект был достигнут в 6 случаях [24]. Описаны единичные случаи развития абсцесса трансплантата через несколько месяцев после эмболизации [45, 47]. Учитывая, что эффект интервенционного лечения во всех работах оценивался только по разрешению GIS-синдрома, Ayus J.C. и Achinger S.G. [17] в 2005 году не рекомендовали рутинное использование эмболизации, ссылаясь на то, что не известно, оказывает ли какое-либо воздействие метод на системное хроническое воспаление, которое является существенным фактором негативного прогноза. В том же году появилось исследование Pérez Martínez J. в соавт., где было показано, что через 6 мес. после интервенционного лечения отмечается значительное улучшение таких параметров, как уровень ферритина, СРБ, альбумина, гемоглобина, уменьшается потребность в эритропоэтине. У двух из семи больных была выполнена повторная пересадка почки без осложнений [48].
Учитывая, что эмболизация противопоказана при инфекционном воспалении трансплантата, очень важно проведение дифференциальной диагностики между кризом отторжения и острым пиелонефритом трансплантата. В выявлении инфекций мочевой системы (ИМС) ведущую роль продолжают сохранять традиционные методы: общий анализ мочи, исследование мочи по Нечипоренко, бактериологическое исследование, ультразвуковое исследование почечного трансплантата и собственных почек. Однако из-за нарушений воспалительного ответа на фоне иммуносупрессивной терапии трактовка результатов рутинных лабораторных исследований затруднена. Поэтому в трансплантологии делаются попытки разработать методы системной диагностики ИМС. Предложено определение в плазме комплексов из миелоид-связанных белков MRP8 и MRP14. Увеличение уровня содержания в сыворотке миелоид-связанного белка примерно с 6-го дня после трансплантации до 4,2 мкг/мл и выше со стопроцентной специфичностью и высокой степенью чувствительности позволяет предсказать развитие отторжения трансплантата почки. Показатели MRP8/14 при наличии мочевых инфекций, отсроченной функции трансплантата и ЦМВ-инфекции не изменяются по сравнению с исходными [49]. В случаях развития бактериальных инфекций мочевых путей, при ЦМВ-инфекции легкого течения и остром отторжении трансплантата подъем уровня интерлейкина-6 (ИЛ-6) в моче характеризует степень выраженности воспалительных процессов. Определение ИЛ-6 в моче просто, информативно и неинвазивно, поэтому может широко применяться в клинической практике [50]. Выявление отрицательной реакции на альфа-2-макроглобулин в моче в сочетании положительным тестом на СРБ является патогномоничным для экстраренальной бактериальной инфекции (чувствительность 100%, специфичность 98,9%). Присутствие одного альфа-2-макроглобулина в моче реципиента ренального трансплантата наводит на мысль о постренальной кровопотере. Если оба белка присутствуют в моче, урогенитальная бактериальная инфекция и отторжение трансплантата должны быть исключены дальнейшим обследованием [51]. Реципиентам, не отвечающим на анти-биотикотерапию, рекомендуется проводить компьютерную томографию брюшного отдела для исключения острого пиелонефрита трансплантата [52].
С увеличением количества «маргинальных» доноров, расширением показаний для трансплантации возрастает вероятность развития опухолевого процесса в пересаженной почке [53-55]. В зависимости от распространенности процесса, функции трансплантата может быть выполнена радикальная нефрэктомия или органсохраняющее оперативное пособие, описаны случаи применения радиочастотной аблации, криодеструкции [54]. При сохранении трансплантата необходимо учитывать более высокий риск местного рецидива по сравнению с общей популяцией пациентов, такие больные подлежат тщательному наблюдению [56].
Разрыв трансплантата достаточно редкое осложнение, встречающееся в среднем у 3,4% рецепиентов и возникает, как правило, в течение 3-4 недель после трансплантации. Острое отторжение, венозный тромбоз и острый тубулярный некроз в отсутствии признаков острой реакции отторжения являются наиболее частыми причинами. Независимо от этиологического фактора в трансплантате развивается интерстициальный отек, приводящий к ишемии и повышению внутрипочечного давления [57]. По мнению ряда авторов, нефрэктомия применима только у тех больных, у которых в противном случае высоко вероятен летальный исход, во всех остальных случаях необходимо стараться сохранить почку. Показанием к ТЭ является венозный тромбоз, нестабильность гемодинамики, наличие выраженной, необратимой реакции острого отторжения. Наложение матрацных швов - наиболее распространенный метод ор-гансохраняющего лечения. В качестве других вариантов предложено использование коллагеновой пены, фибринового клея, различных сеток, лиофилизированной фасции. Эффективность такой сальважной терапии колеблется от 40 до 100% [58, 59].
Лимфопролиферативные заболевания развиваются менее чем у 1% реципиентов, но ассоциированы более чем с 50% смертностью. При вовлечении в процесс почки показано, что выполнение ТЭ существенно (на 50%) повышает выживаемость реципиентов [60].
Удаление нефункционирующего трансплантата приводит к повышению титра анти-HLA-антител по причине отсутствия иммуносупрессии и органа, абсорбировавшего антитела. Rosenberg J.C. и соавт. показали, что у 30% больных, ожидающих повторную пересадку почки, была выявлена тотальная несовместимость по HLA, 60% из этих пациентов перенесли ТЭ [61]. Del Bello A. и соавт. сравнивали количество антител у пациентов в момент возвращения к ГД и прекращения иммуносупрессивной терапии (за исключением кортикостеройдов), затем через 3 и 6 мес. У больных, которым выполнена ТЭ, дополнительно оценивали количество антител через 5 дней, 3 и 9 мес. после вмешательства. Анти-HLA-антитела после начала ГД были выявлены в 14,2%, в ходе дальнейшего наблюдения - у 52,4% больных с сохраненным трансплантатом (I группа) и в 81% после ТЭ (II группа). Анти-HLA-антитела против HLA-I были позитивны в 23,8% в I группе и в 77% во II группе, анти-HLA-антитела против HLA-II верифицированы в 42,8% в I группе и в 62,5% во II группе [62]. В исследовании Sumrani N. и соавт. показано, что предшествующая ТЭ негативным образом сказывается на результатах ретрансплантации. У больных, перенесших нефрэктомию, чаще отмечалась отсроченная функция трансплантата, тенденция в сторону снижения выживаемости донорской почки в течение только первого года, однако через 3 года показатели были идентичные [63]. Abouljoud M.S. и соавт. изучили данные 192 пациентов после ретрансплантации. Многофакторный статистический анализ показал: ранняя потеря функции первичного трансплантата, длительный интервал между ТЭ и ретрансплантацией, возраст более 60 лет - факторы риска низкого успеха повторной пересадки почки [6]. Schleicher C. и соавт., также используя многофакторный анализ, заключают, что ТЭ и повышение уровня тест-антигеновых антител (panel-reactive antibodies - PRA) > 70% являются независимыми, значимымыми факторами, увеличивающими вероятность развития криза отторжения, первичного отсутствия функции [64]. Тем не менее, Ahmad N. и соавт., проанализировав результаты ретрансплантации у 89 пациентов (у 68 ранее выполнена ТЭ, 21 с сохраненной почкой), не выявили статистически достоверной разницы в результатах. Единственным фактором, по мнению исследователей, влияющим на выживаемость трансплантата, является уровень PRA не зависимо от нефрэктомии [65].
Заключение
Увеличение темпов трансплантации почки ведет к росту количества больных с нефункционирующим трансплантатом, которым возобновляется заместительная почечная терапия. Высокие уровни заболеваемости и смертности, в которых ключевое значение играют септические и сердечено-сосудистые осложнения, диктуют необходимость оптимизации тактики лечения. Ряд авторов считают, что продолжение иммуносупрессивной терапии на фоне гемодиализа влечет за собой только отрицательные моменты, способствует росту летальности и заболеваемости. Транс-плантатэктомия, по-видимому, улучшает выживаемость пациентов, влияние на результаты ретрансплантации окончательно не ясно. Все работы характеризуются ретроспективным, однофакторным методом. Единственный крупный анализ, проведенный Ayus J.C. и соавт., основанный на национальной репрезентативной выборки (более 10000 пациентов в США) показал, что ретрансплантация выполнялась чаще в группе пациентов, перенесших ТЭ, но и это исследование имело много ограничений [17]. Можно предположить, если нефрэктомия производилась в связи с иммунными событиями (например, гуморальное отторжение), то процедура является просто маркером высокой иммунологической реактивности, что и обуславливает меньшую эффективность повторной пересадки почки. При досрочной потери функции трансплантата целесообразно раннее выполнение ТЭ и прекращении иммуносупрессивной терапии. В случае возвращения больного к ГД через 12 и более месяцев после пересадки почки, трансплантат может быть оставлен на месте на фоне постепенного снижения дозы иммуносупрессоров с последующей отменой. Однако эти пациенты должны находиться под тщательным наблюдением, так как трети из них потребуется хирургическое вмешательство. Предикторами, указывающими на высокую вероятность развития симптомов хронического отторжения и, соответственно, на необходимость ТЭ, являются: наличие нескольких острых кризов отторжения, прием циклоспорина в анамнезе, лабораторные признаки хронического системного воспаления. Выполнение ТЭ реципиентам с вышеуказанными факторами риска в «холодном» периоде, до появления развернутой клинической картины, ассоциировано с меньшим количеством осложнений и лучшим прогнозом. При отсутствии острого пиелонефрита может быть произведена эмболизация почечного трансплантата, эффективность которой достигает 90%. Интервенционное вмешательство связано с меньшим количеством осложнений, коротким послеоперационном периодом. У небольшого числа больных малоинвазивное лечение оказывается не эффективным, в этом случае показана ТЭ, в отдельных случаях - повторная эмболизации (схема №1).
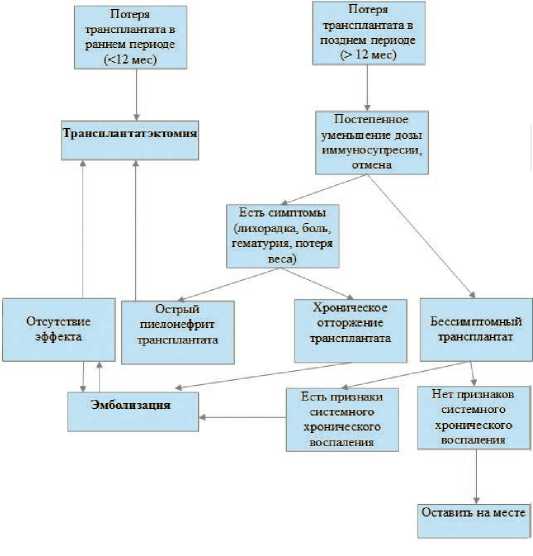
Схема № 1. Алгоритм ведения больных с нефункционирующим трансплантатом
Список литературы Современные взгляды на проблему удаления почечного трансплантата
- Johnston O., Rose C., Landsberg D., Gourlay W.A., Gill J.S. Nephrectomy after transplant failure: current practice and outcomes//Am. J. Transplant. 2007. Vol. 7. P. 1961-1967.
- Kaplan B., Meier-Kriesche H.U. Death after graft loss: an important late study endpoint in kidney transplantation//Am. J. Transplant. 2002. Vol. 2. P. 970-974.
- Ojo A., Wolfe R.A., Agodoa L.Y., Held P.J., Port F.K., Leavey S.F., Callard S.E., Dickinson D.M., Schmouder R.L., Leichtman A.B. Prognosis after primary renal transplant failure and the beneficial effects of repeat Transplantation: multivariate analyses from the United States Renal Data System//Transplantation. 1998. Vol. 66. P. 1651-1659.
- Johnston O., Zalunardo N., Rose C., Gill J.S. Prevention of sepsis during the transition to dialysis may improve the survival of transplant failure patients//J. Am. Soc. Nephrol. 2007. Vol. 18. P. 1331-1337.
- Mazzucchi E., Nahas W.C., Antonopoulos I.M., Piovesan A.C., Ianhez L.E., Arap S. Surgical complications of graft nephrectomy in the modern transplant era//J. Urol. 2003. Vol. 170. P. 734-737.
- Abouljoud M.S., Deierhoi M.H., Hudson S.L., Diethelm A.G. Risk factors affecting second renal transplant outcome, withspecial reference to primary allograft nephrectomy//Transplantation. 1995. Vol. 60. P. 138-144.
- Eng M.M., Power R.E., Hickey D.P., Little D.M. Vascular complications of allograft nephrectomy//Eur. J. Vasc. Endovasc. Surg. 2006. Vol. 32. P. 212-216.
- Zerouali F., Levtchenko E.N., Feitz W.F., Cornelissen E.A., Monnens L.A. Renal transplant nephrectomy in children: can an aggressive approach be recommended?//Pediatr. Transplant. 2004. Vol. 8. P. 561-564.
- Roberts C.S., LaFond J., Fitts C.T., Rajagopalan P.R., Baliga P., Cofer J.B., Bromberg J.S. New patterns of transplant nephrectomy in the cyclosporine era//J. Am. Coll. Surg. 1994. Vol. 178. P. 59-64.
- Secin F.P., Rovegno A.R., del Rosario Brunet M., Marrugat R.E., Davalos Michel M., Fernandez H. Cumulative incidence, indications, morbidity and mortality of transplant nephrectomy and the most appropriate time for graft removal: only nonfunctioning transplants that cause intractable complications should be excised//J. Urol. 2003. Vol. 169. P. 1242-1246.
- O'Sullivan D.C., Murphy D.M., McLean P., Donovan M.G. Transplant nephrectomy over 20 years: factors involved in associated morbidity and mortality//J. Urol. 1994. Vol. 151. P. 855-858.
- Ayus J.C., Achinger S.G., Lee S., Sayegh M.H., Go A.S. Transplant nephrectomy improves survival following a failed renal allograft//J. Am. Soc. Nephrol. 2010. Vol. 21. P. 374-380.
- Goldstein S.L., Mattoo T.K., Morgenstern B., Martz K., Stablein D., Talley L. Anemia and growth status in pediatric patients receiving maintenance dialysis after a failed renal transplant course: an NAPRTCS report//Pediatr. Transplant. 2007. Vol. 11. P. 201-204.
- Morales A., Gavela E., Kanter J., Beltran S., Sancho A., Escudero V., Crespo J., Pallardo L.M. Treatment of renal transplant failure//Transplant. Proc. 2008. Vol. 40. P. 2909-2911.
- Langone A.J., Chuang P. The management of the failed renal allograft: an enigma with potential consequences//Semin. Dial. 2005. Vol. 18. P. 185-187.
- Toledo-Pereyra L.H., Gordon C., Kaufmann R., Whitten J.I., Mittal V.K. Role of immediate versus delayed nephrectomy for failed renal transplants//Am. Surg. 1987. Vol. 53. P. 534-536.
- Ayus J.C., Achinger S.G. At the peril of dialysis patients: ignoring the failed transplant//Semin. Dial. 2005. Vol. 18. P. 180-184.
- Shapiro D.J., Blumenkrantz M.J., Shenaberger J.H., Coburn J.W. Useful function of'non-functioning' renal homograft//Br. Med. J. 1975. Vol. 3. P. 140.
- Vanrenterghem Y., Khamis S. The management of the failed renal allograft//Nephrol. Dial. Transplant. 1996. Vol. 11. P. 955-957.
- Hansen B.L., Rohr N., Svendsen V., Birkeland S.A. Graft failure and graft nephrectomy without severe complications//Nephrol. Dial.Transplant. 1987. Vol. 2. P. 189-190.
- Gregoor P.J., Kramer P., Weimar W., van Saase J.L. Infections after renal allograft failure in patients with or without lowdose maintenance immunosuppression//Transplantation. 1997. Vol. 63. P. 1528-1530.
- Smak Gregoor P.J., Zietse R., van Saase J.L., op de Hoek C.T., IJzermans J.N., Lavrijssen A.T., de Jong G.M., Kramer P., Weimar W. Immunosuppression should be stopped in patients with renal allograft failure//Clin. Transplant. 2001. Vol. 15. P. 397-401.
- Naini A.E., Harandi A.A., Daemi P., Kosari R., Gharavi M. Outcome of patients without any immunosuppressive therapy after renal allograft failure//Saudi J. Kidney Dis. Transpl. 2008. Vol. 19. P. 59-61.
- Delgado P., Diaz F., Gonzalez A., Sanchez E., Gutierrez P., Hernandez D. et al. Intolerance syndrome in failed renal allografts: incidents and efficacy of percutaneous embolization//Am. J. Kidney Dis. 2005. Vol. 46. P. 339-344.
- Madore F., Hebert M.J., Leblanc M., Girard R., Bastien E., Morin M., Beaudry C., Boucher A., Dandavino R. Determinants of late allograft nephrectomy//Clin. Nephrol. 1995. Vol. 44. P. 284-289.
- Kiberd B.A., Belitsky P. The fate of the failed renal transplant//Transplantation. 1995. Vol. 59(4). P. 645-647.
- Lopez-Gomez J.M., Perez-Flores I., Jofre R., Carretero D., Rodriguez-Benitez P., Villaverde M., Perez-Garcia R., Nassar G.M. Niembro E., Ayus J.C. Presence of a failed kidney transplant in patients who are on hemodialysis is associated with chronic inflammatory state and erythropoietin resistance//J. Am. Soc. Nephrol. 2004. Vol. 15. P. 2494-2501.
- Touma N.J., Sener A., Caumartin Y., Warren J., Nguan C.Y., Luke P.P. Extracapsular versus intracapsular allograft nephrectomy: impact on allosensitization and surgical outcomes//Can. Urol. Assoc. J. 2011. Vol. 5(1). P. 49-52.
- Ghinolfi D., Arcuri V., Fontana I., Beatini M., Bertocchi M., Valente U.A. simple new technique to prevent bleeding in transplant nephrectomy//Int. J. Urol. 2005. Vol. 12. P. 522-524.
- Vavallo A.I., Lucarelli G., Bettocchi C., Tedeschi M., Palazzo S., Losappio V., Gesualdo L., Grandaliano G., Selvaggi F.P., Battaglia M., Ditonno P. Allograft nephrectomy: what is the best surgical technique?//Transplant. Proc. 2012. Vol. 44(7). P. 1922-1925.
- Zomorrodi A., Buhluli A. Debulking transplant nephrectomy leaving an intact ureter and instillation of betadine intracapsular is safe nephrectomy: fifteen years' experience//Transplant. Proc. 2008. Vol. 40. P. 205-207.
- Grochowiecki T., Szmidt J., Galazka Z., Nazarewski S., Bojakowska M., Bojakowski K., Swiercz P. Influence of timing of transplant nephrectomy on surgical complications//Transplant. Proc. 2000. Vol. 32. P. 1381.
- Sharma D.K., Pandey A.P., Nath V., Gopalakrishnan G. Allograft nephrectomya 16-year experience//Br. J. Urol. 1989. Vol. 64. 122-124
- Lund Hansen B., Rohr N., Starklint H., Svendsen V., Birkeland S.A. Indications for and timing of removal of non-functioning kidney transplant//Scand. J. Urol. Nephrol. 1986. Vol. 20. P. 217-220.
- Sienko J., Tejchman K., Cnotliwy M., Falkowski A., Nowacki M., Ostrowski M. Crossed bypass femoro-femoralis in patient with external iliac artery occlusion in the course of septic hemorrhage after renal graft explantatation//Ann. Transplant. 2006. Vol. 11. P. 12-14.
- Blohme I., Brynger H. Emergency ligation of the external iliac artery//Ann. Surg. 1985. Vol. 201. P. 505-510.
- Diller R., Holzen J., Senninger N., Kramer S. Interventional stenting for ruptured iliac aneurysm following transplant nephrectomy//Transplant. Proc. 2006. Vol. 38 P. 718-720.
- McIntosh B.C., Bakhos C.T., Sweeney T.F., DeNatale R.W., Ferneini A.M. Endovascular repair of transplant nephrectomy external iliac artery pseudoaneurysm//Conn. Med. 2005. Vol. 69. P. 465-466.
- Moosavi C.A., Gujrathi S.K., Friedman A., Fox D., Silberzweig J.E. Endovascular repair of symptomatic renal transplant site pseudoaneurysm//Vasc. Endovasc. Surg. 2008. Vol. 42. P. 607-609.
- Neschis D.G., Gutta R., Al-Qudah H.S., Bartlett S.T., Philosophe B., Schweitzer E.J., Flinn W.R., Campos L. Intraoperative coil embolization reduces transplant nephrectomy transfusion requirement//Vasc. Endovasc. Surg. 2007. Vol. 41. P. 335-338.
- Osman I., Barrero R., Leon E., Medina R., Torrubia F. Mycotic pseudoaneurysm following a kidney transplant: a case report and review of the literature//Pediatr. Transplant. 2009. Vol. 13. P. 615-619.
- Lorenzo V., Diaz F., Perez L., Dominguez M., Machado M., Rodriguez A., Gonzalez-Posada J., Hernandez D., De Bonis E., Torres A. Ablation of irreversibly rejected renal allograft by embolization with absolute ethanol: a new clinical application//Am. J. Kidney Dis. 1993. Vol. 22. P. 592-595.
- Gonzalez-Satue C., Riera L., Franco E., Escalante E., Dominguez J., Serrallach N. Percutaneous embolization of the failed renal allograft in patients with graft intolerance syndrome.//BJU Int. 2000. Vol.86. P. 610-612.
- Cofan F., Vilardell J., Gutierrez R., Real M., Montanya X., Oppenheimer F., Talbot-Wright R., Carretero P. Efficacy of renal vascular embolization versus surgical nephrectomy in the treatment of nonfunctioning renal allografts//Transplant. Proc. 1999. Vol. 31. P. 2244-2245.
- Gonzalez-Satue C., Riera L., Franco E., Castelao A., Sancho C., Ponce A., Serrallach N. Percutaneous embolization of non-functioning renal graft as therapeutic alternative to surgical transplantation//Actas. Urol. Esp. 2000. Vol. 4. P. 319-324.
- Atar E., Belenky A., Neuman-Levin M., Yussim A., Bar-Nathan N., Bachar G. Nonfunctioning renal allograft embolization as an alternative to graft nephrectomy: report on seven years' experience//Cardiovasc. Intervent. Radiol. 2003. Vol. 26. P. 37-39.
- Perez Martinez J.I., Gallego E., Julia E., Llamas F., Lopez A., Palao F., Lorenzo I., Lopez E., Illescas M.L., Gomez Roldan C. Embolization of non-functioning renal allograft: efficacy and control of systemic inflammation//Nefrologia. 2005. Vol. 25(4). P. 422-427.
- Steinhoff J., Faerber P., Preuss R. Alpha 2-macroglobulin in urine. Significance for differential diagnosis of rejection and infections after kidney transplantation//Dtsch. Med. Wochenschr. 1994. Vol. 1(2). P. 1-6.
- Kaden J., Priesterjahn R. Increasing urinary IL-6 levels announce kidney graft rejection//Transpl. Int. 2000. Vol. 13. P. 34-41.
- Burkhardt K., Radespiel-Troger M., Rupprecht H.D. An increase in myeloid-related protein serum levels precedes acute renal allograft rejection//J. Am. Soc. Nephrol. 2001. Vol. 9. P. 1947-1957.
- Yang C.W., Lee S.H., Choi Y.J. Evaluation of acute renal failure in bacterial allograft pyelonephritis using abdominal CT and graft biopsy//Am. J. Nephrol. 1997. Vol. 1. P. 42-45.
- Llamas F., Gallego E., Salinas A., Virseda J., Perez J., Ortega A., Nam S.H., Gomez C. Sarcomatoid renal cell carcinoma in a renal transplant recipient//Transplant. Proc. 2009. Vol. 41. P. 4422-4424.
- Diller R., Senninger N. Treatment options and outcome for renal cell tumors in the transplanted kidney//Int. J. Artif. Organs. 2008. Vol. 31. P. 867-874.
- Schena S., Bogetti D., Setty S., Kadkol S., Bruno A., Testa G., Panaro F., Benedetti E., Sankary H. Squamous cell carcinoma in a chronically rejected renal allograft//Am. J. Transplant. 2004. Vol. 4. P. 1208-1211.
- Hoda M.R., Hamza A., Wagner S., Greco F., Fornara P. Recurrence of renal cell carcinoma in a renal allograft after partial transplant nephrectomy: a case report//Urol. Int. 2009. Vol. 83. P. 239-241
- Busi N., Capocasale E., Mazzoni M.P., Benozzi L., Valle R.D., Cambi V., Sianesi M. Spontaneous renal allograft rupture without acute rejection//Acta. Biomed. 2004. Vol. 75. P. 131-133.
- Heimbach D., Miersch W.D., Buszello H., Schoeneich G., Klehr H.U. Is the transplant-preserving management of renal allograft rupture justified?//Br. J. Urol. 1995. Vol. 75(6). P. 729-732.
- Hochleitner B.W., Kafka R., Spechtenhauser B., Bosmuller C., Steurer W., Konigsrainer A., Margreiter R. Renal allograft rupture is associated with rejection or acute tubular necrosis, but not with renal vein thrombosis//Nephrol. Dial. Transplant. 2001. Vol. 16(1). P. 124-127.
- Trofe J., Buell J.F., Beebe T.M., Hanaway M.J., First M.R., Alloway R.R., Gross T.G., Succop P., Woodle E.S. Analysis of factors that influence survival with post-transplant lymphoproliferative disorder in renal transplant recipients: the Israel Penn International Transplant Tumor Registry experience//Am. J. Transplant. 2005. Vol. 5. P. 775-780.
- Rosenberg J.C., Berri R., Jackowski M., Levis D., Nehlsen-Cannarella S., Oh H. Multi-array antibody screening in detecting antibodies to mismatched HLA in patients awaiting a second transplant//Transplant. Proc. 2006. Vol. 38. P. 3393-3395.
- Del Bello A.I., Congy-Jolivet N., Sallusto F., Guilbeau-Frugier C., Cardeau-Desangles I., Fort M., Esposito L., Guitard J., Cointault O., Lavayssiere L., Nogier M.B., Blancher A., Rostaing L., Kamar N. Donor-specific antibodies after ceasing immunosuppressive therapy, with or without an allograft nephrectomy//Clin. J. Am. Soc. Nephrol. 2012. Vol. 7(8). P. 1310-1319.
- Sumrani N., Delaney V., Hong J.H., Daskalakis P., Sommer B.G. The influence of nephrectomy of the primary allograft on retransplant graft outcome in the cyclosporine era//Transplantation. 1992. Vol. 53. P. 52-55.
- Schleicher C., Wolters H., Kebschull L., Anthoni C., Suwelack B., Senninger N., Palmes D. Impact of failed allograft nephrectomy on initial function and graft survival after kidney retransplantation//Transpl. Int. 2011. Vol. 24. P. 284-291.
- Ahmad N., Ahmed K., Mamode N. Does nephrectomy of failed allograft influence graft survival after re-transplantation?//Nephrol. Dial. Transplant. 2009.Vol. 24. P. 639-642.


