Создание математических моделей, определяющих поражение коронарных сосудов по анализу движения миокарда при проведении стресс-эхокардиографии
Автор: Пономарев С.Б., Русяк И.Г., Кривилева С.П., Петров А.Г., Дюндик А.С.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 2 (24) т.8, 2004 года.
Бесплатный доступ
Описано создание математических моделей, способных по результатам оценки нарушения движения стенок миокарда при проведении фармакологической стресс-эхокардиографии дать вероятностную оценку поражения коронарных артерий стенозирующим коронароангиосклерозом. Проведен анализ результатов, полученных для 11 сегментов магистральных коронарных сосудов у группы пациентов с ишемической болезнью сердца. Описан алгоритм исследования и применяемый методологический подход. Дано описание программного комплекса. Созданная система может быть рекомендована при обследовании больных ишемической болезнью сердца на поликлиническом и раннем госпитальном этапах лечения.
Коронарные артерии, фармакологическая стресс- эхокардиография, коронароангиография, движение (кинез) стенок миокарда, математическое моделирование
Короткий адрес: https://sciup.org/146215798
IDR: 146215798 | УДК: 531/534:57+612.7
Текст научной статьи Создание математических моделей, определяющих поражение коронарных сосудов по анализу движения миокарда при проведении стресс-эхокардиографии
Известно, что ряд параметров неинвазивного и легковыполнимого метода стресс-эхокардиографии с использованием фармакологических агентов (фармакологическая стресс-эхокардиография) хорошо коррелирует с результатами коронароангиографии, являющейся «золотым стандартом» обследования больного ишемической болезнью сердца [1, 3, 6, 18, 21, 25, 26, 28]. При этом достоверно установлено, что снижение кинеза отдельных сегментов сердечной мышцы при выполнении фармакологической стресс-эхокардиографии отражает нарушение регионального кровотока в бассейне соответствующей коронарной артерии [17, 20, 24, 25, 28], что делает возможным использование информации, получаемой при проведении фармакологической стресс-эхокардиографии, для идентификации поражения основных сегментов магистральных коронарных сосудов [7]. Вместе с тем, несмотря на очевидность связи асинергичного движения участков миокарда с локализацией стенозирующего коронароангиосклероза, до сих пор не было предложено математически выверенных систем идентификации локализации стенозов коронарной артерии по данным фармакологической стресс-эхокардиографии. В настоящее время
предсказание поражения коронарной артерии по результатам фармакологической стресс-эхокардиографии, как правило, осуществляется врачом на основании интуиции и эмпирически полученных (в результате практической работы и изучения литературы) знаний.
Целью исследований было создание комплекса математических моделей, способных с приемлемой точностью прогнозировать стенотические поражения отдельных сегментов магистральных коронарных артерий у больных ишемической болезнью сердца, используя данные об изменении механики движения стенок миокарда при проведении фармакологической стресс-эхокардиографии .
Материалы и методы
Объектом изучения явилась группа больных ишемической болезнью сердца (206 человек), мужчин трудоспособного возраста, прошедших фармакологическую стресс-эхокардиографию и коронароангиографию в рамках разработанной и успешно применявшейся ранее комплексной системы диагностики ишемической болезни сердца [4, 9, 11]. Практическое использование указанного исследовательского комплекса повлекло за собой разработку информационно-аналитической системы, моделирующей ход врачебной мысли при определении поражения коронарной артерии (в частности, по данным сонографических методов исследования). При этом формализация данных физического и инструментального исследований проводилась в соответствии с методикой планирования эксперимента [15].
Для проведения исследований была разработана компьютерная карта больного ишемической болезнью сердца [23], которая предполагала следующее:
-
• возможность внесения формализованных данных анамнеза и обследования больного в память ЭВМ,
-
• адаптацию получаемой «базы данных» для математической обработки в известных информационных оболочках с применением пакетов специализированных статистических программ,
-
• возможность качественной проверки разработанных методов прогноза на «независимых» информационных массивах,
-
• связь указанной компьютерной карты со специализированной программой вероятностного определения локализации участков стенозирующего коронароангиосклероза.
Попутно, в соответствии с общим алгоритмом разработки прогностических методик [11, 12], были сформулированы правила формализации и структуризации, относящиеся к рассматриваемой задаче клинической информации.
При проведении фармакологической стресс-эхокардиографии фиксировалось появление нарушений сократимости миокарда (по пятибальной шкале) в 16-сегментарной системе картирования левого желудочка [16] (рис. 1). Всем больным была выполнена медикаментозная стресс-эхокардиография при строгом соблюдении протокола исследования и общепринятых принципов безопасности последнего с использованием дипиридамола в дозе 0,56 мг/кг, добутамина в дозе до 40 мг/кг или малых доз добутамина 5-10 мг/кг [4, 9]. Качественная оценка стресс-индуцированной ишемии определялась по региональному нарушению движения стенок камер сердца. Также изучалась динамика фракции выброса до и после фармакологической стресс-эхокардиографии.
У всех пациентов была проведена коронарная ангиография по общепринятой методике, как минимум, в 5 проекциях для левой коронарной артерии и в 3 проекциях для правой коронарной артерии. Выявленные стенотические поражения коронарного русла оценивались денситометрически. При этом определялась степень облитерации просвета сосуда в процентах и отмечалась локализация стеноза относительно сегментов крупных артерий системы кровоснабжения миокарда.
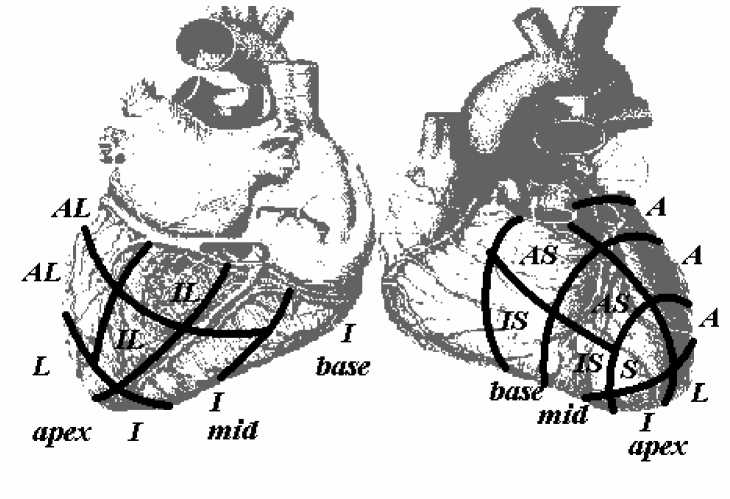
Рис. 1. Схема деления поверхности левого желудочка сердца на 16 сегментов
Расчеты проводились в оболочках статистических пакетов Excel , SPSS 8.0, Statgraphics и Statistica в соответствии с концепцией разработки медицинских прогностических систем [5, 11, 12, 23].
Общий принцип, используемый при распознавании поражения участков коронарных артерий, состоял в следующем: пусть высказывания Z 1, ... , Zk означают какие-либо свойства распознаваемых объектов, (в рассматриваемом случае поражение той или иной части коронарной артерии), а высказывания X 1 , ... , Xi – регистрируемые в эксперименте признаки, по определённым совокупностям которых можно установить наличие одних и отсутствие других свойств распознаваемых объектов (в рассматриваемой задаче регистрируемые в ходе проведения фармакологической стресс-эхокардиографии участки асинергии стенок миокарда). Априорные сведения о них, выражающие, с одной стороны, связь между высказываниями Z 1 , ... , Zk и X 1, ... , Xi , с другой, – зависимость только между Z 1, ... , Zk , или только между элементами X 1 , ... , Xi в общем случае можно представить в форме одного соотношения эквивалентности следующего вида [2]:
E ( X 1 ,..., X i ; Z 1 ,..., Z k ) = I , (1)
где E – известная булева функция.
Распознать наблюдаемый объект – значит установить, опираясь на априорные зависимости и экспериментальные данные о признаках X 1, ... , Xi , какими свойствами из числа Z 1, ... , Zk этот объект обладает, а какими не обладает.
Практическая реализация данного метода применительно к поставленной задаче выглядела следующим образом: в распоряжении исследователей, как говорилось выше, имелась информация о состоянии 16 секторов сердца, определяемом в ходе проведения фармакологической стресс-эхокардиографии. При этом наличие или отсутствие асинергичного движения рассматриваемого участка миокарда рассматривалось в описываемой части исследований как кодируемое единицей или нулем. Функция отклика представляла собой набор данных о состоянии 11 основных отделов коронарной сети, выявляемом при проведении коронароангиографии.
Экспериментально был осуществлен анализ всевозможных сочетаний описанных признаков, начиная от 1 признака из имеющихся 16 и до N признаков из 16. Однако анализу могли подвергнуться далеко не все возможные сочетания признаков. Выходом из положения было использование хеммингова расстояния [2], которое обычно применяется в качестве меры близости объектов, описываемых дихотомическими признаками:
n
Р X ( “ q , “ g ) = £ И— 4 • (2) j = 1
В результате все наборы возможных сочетаний признаков можно разбить на ряд групп с равным хемминговым расстоянием, а за неопределённое значение функции принимать то, которое наиболее часто встречается в той группе, к которой этот набор относится.
Таким образом, прогнозными показателями (или индексами) в описываемой части исследований являлись булевы функции с оптимальным сочетанием переменных, определяющих, в конечном счете, наличие или отсутствие поражения того или иного участка коронарной артерии, минимизированные при помощи метода Мак-Класски.
В результате проведенных исследований была получена математически обоснованная информация о группах сочетаний признаков, характерных для поражения того или иного участка коронарного русла, данные о которых были занесены в память компьютера. Последние составили базовую матрицу для обработки опытных данных с целью определения прогноза локализации обструктивных изменений коронарного русла.
В целях обеспечения высокого качества проводимых исследований группа наблюдения была «разбита» на 2 группы: группу «обучения» (103 наблюдения), или группу I, и группу «контроля» (также 103 наблюдения), или группу II, которые были сравнены по ряду клинико-инструментальных характеристик с использованием критерия Стьюдента [13]. При этом было выяснено, что они были однородны по всем рассматриваемым параметрам. Кроме того, данные фармакологической стресс-эхокардиографии также были исследованы на однородность при помощи критерия знаков. Полученные результаты сравнения показали однородность групп «контроля» и «обучения» по результатам оценки визуализации (в ходе проведения стресс-эхокардиографии) всех анализируемых сегментов левого желудочка.
Затем на данных первой группы были проведены исследования по описанному выше плану (или алгоритму) в оболочке статистического пакета SPSS 8.0. При этом, как указывалось, были выяснены сочетания элементов, характерных для поражения того или иного участка коронарной сети.
Так как булеву функцию можно записать как в виде матрицы, так и при помощи совершенной дизъюнктивной нормальной формы (которую необходимо минимизировать), в результате проведенных расчетов были получены минимизированные прогнозные функции для всех 11 откликов, в роли которых выступало состояние коронарного русла на том или ином рассматриваемом участке коронарной сети.
Результаты
Первые результаты были получены для ствола левой коронарной артерии. В результате применения описанного выше метода была получена прогнозная модель вида:
Y = X 5 X 7 X 9 X 14 X 15 V X 5 X 7 X 9 X 14 X 15 V X 5 X 7 X 9 X 14 X 15 ,
где:
-
Y 1 – прогностический индекс, прогнозирующий поражение ствола левой коронарной артерии стенозирующим коронароангиосклерозом,
X 5 – уровень кинеза в области заднеперегородочного сегмента базальной части левого желудочка при проведении фармакологической стресс-эхокардиографии,
X 7 – уровень кинеза в области переднего сегмента средней части левого желудочка при проведении фармакологической стресс-эхокардиографии ,
X 9 – уровень кинеза в области переднебокового сегмента базальной части левого желудочка при проведении фармакологической стресс-эхокардиографии,
X 14 – уровень кинеза в области бокового сегмента верхушечной части левого желудочка при проведении фармакологической стресс-эхокардиографии,
X 15 – уровень кинеза в области заднего сегмента верхушечной части левого желудочка при проведении фармакологической стресс-эхокардиографии.
Здесь и в дальнейшем переменная X означает наличие асинергичного движения соответствующего участка миокарда, переменная X – отсутствие такового.
При этом прогноз считался положительным (т.е. свидетельствующим о сужении просвета ствола левой коронарной артерии) при наличии описанного приведенной формулой сочетания отсутствия или наличия асинергичного движения сегментов миокарда, информация о которых использовалась в приведенном уравнении.
Следующие расчеты были осуществлены для передней межжелудочковой ветви, являющейся основным ответвлением от ствола левой коронарной артерии и состоящей из трех отделов. При этом расчеты были проведены для каждого из отделов изолированно.
Прогнозная функция для проксимального отдела передней межжелудочковой ветви (участка от устья указанной ветви до отхождения первой перегородочной или диагональной ветви) имела вид:
Y 2 = X 1 X 2 X 5 X 15 v X 2 X 5 X 15 v X 1 X 5 X 15 v X 1 X 5 X 15 v X 1 X 2 X 15 v X 1 X 2 X 5, (4)
где:
-
Y 2 – прогностический индекс, прогнозирующий поражение проксимальной части передней межжелудочковой ветви,
-
X 1 – уровень кинеза в области переднего сегмента базальной части левого желудочка при проведении фармакологической стресс-эхокардиографии,
X 2 – уровень кинеза в области заднебокового сегмента базальной части левого желудочка при проведении фармакологической стресс-эхокардиографии.
Суждение о прогнозе наличия облитерации рассматриваемого участка передней межжелудочковой ветви принималось по принципам, описанным выше.
Следующий расчет был осуществлен для среднего отдела передней межжелудочковой ветви, который является продолжением проксимального отдела и продолжается до отхождения второй или третьей диагональных ветвей. Булева функция прогноза, рассчитанная по анализируемым факторам, имела вид:
Y. = X 8 X 9 X 14 X 15 V X 8 X 9 X 14 X 15 ,
где:
Y3 – прогностический индекс, прогнозирующий поражение средней части передней межжелудочковой ветви,
X 8 – уровень кинеза в области переднеперегородочного сегмента средней части левого желудочка при проведении фармакологической стресс-эхокардиографии.
Суждение о прогнозе наличия стеноза рассматриваемого участка передней межжелудочковой ветви также принималось по принципам, описанным выше.
Следующий расчет был проведен для дистального отдела передней межжелудочковой ветви. Для создания методики прогноза поражения этого участка также были определены наиболее информативные факторы. Функция прогноза для дистального отдела передней межжелудочковой ветви выглядела следующим образом:
Y 4 = X 1 X 3 X 13 X 15 V X 1 X 3 X 13 X 15 V X 1 X 3 X 13 X 15 ,
где:
Y 4 – прогностический индекс, прогнозирующий поражение дистальной части передней межжелудочковой ветви,
X 3 – уровень кинеза в области переднебокового сегмента базальной части левого желудочка при проведении фармакологической стресс-эхокардиографии,
X 13 – уровень кинеза в области переднего сегмента верхушечной части левого желудочка при проведении фармакологической стресс-эхокардиографии.
Суждение о прогнозе наличия облитерации рассматриваемого участка передней межжелудочковой ветви также принималось по описанному выше принципу, примененному для вышележащих участков передней межжелудочковой ветви.
Следующие расчеты были проведены для огибающей ветви левой коронарной артерии. При этом для проксимального отдела огибающей ветви (т.е. участка от устья огибающей ветви до отхождения первой краевой ветви) была получена прогнозная функция, построенная при помощи четырех факторов:
Y 5 = X 1 X 9 X 14 V X 1 X 9 X 15 , (7)
где:
Y5 – прогностический индекс, прогнозирующий поражение проксимальной части огибающей ветви.
Суждение о прогнозе наличия облитерации рассматриваемого участка огибающей ветви принималось по принципам, описанным выше.
Следующий расчет был проведен для среднего отдела огибающей ветви (т.е. участка между отхождением первой и второй (в ряде случаев третьей) краевых ветвей). При этом была получена булева функция, предсказывающая наличие стеноза в указанном участке огибающей ветви вида:
Y, = X 9 X 12 X 13 X 16 V X 11 X 12 X 13 X 16 V X 9 X 11 X 13 X 16 ,
где:
Y6 – прогностический индекс, прогнозирующий поражение средней части огибающей ветви,
-
X 11 – уровень кинеза в области заднеперегородочного сегмента средней части левого желудочка при проведении фармакологической стресс-эхокардиографии,
X 12 – уровень кинеза в области заднебокового сегмента средней части левого желудочка при проведении фармакологической стресс-эхокардиографии,
X 16 – уровень кинеза в области перегородочного сегмента верхушечной части левого желудочка при проведении фармакологической стресс-эхокардиографии.
Суждение о прогнозе стенозирования рассматриваемого участка огибающей ветви принималось по принципам, описанным выше.
Для определения наличия стеноза в дистальном отделе огибающей ветви была предложена следующая булева функция:
Y 7 = X 8 X 11 X 14 X 15 X 16 V X 8 X 11 X 14 X 15 X 1 6 V X 8 X 11 X 14 X 15 X 16 V V X 8 X 11 X 14 X 15 X 16 V X 8 X 11 X 14 X 15 ,
где:
-
Y 7 – прогностический индекс, прогнозирующий поражение дистальной части огибающей ветви.
Суждение о прогнозе стеноза рассматриваемого участка огибающей ветви принималось по принципам, описанным выше.
Следующий расчет был проведен для проксимального участка правой коронарной артерии, т.е. отрезка от начала правой коронарной артерии до отхождения ветви к правому желудочку. Для получения данных о наличии стеноза в проксимальном отделе правой коронарной артерии было предложено воспользоваться прогнозной булевой функцией, которая имеет вид:
Y 8 = X 2 X 9 X 11 X 13 X 16 V X 2 X 9 X 13 X 16 V X 2 X 9 X 11 X 16 V X 2 X 9 X 11 X 16 ,
где:
-
Y 8 – прогностический индекс, прогнозирующий поражение проксимальной части правой коронарной артерии.
Суждение о прогнозе наличия облитерации рассматриваемого участка правой коронарной артерии принималось по принципам, описанным выше.
Для прогнозирования наличия стеноза среднего участка правой коронарной артерии (который продолжается до отхождения нижней краевой ветви) было получено следующее прогностическое соотношение:
Y 9 = X3X8XnX15 v XX n X5 v XX n X5 v XXX5 v XX 3, 9 3 8 11 15 3 11 15 3 11 15 3 8 15 8 11
где:
-
Y 9 – прогностический индекс, прогнозирующий поражение средней части правой коронарной артерии.
Суждение о прогнозе наличия облитерации рассматриваемого участка правой коронарной артерии принималось по принципам, описанным выше.
Для идентификации стеноза дистального участка правой коронарной артерии была предложена булева функция:
Y o = X 2 X 9 X 11 X 13 X 16 v X 2 X 9 X 11 X 13 X 16 v X 2 X 9 Xn X 13 X 16 v V X 2 X 9 X 11 X 13 X 16 V X 2 X 9 X 11 X 13 X 16 ,
где:
-
Y 10 – прогностический индекс, прогнозирующий поражение дистальной части правой коронарной артерии.
Суждение о прогнозе наличия облитерации рассматриваемого участка правой коронарной артерии принималось по принципам, описанным выше.
Применяя разработанный алгоритм определения стенозов коронарных артерий, было также получено уравнение для идентификации поражения задней межжелудочковой ветви:
Y i = X з X 4 X 14 X 16 v X з X 4 X 14 X 16 ,
где:
-
Y 11 – прогностический индекс, прогнозирующий поражение задней межжелудочковой ветви.
Суждение о прогнозе наличия облитерации задней межжелудочковой ветви принималось по принципам, описанным выше.
Как видно из приведенных уравнений, функция отклика (т.е. наличие или отсутствие поражения того или иного сегмента коронарной сети) зависит как от наличия асинергии в том или ином участке «координированной» (в соответствии с примененной схемой картирования) поверхности левого желудочка, так и от ее отсутствия; при этом различные сочетания этих бинарных величин приводят к различным конечным ответам. Последнее подтверждает лежащее в основе метода положение о том, что «эвристическое» опознавание объекта врачом-функционалистом – это сложный и труднотрактуемый мыслительный процесс.
Как было сказано выше, эффективность разработанной методики была проверена на независимой группе «контроля», рандомизированной с группой «обучения». При этом, как указывалось, результаты сравнения (проведенные с применением критерия Стьюдента и при помощи критерия знаков) показали однородность групп по всем анализируемым параметрам, что делало проводимые иследования статистически обоснованными.
Суммарные результаты верификации предсказательной способности построенных уравнений на «контрольной» группе представлены в таблице. При этом эффективность созданных булевых функций анализировалась при помощи таких параметров, как точность, специфичность и чувствительность, определяемых по формулам [14]:
ИП+ИО
ИП+ИО+ЛО+ЛП ,
ИП
Чувствительность= ,
ИО
Специфичность= ,
где ИП – истинно положительный результат, т.е. правильно предсказанный стеноз рассматриваемого коронарного сосуда, ИО – истинно отрицательный результат, т.е. правильно предсказанное отсутствие стеноза рассматриваемого коронарного сосуда, ЛП – ложноположительный результат, т.е. предсказание наличия стеноза при его априорном отсутствии, ЛО – ложноотрицательный результат, т.е. предсказание отсутствия стеноза при его априорном наличии.
Таблица
Анализ эффективности полученных моделей при разработке системы определения поражения участков коронарной сети
|
Артерии |
Точность, % |
Специфичность, % |
Чувствительность, % |
|
Ствол левой коронарной артерии |
86,41 |
88,78 |
40,00 |
|
Проксимальный участок передней межжелудочковой артерии |
79,61 |
78,05 |
80,64 |
|
Средний участок передней межжелудочковой артерии |
77,67 |
82,89 |
62,96 |
|
Дистальный участок передней межжелудочковой артерии |
83,50 |
84,21 |
75,00 |
|
Проксимальный участок огибающей ветви левой коронарной артерии |
77,67 |
77,38 |
78,95 |
|
Средний участок огибающей ветви левой коронарной артерии |
84,47 |
84,00 |
95,00 |
|
Дистальный участок огибающей ветви левой коронарной артерии |
83,50 |
82,65 |
95,00 |
|
Проксимальный участок правой коронарной артерии |
77,67 |
78,41 |
73,33 |
|
Средний участок правой коронарной артерии |
74,76 |
82,81 |
61,54 |
|
Дистальный участок правой коронарной артерии |
66,99 |
68,37 |
40,00 |
|
Задняя межжелудочковая ветвь |
87,34 |
86,73 |
95,00 |
Обсуждение
Как видно из таблицы, отличаясь высоким уровнем точности (до 87,34%), специфичности (68,37 – 88,78% для различных участков коронарной сети) и чувствительности (до 95% в отдельных случаях), полученные данные характеризовались достаточно большой вариабельностью результатов. Так, например, при высоком уровне точности (86,41%) и специфичности (88,78%) чувствительность при определении поражения ствола левой коронарной артерии стенозирующим коронароангиосклерозом составляла всего 40%; другими словами, предсказывать (используя предложенную методику) «непоражение» ствола левой коронарной артерии легче, нежели его поражение. Последнее связано, как представляется, с особенностями процессов атеросклеротических изменений левой коронарной артерии, которые характеризуются частым наличием сразу нескольких участков сужения артерии, дающего труднотрактуемую сонографическую картину, что обуславливает сложность в определении поражения начального участка левой коронарной артерии – её ствола (участка левой коронарной артерии, представляющего максимальный интерес для исследователей (т.н. «артерии смерти» [22], получившей это образное название из-за высокой роли ее обтурации в развитии тяжелого течения коронарной болезни и ее осложнений [8, 19, 27]).
Приемлемые результаты были получены в ходе исследований для предсказания стенозов всех трех сегментов передней межжелудочковой ветви, при этом максимальная предсказательная способность предложенной системы характерна для определения поражений дистального участка передней межжелудочковой ветви (точность – 83,5%, специфичность – 84,21%, чувствительность – 75%), что, на первый взгляд, кажется несколько неожиданным (известна высокая вариабельность кровоснабжения верхушки сердца, а также наличие зон «спорного» кровоснабжения в апикальных сегментах по Salcedo ). С другой стороны, такой результат представлялся закономерным, исходя из свойств предлагаемой системы идентификации стенозов, так как при определении поражения дистального участка передней межжелудочковой ветви полностью исключаются «информационные помехи», возникающие в случае наличия поражения сразу нескольких отделов передней межжелудочковой ветви (в частности – нижележащих участков артерии); последним можно объяснить также и относительно высокий предсказательный результат для определения поражения дистального участка огибающей ветви стенозирующим коронаросклерозом (точность – 81,55%, специфичность – 82,3%, чувствительность – 71,42%).
Нужно отметить, что результаты, полученные при предсказании атеросклеротического поражения трех отделов огибающей ветви, представляют значительный интерес; наблюдается определенная «диссоциация» между сравнительно невысокими результатами определения обструкции проксимального отдела огибающей ветви (точность – 77,67%, специфичность – 77,38%, чувствительность – 78,95%) и высокими результатами, полученными для среднего (точность – 84.47%, специфичность – 84,69%, чувствительность – 71,42%) и дистального участков огибающей ветви. Повышенная предсказательная способность метода в определении поражения среднего и дистального участков огибающей ветви может быть обусловлена, на наш взгляд, как особенностями анатомии огибающей ветви, так и описанным выше феноменом роста эффективности прогноза, рассчитанного с помощью предложенной информационно-аналитической системы, по мере удаления анализируемого участка венечной сети от магистрального артериального ствола.
Впрочем, последнее, как выяснилось, частично не распространяется на правую коронарную артерию, результаты предсказания поражения дистальных отделов которой оказались меньшими при сравнении их с итогами прогноза поражения остальных отделов правой коронарной артерии (надо отметить, что наибольшую сложность, судя по полученным результатам, представляло именно определение поражения отделов правой коронарной артерии). Последнее обусловлено особенностью анатомического расположения правой коронарной артерии (известно, что правая коронарная артерия в своих начальных отделах следует вдоль правой атриовентрикулярной борозды в направлении ее соединения с задней межжелудочковой бороздой, захватывая правые отделы сердца, кинез которых весьма часто трудно идентифицируем при проведении эхокардиографии). Несколько неожиданными (в связи с вариабельностью анатомии задней межжелудочковой ветви, определяющей тип кровоснабжения сердца) оказались высокие результаты, полученные для задней межжелудочковой ветви.
Таким образом, как видно из представленных материалов, в настоящем исследовании впервые были получены данные, позволяющие с приемлемой информативностью (т.е. на «уровне» радионуклидных методик) прогнозировать поражение не только магистральных стволов венечной сети сердца, но и локальных участков коронарных артерий на основании информационной обработки результатов картирования поверхности миокарда левого желудочка при проведении фармакологической стресс-эхокардиографии по дихотомическому признаку.
На основании описанного выше алгоритма предсказания локализации стенозов коронарной артерии и анализа полученных результатов, был разработан макрос на языке программирования Visual Basic , который в дальнейшем был включен в специализированную компьютерную программу, созданную для предсказания атеросклеротического поражения коронарных сосудов, позволяющую, во-первых, разрабатывать способы математического определения локализации стенозов коронарной артерии и, во-вторых, проверять полученные в результате расчетов данные (рис. 2). Данная компьютерная программа была выполнена в интерактивном режиме, что позволяло пользователю выбирать для занесения в электронную карту пациента информацию, необходимую для расчетов.
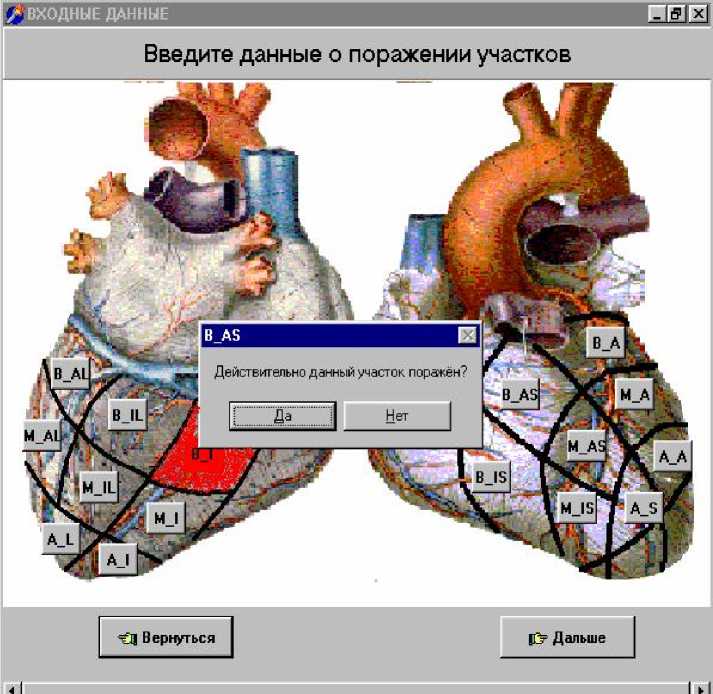
Рис. 2. Фрагмент графического интерфейса разработанной компьютерной программы
К основным возможностям данной компьютерной программы относились:
-
1. Возможность дальнейшего (по мере расширения объема исследований) обновления базы данных для прогнозирования атеросклеротического поражения коронарных сосудов.
-
2. Возможность совершенствования прогнозных функций на основании обновленной базы данных (т.н. «самообучение» и «самосовершенствование» компьютерной программы).
-
3. Индивидуальное прогнозирование результатов коронароангиографии по данным стресс-эхокардиографии для конкретного клинического случая.
Для разработки описываемого программного комплекса было выбрано следующее программное обеспечение:
-
• Операционная система Windows 9x (данный выбор был обусловлен тем, что представленные операционные системы получили в настоящие время широкое распространение и имеют развитый графический интерфейс).
-
• Язык программирования Object Pascal , визуальная среда разработки Borland Delphi 3.0 Client/Server Suite фирмы Borland .
-
• Для проектирования базы данных использовался DataBase Desktop .
Выводы
В исследованиях продемонстрирована возможность эффективного использования математического моделирования в оценке нарушений движения миокарда при проведении стресс-индуцированного теста для повышения точности диагностики поражения венечной сети стенозирующим коронароангиосклерозом.
В ходе работ был получен круг математических моделей, использующих формулы булевой алгебры. На их основе была разработана информационноаналитическая система, позволяющая с приемлемой точностью определять предполагаемую локализацию стенозов коронарного русла, исходя из результатов нагрузочного теста с проведением эхокардиографии. Применяемый при расчетах метод признан объектом изобретения [10].
Описанный метод, улучшающий диагностику ишемической болезни сердца, может быть использован в комплексной системе обследования коронарных больных на поликлиническом и раннем госпитальном этапах лечения.


