Способ формирования эзофагоеюноанастомоза после тотальной гастрэктомии: техника и непосредственные результаты
Автор: Тонеев Е.А., Берестов Н.А., Прохоров Д.Д., Полякова Е.В., Мартынов А.А., Асанов Б.М.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 1, 2026 года.
Бесплатный доступ
Рак желудка остается одной из ведущих причин онкологической смертности, а успешность реконструктивного этапа тотальной гастрэктомии во многом определяет ближайшие и отдаленные результаты лечения. Одним из наиболее ответственных моментов является формирование эзофагоеюноанастомоза (ЭЕА), частота несостоятельности которого достигает 2–10 %, что напрямую влияет на летальность и качество жизни пациентов. Несмотря на развитие механических способов анастомозирования ручные методики сохраняют актуальность благодаря лучшей адаптации слизистой и меньшему риску рефлюкс-эзофагита. Цель. Оценить непосредственные хирургические и функциональные результаты предложенной техники ручного формирования эзофагоеюноанастомоза после тотальной гастрэктомии. Материалы и методы. Проведено одноцентровое ретроспективное когортное исследование с участием 74 пациентов, оперированных в ГУЗ Областной клинический онкологический диспансер г. Ульяновска в период с 01.01.2019 по 01.09.2025. Всем больным выполнена тотальная гастрэктомия с лимфодиссекцией D2 и реконструкцией по Ру. ЭЕА формировали ручным способом, применяя рассасывающуюся нить ПГА 3-0, по оригинальной методике с инвагинацией линии швов. Оценивались интраоперационные и послеоперационные показатели, осложнения по Clavien – Dindo, а также функциональные результаты (рентгенологические, эндоскопические и сцинтиграфические данные). Результаты. Среднее время наложения ЭЕА составило 34,7±7,9 мин, частота осложнений IIIb–V степени по Clavien – Dindo – 6,8 %. При эндоскопическом контроле через 6 мес. признаки эзофагита выявлены у 54,1 % пациентов, через 12 мес. – у 36,5 %, при этом клинически значимые формы (LA C–D) – у 4,1 %. Сцинтиграфия с технецием-99m у 5 больных не выявила признаков дуоденогастроэзофагеального рефлюкса. Несостоятельности анастомоза не зарегистрировано. Выводы. Предложенный способ ручного формирования эзофагоеюноанастомоза обеспечивает высокую герметичность, минимизирует риск развития несостоятельности и рефлюкс-эзофагита, отличается технической воспроизводимостью и экономической целесообразностью. Полученные результаты подтверждают надежность и функциональную состоятельность метода при тотальной гастрэктомии.
Рак желудка, тотальная гастрэктомия, эзофагоеюноанастомоз, ручной анастомоз, реконструкция по Ру, рефлюкс-эзофагит, Clavien – Dindo
Короткий адрес: https://sciup.org/14134855
IDR: 14134855 | УДК: 616.33-006.6-089.87:616.329+616.343-089 | DOI: 10.34014/2227-1848-2026-1-73-87
Esophagojejunal anastomosis after total gastrectomy: technique and immediate results
Gastric cancer remains a leading cause of cancer-related mortality, and the success of the reconstructive stage in total gastrectomy largely determines the immediate and long-term treatment outcomes. One of the most crucial steps in the procedure is esophagojejunostomy. The incidence of esophagojejunoanal anastomosis leakage reaches 2–10 %, directly correlating with increased mortality rates and diminished quality of life. Despite advancements in mechanical anastomotic techniques, manual methods remain relevant due to better mucosal adaptation and a reduced risk of reflux esophagitis. Objective. The aim of the study is to evaluate the immediate surgical and functional outcomes of the proposed esophagojejunostomy with manual suture after total gastrectomy. Materials and Methods. A single-center retrospective cohort study was conducted involving 74 patients who underwent surgery at the Ulyanovsk Regional Clinical Oncology Dispensary between January 1, 2019, and September 1, 2025. All patients underwent total gastrectomy with D2 lymphadenectomy and Roux-en-Y reconstruction. The esophagojejunoanal anastomosis was formed manually using 3-0 PGA absorbable sutures and an original technique involving suture line invagination. Intraoperative and postoperative parameters, complications according to Clavien-Dindo classification, and functional outcomes (radiological, endoscopic, and scintigraphic data) were evaluated. Results. The average time of esophagojejunostomy was 34.7±7.9 min. The incidence of grade IIIb–V complications according to Clavien-Dindo classification was 6.8 %. Endoscopic follow-up at 6 months revealed signs of esophagitis in 54.1 % of patients, decreasing to 36.5 %, at 12 months; notably, clinically significant forms (LA Grade C–D) were observed only in 4.1 % of cases. Technetium-99m scintigraphy performed in 5 patients revealed no signs of duodenogastroesophageal reflux. No cases of anastomotic leaks were recorded. Conclusion. The proposed esophagojejunostomy with manual suture ensures high integrity, minimizes the risk of anastomotic leakage and reflux esophagitis. Moreover, the method is technically reproducible and cost-effective. The results confirm the reliability and functional viability of the technique in patients undergoing total gastrectomy.
Текст научной статьи Способ формирования эзофагоеюноанастомоза после тотальной гастрэктомии: техника и непосредственные результаты
В настоящий момент предложены многочисленные варианты формирования ЭЕА – механические, ручные и комбинированные [4, 5]. Механические анастомозы имеют преимущество в воспроизводимости и непродолжительном времени формирования, но отмечаются проблемы с адаптацией слизистой, что впоследствии приводит к развитию стриктур или, ввиду отсутствия клапанного механизма, к стойкому рефлюкс-эзофагиту [6–8]. На практике выбор техники обусловлен анатомическими особенностями пациента, опытом хирургической бригады и требованиями к функциональному результату [9, 10].
Таким образом, несмотря на развитие механических способов анастомозирования, ручной способ формирования ЭЕА остается актуальным [11].
Цель исследования. Оценить непосредственные хирургические и функциональные результаты применения предложенной техники ручного формирования эзофагоеюноана-стомоза после тотальной гастрэктомии.
Материалы и методы. Проведено одноцентровое ретроспективное когортное исследование историй болезни пациентов, оперированных в ГУЗ Областной клинический онкологический диспансер (г. Ульяновск). В анализ включали последовательные наблюдения за период с 01.01.2019 по 01.09.2025.
Все операции выполнялись в объеме тотальной гастрэктомии с реконструкцией по Ру и лимфодиссекцией D2.
Исследование соответствовало принципам Хельсинкской декларации и получило одобрение локального этического комитета (протокол № 12 от 10.01.2025).
Изучались обезличенные данные; все пациенты подписали информированное согласие на хирургическое лечение и последующее использование клинической информации.
Статистический анализ данных проводился с использованием программного обеспечения R версии 4.2.2. и StatTech v. 4.1.2 (ООО «Статтех», Россия).
Формирование анастомоза выполнялось с применением рассасывающейся плетеной нити ПГА 3-0 («МиМ», Россия) атравматической иглой следующим образом.
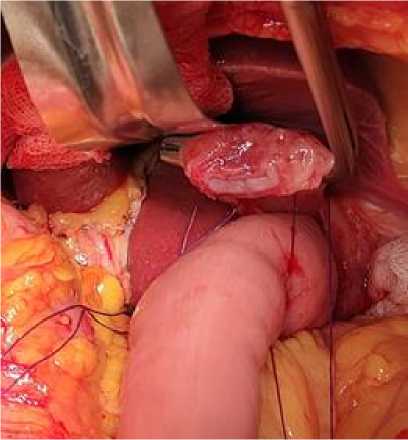
Рис. 1. Наложение 2 швов проксимальнее зажима Сатинского
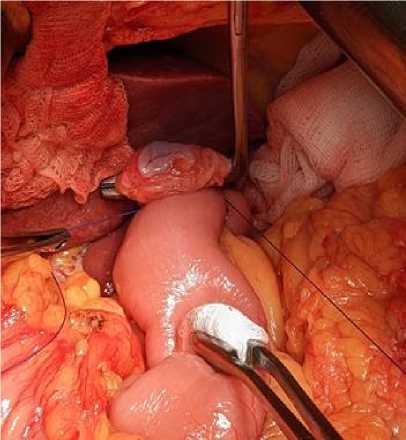
Рис. 2. Вид анастомоза после затягивания 2 швов
Fig. 1. Application of two sutures proximal to the Satinsky clamp
Fig. 2. Anastomosis after tightening two sutures
В 3–4 мм от линии первого ряда делается рассечение передней (противобрыжеечной)
стенки тонкой кишки размером около 5–7 мм (рис. 3).
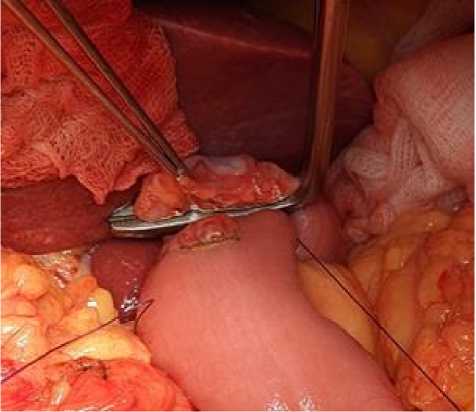
Рис. 3. Рассечение передней стенки тонкой кишки
Fig. 3. Incision of the small intestine anterior wall
Формирование второго ряда задней губы анастомоза осуществляется посредством наложения 5 узловых швов, захватывающих все слои соединяемых органов. Вкол иглы производится со стороны слизистой оболочки тонкой кишки, выкол – со стороны слизистой оболочки пищевода, что обеспечивает инверсию шва. Первый стежок локализуется за латеральным «углом» анастомотического отверстия со стороны кишки. Описанная техника позволяет расположить все узлы в просвете кишки (рис. 4).
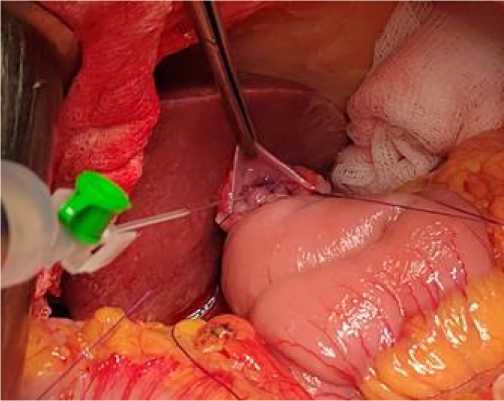
Рис. 4. Вид узлов после окончания формирования задней губы анастомоза
Fig. 4. Knots after completing the posterior wall of the anastomosis
После завершения наложения швов второго ряда задней губы анастомоза формируются два «переходных» шва, соединяющих заднюю и переднюю стенки анастомоза. Вкол иглы осуществляется со стороны слизистой оболочки тонкой кишки, выкол – со стороны слизистой оболочки пищевода (рис. 5).
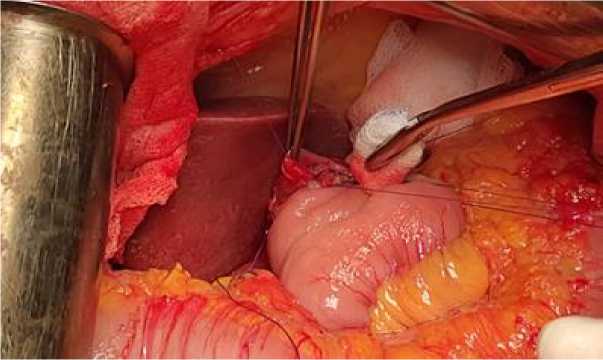
Рис. 5. Вид швов, соединяющих заднюю и переднюю стенки анастомоза
Fig. 5. Sutures connecting the posterior and anterior walls of the anastomosis
После фиксации «переходных» швов начинается формирование передней стенки анастомоза. Каждый стежок выполняется следующим образом. Вкол иглы осуществляется со стороны серозной оболочки тонкой кишки с выколом у края слизистой оболочки, что предотвращает инвагинацию слизистой в зону сопоставления пищевода и кишки. Затем вкол иглы выполняется со стороны слизистой оболочки пищевода на расстоянии
2–3 мм от края с последующим проксимальным смещением слизистой и выколом со стороны адвентиции (рис. 6). Обычно для формирования передней губы достаточно 3–4 швов. Швы временно фиксируются без затягивания. Перед окончательным затягиванием швов через анастомоз на глубину 3–4 см устанавливается назоинтестинальный зонд диаметром 24–26 Fr. Затягивание швов осуществляется над зондом.
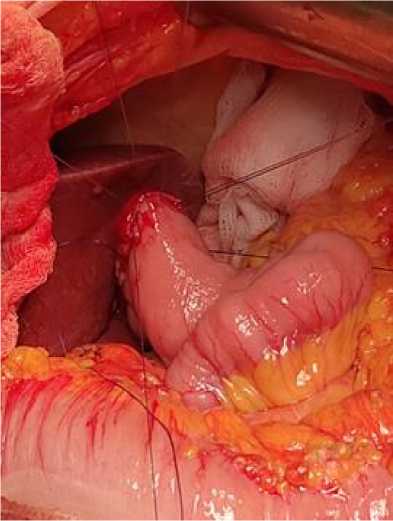
Рис. 6. Вид швов передней стенки перед затягиванием
Fig. 6. Anterior wall sutures before tightening
Завершающим этапом является инвагинация области анастомоза с использованием серозно-мышечных П-образных (салазочных) швов. Первый стежок накладывается на серозную оболочку тонкой кишки параллельно ее продольной оси, второй – перпендикулярно оси пищевода, а третий – снова параллельно оси тонкой кишки. Последовательное затяги- вание швов приводит к инвагинации области анастомоза (рис. 7). В случае затруднений при затягивании швов и недостаточной инвагинации рекомендуется аккуратное мануальное давление на область анастомоза для облегчения ее погружения под П-образный шов. После проверки на герметичность назоинтестинальный зонд удаляется.
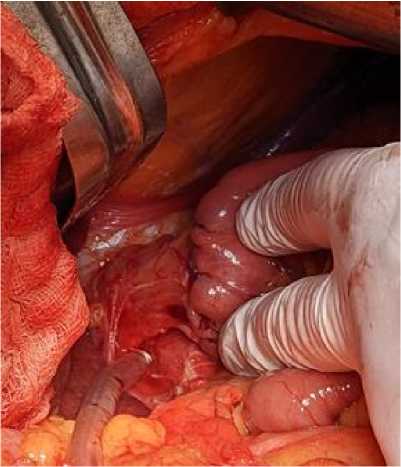
Рис. 7. Последовательное затягивание швов, инвагинация зоны анастомоза
Fig. 7. Sequential suture tightening and anastomosis invagination
Для оценки функциональных результатов 35 пациентам из выборки было выполнено рентгенологическое исследование проходимости пищевода с рентгенконтрастным веществом, а 5 пациентам – сцинтиграфия с техне-цием-99m. Степень тяжести послеоперационных осложнений, возникших в течение первых 30 сут после операции, определялась по классификации Clavien – Dindo. Для оценки отдаленных результатов лечения проводилась эзофагогастродуоденоскопия с верификацией данных по Лос-Анджелесской классификации.
Результаты. В исследование включены 74 пациента, которым выполнена тотальная гастрэктомия с D2-лимфодиссекцией и формирова- нием эзофагоеюноанастомоза ручным способом по предложенной методике, на которую получен патент РФ [12]. Интраоперационная проба на герметичность в отдельных случаях требовала усиления линии шва дополнительными серозно-мышечными швами. В раннем послеоперационном периоде несостоятельности анастомоза не зарегистрировано (0 %).
Клинико-демографические показатели исследуемых пациентов представлены в табл. 1, клинические и онкологические параметры оперативного лечения – в табл. 2, послеоперационные осложнения – в табл. 3, результаты эндоскопической оценки зоны анастомоза через 6 и 12 мес. – в табл. 4.
Таблица 1
Table 1
Clinical and demographic parameters of patients
|
Стадия TNM TNM stage |
Т1, n (%) |
3 (4,1), |
|
Т2, n (%) |
4 (5,4), |
|
|
Т3a, n (%) |
28 (37,8) |
|
|
Т3b, n (%) |
21 (28,4) |
|
|
T4b, n (%) |
10 (13,5) |
|
|
T4b, n (%) |
8 (10,8) |
|
|
N0, n (%) |
30 (40,5) |
|
|
N1, n (%) |
22 (29,7) |
|
|
N2, n (%) |
20 (27,1) |
|
|
N3, n (%) |
2 (2,7) |
|
|
M0, n (%) |
74 (100) |
|
|
M1, n (%) |
0 |
|
|
Получили 4 курса неоадьюватной полихимиотерапии, n (%) Patients who underwent four courses of neoadjuvant polychemotherapy, n (%) |
65 (87,8) |
|
Таблица 2
Table 2
Клинические и онкологические параметры оперативного леченияClinical and oncological parameters of surgical treatment
|
Показатель Parameter |
Значение Value |
|
Время операции, мин, M±SD Operation time, min, M±SD |
224,8±29,4 |
|
Кровопотеря, мл, M±SD Blood loss, ml, M±SD |
318,7±88,9 |
|
Время формирования ЭЕА, мин, M±SD Esophagojejunal anastomosis formation time, min, M±SD |
34,7±7,9 |
|
Удаленные лимфоузлы, абс., Me [Q1; Q3] Lymph nodes removed, abs., Me [Q1; Q3] |
29 [23;37] |
Таблица 3
Table 3
Послеоперационные исходы (30 сут) по Clavien – Dindo, n (%)30-day postoperative outcomes according to the Clavien – Dindo classification, n (%)
|
Показатель Parameter |
Значение Value |
|
Grade 0-I |
56 (75,7) |
|
Grade II |
10 (13,5) |
|
Grade IIIa |
3 (4) |
|
Grade IIIb |
2 (2,7) |
|
Grade IVa |
2 (2,7) |
|
Grade IVb |
0 (0) |
|
Grade V |
1 (1,4) |
|
Grade II-V |
18 (24,3) |
Таблица 4
Table 4
|
Показатель Parameter |
Значение Value |
|
Через 6 мес. 6-month follow-up |
|
|
N (норма / norm) |
34 (45,9) |
|
LA A |
21 (28,4) |
|
LA B |
12 (16,2) |
|
LA C |
5 (6,8) |
|
LA D |
2 (1,4) |
|
Любые изменения A–D Any changes A–D |
40 (54,1) |
|
Клинически значимые C–D Clinically significant C–D |
7 (9,5) |
|
Через 12 мес. 12-month follow-up |
|
|
N (норма / norm) |
41 (55,4) |
|
LA A |
15 (20,3) |
|
LA B |
8 (10,8) |
|
LA C |
3 (4,1) |
|
LA D |
0 (0) |
|
Любые изменения A–D Any changes A–D |
27 (36,5) |
|
Клинически значимые C–D Clinically significant C–D |
3 (4,1) |
Клинико-демографическая характеристика пациентов
Результаты эндоскопического исследования (LA‐классификация), n (%) Endoscopic findings (LA classification), n (%)
При оценке эндоскопических данных через 6 и 12 мес. отмечается снижение частоты и степени эзофагита, что свидетельствует о благоприятном течении послеоперационного периода.
Для оценки функционального заброса желчи выборочно проведена сцинтиграфия с технецием-99m. Ни у одного из 5 пациентов не было обнаружено признаков заброса.
На рис. 8 можно видеть зоны накопления желчи, обозначенные оранжевым цветом (1), и сине-фиолетовое «рассеивание» (2) препарата при сцинтиграфии, которые не распространялись выше зоны анастомоза, что демонстрирует его антирефлюкс-ные свойства.
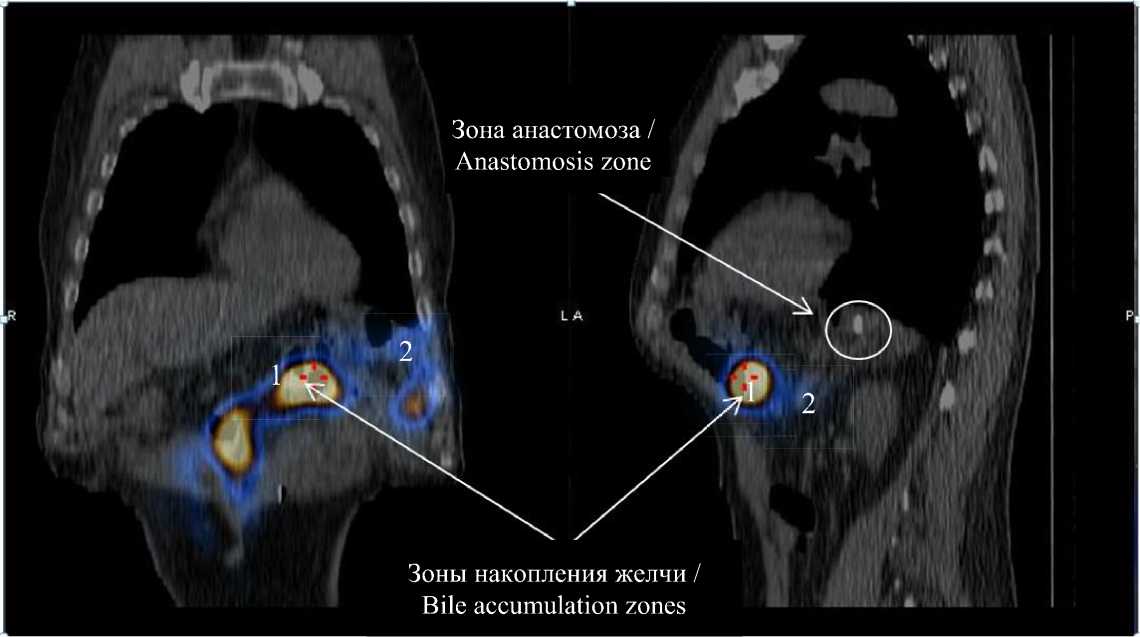
Рис. 8. Проведение сцинтиграфии: 1 – зоны накопления желчи, 2 – зоны рассеивания препарата
Fig. 8 . Scintigraphy: 1 – bile accumulation zones, 2 – drug dispersion zones
Дополнительно для оценки состоятельности и функционального статуса ЭЕА проведена рентгенография с водорастворимым контрастом на 7–10-е сут после оперативного лечения (рис. 9). В анализ было включено 35 пациентов.
Во всех случаях контрастная взвесь свободно проходила через анастомоз без задержек и признаков анастомозита. При повышении внутри-брюшного давления на вдохе рефлюкса контрастного вещества не отмечено.
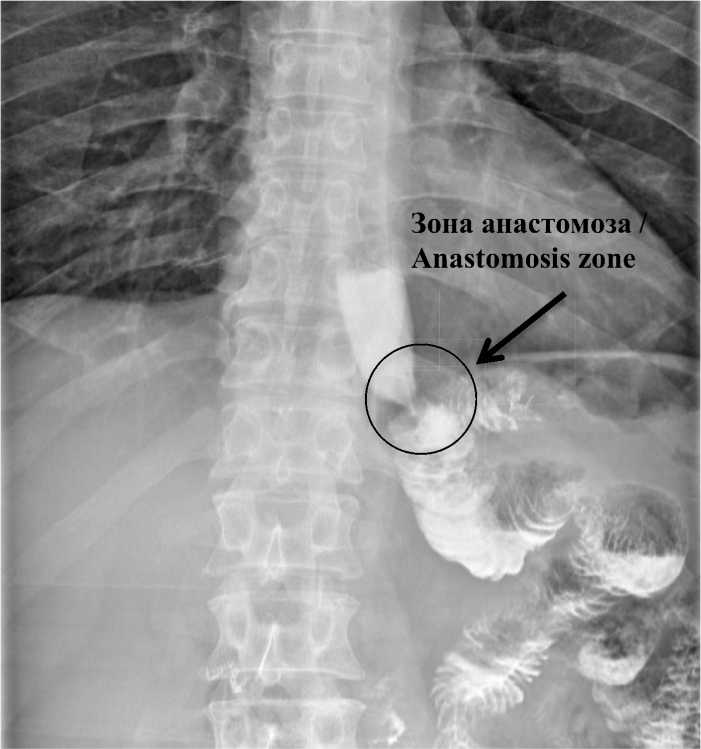
Рис. 9. Рентгенография пациента на 8-е сут после оперативного лечения, Снимок сделан на вдохе
Fig. 9. Patient’s X-ray, postoperative day 8. The image was taken while inhaling
Обсуждение. Формирование ЭЕА после тотальной гастрэктомии остается одним из наиболее важных этапов вмешательства, так как определяет частоту развития послеоперационных осложнений и качество жизни пациентов. На сегодняшний день описано множество техник наложения ЭЕА, каждая из которых имеет как преимущества, так и ограничения [4, 5]. Основные проблемы, требующие решения, – это профилактика несостоятельности швов и рефлюкс-эзофагита, а также обеспечение адекватной проходимости анастомоза.
Предложенный в настоящем исследовании способ формирования ЭЕА позволяет достичь прочного, герметичного и физиологически выгодного соединения за счет постепенного погружения линии шва в просвет кишки. Использование зонда во время затягивания швов способствует сохранению оптимального диаметра анастомоза и предотвращает его сужение.
Отсутствие развития несостоятельности анастомоза (0 %) и низкая частота осложнений IIIb-V степени по Clavien – Dindo (6,8 %) свидетельствуют о высокой надежности и воспроизводимости предложенного метода. Полученные показатели сопоставимы с опубликованными результатами для аппаратных и ручных анастомозов, где частота несостоятельности колеблется от 1,5 % до 7 % [1–3]. Функциональные исходы характеризуются благоприятным антирефлюксным профилем. Доля пациентов без эндоскопических признаков эзофагита увеличилась с 45,9 % до 55,4 % за год наблюдения, а количество больных с клинически значимыми формами (LA C–D) не превышало 4,1 %. Эти результаты сопоставимы с данными специализированных центров, где при тщательном соблюдении техники наблюдаются незначительное число случаев несостоятельности и осложнения невысокой тяжести [13].
Дополнительным преимуществом метода является его техническая простота и возможность выполнения в условиях ограниченного доступа без необходимости применения дорогостоящих сшивающих аппаратов. За- траты на нити ПГА на все этапы формирования анастомоза составили около 4 тыс. руб., тогда как стоимость циркулярного сшивающего аппарата достигает 35 тыс. руб. То есть имеет место экономия средств более чем в 8 раз [6, 14].
Таким образом, полученные результаты демонстрируют устойчивую тенденцию к снижению частоты осложнений и улучшению функциональных исходов, что позволяет рассматривать предложенный способ как один из вариантов формирования ЭЕА после гастрэктомии.
Использование сцинтиграфии является информативным и неинвазивным методом оценки дуоденогастроэзофагеального рефлюкса, позволяющим объективно подтвердить или исключить заброс желчи в просвет пищевода [15]. Именно желчные кислоты и панкреатические ферменты рассматриваются как основные повреждающие факторы, способствующие развитию рефлюкс-эзофагита после гастрэктомии.
Реконструкция пищеварительного тракта по типу Ру-петли традиционно считается ан-тирефлюксной [16]. Однако, как показано в ряде исследований, она не обеспечивает полной защиты, а частота выявления желчного рефлюкса после гастрэктомии с реконструкцией по Ру составляет от 10 до 30 % случаев в зависимости от длины петли и техники анастомозирования [17, 18]. В проведенном исследовании полное устранение желчного рефлюкса подтверждено у 5 пациентов: по данным сцинтиграфии, распространения радиофармпрепарата выше уровня анастомоза не наблюдалось ни у одного из пяти исследованных пациентов.
Операционная эффективность метода остается клинически приемлемой: среднее время наложения анастомоза составило 34,7±7,9 мин. Этот показатель выше, чем у механических способов, однако дополнительное время компенсируется контролем над слоями сшиваемых слизистых и воспроизводимой адаптацией подслизистого слоя, что обеспечивает более благоприятные условия для репарации [19, 20].
Заключение. Представленный способ формирования ЭЕА обеспечивает надежную герметичность, минимизирует риск развития несостоятельности и рефлюкс-эзофагита, а также характеризуется технической возпроиз-водимостью. Он позволяет достигать приемлемых ближайших хирургических и отдаленных функциональных результатов.


