Способ синтеза бензолсульфоната тетра(пара-толил)стибония из хлорида тетра(пара-толил)стибония и бензолсульфоновой кислоты
Автор: Шарутин Владимир Викторович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 4 т.14, 2022 года.
Бесплатный доступ
Взаимодействием хлорида тетра(пара-толил)стибония p-Tol4SbCl (1) с бензолсульфоновой кислотой в воде синтезирован бензолсульфонат тетра(пара-толил)стибония p-Tol4SbOSO2Ph (2). Строение соединений 1, 2 установлено методом рентгеноструктурного анализа (РСА). По данным РСА, хлорид тетра(пара-толил)стибония p-Tol4SbCl (1) [C28H28ClSb, M = 521,70; моноклинная сингония, пр. гр. P21/n; параметры ячейки: a = 9,786(3) Å, b = 23,168(8) Å, c = 12,026(5) Å; a = 90,00°, β = 113,689(16)°, g = 90,00°, V = 2496,6(16) Å3, Z = 4; r(выч.) = 1,388 г/см3; m = 1,224 мм-1; F(000) = 1056,0; обл. сбора по 2q: 6,44-56,72°; -13 ≤ h ≤ 13, -30 ≤ k ≤ 30, -15 ≤ l ≤ 15; всего отражений 59454; независимых отражений 6189 (Rint = 0,0394); GOOF = 1,055; R-фактор 2,72 %] имеет молекулярное строение с искаженной тригонально-бипирамидальной координацией атома сурьмы (углы CSbC варьируются в пределах 96,12(8)-124,83(8)°, аксиальный угол CSbCl составляет 174,91(6)°, расстояния Sb-C и Sb-Cl составляют 2,107(2)-2,170(2) и 2,7230(13) Å). Аналогичное строение имеет бензолсульфонат тетра(пара-толил)стибония p-Tol4SbOSO2Ph (2) [C34H33O3SSb, M = 643,1; ромбическая сингония, пр. гр. Pbca; параметры ячейки: a = 9,923(8) Å, b = 18,923(16) Å, c = 32,72(3) Å; a = 90,00°, β = 90,00°, g = 90,00°, V = 6146(9) Å3, Z = 8; r(выч.) = 1,391 г/см3; m = 0,997 мм-1; F(000) = 2624,0; обл. сбора по 2q: 5,954-56,644°; -8 ≤ h ≤ 12, -25 ≤ k ≤ 25, -43 ≤ l ≤ 43; всего отражений 73682; независимых отражений 7553 (Rint = 0,0589); GOOF = 1,076; R-фактор 4,93 %, углы CSbC варьируются в пределах 97,72(14)-118,77(15)°, аксиальный угол CSbO составляет 176,44(13)°, расстояния Sb-C и Sb-O составляют 2,105(4)-2,150(4) и 2,409(3) Å]. Полные таблицы координат атомов, длин связей и валентных углов соединений 1 и 2 депонированы в Кембриджском банке структурных данных (CCDC 2167562 и 2126493; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Хлорид, бензолсульфонат, тетра(пара-толил)стибоний, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147239536
IDR: 147239536 | УДК: 546.865+547.53.024+548.312.5 | DOI: 10.14529/chem220406
Synthesis method of tetra(para-tolyl)stibonium benzenesulfonate from tetra(para-tolyl)stibonium chloride and benzenesulphonic acid
The interaction of tetra(para-tolyl)stibonium chloride p-Tol4SbCl (1) with benzenesulfonic acid was used to synthesize tetra(para-tolyl)stibonium benzenesulfonate p-Tol4SbOSO2Ph (2). The structure of compounds 1, 2 was established by X-ray diffraction analysis (XRD). According to XRD data, tetra(para-tolyl)stibonium chloride p-Tol4SbCl (1) [C28H28ClSb, M = 521,70; monoclinic syngony, sp. gr. P21/n; cell parameters: a = 9.786(3) Å, b = 23.168(8) Å, c = 12.026(5) Å; a = 90.00°, β = 113.689(16)°, g = 90.00°, V = 2496.6(16) Å3, Z = 4; r(calc.) = 1.388 g/cm3; m = 1.224 mm-1; F(000) = 1056.0; region 2q collection: 6.44-56.72°; -13 ≤ h ≤ 13, -30 ≤ k ≤ 30, -15 ≤ l ≤ 15; total reflections 59454; independent reflections 6189 (Rint = 0.0394); GOOF = 1.055; R-factor 2.72%] has a molecular structure with a distorted trigonal-bipyramidal coordination of the antimony atom (the CSbC angles vary within 96.12(8)-124.83(8)°, the CSbCl axial angle is 174.91(6)°, the Sb-C and Sb-Cl distances are 2.107(2)-2.170(2) and 2.7230(13) Å). Tetra(para-tolyl)stibonium benzenesulfonate p-Tol4SbOSO2Ph (2) [C34H33O3SSb, M = 643,1; rhombic system, sp. gr. Pbca; cell parameters: a = 9.923(8) Å, b = 18.923(16) Å, c = 32.72(3) Å; a = 90.00°, β = 90.00°, g = 90.00°, V = 6146(9) Å3, Z = 8; r(calc.) = 1.391 g/cm3; m = 0.997 mm-1; F(000) = 2624.0; region collection for 2q: 5.954-56.644°; -8 ≤ h ≤ 12, -25 ≤ k ≤ 25, -43 ≤ l ≤ 43; total reflections 73682; independent reflections 7553 (Rint = 0.0589); GOOF = 1.076; R-factor 4.93%, the CSbC angles vary within 97.72(14)-118.77(15)°, the CSbO axial angle is 176.44(13)°, the Sb-C and Sb-O distances are 2.105(4)-2.150(4) and 2.409(3) Å] has similar structure. Complete tables of atomic coordinates, bond lengths, and bond angles for compounds 1 and 2 have been deposited with the Cambridge Crystallographic Data Centre (CCDC 2167562 and 2126493) and are available, free of charge, at deposit@ccdc.cam.ac.uk and http://www.ccdc.cam.ac.uk.
Текст научной статьи Способ синтеза бензолсульфоната тетра(пара-толил)стибония из хлорида тетра(пара-толил)стибония и бензолсульфоновой кислоты
Возрастающий интерес к органическим соединениям сурьмы во многом определяется растущим потенциалом их применения в самых разнообразных областях практической деятельности: в качестве лекарственных препаратов, биоцидов, фунгицидов, в качестве реагентов и компонентов каталитических систем при полимеризации, в тонком органическом синтезе, в качестве антиоксидантов и др. [1]. Одними из наиболее исследованных сурьмаорганических соединений являются фенильные производные пятивалентной сурьмы общей формулы Ph 4 Sb]X (Х – электроотрицательная группа) [2]. В меньшей степени изучены подобные толильные производные [3 - 24]. С целью расширения экспериментального материала по данному направлению в настоящей работе изучена реакция хлорида тетра( пара -толил)стибония ( 1 ) с бензолсульфоновой кислотой, един-ственым сурьмаорганическим продуктом которой является бензолсульфонат тетра( пара -толил)стибония ( 2 ). Для комплексов 1 и 2 приведены результаты рентгеноструктурного исследования.
Экспериментальная часть
Синтез бензолсульфоната тетра( пара -толил)стибония p -Tol 4 SbOSO 2 Ph (2). К раствору 261 мг (0,50 ммоль) хлорида тетра( пара -толил)стибония ( 1 ) в 15 мл воды прибавляли при перемешивании раствор 79 мг (ммоль) бензолсульфоновой кислоты в 5 мл воды. После испарения воды из фильтрата получили 310 мг (97 %) бесцветных кристаллов комплекса 2 с т. пл. 146 ° С .
ИК-спектр ( ν , см–1): 1280 ср.,1170 оч.с.,1130 с. (SO 2 ). Найдено, %: C 63,26; H 5,20. C 34 H 33 O 3 SSb. Вычислено, %: C 63,45; H 5,13.
ИК-спектр соединения 2 записывали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S; образец готовили таблетированием с KBr (область поглощения 4000 - 400 см - 1).
Рентгеноструктурный анализ проводили на автоматическом четырехкружном дифрактометре Bruker D8 QUEST (Mo K α -излучение, λ = 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [25]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [26] и OLEX2 [27]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структур приведены в табл. 1.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1 и 2
|
Параметр |
1 |
2 |
|
Формула |
C 28 H 28 ClSb |
C 34 H 33 O 3 SSb |
|
М |
521,70 |
643,41 |
|
Сингония |
Моноклинная |
Ромбическая |
|
Пространственная группа |
P 2 1 / n |
Pbca |
|
a , Å |
9,786(3) |
9,923(8) |
|
b, Å |
23,168(8) |
18,932(16) |
|
c, Å |
12,026(5) |
32,72(3) |
|
α, град. |
90,00 |
90,00 |
|
β , град. |
113,689(16) |
90,00 |
|
γ , град. |
90,00 |
90,00 |
|
V , Å3 |
2496,6(16) |
6146(9) |
|
Z |
4 |
8 |
|
ρ (выч.), г/см3 |
1,388 |
1,391 |
|
µ , мм–1 |
1,224 |
0,997 |
|
F (000) |
1056,0 |
2624,0 |
|
Форма кристалла (размер, мм) |
0,47 × 0,32 × 0,1 |
0,21 × 0,2 × 0,13 |
|
Область сбора данных по 2 θ , град. |
6,44–56,72 |
5,954–56,644 |
|
Интервалы индексов отражений |
–13 ≤ h ≤ 13, –30 ≤ k ≤ 30, –15 ≤ l ≤ 15 |
–8 ≤ h ≤ 12, –25 ≤ k ≤ 25, –43 ≤ l ≤ 43 |
|
Измерено отражений |
59454 |
73682 |
|
Независимых отражений ( R int ) |
6189 (0,0394) |
7553 (0,0589) |
|
Отражений с I > 2 σ ( I ) |
5133 |
4775 |
|
Переменных уточнения |
275 |
359 |
|
GOOF |
1,055 |
1,076 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0272, wR 2 = 0,0581 |
R 1 = 0,0493, wR 2 = 0,0981 |
|
R -факторы по всем отражениям |
R 1 = 0,0383, wR 2 = 0,0620 |
R 1 = 0,0955, wR 2 = 0,1148 |
|
Остаточная электронная плотность (min/max), e /Å3 |
–0,52/0,23 |
–0,58/0,60 |
Полные таблицы координат атомов, длин связей и валентных углов соединения 1 и 2 депонированы в Кембриджском банке структурных данных (№ 2167562 и 2126493; ; .
Обсуждение результатов
Известно, что реакции обмена галогенид-аниона в галогенидах тетраарилстибония используются для получения различных комплексов металлов [2]. Интересный случай замещения гало-генид-аниона на остаток более сильной кислоты описан авторами работы [28], в которой описываются реакции галогенидов органилтрифенилфосфония с аренсульфоновыми кислотами в воде, приводящие к образованию аренсульфонатов органилтрифенилфосфония.
В продолжение исследований в области реакций замещения галогенид-аниона в арильных производных сурьмы изучена реакция хлорида тетра( пара -толил)стибония ( 1 ) с бензолсульфоновой кислотой. Показано, что единственным продуктом указанной реакции является бензолсуль-фонат тетра( пара -толил)стибония p -Tol 4 SbOSO 2 Ph ( 2 ):
p -Tol 4 SbCl + HOSO 2 Ph p -Tol 4 SbOSO 2 Ph + HCl
Строение хлорида тетра( пара -толил)стибония 1 (рис. 1) с низкими значениями R -фактора было ранее описано в [3, 4]; в настоящей работе его структура уточнена до R = 2,7 %. Комплекс имеет молекулярное строение с искаженной тригонально-бипирамидальной координацией атома сурьмы (углы CSbC варьируются в пределах 96,12(8) - 124,83(8) ° , аксиальный угол CSbCl составляет 174,91(6) ° , расстояния Sb-C и Sb - Cl составляют 2,107(2)-2,170(2) и 2,7230(13) А).
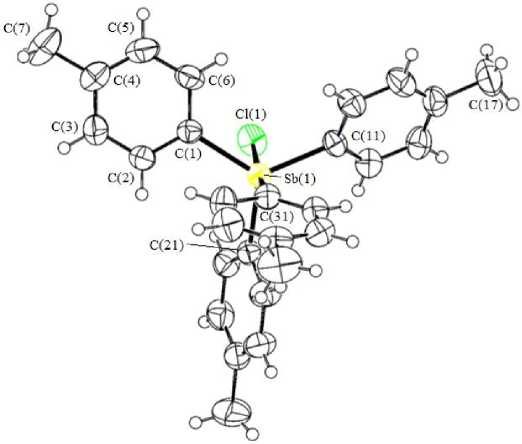
Рис. 1. Строение хлорида тетра( пара -толил)стибония p -Tol 4 SbCl (1)
О структуре комплекса 2 (рис. 2) ранее сообщалось в работах [6 - 8].
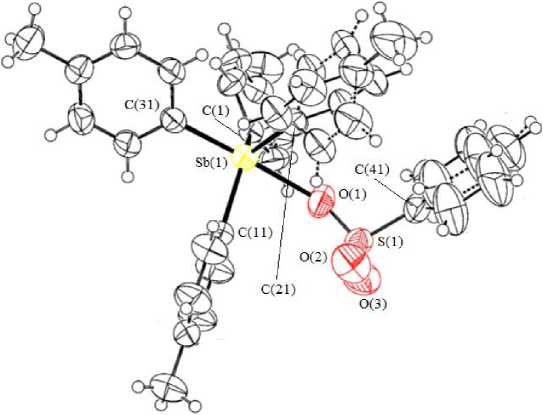
Рис. 2. Строение бензолсульфоната тетра( пара -толил)стибония p -Tol 4 SbOSO 2 Ph (2)
По данным РСА, молекулы 2 имеют тригонально-бипирамидальное строение. Сульфонатная группа находится в аксиальном положении, что полностью согласуется с теорией отталкивания электронных пар валентных орбиталей, причем наблюдаемая длина связи Sb–О (2,409(3) Å) превосходит сумму ковалентных радиусов связанных между собой атомов (2,14 Å [29]). Углы CSbC варьируются в пределах 97,72(14) - 118,77(15) ° , аксиальный угол CSbO составляет 176,44(13) ° , расстояния Sb–C составляют 2,105(4)–2,150(4) Å.
Заключение
Таким образом, впервые по реакции замещения из хлорида тетра( пара -толил)стибония ( 1 ) и бензолсульфоновой кислоты получен бензолсульфонат тетра( пара -толил)стибония ( 2 ) с выходом 97 %; строение комплексов 1 и 2 доказано методом рентгеноструктурного анализа.
Список литературы Способ синтеза бензолсульфоната тетра(пара-толил)стибония из хлорида тетра(пара-толил)стибония и бензолсульфоновой кислоты
- Кочешков К.А., Сколдинов А.П., Землянский Н.Н. Методы элементоорганической химии. Сурьма, висмут. М.: Наука, 1976. 483 с.
- Шарутин В.В., Поддельский А.И., Шарутина О.К. Синтез, реакции и строение арильных соединений пятивалентной сурьмы // Коорд. химия. 2020. Т. 46, № 10. С. 579-648. DOI: 10.31857/S0132344X20100011.
- Кристаллическая структура C28H28ClSb / К.Н. Акатова, Р.И. Бочкова, В.А. Лебедев и др. // Докл. АН СССР. 1983. Т. 268, № 6. С. 1389-1391.
- Строение галогенидов тетраарилсурьмы и изотиоцианата тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др. // Коорд. химия. 2005. Т. 31, № 2. С. 117-124.
- Синтез и строение Д^-диметилдитиокарбаматов тетрафенилсурьмы и тетра-п-толилсурьмы / В.В. Шарутин, О.К. Шарутина, Т.П. Платонова и др. // Коорд. химия. 2003. Т. 29, № 1. С. 13-17.
- Сульфонаты тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, Л.П. Панова, В.К. Бельский // Журн. общ. химии. 1997. Т. 67, № 9. С. 1531-1535.
- Синтез и строение 4-метилбензолсульфоната тетра-п-толилсурьмы / В.В. Шарутин, А.П. Пакусина, И.В. Егорова и др. // Коорд. химия. 2003. Т. 29, № 5. С. 336-340.
- Реакции пентаарилсурьмы с диацилатами триарилсурьмы / В.В. Шарутин, О.К. Шарутина, A.П. Пакусина, В.К. Бельский // Журн. общ. химии. 1997. Т. 67, № 9. С. 1536-1541.
- Синтез и строение 4-метилбензолсульфоната тетра-п-толилсурьмы / В.В. Шарутин, О.К. Шарутина, Т.А. Тарасова, А.Н. Харсика, В.К. Бельский // Журн. общ. химии. 1999. Т. 69, № 12. С. 1979-1981.
- Внедрение триоксида серы по связи Sb-C в пентаарилсурьме / В.В. Шарутин, О.К. Шарутина, Т.П. Платонова и др. // Журн. общ. химии. 2000. Т. 70, № 11. С. 1932.
- Синтез и строение оксиматов тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, О.В. Молокова и др. // Коорд. химия. 2002. Т. 28, № 8. С. 581-590.
- Синтез и строение оксиматов тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, О.В. Молокова и др. // Журн. общ. химии. 2001. Т. 71, № 8. С. 1317-1321.
- Арокситетраарильные соединения сурьмы. Синтез, строение и термическое разложение / B.В. Шарутин, О.К. Шарутина, П.Е. Осипов и др. // Журн. общ. химии. 2000. Т. 70, № 6. С. 931936.
- Сопшина Д.М. Синтез и строение продукта реакции пента-пара-толилсурьмы с гептаф-торпропил(г-бутил)дикетоном-1,3 ^-Tol4Sb[^BuC(O)СHС(О)С3F7] // Вестник ЮУрГУ. Сер. «Химия». 2022. Т. 14, № 1. С. 50-58. DOI: 10.14529/chem220106.
- Ефремов А.Н., Шарутин В.В. Реакции пентафенилсурьмы и пента(пара-толил)сурьмы с каликсареном [4-i-BuC6H2OH(S-2)]4 // Вестник ЮУрГУ. Сер. «Химия». 2021. Т. 13, № 1. С. 4757. DOI: 10.14529/chem210105.
- Шарутина О.К. Ферроценкарбоксилат тетра(пара-толил)сурьмы. Синтез и строение // Вестник ЮУрГУ. Сер. «Химия». 2021. Т. 13, № 4. С. 63-71. DOI: 10.14529/chem210404.
- Сенчурин В.С., Орленко Е.Д. 4-Нитрофенилацетаты тетра- и три(пара-толил)сурьмы. Синтез и особенности строения // Вестник ЮУрГУ. Сер. «Химия». 2019. Т. 11, № 2. С. 66-74. DOI: 10.14529/chem190207.
- Синтез и строение фторбензоатов тетра- и триарилсурьмы. / В.В. Шарутин, О.К. Шарути-на, Е.А. Бондарь и др. // Коорд. химия. 2002. Т. 28, № 5. С. 356-363.
- Синтез и строение пентафтор- и пентахлорфеноксидов тетра- и триарилсурьмы / В.В. Шарутин, О.К. Шарутина, А.Н. Ефремов, П.В. Андреев // Журн. неорг. химии. 2017. Т. 62, № 10. С. 1330-1336. DOI: 10.7868/S0044457X17100075.
- Шарутин В.В., Шарутина О.К. Синтез и строение производных тетра(пара-толил)сурьмы (4-МеСбЩ^ЬХ, X = OC(O)C6H4(NO2-2), OC(O)C=CPH, ON=CHC6H4(NMe2-4) // Журн. неорг. химии. 2017. Т. 62, № 7. С. 925-929. DOI: 10.7868/S0044457X17070224.
- Синтез и строение комплексов иридия [p-Tol4Sb][p-Tol4Sb(DMSO)][IrBr6]2- и [p-Tol4Sb(DMSO)]+[IrBr4(DMSO)2]- / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин, Н.В. Сомов // Журн. неорг. химии. 2016. Т. 61, № 8. С. 1017-1022. DOI: 10.7868/S0044457X16080146.
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. Исследование кристаллических структур 2,4,6-трихлорфеноксида и 3,4,5-трифторбензоата тетра(п-толил)сурьмы // Журн. структ. химии. 2020. Т. 61, № 9. С. 1490-1497. DOI: 10.26902/JSC_id60682.
- Шарутин В.В., Шарутина О.К., Ефремов А.Н. Арильные сурьмаорганические производные трехкоординированного углерода // Журн. неорг. химии. 2020. Т. 65, № 1. С. 49-55. DOI: 10.31857/S0044457X20010158.
- Фторсодержащие карбоксилаты тетраарилсурьмы. Синтез и строение / В.В. Шарутин, О.К. Шарутина, А.Н. Ефремов, Е.В. Артемьева // Журн. неорг. химии. 2020. Т. 65, № 4. С. 482486. DOI: 10.31857/S0044457X20040170.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data collection and processing software for the SMART system. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An integrated system for solving, refining and displaying crystal structures from diffraction data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea, J.A.K. Howard, H. Puschmann // J. Appl. Cryst. 2009. Vol. 42. P. 339-341. DOI: 10.1107/S0021889808042726.
- Шарутин В.В., Шарутина О.К., Механошина Е.С. Синтез и строение органосульфонатов органилтрифенилфосфония [Ph3PR][OSO2R'], R = Ph, R' = C6H3Cl2-2,5; R = C6Hn-cyclo, R' = C6H3Cl2-2,5; R = CH2OMe, R' = С6ЩШ2)2-2,4; R = CH2OMe, R' = C6H4COOH-2) // Вестник ЮУрГУ. Сер. «Химия». 2022. Т. 14, № 2. С. 41-51. DOI: 10.14529/chem220205.
- Covalent radii revisited / B. Cordero, V. Gómez, A.E. Platero-Prats et al. // Dalton Trans. 2008. P. 2832-2838. DOI: 10.1039/B801115J.


