Сравнительная характеристика болевой и обонятельной чувствительности у лиц с аффективными и аддиктивными расстройствами
Автор: Савочкина Дарья Николаевна, Невидимова Т.И., Батухтина Е.И., Бохан Н.А., Лебедева Е.В., Редченкова Е.М., Краснятова Ю.А., Абушаева М.О., Баранов И.В.
Журнал: Сибирский вестник психиатрии и наркологии @svpin
Рубрика: Биологические исследования
Статья в выпуске: 2 (87), 2015 года.
Бесплатный доступ
Сенсорные нарушения у лиц с зависимостью от психоактивных веществ и лиц с депрессивными расстройствами имеют различный характер.
Алгометрия, ольфактометрия, депрессия, аддикция
Короткий адрес: https://sciup.org/14295817
IDR: 14295817 | УДК: 616.895.4:616.8-009.7
Comparative characterization of nociceptive and olfactory sensitivity in persons with affective and addictive disorders
Sensory disturbances in drug dependent persons and persons with depressive disorders have different manifestations.
Текст научной статьи Сравнительная характеристика болевой и обонятельной чувствительности у лиц с аффективными и аддиктивными расстройствами
чувствительности, поскольку пороги боли используются для экспертной оценки алгических синдромов разного генеза и эффективности обезболивающей терапии, а также могут быть использованы для оценки течения психических расстройств. Психические расстройства могут сопровождаться развитием болевых синдромов. Наиболее часто хроническая боль сочетается с депрессией. У 30—40 % пациентов с хроническими болевыми синдромами диагностируется депрессия в соответствии с принятыми диагностическими критериями. Показано, что имеющаяся у пациента депрессия приводит к возникновению того или иного болевого синдрома – так называемого синдрома «депрессия – боль». Обсуждаются три возможных механизма взаимосвязи боли и депрессии: длительно существующий болевой синдром приводит к развитию депрессии; депрессия предшествует возникновению болевого синдрома; депрессия и боль развиваются независимо друг от друга и существуют параллельно [1, 7, 11, 16].
Имеются исследования, подтверждающие разные представления о взаимосвязи боли и депрессии. Установлено, что депрессия приводит к эмоциональной дисфункции в интерпретации боли у пациентов с хронической болью, не влияя при этом на пороги чувствительности [13]. В ряде работ выдвинуто предположение, что депрессивный или недепрессивный фон настроения влияет на поведенческий компонент ответа на болевой стимул, а не на интенсивность болевых ощущений, т. е. определяет способность справляться с болью [2]. В эксперименте показано, что длительная невропатическая боль приводит к тревожнодепрессивным поведенческим реакциям, которые более выражены, чем снижение порогов болевой чувствительности [8]. При расстройствах депрессивного спектра обнаруживается недостаточность обоняния как проявление ан-гедонии, его обострение при сезонных аффективных расстройствах, формирование какосмии – ощущения неприятных запахов при отсутствии адекватных раздражителей [19, 10, 21, 15].
Длительное употребление опиоидов приводит к повышению болевой чувствительности – возникновению опиоидно-индуцированной ги-пералгезии. Показано, что как у героиновых наркоманов, так и у лиц, находящихся на длительной терапии наркотическими анальгетиками, наблюдается снижение порогов болевой чувствительности [14, 20, 9, 22]. К предполагаемым механизмам опиоидно-индуцированной гипералгезии относят сенситизацию периферических ноцицепторов, повышенную продукцию глутамата и нейропептидов в спинном мозге, протеин киназу Су-индуцированный сигналинг, участие хемокинов [23]. В эксперименте показано, что систематическое введение антагони- ста кортикотропин-рилизинг-фактора приводит к снижению гиперчувствительности у крыс с героиновой или алкогольной зависимостью [17]. Обсуждается гипотеза, согласно которой при хроническом введении морфина происходит постепенное увеличение активности энке-фалиназы, как ответной реакции организма на постоянное повышение выделения эндогенных опиоидов вследствие хронических экзогенных воздействий. Возрастание активности фермента приводит к увеличению скорости дезактивации эндогенных опиоидов и тем самым к исчезновению их аналгетического эффекта и развитию состояния толерантности [3]. Этими же авторами показано, что у героиновых наркоманов в динамике протекания абстинентного синдрома наблюдается снижение порогов ноцицептивных реакций, сочетающееся с увеличением энкефалиназной активности.
При депрессии наблюдаются совокупные нарушения обоняния и вкуса [21]. При комор-бидных депрессивных и аддиктивных расстройствах встречаются случаи пикацизма – поедания несъедобного, сопровождающегося извращением вкуса и обоняния. У подростков подобного рода нарушения не только свидетельствуют о нарушении минерального обмена, но и трактуются как обсессивно-компульсивное расстройство, скрытая депрессия. Нарушение восприятия вкусовых ощущений (агевзия) при депрессиях входит в структуру синдрома отчуждения витальных чувств. Нарушения вкусовой чувствительности и аппетита при депрессии связывают с выраженностью тревоги, с уровнем серотонина и норадреналина, иногда с побочными эффектами терапии. Вместе с тем антидепрессанты способны повышать вкусовую и обонятельную чувствительность [4, 18].
Целью исследования было проведение сравнительной оценки болевой и обонятельной чувствительности у лиц с психическими и поведенческими расстройствами, вызванными употреблением психоактивных веществ, и у лиц с депрессивными расстройствами.
Материалы и методы. Было обследовано 24 человека мужского пола с признаками психических и поведенческих расстройств, вызванных употреблением психоактивных веществ (F1x.2), в период постабстинентного состояния. Группу сравнения для пациентов с зависимостью от психоактивных веществ составили 25 условно здоровых лиц мужского пола, сопоставимых по возрасту. В качестве дополнительной группы были выбраны ранее обследованные 89 лиц женского пола с депрессивным эпизодом и рекуррентным депрессивным расстройством (F32, F33 соответственно) до проведения анти-депрессивной терапии. Для лиц с депрессивными расстройствами группой сравнения были 20 женщин сопоставимого возраста без психи- ческих расстройств и соматической патологии в стадии обострения.
Пороги болевой чувствительности и переносимость боли определялись с помощью запатентованного нами собственного варианта тен-зоалгометрии (ТАМ) [5]. Параллельно использовали алгометр (Commander Algometer JTECH Medical, США). Для оценки пороговой обонятельной чувствительности в нашем исследовании использовали ольфактометрический тест AST (Davidson T. M. et al., 1997). Использовалась одноразовая дезинфицирующая салфетка с раствором спирта (изопропиловый спирт 70 %) производства ООО «Фирма «ВИПС-МЕД», Московская обл., г. Фрязино. Пороговая чувствительность измеряется в сантиметрах и соответствует расстоянию, на котором испытуемый чувствует запах изопропилового спирта. Кроме того, исследовали обонятельную чувствительность к запахам андростенона, тимола, изопропанола и оценивали эмоциональное восприятие данных запахов с помощью визуально-аналоговой шкалы (ВАШ) в условных единицах.
Клинико-анамнестическим методом выявляли потребность в зрительной, слуховой стимуляции и склонность к поиску ощущений, сопряженных с риском. Для оценки состояния вегетативной нервной системы учитывали результаты кожно-сосудистой реакции (дермографизм). Фиксировали время появления розового дермографизма в секундах. Оценивали ситуационную и личностную тревожность по Спилбергеру-Ханину.
При проведении исследования были соблюдены принципы информированного согласия Хельсинкской декларации Всемирной медицинской ассоциации.
Статистическую обработку результатов проводили с помощью программы STATISTICA 6.0 с использованием непараметрических методов.
Результаты. В результате проведенной тензоалгометрии были оценены пороги болевой чувствительности – минимальное болевое ощущение, которое субъект в состоянии распознать (нижний порог боли) (БН), а также порог переносимости боли (верхний порог боли) (БВ). Результаты двух тензоалгометрических методов выражались в условных единицах (усл. ед.) и ньютонах (N).
Визуально-аналоговая шкала позволяет оценить субъективную оценку верхнего и нижнего порогов болевой чувствительности, а также эмоциональный компонент восприятия запахов при ольфактометрии.
При исследовании болевой чувствительности у лиц, зависимых от психоактивных веществ, обнаружено возрастание нижнего и верхнего порогов болевой чувствительности по сравнению с контрольной группой (табл. 1).
В то же время негативная эмоциональная оценка болевых ощущений и страх боли наблюдаются лишь у пациентов этой группы (p<0,05).
Таблица 1
Параметры тензоалгометрии у зависимых от ПАВ, лиц с аффективными расстройствами и в соответ- ствующих контрольных группах [Median (LQ; UQ)]
|
Показатель |
Контрольная группа для лиц, зависимых от ПАВ (n=25) |
Зависимые от ПАВ лица (n=24) |
Контрольная группа для лиц с депрессивными расстройствами (n=20) |
Лица с депрессивны-ми расстройства-ми (n=89) |
|
Возраст, лет |
20,0 (18,0 ;20,0) |
20,0 (19,0; 24,0) |
51,0 (45,0; 55,0) |
53, 0 (46,0; 59,0) |
|
БН, усл. ед. |
8,5 (8,0; 9,0) |
10,5 (7,0; 12) * |
6,6 (6,0; 7,0) |
7,5 (5,0; 10,0) |
|
БН, N |
19,55 (15,35; 22,15) |
23,75 (20,2; 30,3)* |
12,0 (11,5; 22,0) |
13,6 (11,0; 22,4) |
|
БВ, усл. ед. |
13,0 (11,0; 15,0) |
15,50 (15,0; 16,0)* |
12,3 (12,0; 13,0) |
12,0 (10,0; 15,0) |
|
БВ, N |
36,95 (29,90;47,90) |
51,45 (44,4; 61,6)* |
23,5 (21,5; 25,0) |
25,0 (20,6; 25,8) |
|
ОБ ВАШ, усл. ед. |
5,0 (4,0; 6,0) |
7,5 (4,5; 9,0)* |
6,4 (6,0; 7,0) |
4,0 (2,0; 7,0)* |
|
БН ВАШ, усл. ед. |
2,0 (1,0; 4,0) |
3,5 (2,0; 4,0) |
3,8 (3,0; 4,0) |
2,0 (2,0; 4,0) * |
|
БВ ВАШ, усл. ед |
5,0 (4,0; 6,0) |
6,0 (4,0; 8,0) |
6,5 (6,0; 7,0) |
6,0 (4,0; 8,0) |
Примечание . * – p<0,05 при сравнении с соответствующей контрольной группой по критерию Манна-Уитни, ВАШ – визуально-аналоговая шкала, ОБ – отношение к боли.
В результате алгометрического исследования у лиц с депрессивными расстройствами выявлено незначительное повышение нижнего и верхнего порогов болевой чувствительности и эмоциональную устойчивость к болевым ощущениям.
Клинико-анамнестический анализ группы лиц, имеющих зависимость от психоактивных веществ, выявил возрастание процента случаев наличия потребности в слуховой, зрительной, вестибулярной стимуляции (80,6, 63,9 и 69,0 % соответственно), склонности к поведению, связанному с риском (49,0 %), по сравнению с контрольной группой.
Исследование кожно-сосудистой реакции позволило установить возрастание времени появления розового дермографизма у лиц с зависимостью от ПАВ, что свидетельствует о дисбалансе тонуса симпатической и парасимпатической иннервации кровеносных сосудов и позволяет косвенно оценить наличие стресса (более высокого уровня, чем при депрессивных расстройствах).
Результаты проведенной ольфактометрии представлены в таблице 2. При исследовании обонятельной чувствительности с помощью теста AST было выявлено, что у лиц с зависимостью от психоактивных веществ наблюдается снижение чувствительности к изопропанолу по сравнению с контрольной группой.
Проведенное исследование обонятельной чувствительности у 60 лиц женского пола с депрессивными расстройствами на данном этапе носит описательный характер. Проведенный тест AST выявил значительное снижение порога обонятельной чувствительности у лиц с депрессивными расстройствами, что соответствует гипоосмии. По данным T. M. Davidson et al. (1997), нормальные значения теста AST соответствуют 18—20 см вне зависимости от пола и возраста, поэтому для сравнения была использована контрольная группа молодых лиц мужского пола.
Таблица 2
Сенсорные характеристики у лиц с зависимостью от ПАВ, депрессивных лиц и в контрольной группе [Median (LQ; UQ]
|
Показатель |
Контрольная группа для лиц, зависимых от ПАВ (n=25) |
Зависимые от ПАВ лица (n=24) |
Лица с депрессивны-ми расстройства-ми (n=60) |
|
Андростенон по ВАШ, усл. ед. |
5,0 (3,0; 6,5) |
8,5 (7,0; 9,5)* |
8,0 (4,0; 10,0) |
|
Тимол по ВАШ, усл. ед. |
3,0 (2,0;5,0) |
6,0 (4,0; 8,0)* |
4,0 (3,0; 6,0) |
|
Изопропанол по ВАШ, усл. ед. |
4,0 (3,0; 6,0) |
5,5 (4,0; 7,0) |
6,0 (4,0; 8,0) |
|
Дермографизм, сек |
12,0 (10,0; 14,0) |
24,0 (15,0; 35,0)* |
17,0 (12,0;25,0) |
|
AST, см |
19,0 (5,0; 33,0) |
16,5 (10,0; 33,0) |
10,0 (3,0; 28,0)* |
|
AST по ВАШ, усл. уд. |
4,0 (3,0; 6,0) |
6,0 (4,0; 8,0) |
6,0 (5,0; 7,0) |
Примечание . * – p<0,05 при сравнении с контрольной группой по критерию Манна-Уитни.
При исследовании эмоционального реагирования на запахи изопропанола, тимола и анд-ростенона были выделены лица с наличием и отсутствием аверсии. Наличие аверсивной реакции на запах диагностировалось при выборе испытуемым отметки на визуальноаналоговой шкале от 7 усл. ед. и выше, либо при вербальной оценке запаха как неприятного (отвратительного). Данные ВАШ и вербальной оценки не всегда совпадали.
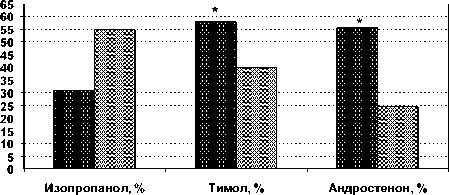
| в Зависимые от ПАВ 0 Лица с депрессией
Рис. 1. Вербальная оценка запахов (отвращение, % случаев) у лиц с зависимостью от ПАВ и депрессивными расстройствами
Примечание. * – p<0,05 при сравнении по критерию Манна-Уитни.
У лиц с зависимостью от ПАВ чаще встречалось отсутствие аверсивной реакции на изопропанол по сравнению с контрольной группой. При проведении обонятельных проб с тимолом и андростеноном среди лиц с зависимостью от ПАВ и депрессивными расстройствами были выявлены различия в эмоциональной оценке данных запахов. Лица с зависимостью от психоактивных веществ демонстрировали значимо большую частоту случаев с оценкой запаха ан-дростенона и тимола как отвратительного при сравнении с контрольной группой.
Заключение. Тестирование сенсорных систем и клинико-анамнестический анализ позволил установить, что лица с зависимостью от психоактивных веществ характеризуются снижением болевой чувствительности, наличием негативной оценки болевых ощущений, аверси-ей на запах изопропанола, увеличением частоты встречаемости потребности в сенсорной стимуляции, поведением, сопряженным с риском, высоким показателем кожно-сосудистой реакции.
У лиц с депрессивными расстройствами наблюдается тенденция к повышению порогов болевой чувствительности, сочетающаяся с эмоциональной толерантностью к боли, снижением порога обонятельной чувствительности.
Таким образом, сенсорные нарушения у лиц с зависимостью от психоактивных веществ и лиц с депрессивными расстройствами имеют различный характер.
Список литературы Сравнительная характеристика болевой и обонятельной чувствительности у лиц с аффективными и аддиктивными расстройствами
- Вознесенская Т. Г., Вейн А. М. Хроническая боль и депрессия//Психиатрия и психофармакология. -2000. -№ 1. -С. 4-7.
- Вейн А. М. Болевые синдромы в неврологической практике. -М., 2001.
- Литвинова С. В., Надеждин А. В., Авдеев С. Н., Хохлов С. Е., Тетенова Е. Ю., Теребилина Н. Н., Панченко Л. Ф., Габаева М. В., Соколов О. Ю., Шульговский В. В. Анализ соотношения порогов ноцицептивных реакций и общей энкефалиназ-ной активности сыворотки крови у больных героиновой наркоманией//Международный Медицинский Журнал. -2000. -№ 5 -С. 54-68.
- Невидимова Т. И. Ольфактометрия в психиатрии//Современные технологии психиатрического и наркологического сервиса/под науч. ред. акад. РАМН В. Я. Семке. -Томск: Изд-во «Иван Федоров», 2011. -Т. 4. -С. 64-65.
- Невидимова, Т. И., Бохан Н. А., Коконова Д. Н. Способ количественной оценки индивидуальных болевых порогов. Патент на изобретение № 2342063. Зарегистрировано в Государственном реестре изобретений 27.12.2008 г.
- Семке В. Я., Счастный Е. Д., Симуткин Г. Г. Аффективные расстройства. Региональный аспект. -Томск, 2004. -234 с.
- Смулевич А. Б. Депрессии в общей медицине. -М.: Медицинское информационное агентство, 2001. -253 с.
- Alba-Delgado C., Llorca-Torralba M., Horrillo I., Ortega J. E., Mico J. A., Sánchez-Blázquez P., Meana J. J., Berrocoso E. Chronic Pain Leads to Concomitant Noradrenergic Impairment and Mood Disorders//Biol. Psychiatry. -2012. -V. 45, № 3. -P. 57-64.
- Aniskin D. B., Fink E., Prosser J., Cohen L. J., Boda N., Steinfeld M., Galynker I. I. The effect of pain on stroop performance in patients with opiate dependence in sustained remission//J. Addict. Med. -2011. -V. 5, № 1. -P. 50-56.
- Atanasova B., Graux J., El Hage W., Hommet C., Camus V., Belzung C. Olfaction: a potential cognitive marker of psychiatric disorders//Neurosci. Biobehav. Rev. -2008. -V. 32 (7). -P. 1315-1325.
- Bair M. J., Robinson R. L., Katon W., Kroenke K. Depression and pain comorbidity: a literature review//Arch. Intern. Med. -2003. -V. 163 (20). -P. 2433-2445.
- Bokhan N. A., Baturin E. V. Gender heteronomy of the formation of heroin addiction in adolescents//Neuroscience and behavioral physiology.
- Bravo L., Mico J. A., Rey-Brea R., Pérez-Nievas B., Leza J. C., Berrocoso E. Depressive-like states heighten the aversion to painful stimuli in a rat model of comorbid chronic pain and depression//Anesthesiology. -2012. -V. 117, № 3. -P. 613-625.
- Compton P. A. The D2 dopamine receptor gene, addiction and personality: Clinical correlates in cocaine abusers//Biol. Psychiatry. -1996. -V. 39, № 4. -P. 302-304.
- Clepce M., Gossler A., Reich K., Kornhuber J., Thuerauf N. The relation between depression, anhedonia and olfactory hedonic estimates -a pilot study in major depression//Neurosci. Lett. -2010. -V. 471 (3). -P. 139-143.
- Greist J. H., Greden J. F., Jefferson J. W., Grivedi M. H. Depression and pain//J. Clin. Psychiatry. -2008. -V. 69 (12). -P. 1970-1978.
- Edwards S., Vendruscolo L. F., Schlosburg J. E., Misra K. K., Wee S., Park P. E., Schulteis G., Koob G. F. Development of mechanical hypersensitivity in rats during heroin and ethanol dependence: alleviation by CRF receptor antagonism//Neuropharmacology. -2012. -V. 62, № 2. -P. 1142-1151.
- Heath T. P., Melichar J. K., Nutt D. J., Donaldson L. F. Human Taste Thresholds Are Modulated by Serotonin and Noradrenaline//The Journal of Neuroscience. -2006. -V. 26 (49). -P. 12664-12671.
- Lombion-Pouthier S., Vandel P., Nezelof S. Odor perception in patients with mood disorders//J. Affect. Disord. -2006. -V. 90 (2-3). -P. 187-191.
- Miller N. S., Gold M. S. Opiate prescription medication dependence and pain perceptions//J. Addict Dis. -2007. -V. 26, № 1. -P. 65-71.
- Swiecicki L., Zatorski P., Bzinkowska D., Sienkiewicz-Jarosz H., Szyndler J., Scinska A. Gustatory and olfactory function in patients with unipolar and bipolar depression//Prog. Neuropsychopharmacol. Biol. Psychiatry. -2009. -V. 33 (5). -P. 827-834.
- Woller S. A., Moreno G. L., Hart N., Wellman P. J., Grau J. W., Hook M. A. Analgesia or addiction?: implications for morphine use after spinal cord injury//J. Neurotrauma. -2012. -V. 29, № 8. -P. 1650-1662.
- White F., Wilson N. Opiate-induced hypernociception and chemokine receptors//Neuropharmacology. -2010. -V. 58, № 1. -P. 35-37.


