Сравнительная эффективность комбинированной терапии препаратами Алфузозин (Алфупрост® МР) и Солифенацин (Везигамп) у больных ДГПЖ и гиперактивным мочевым пузырем с умеренными и выраженными симптомами нарушения функции нижних мочевых путей
Автор: Сивков Андрей Владимирович, Пантелеев В.В., Ромих В.В., Кукушкина Л.Ю., Захарченко А.В., Аполихин О.И., Каприн А.Д.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Андрология
Статья в выпуске: 4 т.17, 2024 года.
Бесплатный доступ
Введение. Недавно были опубликованы первые обобщенные данные об эффективности и безопасности комбинированной терапии (КТ) препаратами алфузозин (Алфупрост® МР) и солифенацин (Везигамп) у больных с симптомами нарушения функции нижних мочевых путей/доброкачественной гиперплазией предстательной железы (СНМП/ДГПЖ) и гиперактивным мочевым пузырем (ГМП) по результатам многоцентрового наблюдательного исследования «АВИАТОР». Это первое многоцентровое исследование комбинации алфузозина и солифенацина, в котором применили комплекс валидизированных анкет для оценки симптомов. Принципиально важно, что в программу не включали пациентов с наличием средней доли предстательной железы и/или внутрипузырной протрузией >10 мм, потенциально имеющих инфравезикальную обструкцию механического типа. Исследование продемонстрировало впечатляющие результаты по влиянию препаратов на частоту и выраженность симптомов. Целью настоящего исследования стала оценка клинической эффективности КТ алфузозином 10 мг/сут и солифенацином 5мг/сут на протяжении трех месяцев у больных СНМП/ДГПЖ и ГМП со средней и тяжелой выраженностью симптомов. Материал и методы. Для исследования пациентов разделили на две подгруппы: ПГ1 (n=89) - с симптомами средней тяжести: IPSS (International Prostate Symptom Score - международная система суммарной оценки симптомов при заболевании предстательной железы) 8-19 баллов; ПГ2 (n=119) - с тяжелой симптоматикой: IPSS 20-35. Мужчины обеих групп не отличались по основным антропометрическим параметрам. Клинически значимую эффективность оценивали по ряду критериев, в том числе: уменьшение IPSS >25% и/или >3 баллов; увеличение максимальной скорости потока мочи (Qmax) более 30%.
Доброкачественная гиперплазия предстательной железы, симптомы нарушения функции нижних мочевых путей, гиперактивность мочевого пузыря, комбинированное медикаментозное лечение, алфузозин, солифенацин
Короткий адрес: https://sciup.org/142243855
IDR: 142243855 | DOI: 10.29188/2222-8543-2024-17-4-56-66
Comparative effectiveness of Alfuzosin (Alfuprost® MR) and Solifenacin (Vesigamp) combination therapy in patients with BPH and overactive bladder, with moderate and severe symptoms of lower urinary tract dysfunction
Introduction. Recently, the first generalized data on the efficacy and safety of alfuzosin (Alfuprost’ MR) and solifenacin (Vesigamp) combination therapy (CT) in patients with LUTS/BPH and hyperactive bladder (ОАВ) have been published based on the results of the multicenter observational «AVIATOR» study. This was the first study of alfuzosin and solifenacin combination, in which a set of validated questionnaires was used to assess symptoms. Crucially, the program did not include BPH patients with the presence of middle lobe and/or intravesical protrusion of more than 10 mm, potentially having a mechanical type of bladder outlet obstruction (BOO). The study showed impressive results on the effect of drugs on the symptoms frequency and severity of symptoms. The aim of this study was to evaluate the clinical efficacy of alfuzosin 10 mg/day and solifenacin 5 mg/day for three months in patients with LUTS/BPH and OAB with moderate to severe symptoms.
Текст научной статьи Сравнительная эффективность комбинированной терапии препаратами Алфузозин (Алфупрост® МР) и Солифенацин (Везигамп) у больных ДГПЖ и гиперактивным мочевым пузырем с умеренными и выраженными симптомами нарушения функции нижних мочевых путей
андрология экспериментальная и клиническая урология № 4 2024
Введение. Недавно были опубликованы первые обобщенные данные об эффективности и безопасности комбинированной терапии (КТ) препаратами алфузозин (Алфупрост® МР) и солифенацин (Везигамп) у больных с симптомами нарушения функции нижних мочевых путей/доброкачественной гиперплазией предстательной железы (СНМП/ДГПЖ) и гиперактивным мочевым пузырем (ГМП) по результатам многоцентрового наблюдательного исследования «АВИАТОР». Это первое многоцентровое исследование комбинации алфузозина и солифенацина, в котором применили комплекс валидизированных анкет для оценки симптомов. Принципиально важно, что в программу не включали пациентов с наличием средней доли предстательной железы и/или внутрипузырной протрузией >10 мм, потенциально имеющих инфравезикальную обструкцию механического типа. Исследование продемонстрировало впечатляющие результаты по влиянию препаратов на частоту и выраженность симптомов.
Целью настоящего исследования стала оценка клинической эффективности КТ алфузозином 10 мг/сут и солифенацином 5мг/сут на протяжении трех месяцев у больных СНМП/ДГПЖ и ГМП со средней и тяжелой выраженностью симптомов.
Материал и методы. Для исследования пациентов разделили на две подгруппы: ПГ1 (n=89) – c симптомами средней тяжести: IPSS (International Prostate Symptom Score – международная система суммарной оценки симптомов при заболевании предстательной железы) 8-19 баллов; ПГ2 (n=119) – с тяжелой симптоматикой: IPSS 20-35. Мужчины обеих групп не отличались по основным антропометрическим параметрам. Клинически значимую эффективность оценивали по ряду критериев, в том числе: уменьшение IPSS >25% и/или >3 баллов; увеличение максимальной скорости потока мочи (Qmax) более 30%.
Результаты. К 3 месяцам в ПГ1 и ПГ2 снизились, соответственно: общий показатель IPSS – с 15,4 до 4,7 и с 23,8 до 6,2 баллов; симптомы накопления – с 8,4 до 2,3 и с 10,1 до 2,7 баллов; симптомы опорожнения – с 7,0 до 2,4 и с 13,7 до 3,5 баллов; ноктурия – с 2,7 до 0,9 и с 2,8 до 0,7; QoL – с 4,7 до 1,0 и 4,8 до 0,9 баллов; общий балл Overactive Bladder Symptom Score (OABSS) – с 9,4 до 1,9 и с 11,4 до 2,2; patient Perception оf Intensity оf Urgency Scale (PPIUS) – с 2,3 до 0,3 и с 2,6 до 0,4 баллов. Одновременно в ПГ1 и ПГ2 зарегистрирован рост Qmax с 12,2 до 17,7 мл/с и с 11,1 до 17,3 мл/с при снижении остаточной мочи с 35,9 до 9,3 мл и с 60,0 до 14,1 мл. Клинически значимый ответ на лечение по IPSS зарегистрировали через месяц у 92,1% больных в ПГ1 и у 89,1% в ПГ2, а через 3 мес. – уже у 98,9% и 99,2% соответственно. Улучшение Qmax >30% наблюдали в ПГ1 и ПГ2 через месяц у 77,7% и 84,0%, а в конце исследования – у 98,9% и у 98,3%.
Заключение. В результате КТ у подавляющего числа пациентов обеих групп достигнут выраженный статистически достоверный эффект по большинству субъективных и объективных клинических показателей, который был зарегистрирован уже через месяц после начала приема препаратов и усилился к 3-му месяцу наблюдения. Корректный отбор пациентов на лечение обеспечил успешность результатов исследования.
№
Comparative effectiveness of alfuzosin (Alfuprost® MR) and solifenacin (Vesigamp) combination therapy in patients with BPH and overactive bladder, with moderate and severe symptoms of lower urinary tract dysfunction
EXPERIMENTAL STUDY
A.V. Sivkov1, V.V. Panteleev1, V.V. Romikh1, L.Yu. Kukushkina1, A.V. Zakharchenko1, O.I. Apolikhin1, A.D. Kaprin2,3,4
-
1 N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology – branch of the National Medical Research Radiological Centre of the Ministry of Health of the Russian Federation; 51, 3-rd Parkovaya street, Moscow, 105425, Russia
-
2 National Medical Research Centre of Radiology of Ministry of health of Russian Federation; 4, st. Koroleva, Kaluga region, Obninsk, 249036, Russia
-
3 P.A. Herzen Moscow Oncology Research Institute – branch of the National Medical Research Radiological Centre of the Ministry of Health of the Russian Federation; 3, 2nd Botkinskiy proezd, Moscow, 125284 , Russia
-
4 RUDN University; 6, st. Miklukho-Maklaya, Moscow, 117198, Russia
Introduction. Recently, the first generalized data on the efficacy and safety of alfuzosin (Alfuprost® MR) and solifenacin (Vesigamp) combination therapy (CT) in patients with LUTS/BPH and hyperactive bladder (ОАВ) have been published based on the results of the multicenter observational «AVIATOR» study. This was the first study of alfuzosin and solifenacin combination, in which a set of validated questionnaires was used to assess symptoms. Crucially, the program did not include BPH patients with the presence of middle lobe and/or intravesical protrusion of more than 10 mm, potentially having a mechanical type of bladder outlet obstruction (BOO). The study showed impressive results on the effect of drugs on the symptoms frequency and severity of symptoms.
The aim of this study was to evaluate the clinical efficacy of alfuzosin 10 mg/day and solifenacin 5 mg/day for three months in patients with LUTS/BPH and OАB with moderate to severe symptoms.
Materials and methods. For this purpose, patients were divided into two subgroups: G1 (n=89) – with moderate symptoms, IPSS 8-19 points; G2 (n=119) – with severe symptoms, IPSS 20-35. The men of both groups did not differ in basic anthropometric parameters. Clinically significant efficacy was assessed by follow criteria, including: reduction of IPSS >25% and/or >3 points, as well as an increase in Qmax of more than 30%.
Results. In 3 months in G1 and G2 the following parameters have been respectively decreased: total IPSS from 15,4 to 4,7 and from 23,8 to 6,2 points; storage symptoms – from 8,4 to 2,3 and from 10,1 to 2,7 points; voiding symptoms – from 7,0 to 2,4 and from 13,7 to 3,5 points; nocturia – from 2,7 to 0,9 and from 2,8 to 0,7; QoL – from 4,7 to 1,0 and 4,8 to 0,9 points; total OABSS score – from 9,4 to 1,9 and from 11,4 to 2,2; PPIUS score – from 2,3 to 0,3 and from 2,6 to 0,4 points. Simultaneously in G1 and G2 an increase in Qmax was recorded from 12,2 to 17,7 ml/s and from 11,1 to 17,3 ml/s, with a decrease in residual urine volume from 35,9 to 9,3 ml and from 60,0 to 14,1 ml. Clinically significant treatment response to IPSS was registered within a month in 92,1% in G1 and in 89,1% in G2, and after 3 months – in 98,9% and 99,2%, respectively. Improvement of Qmax >30% was observed in G1 and G2 after a month – in 77,7% and 84,0%, and at the end of the study – in 98,9% and 98,3%.
Conclusion. The vast majority of patients in both groups achieved a pronounced statistically significant effect on almost all of subjective and objective clinical indicators, which was registered a month after the start of therapy and intensified by the 3rd month of treatment. The correct selection of patients for study ensured its favorable results.
Комбинированную терапию симптомов нарушения функции нижних мочевых путей, связанных с доброкачественной гиперплазией предстательной железы (СНМП/ДГПЖ), широко применяют в клинической практике. Различные схемы комбинированной терапии включены в клинические рекомендации:российские, европейские – EAU и американские – AUA [1-3].
Недавно были опубликованы первые обобщенные данные об эффективности и безопасности комбинированной терапии препаратами алфузозин
(Алфупрост® МР) и солифенацин (Везигамп) у больных СНМП/ДГПЖ и гиперактивным мочевым пузырем (ГМП) по результатам многоцентрового наблюдательного исследования «АВИАТОР».Оно включало несколько инноваций. Во-первых, это было первое исследование комбинации алфузозина и солифенацина. Во-вторых, в нем был применен комплекс валидизиро-ванных анкет для общей оценки симптомов (IPSS – International Prostate Symptom Score – Международный индекс симптомов при заболеваниях предстательной железы), гиперактивности (OABSS – Overactive Bladder Symptom Score – оценка симптомов гиперактивного мочевого пузыря) и ургентности (PPIUS – Patient Perception of Intensity of Urgency Scale), а также авторская анкета для оценки симптомов, не учтенных в вышеуказанных опросниках. В-третьих, впервые регистрировали не только цифровые показатели урофлоуметрии (УФМ), но и форму УФМ-кривой, для чего был разработан специальный шаблон. И, наконец, в-четвертых, что принципиально важно, в программу не включали пациентов с наличием средней доли предстательной железы и/или внутрипузырной протрузией более 10 мм, потенциально имеющих инфравезикальную обструкцию (ИВО) механического типа [4].
Исследование продемонстрировало впечатляющие результаты по влиянию препаратов на частоту и выраженность симптомов как опорожнения,так и накопления, в том числе гиперактивность и ургентность, а также на объективные параметры мочеиспускания [4]. В то же время, в первой публикации были изложены лишь обобщенные данные об эффективности изучаемой комбинации препаратов. Одновременно, большой научный и практический интерес представляют материалы о сравнительной эффективности комбинированной терапии у пациентов с умеренной и значительной выраженностью симптомов.Этому вопросу и посвящена настоящая работа.
Наблюдательное проспективное пострегистрационное многоцентровое исследование «АВИАТОР» (Антимускариновый препарат Везигамп И Алфу-прост® МР: Терапия и Оценка Результатов) проведено в сентябре 2022 г. – июне 2023 г. по протоколу «Оценка влияния комбинированной терапии α1-ад-реноблокатором (алфузозин, Алфупрост® МР, 10 мг, один раз в сутки)и средством с антимускариновой активностью (солифенацин, Везигамп, 5 мг, один раз в сутки) на выраженность СНМП у амбулаторных пациентов с ДГПЖ и ГМП со средней и тяжелой симптоматикой». В нем участвовали 15 специалистов из 8 медицинских учреждений Москвы, Санкт-Петербурга, Нижнего Новгорода, Ростова-на-Дону и Челябинска.
Целью исследования стала оценка клинической эффективности и безопасности комбинированной терапии α1-адреноблокатором (алфузозин, Алфупрост® МР, 10 мг, один раз в сутки) и средством с антимуска-риновой активностью (солифенацин, Везигамп, 5мг, один раз в сутки) на выраженность СНМП у пациентов с ДГПЖ и ГМП со средней и тяжелой выраженностью симптомов.
Задачи исследования, приближенного к реальной клинической практике, – оценка влияния комбинированного применения препаратов через один и три месяца терапии:на СНМП по изменению баллов шкалы IPSS; на максимальную скорость потока мочи (Qmax) по изменению показателей урофлоуметрии (УФМ); на качество жизни больных по изменению баллов шкалы QoL (Quality of Life); на частоту и тяжесть развития нежелательных реакций у больных, а также частоту связанных с ними отказов от лечения (комплаентность).
Все пациенты прошли стандартизированное обследование на визите 1, включавшее сбор анамнеза; физикальный осмотр (наружные половые органы, пальцевое ректальное исследование);заполнение специализированных опросников: IPSS, Q oL, OABSS, PPIUS; лабораторные исследования (общий анализ мочи, общий анализ крови, простатспецифический антиген (ПСА), креатинин и глюкоза крови); ультразвуковое исследование (УЗИ) почек, мочевого пузыря, предстательной железы (объем, степень внутрипузыр-ной протрузии); УФМ (Qmax, средняя скорость мочеиспускания – Qave, объем мочеиспускания – Vcomp); измерение объема остаточной мочи – Vres) ультразвуковым методом.
Для оценки формы УФМ кривых был разработан шаблон с графическим изображением их основных типов: нормальный, обструктивный пологий, обструктивный платообразный, нерегулярный (неправильный), башенный (стремительный), прерывистый.
В наблюдательное исследование включали мужчин в возрасте старше 50 лет с диагнозом ДГПЖ, объемом ПЖ при УЗИ более 30см3 и величиной внут-рипузырной протрузии менее 10 мм, наличием симптомов расстройства мочеиспускания умеренной и значительной степеней выраженности (≥8 баллов по IPSS), Qmax при УФМ ≥7 мл/с и <15 мл/с, объемом остаточной мочи ≤150 мл, уровнем ПСА <4 нг/мл, по опроснику QоL > 3 баллов. Больные должны были предъявлять жалобы на учащенное мочеиспускание ≥ 8 раз в сутки и императивные позывы к мочеиспусканию ≥2 за сутки в течение 3-х и более месяцев. Все пациенты подписали информированное согласие на участие в исследовании и обработку деперсонифици-рованных данных.
В исследование не включали пациентов с предшествующей терапией в течение 6 месяцев любым α1-адреноблокатором (α1-АБ), М-холинолитиком

(MХЛ), антагонистом β3-рецепторов, ингибитором 5α-редуктазы, ингибитором фосфодиэстеразы 5 типа, препаратами на основе растительных экстрактов, применяемыми для лечения расстройств мочеиспускания и мочегонными средствами.В наблюдательную программу не вошли пациенты с: абсолютными показаниями к оперативному лечению ДГПЖ (повторяющаяся после удаления катетера или рецидивирующая острая задержка мочеиспускания, парадоксальная ишурия, устойчивая к терапии макрогематурия, двухсторонний уретерогидронефроз c почечной недостаточностью или без нее, камни и дивертикулы мочевого пузыря); хронической мочевой инфекцией; внутрипу-зырной протрузией предстательной железы >10 мм, определенной при УЗИ.Пациенты,не способные по своему состоянию обеспечить регулярный прием исследуемых препаратов и/или посещать врача в указанное время, также были исключены.
За два дня до включения в исследование пациенты должны были начать прием препаратов: алфузо-зин (Алфупрост® МР) 10 мг/сут и солифенацин (Вези-гамп) 5 мг/сут в строгом соответствии с действующими инструкциями по медицинскому применению.
Контрольные обследования, включавшие оценку жалоб, заполнение опросников IPSS, Q oL, OA BSS, PPIUS, выполнение УФМ с определением объема остаточной мочи, как и мониторинг нежелательных явлений (НЯ) и контроль терапии, проводили на визитах 2 и 3 – через один и три месяца лечения. Анализ приверженности и удовлетворенности лечением пациентов и врачей осуществили с использованием стандартизированной шкалы Лайкерта.
Клинически значимую эффективность оценивали по следующим критериям:уменьшение общего показателя IPSS на 25%; на 50%; на 75% и/или >3 баллов; увеличение Qmax более, чем на 30%.
Исследование по подгруппам
Цель настоящего подгруппового анализа – сравнительная оценка влияния комбинированной терапии алфузозином (Алфупрост® МР, 10 мг, один раз в сутки) и солифенацином (Везигамп, 5мг, одни раз в сутки) на выраженность СНМП и объективных показателей мочеиспускания у пациентов с ДГПЖ и ГМП со средней и тяжелой выраженностью симптомов. Для этого общую группу пациентов разделили на две подгруппы, в зависимости от показателя IPSS: Подгруппа 1 (ПГ1) – c симптомами средней тяжести, IPSS 8-19 баллов; Подгруппа 2 (ПГ2) – с тяжелой симптоматикой, IPSS 20-35.
Статистический анализ
Для обработки полученных результатов были применены методы описательной статистики. Количе- ственные данные представлены центральными тенденциями и рассеянием: среднее арифметическое (M) и стандартное отклонения (SD) в формате М (SD). При распределении признаков, отличающемся от нормального, их описывали в виде медианы (Me) и квартилей Q1 и Q3 в формате Me (Q1; Q3). Величину порогового уровня значимости р принимали равной 0,05. Статистически значимыми считали различия при p<0,05.
Частотный анализ и расчет процентной доли встречаемости признака применяли для качественных данных. Проверку выборок на нормальность осуществляли при помощи теста Колмогорова-Смирнова. U-критерий Манна-Уитни и Т-Стьюдента использовали для сравнения независимых выборок.Взаимо-связь параметров определяли с использованием метода корреляционного анализа Спирмена. Непараметрический критерий %2 с поправкой Йеитса был использован для установления различия частот признаков в независимых группах. Математическую и статистическую обработку полученных данных проводили с использованием стандартных пакетов программ Statistica (V7.0) и SPSS Statistics (V17.0).
Всего в наблюдательную программу было включено 208 больных СНМП/ДГПЖ. В зависимости от показателя IPSS они были разделены на подгруппы: ПГ1 – 89 пациентов с СНМП средней выраженности (IPSS 8-19); ПГ2 – 119 больных с тяжелой симптоматикой (IPSS > 20). Мужчины обеих групп не отличались по основным антропометрическим параметрам:росту, весу, индексу массы тела. Однако больные из ПГ2, с тяжелыми симптомами,были статистически достоверно моложе: 59,4 года против 62,5. Этот факт мы объясняем более ранним обращением пациентов с беспокоящей симптоматикой за медицинской помощью и оперативным лечением.
Основные исходные клинические показатели, ожидаемо, были достоверно хуже у пациентов ПГ2, по сравнению с ПГ1 (табл. 1).
Влияние на СНМП
В результате лечения у подавляющего числа пациентов обеих групп достигнут статистически достоверный и выраженный эффект по большинству субъективных и объективных клинических показателей, который был зарегистрирован уже через месяц после начала приема препаратов и усилился к 3-му месяцу наблюдения.
Шкала IPSS/QoL. Комбинированная терапия привела к статистически значимому улучшению через один и 3 месяца наблюдения в ПГ1 и ПГ2 соответственно: общего показателя IPSS на 40,3% и 69,5% против 48,3% и 73,9%; симптомов фазы накопления на 41,7% и 72,6% против 47,5% и 73,3%; симптомов фазы опорожнения на 38,6% и 65,7% против 48,2% и 74,4%; общего показателя QoL на 51,1% и 78,7% против 50,0% и 81,3% (рис. 1). Обращает на себя внимание более выраженная динамика показателей IPSS у пациентов ПГ2, по сравнению с ПГ1, хотя абсолютные значения QoL оказались очень близки (табл. 2).
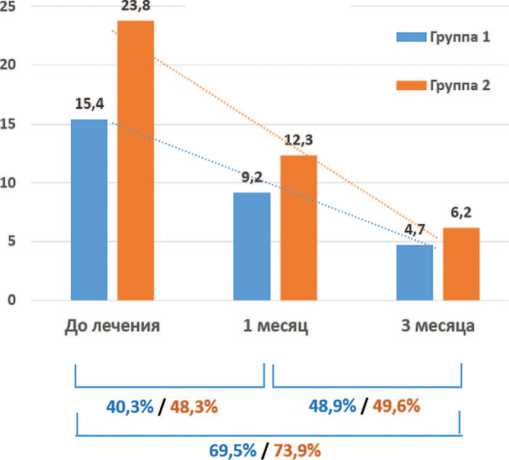
Рис. 1. Динамика общего показателя IPSS в подгруппах с различной выраженностью симптомов СНМП.
Fig. 1. Dynamics of the overall IPSS index in subgroups with different severity of LUTS symptoms
В то же время, при оценке динамики симптомов фаз накопления и опорожнения, как и отдельных симптомов, отмечено, что в ПГ1 исходно преобладали симптомы накопления,тогда как в ПГ2 «вклад» симптомов опорожнения был бóльшим.К концу лечения показатели всех симптомов сблизились, хотя выявленная тенденция сохранялась (рис. 2). Эти данные могут свидетельствовать об относительности разделения симптомов на т.н. «ирритативные» и «обструктивные» и о том, что выраженная гиперактивность может проявляться и ростом симптомов опорожнения за счет нарастания функциональной ИВО.
Также у пациентов ПГ1 отмечена более выраженная динамика показателя соотношения симптомов накопления /опорожнения в виде его уменьшения с исходных 1,21 до 1,15 через месяц и до 0,95 через три, тогда как в ПГ2 это соотношение было практически неизменным, соответственно: 0,74; 0,74 и 0,77. Показательно, что через 3 месяца комбинированного лечения доля пациентов, предъявлявших какие-либо жалобы на СНМП, снизилась со 100% до 68,9-69,7%. То есть, около 30% больных обеих подгрупп к концу исследования перестали предъявлять жалобы на нарушенное мочеиспускание!
Шкала гиперактивности OABSS (Homma). В результате лечения зарегистрировано в высокой степени статистически значимое и симметричное по группам снижение общего показателя ГМП по шкале OABSS у пациентов ПГ1 и ПГ2, соответственно: через один
Таблица 1. Исходные клинические показатели в подгруппах с различной выраженностью симптомов СНМП Table 1. Initial clinical parameters in subgroups with different severity of LUTS symptoms
|
Показатели Indicators |
Подгруппа 1, (n = 89) Subgroup 1, (n = 89) |
Подгруппа 2, (n = 119) Subgroup 2, (n = 119) |
Достоверность ( р ) Reliability ( p ) |
|
Объем ПЖ, см3 Prostate volume, sm3 |
46,7 (±9,1) |
52,2 (±13,4) |
0,001 |
|
IPSS, баллы, IPSS, points |
15,4 (±2,9) |
23,8 (±2,5) |
0,001 |
|
IPSS (опорожнения), баллы IPSS (emptying), points |
7,0 (±3,0) |
13,7 (±2,1) |
0,001 |
|
IPSS (накопления), баллы IPSS (saving), points |
8,4 (±2,1) |
10,1 (±1,8) |
0,001 |
|
IPSS (ноктурия), баллы IPSS (nocturia), points |
2,7 (±0,8) |
2,8 (±1,1) |
0,859 |
|
QOL, баллы QOL, points |
4,7 (±0,5) |
4,8 (±0,44) |
0,311 |
|
OABSS, баллы OABSS, points |
9,4 (±2,1) |
11,4 (±2,3) |
0,001 |
|
PPIUS, баллы PPIUS, points |
2,3 (±0,6) |
2,6 (±0,7) |
0,002 |
|
Qmax, мл/с Qmax, ml/s |
12,2 (±1,9) |
11,1 (±2,1)* |
0,001 |
|
Qave, мл/с Qave, ml/s |
7,1 (±1,7) |
6,2 (±1,26) |
0,001 |
|
Vcomp (мл) Vcomp (ml) |
206,3 (±53,8) |
202,5 (±49,7) |
0,627 |
|
Vres (мл) Vres (ml) |
35,9 (±31,5) |
60,0 (±34,6) |
0,001 |
месяц – на 51,1% и 50,9%, а через три месяца – на 79,6% и 81,1%. Одновременно, в ПГ1 и ПГ2 через три месяца выявлено достоверное снижение как ургентных позывов на мочеиспускание на 88,6% и 85,9%, так и эпизодов императивного недержания мочи на 83,8% и 81,3%, причем в последнем случае были значимые различия между группами на всех визитах.
Ноктурия – один из важнейших симптомов нарушенного мочеиспускания. Показано практически оди- наковое и достоверное снижение показателя ноктурии через один и три месяца в ПГ1 и ПГ2, соответственно, как по шкале IPSS (на 40,7% и 66,7% против 50,0% и 75,0%), так и по шкале OABSS (на 30,4% и 60,9% против 45,8% и 70,8%), причем более значимое в ПГ2, что на 3 визите было статистически достоверно. Некоторые различия в показателях связаны с необходимостью заполнения пожилыми пациентами двух разных анкет, в ходе которого и возможно появление неточностей,
Таблица 2. Динамика основных клинических показателей в подгруппах на визитах 1-3
Table 2. Dynamics of the main clinical indicators in subgroups at visits 1-3
|
Показатели Indicators |
Подгруппа 1, (n = 89) Subgroup 1, (n = 89) |
Подгруппа 2, (n = 119) Subgroup 2, (n = 119) |
Достоверность ( р ) Reliability ( p ) |
|
|
IPSS, баллы IPSS, points |
Исходно/Initially |
15,4 (±2,9) |
23,8 (±2,5) |
0,001 |
|
1 месяц/1 month |
9,2 (±3,5) |
12,3 (±3,7) |
0,001 |
|
|
3 месяца/3 months |
4,7 (±2,7) |
6,2 (±3,7) |
0,008 |
|
|
IPSS накопления, баллы IPSS aving, points |
Исходно/Initially |
8,4 (±2,1) |
10,1 (±1,8) |
0,001 |
|
1 месяц/1 month |
4,9 (±1,6) |
5,3 (±1,7) |
0,238 |
|
|
3 месяца/3 months |
2,3 (±1,2) |
2,7 (±1,6) |
0,149 |
|
|
IPSS опорожнения, баллы IPSS (emptying), points |
Исходно/Initially |
7,0 (±3,0) |
13,7 (±2,1) |
0,001 |
|
1 месяц/1 month |
4,3 (±2,6) |
7,1 (±2,5) |
0,001 |
|
|
3 месяца/3 months |
2,4 (±1,8) |
3,5 (±2,4) |
0,003 |
|
|
IPSS ноктурия, баллы IPSS (nocturia), points |
Исходно/Initially |
2,7 (±0,8) |
2,8 (±1,1) |
0,859 |
|
1 месяц/1 month |
1,6 (±0,7) |
1,4 (±0,8) |
0,070 |
|
|
3 месяца/3 months |
0,9 (±0,6) |
0,7 (±0,6) |
0,050 |
|
|
QoL, баллы QoL, points |
Исходно/Initially |
4,7 (±0,5) |
4,8 (±0,4) |
0,311 |
|
1 месяц/1 month |
2,4 (±1,0) |
2,4 (±1,1) |
0,494 |
|
|
3 месяца/3 months |
1,0 (±0,8) |
0,9 (±0,9) |
0,397 |
|
|
OABSS, баллы OABSS, points |
Исходно/Initially |
9,4 (±2,1) |
11,4 (±2,3) |
0,001 |
|
1 месяц/1 month |
4,6 (±2,4) |
5,6 (±2,9) |
0,017 |
|
|
3 месяца/3 months |
1,9 (±1,7) |
2,2 (±2,0) |
0,622 |
|
|
OABSS ургентность, баллы OABSS urgency, points |
Исходно/Initially |
4,2 (±0,4) |
4,4 (±0,5) |
0,025 |
|
1 месяц/1 month |
1,5 (±1,0) |
2,1 (±1,3) |
0,004 |
|
|
3 месяца/3 months |
0,5 (±0,7) |
0,6 (±0,8) |
0,401 |
|
|
OABSS недержание, баллы OABSS incontinence, points |
Исходно/Initially |
1,5 (±1,4) |
3,0 (±1,6) |
0,001 |
|
1 месяц/1 month |
0,7 (±1,0) |
1,6 (±1,3) |
0,001 |
|
|
3 месяца/3 months |
0,3 (±0,6) |
0,6 (±0,8) |
0,013 |
|
|
OABSS ноктурия, баллы OABSS nocturia, points |
Исходно/Initially |
2,3 (±0,8) |
2,4 (±0,8) |
0,316 |
|
1 месяц/1 month |
1,6 (±0,7) |
1,3 (±0,8) |
0,016 |
|
|
3 месяца/3 months |
0,9 (±0,7) |
0,7 (±0,6) |
0,085 |
|
|
PPIUS, баллы PPIUS, points |
Исходно/Initially |
2,3 (±0,6) |
2,6 (±0,7) |
0,002 |
|
1 месяц/1 month |
1,2 (±0,6) |
1,2 (±0,6) |
0,913 |
|
|
3 месяца/3 months |
0,3 (±0,5) |
0,4 (±0,5) |
0,475 |
|
|
Qmax, мл/с Qmax, ml/s |
Исходно/Initially |
12,2 (±1,9) |
11,1 (±2,1) |
0,001 |
|
1 месяц/1 month |
15,8 (±5,3) |
14,8 (±4,3) |
0,001 |
|
|
3 месяца/3 months |
17,7 (±5,4) |
17,3 (±4,8) |
0,570 |
|
|
Остаточная моча, мл Residual urine, ml |
Исходно/Initially |
35,9 (±31,5) |
60,0 (±34,6) |
0,001 |
|
1 месяц/1 month |
20,3 (±23,4) |
28,6 (±22,6) |
0,001 |
|
|
3 месяца/3 months |
9,3 (±13.4) |
14,1 (±17,8) |
0,012 |
|
однако общий положительный тренд не вызывает сомнений (табл. 2).
Шкала ургентности PPIUS. Выявлено достовер- ное и симметричное снижение в подгруппах такого важного симптома, как ургентность, для чего исполь- зовали специализированную шкалу. В течение первого
месяца лечения общий показатель ургентности в ПГ1 снизился на 47,8%, против 53,8% в ПГ2, а через три месяца – на 87,0% и 84,6%, соответственно. Показательно, что если до начала программы в обеих группах отсутствовали пациенты без ургентности или с ее легкой степенью,то через месяц уже не было больных с императивным недержанием мочи, а в ПГ1 – и с ургент-ностью тяжелой степени.Через три месяца в обеих группах остались мужчины только с ургентностью легкой степени или ее отсутствием (табл. 2-3).
Влияние на объективные показатели мочеиспускания
Qmax. Симптоматический эффект сопровождался выраженным и статистически достоверным улучшением объективных показателей мочеиспускания у пациентов обеих подгрупп. Зарегистрирован рост Qmax на 29,5% и 33,3% через месяц применения комбинации препаратов и на 45,1% и 55,9 % через три месяца в ПГ1 и ПГ2 соответственно (табл. 2, рис. 3).
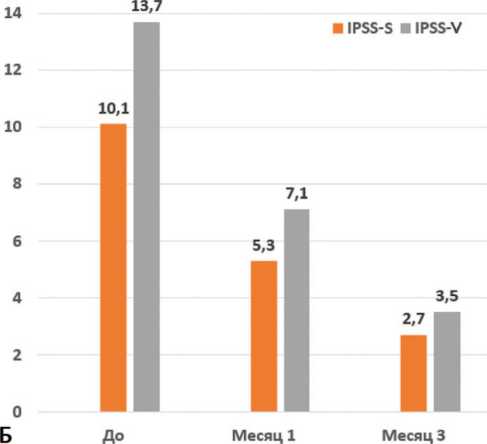
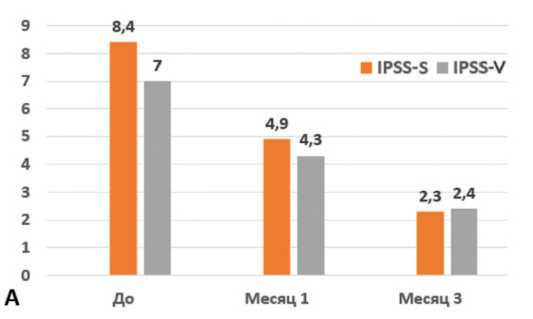
Рис. 2. Динамика симптомов накопления (IPSS-S) и опорожнения (IPSS-V) в подгруппах: ПГ1 (A); ПГ2 (Б)
Fig. 2. Dynamics of symptoms of saving (IPSS-S) and emptying (IPSS-V) in subgroups: PG1 (A); PG2 (Б)
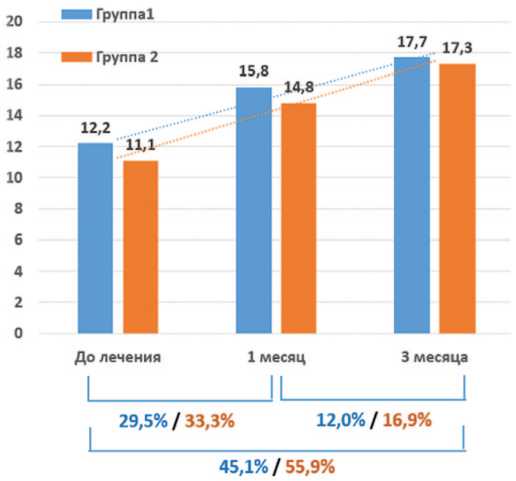
Рис. 3. Динамика Qmax в подгруппах на визитах 1-3
Fig. 3. Dynamics of Qmax in subgroups at visits 1-3
Таблица 3. Доля пациентов в подгруппах с различной степенью ургентности по шкале PPIUS на визитах 1-3 (%)
Table 3. Proportion of patients in subgroups with different degrees of urgency according to the PPIUS scale at visits 1–3 (%)
|
Показатели Indicators |
Группа 1 / Group 1 |
Группа 2 / Group 2 |
||||
|
Визит 1 Vizit 1 |
Визит 2 Vizit 2 |
Визит 3 Vizit 3 |
Визит 1 Vizit 1 |
Визит 2 Vizit 2 |
Визит 3 Vizit 3 |
|
|
Ургентность отсутствует No urgency |
0 |
13,5 |
69,7 |
0 |
10,1 |
63,9 |
|
Легкая степень Mild degree |
0 |
57,3 |
30,3 |
0 |
63,3 |
36,1 |
|
Средняя степень Moderate degree |
75,3 |
29,2 |
0 |
51,2 |
25,2 |
0 |
|
Тяжелая степень Severe degree |
20,2 |
0 |
0 |
33,6 |
1,7 |
0 |
|
Недержание мочи Urinary incontinence |
4,5 |
0 |
0 |
14,3 |
0 |
0 |
Объем остаточной мочи – важный клинический показатель, отражающий, в том числе, безопасность проводимого лечения.Отмечено статистически достоверное уменьшение этого показателя и в ПГ1, и в ПГ2 на 43,5% и 52,3% через месяц терапии и на 74,1% и 76,5% через три месяца (табл. 2).
Клинически значимый ответ на лечение
При оценке результатов лекарственной терапии СНМП/ДГПЖ важной характеристикой является достижение показателей клинически значимого ответа, под которым понимают уменьшение IPSS более, чем на 25% и/или 3 балла, а также увеличение Qmax на 30% и более. Настоящее исследование продемонстрировало впечатляющие результаты: клинически значимый ответ на лечение по IPSS был зарегистрирован через месяц у 92,1% больных в ПГ1 и у 89,1% в ПГ2, тогда как через три месяца – уже у 98,9% и 99,2%, соответственно. Улучшение Qmax >30% наблюдали в ПГ1 и ПГ2 через месяц у 77,7% и 84,0%, а в конце исследования – у 98,9% и у 98,3% (табл. 4).
Безопасность лечения
В ходе наблюдательной программы зарегистрировано всего 5 нежелательных явлений у 5 (2,5%) пациентов: сухость во рту – 4 (2,0%), ретроградная эякуляция – 1 (0,5%). В связи с их небольшим числом раздельный анализ не проводили.Эпизодов острой задержки мочеиспускания (ОЗМ) не было. Ни один пациент не прервал лечения из-за развития нежелательных явлений [4].
Настоящая работа является результатом дальнейшего анализа данных наблюдательного проспективного многоцентрового исследования «АВИАТОР», изучавшего влияние комбинированной терапии α1-ад- реноблокатором алфузозин (Алфупрост® МР, 10 мг, один раз в сутки) и антимускариновым препаратом со-лифенацин (Везигамп, 5мг, один раз в сутки) на выраженность СНМП и объективных показателей мочеиспускания у пациентов с ДГПЖ и ГМП со средней и тяжелой симптоматикой [4]. Как мы указывали ранее, эта работа является оригинальной как по комбинации выбранных препаратов, так и по особенностям дизайна. В ней впервые использовали комбинацию алфузозина и солифенацина, а в качестве критерия невключения – величину внутрипузырной протрузии >10 мм, что ограничило попадание в исследуемую группу пациентов с выраженной ИВО механического типа.Кроме того, в базах научной литературы нами не найдено исследований комбинированной терапии СНМП/ДГПЖ с использованием α1-АБ и М-холинолитика, где бы сравнивали группы пациентов, в зависимости от выраженности симптомов нарушения мочеиспускания. В связи с этим, прямое сравнение результатов, полученных в настоящем исследовании, с другими подобными работами невозможно [4].
Анализ подгрупп пациентов, сформированных в зависимости от выраженности симптомов по IPSS, показал, что у мужчин с тяжелой симптоматикой достоверно хуже выглядели и другие основные клинические показатели: IPSS, OABSS, Qmax, объем остаточной мо-чи (табл. 1). Причем, в ПГ1 представленность симптомов фазы накопления была исходно выше, тогда как в ПГ2 преобладали симптомы опорожнения (рис. 2).
Известно, что больные с выраженными СНМП хуже поддаются консервативному лечению α1-АБ [2]. Однако в нашей работе сравнение результатов комбинированного лечения пациентов с умеренной и выраженной симптоматикой продемонстрировало высокую эффективность в обеих подгруппах и в отношении симптомов по шкалам IPSS, OABSS, PPIUS, и по объективным показателям мочеиспускания (табл. 2).
В контролируемых исследованиях α1-АБ, обычно, демонстрируют снижение IPSS примерно на 30-40%
Таблица 4. Частота клинически значимого ответа на лечение в подгруппах (%)
Table 4. Frequency of clinically significant response to treatment in subgroups (%)
|
Показатели Indicators |
Группа 1 / Group 1 |
Группа 2 / Group 2 |
||
|
Визит 1 Vizit 1 |
Визит 2 Vizit 2 |
Визит 1 Vizit 1 |
Визит 2 Vizit 2 |
|
|
IPSS≥ 25% |
92,1 |
98,9 |
89,1 |
99,2 |
|
IPSS≥ 50% |
34,8 |
94,4 |
46,2 |
89,9 |
|
IPSS≥ 75% |
4,5 |
33,7 |
1,7 |
52,9 |
|
IPSS≥ 3 баллов |
96,6 |
100 |
99,2 |
100 |
|
Увеличение Qmax≥ 30% Increase Qmax≥ 30% |
77,7 |
98,9 |
84,0 |
98,3 |
или 5-8 баллов и увеличение Qmax примерно на 1625%, а в открытых исследованиях – улучшение IPSS до 50% и рост Qmax до 40% [2, 3, 5]. Данные систематического обзора свидетельствуют, что при СНМП/ДГПЖ монотерапия алфузозином вела к улучшению симптомов по IPSS на 31-42% и увеличению Qmax на 1,4-3,2 мл/с [6]. В открытом российском исследовании у пациентов с умеренной выраженностью СНМП/ДГПЖ алфу-зозин (Алфупрост® МР) 10 мг/сут показал статистически значимое улучшение симптомов по IPSS на 55% и увеличение Qmax на 52,7% [7]. Также показано, что терапия алфузозином, в том числе длительная, эффективна в отношении симптомов фаз как накопления, так и опорожнения [8].
Монотерапия солифенацином у пациентов с умеренными и выраженными СНМП не показала улучшения симптомов по сравнению с плацебо [9]. Это, отчасти, может быть обусловлено тем, что в этом исследовании специально не выделяли пациентов с ГМП и/или ургентностью.
По данным метаанализа 16 исследований, комбинированная терапия α1-АБ и М-холинолитика (МХЛ) при ДГПЖ/ГМП ведет к улучшению симптомов и ка-чествa жизни пациентов, по сравнению с монотерапией α1-АБ, не вызывая значительного ухудшения функции мочеиспускания.Однако достоверной разницы по показателям IPSS и Qmax между двумя группами достигнуто не было [10].
Опубликовано лишь несколько исследований комбинации солифенацина и тамсулозина у мужчин с СНМП. В одном из них у пациентов с умеренными и выраженными СНМП и ГМП (IPSS 17,5±5,8) на фоне ИВО (Qmax 8,2±3,1 мл/с) через 12 недель лечения удалось достигнуть статистически значимого снижения IPSS, в среднем, на 45,7%, частоты мочеиспусканий – на 17,8%, эпизодов ургентности – на 51,7% и увеличения Qmax на 19,4% [11]. В целом, сравнивать подобные исследования достаточно сложно, так как они различаются по составу изучаемых групп, используемым препаратам и их дозам, исходным показателям симптомов и объективных данных.
Тем не менее, наше исследование продемонстрировало превосходящие результаты, по сравнению с опубликованными ранее. Через три месяца комбинированной терапии достигнуто статистически достоверное улучшение в подгруппах с исходно умеренными и выраженными симптомами:по общему баллу IPSS – на 69,5% и 73,9%; по симптомам накопления – на 72,6% и 73,3%; по симптомам опорожнения – на 65,7% и 74,5%, по величине Qmax – на 45,1% и 55,9%, а также по показателю качества жизни QoL – на 78,7% и 81,3% соответственно. Также зарегистрировано статистически значимое уменьшение показателей по шкалам гиперактивности – OABSS и ургентности – PPIUS.
При оценке результатов применения того или иного метода лечения важным является достижение «клинически значимого ответа», что является не только некоторой эмпирической величиной,но и медико-экономической характеристикой. Представления об эффективности терапии СНМП/ДГПЖ сформировались на основании нескольких исследований и постулатов. В 1991 г Y. Aso и соавт. предложили считать выраженным эффектом снижение симптомов по шкале IPSS на 50% и более, эффективным – на 25% и более и неэффективным – менее 25% [12]. По результатам масштабного исследования М.J. Ваrry и соавт. установили, что улучшение IPSS на 3 балла, по сравнению с базовым уровнем, соответствует оптимальным показателям чувствительности (0,68) и специфичности (0,70) при разделении пациентов «с улучшением» и «без улучшения» [13]. Этот критерий позже был признан Американской урологической ассоциацией (AUA) как «установленный клинически значимый порог» эффективности для лекарственной терапии [14 ]. Пациенты, достигшие или превысившие этот уровень улучшения, могут рассматриваться как клинически значимо ответившие на лечение.В дальнейшем ряд исследователей применили критерий улучшения СНМП по шкале IPSS на 25% и более при организации масштабных исследований лекарственных препаратов [15-17]. Некоторые авторы использовали не только критерий снижения суммы баллов по шкале IPSS на 25%, 50% и 75%, но одновременно и еще один критерий – уменьшение симптомов более чем на 3 балла [18]. При изучении методами Data mining ответа на лекарственную терапию СНМП/ДГПЖ F. Fusco и соавт. [19] и А.В. Сивков и соавт. [20] также применили в качестве значимого критерий улучшения по IPSS на 25% и более. И, наконец, Н. Lepor, помимо критерия симптоматического улучшения, применил уро-динамический критерий улучшения параметров мочеиспускания – увеличение исходного показателя Qmax на 30% и более [15].
В настоящем исследовании наглядно продемонстрировано, что клинически значимый ответ и по показателю IPSS, и по Qmax был достигнут к трем месяцам лечения в обеих подгруппах пациентов: и при умеренных, и при выраженных исходных симптомах. Уже после месяца терапии клинически значимое симптоматическое улучшение наблюдали у пациентов обеих групп, тогда как улучшение Qmax более 30% – только у мужчин с исходно выраженной симптоматикой (рис. 1, 3). При этом необходимо учитывать известный факт «начальной базы»:чем выше исходный балл – тем больше снижение показателя [13].
По результатам ранее опубликованных работ известно, что применение МХЛ как в монотерапии, так и в комбинации с α1-АБ изменяют параметры мочеиспускания и несколько увеличивают объем остаточ- ной мочи и частоту ОЗМ [21, 22], в том числе в исследованиях с участием алфузозина и солифенацина [11, 23]. В нашем исследовании у пациентов обеих подгрупп, на фоне увеличения Qmax на 45,1% и 55,9%, через три месяца лечения зарегистрировано достоверное снижение остаточной мочи на 74,1% и 76,5%, соответственно, хотя ее объем исходно и не был значительным (таб. 2).
Безусловно, результаты лекарственной терапии СНМП/ДГПЖ зависят от параметров качества отбора больных. Для повышения ее эффективности, в частности c применением α1-АБ, рекомендуют выстраивать стратегии лечения исходя из дополнительного учета фенотипа пациента, например, путем исключения лиц с чрезмерно большой предстательной железой, выраженной внутрипузырной протрузией и/или средней долей [3, 24]. В обсуждаемом исследовании впечатляющие результаты достигнуты,помимо использования эффективной комбинации препаратов,именно благодаря отбору пациентов с наличием ургентности и гиперактивности мочевого пузыря и исключению лиц с выраженной ИВО механического типа.
Таким образом, настоящее оригинальное наблюдательное исследование продемонстрировало высокую эффективность и безопасность комбинации алфузо-зина (Алфупрост® МР) 10 мг/сут и солифенацина (Везигамп) 5 мг/сут у больных ДГПЖ и ГМП, как с умеренной, так и со значительной исходной выраженностью симптомов нарушенного мочеиспускания. Корректный отбор на лечение обеспечил его благоприятные результаты.
ПШАТШ/ШИИШ
ЛПЕРАТУРА/REFERENCES tadalafil-treated patients with clinically meaningful improvement in lоwеr urinary tгасt symptoms associated with benign prostatic hуроrрlаsiа – integrated data frоm 1,499 study participants. BJU Int 2015;115(5):815-21.
Information about authors:
Сивков А.В. – к.м.н., заместитель директора по научной работе НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия; РИНЦ Author ID 622663,
Пантелеев В.В. – к.м.н., зав. отделом постдипломного образования НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия;
РИНЦ Author ID 989220
Ромих В.В. – зав. отделом уродинамики и нейроурологии НИИ урологии и интер-венционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия; РИНЦ Author ID 691395,
Кукушкина Л.Ю. – научный сотрудник группы уродинамики и нейроурологии отдела общей и реконструктивной урологии НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия; РИНЦ Author ID 6597336
Захарченко А.В. – научный сотрудник отдела уродинамики и нейроурологии НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия;
РИНЦ Author ID 691391
Аполихин О.И. – д.м.н., профессор, чл.-корр. РАН, директор НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия; РИНЦ Author ID 683661,
Каприн А.Д. – д.м.н., профессор, академик РАН, генеральный директор ФГБУ «НМИЦ радиологии» Минздрава России, директор МНИОИ имени П.А. Герцена, зав. кафедрой онкологии и рентгенорадиологии им. В.П. Харченко РУДН, главный внештатный онколог Минздрава России; Москва, Россия; РИНЦ AuthorID 96775,
Вклад авторов:
Сивков А.В. – написание и редактирование текста статьи, 45%
Пантелеев В.В. – сбор и обработка данных, написание текста статьи, 15%
Ромих В.В. – сбор и обработка данных, 10%
Кукушкина Л.Ю. – сбор и обработка данных, 10%
Захарченко А.В. - сбор и обработка данных, 10%
Аполихин О.И. – общее руководство работой, 5%
Каприн А.Д. – общее руководство работой, 5%
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Финансирование: Исследование проведено и опубликовано при финансовой поддержке АО «Ранбакси» (группа компаний SUN PHARMA).
Статья поступила: 15.09.24
Sivkov A.V. – PhD, Deputy Director of N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology – Branch of the National Medical Research Centre of Radiology of the Ministry of Health of Russian Federation; Moscow, Russia;
RSCI Author ID 622663,
Panteleev V.V. – PhD, Head of the Department of Postgraduate Education of
N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology – Branch of the National Medical Research Centre of Radiology of the Ministry of Health of Russian Federation; Moscow, Russia; RSCI Author ID 989220
Romikh V.V. – head of department of urodynamics and neurourology of N. Lopatkin ScientificResearchInstitute of Urology and Interventional Radiology – Branch of the National Medical Research Centre of Radiology of the Ministry of Health of Russian Federation; Moscow, Russia; RSCI Author ID 691395,
Kukushkina L.Yu. – researcher of department of urodynamics and neurourology of
N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology – Branch of the National Medical Research Centre of Radiology of the Ministry of Health of Russian Federation; Moscow, Russia; RSCI Author ID 6597336
Zakharchenko A.V. – researcher of department of urodynamics and neurourology of
N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology – Branch of the National Medical Research Centre of Radiology of the Ministry of Health of Russian Federation; Moscow, Russia; RSCI Author ID 691391
Apolikhin O.I. – Dr. Sci., professor,сor.-member ofRAS, director of N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology – branch of the NationalMedical Research Centreof Radiology of Ministry of health of Russian Federation; Moscow, Russia; RSCI AuthorID 683661;
Kaprin A.D.– Dr. Sci., professor, academician of RAS, general director of the National Medical Research Centre of Radiology of Ministry ofhealth ofRussian Federation, director of
P.A. Herzen Institution, Head of Department of Oncology and Radiology named after
V.P. Kharchenko of RUDN University; Moscow, Russia; RSCI Autor ID 96775;
Authors’ contributions:
Sivkov A.V. – writing and editing the article text, 45%
Panteleev V.V. – data collection and processing, writing the article text, 15%
Romikh V.V. – data collection and processing, 10%
Kukushkina L.Yu. – data collection and processing, 10%
Zakharchenko A.V. – data collection and processing, 10%
Apolikhin O.I. – general supervision of the work, 5%
Kaprin A.D. – general supervision of the work, 5%
Conflict of interest. The authors declare no conflict of interest.
Financing. The study was conducted and published with the financial support of Ranbaxy JSC (SUN PHARMA group of companies).
Received: 15.09.24
Результаты рецензирования: 27.10.24
Исправления получены: 6.11.24
Список литературы Сравнительная эффективность комбинированной терапии препаратами Алфузозин (Алфупрост® МР) и Солифенацин (Везигамп) у больных ДГПЖ и гиперактивным мочевым пузырем с умеренными и выраженными симптомами нарушения функции нижних мочевых путей
- Раснер П.И., Сивков А.В., Харчилава Р.Р. Доброкачественная гиперплазия предстательной железы. Клинические рекомендации. Министерство здравоохранения Российской Федерации 2024:95. [Электроный ресурс]. [Rasner P.I., Sivkov A.V., Kharchilava R.R. Benign prostatic hyperplasia. Clinical guidelines. Ministry of Health of the Russian Federation 2024:95. [Electronic resource]. (In Russian)] URL: https://cr.minzdrav.gov.ru/recomend/6_2.
- Cornu JN, Gacci M, Hashim H, Herrmann TRW, Malde S, Netsch C, et al. Management of non-neurogenic male LUTS. EAU Guidelines. [Electronic resource]. URL: https://uroweb.org/guidelines/management-of-non-neurogenic-male-luts/cha....
- Management of lower urinary tract symptoms attributed to benign prostatic hyperplasia: AUA Guideline. Published 2021; Amended 2023. [Electronic resource]. URL: https://www.auanet.org/guidelines-and-quality/guidelines/benign-prostatic-hyperplasia(bph)-guideline#x18765.
- Сивков А.В., исследовательская группа «АВИАТОР». Эффективность и без-опасность комбинированной терапии препаратами алфузозин (Алфупрост® МР) и солифенацин (Везигамп) у больных доброкачественной гиперплазией предста тельной железы и гиперактивным мочевым пузырем: первые результаты наблюдательного многоцентрового исследования «АВИАТОР». Экспериментальная и клиническая урология 2023;16(4):44-56. [Sivkov A.V., the AVIATOR research group. Efficacy and safety of combination therapy with alfuzosin (Alfuprost® MR) and solifenacin (Vesigamp) in patients with benign prostatic hyperplasia and overactive bladder: first results of the observational multicenter «AVIATOR» study. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and Clinical Urology 2023;16(4):44-56. (In Russian)]. https://doi.org/10.29188/2222–8543–2023–16–4–44–56.
- Djavan B, Marberger M. A meta-analysis on the efficacy and tolerability of alpha1-adrenoceptor antagonists in patients with lower urinary tract symptoms suggestive of benign pros-tatic obstruction. Eur Urol 1999;36:1-13. https://doi.org/10.1159/000019919.
- Mari A, Antonelli A, Cindolo L, Fusco F, Minervini A, De Nunzio C. Alfuzosin for the medical treatment of benign prostatic hyperplasia and lower urinary tract symptoms: a systematic review of the literature and narrative synthesis. Ther Adv Urol 2021;13:1756287221993283. https://doi.org/10.1177/1756287221993283.
- Пушкарь Д.Ю., Лоран О.Б., Берников А.Н. Результаты реальной клинической практики влияния монотерапии алфузозином на сексуальную функцию пациентов с доброкачественной гиперплазией предстательной железы (итоги Российского многоцентрового исследования). Урология 2022;(6):21-9. [Pushkar D.Yu., Loran O.B., Bernikov A.N. The influence of alfuzosin monotherapy on the sexual function of patients with benign prostatic hyperplasia in real clinical practice (results of a Russian multicenter study). Urologiya = Urologiia 2022;(6):21-9. (In Russian)]. https://dx.doi.org/10.18565/urology.2022.6.21-29.
- Song K, Choo MS, Lee KS, Han JY, Lee YS, Kim JC, Cho JC. The long-term effect of alfuzosin in patients with lower urinary tract symptoms suggestive of benign prostate hyperplasia: evaluation of voiding and storage function with respect to bladder outlet obstruction grade and contractility. Urology 2011;77(5):1177–82. https://doi.org/10.1016/j.urology.2010.10.012.
- Van Kerrebroeck P, Haab F, Angulo JC, Vik V, Katona F, Garcia-Hernandez A, et al. Efficacy and safety of solifenacin plus tamsulosin ocas in men with voiding and storage lower urinary tract symptoms: Results from a phase 2, dose-finding study (saturn). Eur Urol 2013;64:398-407. https://doi.org/10.1016/j.eururo.2013.03.031.
- Kim HJ, Sun HY, Choi H, Park JY, Bae JH, Doo SW, et al. Efficacy and safety of initial combination treatment of an alpha blocker with an anticholinergic medication in benign pros-tatic hyperplasia patients with lower urinary tract symptoms: updated metaanalysis. PLoS One 2017;12(1):e0169248. https://doi.org/10.1371/journal.pone.0169248.
- Kaplan SA, He W, Koltun WD, Cummings J, Schneider T, Fakhoury A. Solifenacin plus tamsulosin combination treatment in men with lower urinary tract symptoms and bladder outlet obstruction: a randomized controlled trial. Eur Urol 2013;63(1):158-65. https://doi.org/10.1016/j.eururo.2012.07.003.
- Aso Y, Boccon-Gibod L, Calais Da Silva F, et al. Subjective response, objective response, impact on quality of life. The International Consultation оп Benign Prostatic Нуреrрlаsiа (BPH), Proceedings 1991:87-90. [Electronic resource]. URL: https://iris.who.int/handle/10665/41818.
- Barry MJ, Williford WO, Сhапg Y, Machi M, Jones KM, Walker-Corkery E, Lepor H. Benign рrоstatic hyperplasia specific health status measures in clinical research: how much change in the American Urological Association symptom index and the benign prostatic hyperplasia impact index is perceptible to patients? J Urоl 1995;154(5):1770-4. https://doi.org/10.1016/s0022-5347(01)66780-6.
- American Urological Association (AUA) Benign Prostatic Hyperplasia Guideline Update Рапеl. American Urological Association Guideline: management of Benign Prostatic Hyperplasia (BPH) 2010. [Electronic resource]. URL: https://www.auanet.org/guidelinesand-quality/guidelines/benign-prostatic-hyperplasia-(bph)-guideline.
- Lepor Н. Phase III multicenter placebo-controlled study of tаmsulоsiп in benign prostatic hyperplasia. Tamsulosin Investigator Grоuр. Urology 1998;51(6):892-900. https://doi.org/10.1016/s0090-4295(98)00126-5.
- Nаrауап Р, Tewari A. Меmbеrs of the United States 93-01 study Grоuр. A second phase III multicenter рlасеbо controlled study of 2 dosages of modified rеlеаsе tamsulosin in patients with symptoms of benign prostatic hyperplasia. J Urol 1998;160(5):1701-6.
- Chapple CR, Moпtorsi F, Таmmеlа TL, Wirth M, Koldewijn E, Fernández et al. Silodosin therapy fоr lоwеr urinary tract symptoms in mеn with suspected benign prostatic hyperplasia: results of ап international, randomized, double-blind, placeboand active-controlled clinical trial реrfоrmеd in Еurоре. Еur Urоl 2011;59(3):342-52. https://doi.org/10.1016/j.eururo.2010.10.046.
- Nickel JC, Brock GB, Неrsсhоrп S, Dickson R, Henneges С, Viktrup L. Proportion of tadalafil-treated patients with clinically meaningful improvement in lоwеr urinary tгасt symptoms associated with benign prostatic hуроrрlаsiа – integrated data frоm 1,499 study participants. BJU Int 2015;115(5):815-21. https://doi.org/10.1111/bju.12926.
- Fusсо F, D'Anzео G, Неnnеgеs С, Rоssi I, Вuttner Н, Nickel С. Рrеdiсtоrs of individual response to placebo оr tadalafil 5mg аmопg меn with lоwеr urinary тrасt symptoms secondary to benign prostatic hyperplasia: Аn integrated clinical data mining analysis. PLoS One 2015;10(8):e0135484. https://doi.org/10.1371/journal.pone.0135484.
- Сивков А.В., Голованов С.А., Жукова Л.В. Прогнозирование эффективности терапии СНМП/ДГПЖ экстрактом Serenoa Repens. Урология 2019;(3):14-22. [Sivkov A.V., Golovanov S.A., Zhukova L.V. Prediction of the effectiveness of the therapy of LUTS/BPH by Serenoa Repens extracts. Urologiya = Urologiia 2019;(3):14-22. (In Russian)]. https://doi.org/10.18565/urology.2019.3.14-22.
- Kaplan SA, Roehrborn CG, Rovner EC, Carlsson M, Bavendam T, Guan Z. Tolterodine and tamsulosin for treatment of men with lower urinary tract symptoms and overactive bladder: a randomized controlled trial. JAMA 2006;296(19):2319-28. https://doi.org/10.1001/jama.296.19.2319.
- Blake-James BT, Rashidian A, Ikeda Y, Emberton M. The role of anticholinergics in men with lower urinary tract symptoms suggestive of benign prostatic hyperplasia: a systematic review and meta-analysis. BJU Int 2007;99(1):85-96. https://doi.org/10.1111/j.1464-410X.2006.06574.x.
- Cho HJ, Shin SC, Seo DY, Cho JM, Kang JY, Yoo TK, et al. Comparison of alfuzosin 10 mg with or without propiverine 10 mg, 20 mg in men with lower urinary tract symptom and an overactive bladder: randomised, single-blind, prospective study. Int J Clin Pract 2014;68(4):471-7. https://doi.org/10.1111/ijcp.12339.
- Yuan JQ, Mao C, Wong SY, Yang ZY, Fu XH, Dai XY, Tang JL. Comparative Ef-fectiveness and Safety of Monodrug Therapies for Lower Urinary Tract Symptoms Associated With Benign Prostatic Hyperplasia: A Network Meta-analysis. Medicine (Baltimore) 2015;94(27):e974. https://doi.org/10.1097/MD.0000000000000974.


