Сравнительная эффективность синтетического и биологического протезов в подмышечно-бедренной позиции при лечении критической ишемии нижних конечностей
Автор: Суковатых Б.С., Беликов Л.Н., Родионов О.А., Родионов А.О., Боломатов Н.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.12, 2017 года.
Бесплатный доступ
Представлен анализ комплексного обследования хирургического лечения 60 пациентов с критической ишемией нижних конечностей на почве атеросклеротического поражения аорто-подвздошно-бедренного сегмента и с тяжелыми соматическими заболеваниями, препятствующими выполнению прямых реконструктивных операций на аорте. Все лица были мужского пола, возраст больных колебался от 56 до 78 лет. Пациенты по технологии подмышечно-бедренного шунтирования были разделены на 2 статистически однородные группы по 30 человек в каждой. Пациентам первой группы в качестве шунта применялся синтетический политетрафторэтиленовый протез, а во второй группе - биологический протез из внутренней грудной артерии быка.
Критическая ишемия, нижние конечности, синтетический политетрафторэтиленовый протез, биологический протез из внутренних грудных артерий быка
Короткий адрес: https://sciup.org/140188633
IDR: 140188633 | УДК: 616.718-005.4:615.477.2
Comparative efficacy of synthetic and biological prostheses in axillary-femoral position in the treatment of critical limb ischemia
The analysis of complex examination of surgical treatment of 60 patients with critical lower limb ischemia on the basis of atherosclerotic lesions of the aorto-iliac-femoral segment and with severe medical conditions that prevent the implementation of direct reconstructive operations on the aorta. All the faces were male, age of the patients ranged from 56 to 78 years. Patients on the axillary-femoral bypass technology were divided into 2 statistically homogeneous groups of 30 people each. Patients of the first group was used as a synthetic polytetrafluoroethylene graft prosthesis, while the second group - biological prosthesis of bovine internal thoracic artery.
Текст научной статьи Сравнительная эффективность синтетического и биологического протезов в подмышечно-бедренной позиции при лечении критической ишемии нижних конечностей
Одной из основных причин развития критической ишемии является атеросклеротическое поражение аорто-подвздошного и бедренно-подколенного сегментов артериального русла нижних конечностей [6, 7]. Прямые реконструктивные операции на аорте в виде аорто-бедренного шунтирования или протезирования достаточно эффективны. Через 5 лет функционируют от 70 до 85% шунтов, избежать потери конечности удается в 90–95% случаев [4, 11]. Нерешенной проблемой является лечение больных с тяжелой соматической патологией, у которых имеется высокий операционноанестезиологический риск IV степени по шкале ASA, что препятствует выполнению прямых реконструктивных операций на аорте [1, 14]. Даная группа больных обычно страдает 2–3 сопутствующими заболеваниями, которые находятся в стадии декомпенсации и плохо коррегиру-ются традиционной лекарственной терапией [3, 10]. Единственной реальной возможностью спасения пораженной конечности при двухстороннем поражении подвздошных артерий является операция аллошунти-рования из отдаленных сосудистых бассейнов: из подключичной или подмышечной артерии в бедренную [2, 9]. При бедренно-подмышечных транспозициях в качестве шунта используются синтетические протезы из пористого политетрафторэтилена. Результаты их применения в подмышечно-бедреной позиции оставляют желать лучшего. Синтетические шунты функционируют не более 1 года, спасти конечность удается не более чем у 30–35% больных, что обусловлено низкой фракцией выброса левого желудочка у пациентов менее 40%, плохой биосовместимостью синтетического протеза с анастомозируемыми артериями, многоуровневым поражение дистального русла [12]. Отрицательно влияет на результаты лечения традиционная технология проведения шунта по передней поверхности туловища, при которой хирург формирует канал в подкожной клетчатке в слепую, путем разрушения тканей пальцами. При этом возникает необходимость выполнения дополнительных разрезов на грудной клетке, передней брюшной стенке, что приводит к травматизации тканей, околопротезным гематомам и инфицированию протеза. Кроме того, в традиционной технике операции канал проходит по передней подмышечной линии, что может вызывать сдавление шунта во время сна при повороте больного на бок [13].
Проведенные в нашей клинике экспериментальные исследования раневого процесса в стенке артерии показали, что при имплантации биологического протеза репаративные соединительнотканые процессы в стенке артерии в 3 раза менее выражены, чем при имплантации синтетического протеза. Очень интенсивный репаративный процесс приводит к увеличению жесткости сосуда, что ухудшает гемодинамику зоны анастомозов и способствует прогрессированию атеросклеротического

процесса [8]. Поэтому представляется целесообразным сравнить эффективность синтетического и биологического протезов в подмышечно-бедренной позиции у пациентов с высоким операционно-анестезиологическим риском.
Цель исследования : улучшить результаты лечения больных с критической ишемией нижних конечностей и высоким операционно-анестезиологическим риском путем оптимизации методики подмышечно-бедренного шунтирования.
Материалы и методы
Проведен анализ хирургического лечения 60 больных мужского пола, страдающих критической ишемией нижних конечностей. Возраст больных колебался от 56 до 78 лет. Причиной заболеваний было двухстороннее атеросклеротическое поражение аорто-подвздошного сегмента (синдром Лериша). Больные были разделены на две группы. Первую группу составили 30 пациентов, которым выполнено подмышечно-бедренное шунтирование синтетическим политетрафторэтиленовым протезом. Во вторую группу вошли 30 пациентов, которым было выполнено протезирование биологическим протезом из внутренних грудных артерий быка. Диаметр синтетического протеза 8 мм, биологического протеза – дистальный конец 4мм, проксимальный – 6 мм.
Оперативное вмешательство проводили под интубационным наркозом. Положение больного на операционном столе – на спине. Операцию начинали с выделения бедренных сосудов в паховой области. Визуально и пальпаторно оценивалось состояние сосудов и возможность их реконструкции. Если была проходима хотя бы одна из артерий (поверхностная или глубокая), начинали выделять терминальный отдел подключичной и проксимальный отдел подмышечной артерий. Кожный разрез выполняли на 2 см ниже и параллельно ключице, на 2 см латеральнее от края грудины. Разрез продолжали до края подключичной мышцы, по ходу sulcus deltoideapectoralis до уровня головки плечевой кости. Тупо разделяли волокна ключичной порции большой грудной мышцы. Рассекали ключично-грудную фасцию и выделяли в рыхлой клетчатке грудинно-ключичного треугольника дистальный конец подключичной и начальный отдел подмышечной артерий. Выделяли и пересекали сухожильную часть малой грудной мышцы. Продолжали выделять подмышечную артерию в дистальном направлении. Мелкие артерии – артерия грудной клетки и плечевого отростка, боковая артерия груди, а также мышечные веточки и сопутствующие им вены пересекали и перевязывали. Общая длина выделенного артериального ствола составляла 6–8 см. Затем приступали к созданию канала для проведения шунта. Следует подчеркнуть, что формирование канала – самый травматичный и ответственный момент операции подмышечно-бедренного шунтирования. С целью устранения вышеизложенных недостатков нами для формирования туннеля и проведения в нем сосудистого протеза, сконструировано специальное устройство, по форме напоминающее костыль. Устройство состоит из металлической трубы из нержавеющей стали диаметром 10 мм и длиной 900 мм с навинчивающейся на обеих концах резьбой, съемной ручки и двух олив диаметром 10 и 20 мм (рис. 1).
Меньшая олива (направляющая) предназначена для создания туннеля от бедренной до подмышечной артерии. Большая олива (разрушающая) предназначена для расширения туннеля и разрыва паратуннельных фиброзных тяжей, что позволяет избежать его сдавления в периоперационном периоде. На конце большой оливы имеется набалдашник диаметром 5 мм, к которому фиксируется протез. На дистальный конец трубы навинчивается изогнутая под углом 1200 ручка, что облегчает введение туннелизатора в рану, а на проксимальный – съемные оливы, снабженные на одном конце резьбой для ввинчивания в трубу. Формирование туннеля начинали из раны в паховой области. Туннелизатор с оливой 10 мм проводили под пупартовую связку, а затем под апоневрозом наружной косой мышцы живота. На уровне реберной дуги канал формировали в подкожной клетчатке, а на грудной клетке – под большой грудной мышцей по среднеключичной линии. Накладывали анастомоз между подмышечной артерии и протезом по типу “конец в бок” с расположением «пятки» анастомоза проксимально и «носка» протеза дистально, что позволяет направить поток крови по передней поверхности туловища. После оценки герметичности и проходимости проксимального анастомоза путем пробного пуска кровотока меняли оливу 10 мм на головке туннелизатора на оливу 20 мм для увеличения диаметра канала при тракции в обратном направлении. Капроновой нитью фиксировали протез к набалдашнику оливы и обратной тракцией туннелиза-
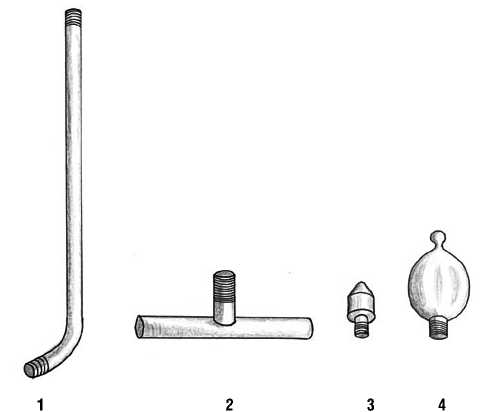
Рис. 1. Устройство для проведения подмышечно-бедренного шунта: 1 – мталлическая труба; 2 – рукоятка; 3 – направляющая олива;
4 – разрушающая олива
тора проводили протез по каналу. Выполняли пробное кровопускание, чтобы убедиться, что сдавление и перегиб протеза отсутствуют.
После того, как сосудистый протез уложен в канале по передней грудной и брюшной стенках, накладывали нижний анастомоз с бедренными сосудами по типу «конец в бок». После пуска кровотока оценивали пульсацию протеза и сосудов в ране. Раны послойно ушивали. Схема подмышечно-бедренного шунтирования представлена на рис. 2.
Диагностическая программа была традиционной и включала функциональные (реовазография, допплерография, фотоплетизмография), ультразвуковые (ангиосканирование) и рентгенологические (аортоарте-риография) методы исследования. Изменение интенсивности артериального кровотока после операции регистрировали по динамике реовазографического индекса (РИ) и лодыжечно – плечевого индекса (ЛПИ); а микроциркуляции – по динамике фотоплетизмографического индекса (ФИ).
Результаты лечения оценивались на основании степени изменения клинического статуса по отношению к периоду до операции по шкале Ruterford et. аl., которая рекомендована в качестве стандарта Российским обществом ангиологов и сосудистых хирургов [5]. В соответствии с международными рекомендациями проведена оценка «качества жизни» больных до и через 12 месяцев после лечения, на основании анкетного обследования пациентов с помощью опросника MOS SF-36, нормированного для сосудистых больных [15]. Для сравнения использовались показатели «качества жизни» в контрольной группе лиц (n = 30) без хронической ишемии нижних конечностей, рандомизированных по полу, возрасту и сопутствующей патологии. Качество жизни оценивали сами больные по 8 шкалам: физическое функционирование (ФФ), физическая роль (ФР), физическая боль (ФБ), общая оценка здоровья (ООЗ), жизненная активность (ЖА), эмоциональная роль (ЭР), социальное функционирование (СФ), психическое здоровье (ПЗ). Шкалы группировали в 2 интегральных показателя: физический компонент здоровья (ФКЗ) и психический компонент здоровья (ПКЗ).
Результаты исследования
Распределение больных по характеру сопутствующей соматической патологии представлено в таблице 1.
Из таблицы видно, что 100% пациентов страдали тяжелыми соматическими заболеваниями. При этом у всех больных отмечалось 2–3 заболевания, которые резко нарушали функцию жизненно важных органов. Фракция выброса крови из левого желудочка сердца у пациентов обеих групп не имела статистически достоверных различий и колебалась в пределах 42 ± 8%. По шкале ASA американского общества анестезиологов у всех пациентов была четвертая степень операционно-анестезиологического риска, препятствующая выполнению прямых реконструктивных операций на аорте.
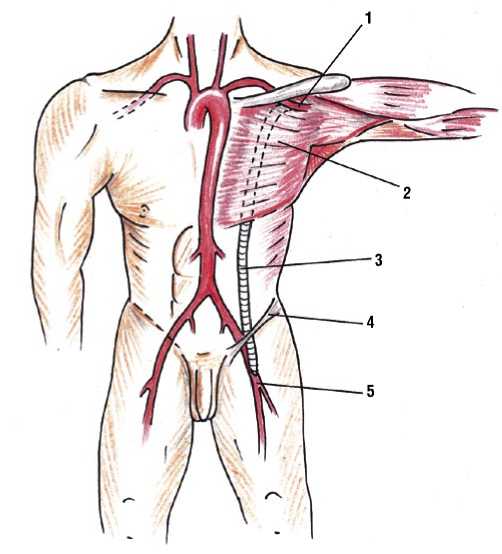
Рис. 2. Схема подмышечно-бедренного шунтирования: 1 – подмышечная артерия; 2 – большая грудная мышца; 3 – шунт; 4 – паховая связка; 5 – бедренная артерия
Табл. 1. Частота сопутствующей соматической патологии
|
Сопутствующие заболевания |
Первая группа (n = 30) |
Вторая группа (n = 30) |
||
|
Абс. |
% |
Абс. |
% |
|
|
ИБС, III-IV функциональный класс, постинфарктный кардиосклероз, сердечная недостаточность II Б–III стадии |
20 |
66,6 |
22 |
73,3 |
|
Артериальная гипертензия III стадии, хроническая сердечная недостаточность II Б стадии |
28 |
93,3 |
28 |
93,3 |
|
Хроническая обструктивная болезнь легких, легочная недостаточность |
8 |
26,6 |
3 |
10 |
|
Сахарный диабет |
10 |
33,3 |
9 |
30 |
|
Церебральный атеросклероз, перенесенный инсульт |
26 |
86,6 |
25 |
83,3 |
Частота и характер поражения артерий нижних конечностей представлены в таблице 2.
У больных как в первой, так и во второй группах зарегистрировано многоуровневое поражение артериального русла нижних конечностей. Аорто-подвздошный сегмент был поражен у 60 (100%), бедренно-подколенный сегмент – у 40 (66,7%), голеностопный – у 12 (20%) больных.
Результаты изучения макрогемодинамики и микроциркуляции пораженной нижней конечности до и после оперативного лечения представлены в таблице 3.
Табл. 2. Частота окклюзионно-стенотических изменений артерий нижних конечностей
|
Характер поражения артерий |
Первая группа (n = 30) |
Вторая группа (n = 30) |
||
|
Абс. |
% |
Абс. |
% |
|
|
Окклюзия обеих подвздошных артерий |
24 |
80 |
23 |
76,7 |
|
Окклюзия одной и стеноз контралатеральной подвздошной артерий |
6 |
20 |
7 |
23,3 |
|
Окклюзия общей бедренной артерии |
7 |
23,3 |
8 |
26,7 |
|
Окклюзия поверхностной бедренной артерии |
7 |
23,3 |
9 |
30 |
|
Стеноз глубокой артерии бедра |
4 |
13,3 |
5 |
16,6 |
|
Стеноз подколенной и берцовых артерий |
5 |
16,6 |
7 |
23,3 |
Табл. 3. Динамика показателей артериального кровотока и микроциркуляции до и после оперативного лечения
|
Показатели исследования |
Первая группа (n = 30) |
Вторая группа (n = 30) |
||
|
До операции |
После операции |
До операции |
После операции |
|
|
РИ |
0,15 ± 0,03 |
0,35 ± 0,03* |
0,17 ± 0,04 |
0,4 ± 0,05* |
|
ЛПИ |
0,24 ± 0,03 |
0,75 ± 0,03* |
0,26 ± 0,05 |
0,77 ± 0,06* |
|
ФИ (%) |
25 ± 5% |
65 ± 5%* |
27 ± 5% |
66 ± 7%* |

Примечание : *– P < 0,05 между показателями после операции и до операции в первой и во второй группах.
Из таблицы видно, что как синтетический, так и биологический протез значительно повышают объемный и магистральный кровоток, уровень микроциркуляции в пораженной нижней конечности. Статистически достоверной разницы в показателях между группами больных не обнаружено.
В первой группе в раннем послеоперационном периоде у 9 (30%) больных развились следующие осложнения: у 3 (10%) – ранний тромбоз шунта, у 3 (10%) – инфицирование шунта и у 2 (6,7%) – аневризма проксимального анастомоза, и у 1 (3,3%) – серома шунта. Во второй группе послеоперационные осложнения обнаружены у 5 (16,7%) больных: в 2 (6,7%) случаях ранний тромбоз шунта, в 2 (6,7%) случаях инфицирование шунтов и в 1 (3,3) случае разрыв шунта. Больные с ранними тромбозами, аневризмами проксимальных анастомозов и разрывов шунтов были повторно прооперированы. Проходимость шунтов восстановлена. Массивная антибиотикотерапия и адекватное дренирование позволили купировать воспалительный парапротезный процесс у больных с инфицированием шунтов. Благодаря применению разработанного нами устройства ни у одного больного не возникли сдавления, перегибы и перекручивания сосудистого протеза в канале, не образовалась парапротезная гематома, и не было необходимости в выполнении дополнительных контролирующих разрезов.
В первой группе в отдаленном послеоперационном периоде у 22 (73,3%) больных наступил тромбоз синтетического протеза. Средний срок функционирования шунта в первой группе составил 305 ± 34 суток. После прекращения работы шунта у 12 (40%) ишемия конечности прогрессировала и этим больным выполнена высокая ампутация конечности. У 10 (33,3%) больных после тромбоза шунта критическая ишемия не рецидивировала. У 8 (26,7%) больных протезы продолжают функционировать.
Во второй группе в отдаленном послеоперационном периоде тромбоз биологического протеза развился у 13 (43,3%) больных. Средний срок функционирования шунтов в основной группе составил 562 ± 32 суток (P < 0,05 по сравнению с первой группой). После тромбоза биологического протеза у 9 (30%) больных ишемия конечности прогрессировала, что потребовало выполнения ампутации бедра. У 4 (13,3%) пациентов ишемия не рецидивировала. У 17 (56,7%) протезы продолжают функционировать.
С нашей точки зрения небольшие средние сроки функционирования как синтетического, так и биологического протезов были обусловлены с одной стороны плохой насосной функцией сердца из-за наличия у пациентов сопутствующей соматической патологии, а с другой стороны – многоуровневым поражением артериального русла нижних конечностей.
Результаты оценки степени изменения клинического статуса по отношению к периоду до операции представлены в таблице 4.
В исследуемой группе количество пациентов со значительным улучшением клинического статуса увеличилось на 16,6%, с умеренным улучшением – на 13,4%, а со значительным ухудшением снизилось на 10%.
В течение первого года после операции умерло 5 пациентов от прогрессирования тяжелых соматических заболеваний.
Результаты оценки «качества жизни» пациентов представлены в табл. 5.
Из таблицы видно, что критическая ишемия снижает все показатели качества жизни больных. При этом интегральный показатель физический компонент здоровья снижается в 2,9 раза, а психический – в 2,2 раза. Традиционная технология лечения с применением синтетического протеза вызывает повышение физического компонента здоровья на 10,8%, а психического – на 14,2%
Табл. 4. Динамика клинического статуса больных ХОЗАНК после проведенного лечения
|
Баллы |
Эффективность |
Первая группа (n = 30) |
Вторая группа (n = 30) |
|
+3 |
Значительное улучшение |
5 (16,7%) |
10 (33,3%) |
|
+2 |
Умеренное улучшение |
3 (10%) |
7 (23,4%) |
|
+1 |
Минимальное улучшение |
10 (33,3%) |
4 (13,3%) |
|
0 |
Без изменений |
– |
– |
|
-1 |
Минимальное ухудшение |
– |
– |
|
-2 |
Умеренное ухудшение |
– |
– |
|
-3 |
Значительное ухудшение |
12 (40%) |
9 (30%) |
Табл. 5. Оценка «качества жизни» больных до и через 12 месяцев после лечения
|
Шкала SF-36 |
Здоровая популяция жителей России (n = 30) |
Больные до лечения (n = 60) |
Первая группа (n = 27) |
Вторая группа (n = 28) |
|
ФФ |
96,1 ± 1,7 |
30,1 ± 2,3# |
34,3 ± 4,5* |
40,2 ± 5,9* ** |
|
РФ |
90,2 ± 1,8 |
19,1 ± 2,1# |
22,4 ± 6,4* |
25,5 ± 9,6* ** |
|
ФБ |
89,4 ± 2,1 |
45,5 ± 3,1# |
51,2 ± 3,2* |
58,8 ± 4,1* ** |
|
ООЗ |
73,2 ± 1,9 |
38,4 ± 1,2# |
42,4 ± 5,7* |
50,4 ± 9,8* ** |
|
ЖА |
60,2 ± 2,8 |
15,2 ± 3,2# |
18,3 ± 4,3* |
20,7 ± 4,7* |
|
СФ |
84,2 ± 3,2 |
47,7 ± 2,3# |
51,2 ± 4,5* |
57,2 ± 4,7* ** |
|
ПЗ |
62,4 ± 1,2 |
18,7 ± 3,2# |
19,3 ± 4,2 |
20,2 ± 5,1 |
|
ЭР |
61,1 ± 1,7 |
30,3 ± 4,5# |
34,3 ± 7,6* |
43,1 ± 10,1* ** |
|
ФКЗ |
87,3 ± 1,9 |
29,5 ± 2,3# |
32,7 ± 2,5* |
36,9 ± 1,9* ** |
|
ПКЗ |
67,0 ± 2,0 |
30,2 ± 1,5# |
35,2 ± 2,4* |
38,4 ± 2,3* ** |
Примечание: # – р < 0,001 в сравнении с показателями больных с показателями до лечения и здоровыми лицами; * – р < 0,05 в сравнении с показателями до лечения; ** – р < 0,05 в сравнении с показателями контрольной группы.
по сравнению с периодом до лечения. Применение биологического протеза позволяет повысить физический компонент здоровья на 12,8%, а психический – на 9,1% по сравнению с группой больных, которым применялся синтетический протез.
Обсуждение
Проведенные исследования показали, что применение разработанного нами устройства позволяет облегчить создание канала для проведения шунта на передней поверхности туловища пациента. В ближайшем послеоперационном периоде вид протеза не влияет на показатели гемодинамики и микроциркуляции в пораженной конечности. В отдаленном послеоперационном периоде увеличение сроков функционирования биологического протеза обусловлено его большей биосовместимостью, чем синтетического протеза. Применение в качестве шунта биологического протеза при подмышечно-бедренных шунтированиях показано при многоуровневом поражении артериального русла нижних конечностей с наложением дистального анастомоза на глубокую артерию бедра. При сохраненной проходимости общей бедренной артерий целесообразно применять синтетический протез с наложением анастомоза на общую бедренную артерию с обязательным выполнением профундопластики.
Выводы
-
1. При подмышечно-бедренном аллопротезировании для проведения шунта целесообразно использовать оригинальный туннелизатор, состоящий из металлической трубки диаметром 10 мм и длиной 900 мм, с ручкой на дистальном конце и со съемными оливами на проксимальном конце диаметром 10 и 20 мм, что позволяет избежать сдавления, перегиба и перекручивания шунта, образования парапротезной гематомы и необходимости выполнения дополнительных разрезов.
-
2. Применение в качестве шунта биологического протеза при подмышечно-бедренных транспозициях патогенетически обосновано, не требует создания специальных конструкций, не вызывает специфические осложнения и позволяет в ближайшем послеоперационном периоде снизить количество ранних послеоперационных осложнений на 13,3% , поздних тромбозов шунта на 30%, удлинить средний срок функционирования шунтов в 1,8 раза, повысить физический компонент здоровья – на 12,8%, а психический – на 9,1%.
Список литературы Сравнительная эффективность синтетического и биологического протезов в подмышечно-бедренной позиции при лечении критической ишемии нижних конечностей
- Кобак А.Е., Лембриков И.А., Немков А.С. и др. Оценка риска развития осложнений после шунтирования брюшного отдела аорты//Вестник хирургии. -2012. -№6. -С. 100-103.
- Леменев В.Л. Операция шунтирования из отдаленных сосудистых бассейнов в лечении критической ишемии нижних конечностей у больных пожилого и старческого возраста//Хирургия. -2003. -№ 12. -С. 27-33.
- Покровский А.В. Клиническая ангиология: руководство для врачей в 2 томах под редакцией А.В. Покровского. -М.: Медицина, 2004. -804 с.
- Родионов П.А., Сонькин И.Н., Крылов О.В. и др. Первый опыт мини-лапаротомии при синдроме Лериша//Вестник хирургии. -2011. -№3. -С. 27-29.
- Российский консенсус «Рекомендованные стандарты оценки результатов лечения пациентов с хронической ишемией нижних конечностей». -М.: Медицина, 2001. -29 с.
- Савельев В.С., Кошкин В.М. Критическая ишемия нижних конечностей. -М.: Медицина, 1997. -160 с.
- Сафонов В.А., Ганичев А.Ф., Ким И.Н. и др. Опыт применения сосудистых биопротезов «Кемангиопротез» в реконструктивной хирургии магистральных артерий нижних конечностей//Ангиология и сосудистая хирургия. -2009. -№2. -С. 103-106.
- Суковатых Б.С., Веденев Ю.И., Родионов А.О. Сравнительная характеристика раневого процесса в артериальной стенки после имплантации синтетического и биологического эндопротезов//Новости хирургии. -2013. -Т. 21, №3. -С. 9-15.
- Ascer E, Veith FJ. Comparison of axillounifemoral and axillobifemoral bypass operations.//Surgery. -1985. -Vol. 97. -P. 169-174.
- Christine J. Olson. Repeat axillofemoral grafting as treatment for axillofemoral graft occlusion//Archives of surgery. -2002. -Vol. 37, № 12. -P. 1364-1368.
- Conte M.S. Bypass versus Angioplasty in Severe Ischemia of the Leg (BASIL) and the (hoped for) dawn of evidence-based treatment for advanced limb ischemia//J. Vasc. Surg. -2010. -Vol.51 (Suppl. S). -P. 69-75.
- Martin D, Katz SG. Axillofemoral bypass for aortoiliac occlusive disease.//Am J Vasc Surg. -2000. -Vol. 180. -P. 100-105.
- Mohan CR, Sharp WJ. A comparative evaluation of externally supported polytetrafluoroethylene axillobifemoral and axillounifemoral bypass grafs.//J Vasc Surg. -1995. -Vol. 21. -P. 801-806.
- Passman MA, Taylor LM. Comparison of axillofemoral and aortofemoral bypass for aortoiliac occlusive disease.//J Vasc Surg. -1996. -Vol. 23. -P. 263-267.
- Ware J.E., Sherbourne C.D. The MOS 36-item short form health survey (SF-36): conceptual framework and item selection//Med. Care -1992 -Vol. 30. -P. 473-483.


