Сравнительная экспрессия рекомбинантной фосфолипазы А2 в Komagataella phaffii в зависимости от модификации сигнального пептида альфа-фактора
Автор: Бытяк Д.С., Гладченко Ю.А., Ряполова А.В., Корнеева О.С., Мотина Е.А.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 1 (87), 2021 года.
Бесплатный доступ
В настоящее время Российский рынок ферментных препаратов фосфолипазы А2 представлен коммерческими препаратами иностранных производителей: Nagase (Япония) и Maxapal (Нидерланды). Однако растущий спрос и необходимость снижения себестоимости производства фосфолипазы А2 требуют разработки новых суперпродуцентов фосфолипазы А2. В связи с чем целью работы является сравнительная экспрессия рекомбинантной фосфолипазы А2 в Komagataella phaffii в зависимости от модификации сигнального пептида альфа-фактора. Объектом исследования является дрожжевой штамм-реципиент Komagataella phaffii X-33. Исследования проводились в соответствии с общепринятыми нормами и подходами. Для работы использованы гены фосфолипазы А2 из Streptomyces violaceoruber. Целевые последовательности синтезированы в компании «Евроген» (Россия) и заклонированы в составе TE-вектора pUC57. В ходе выполнения работы проведена сборка генетических конструкций pPICZaA-Pla2 и PPICZmf4iA-Pla2, содержащих ген фосфолипазы А2 Streptomyces violaceoruber под нативным сигналом a-MF и его модификацией mf4i. Также проведена трансформация дрожжей Komagataella phaffii X-33 полученными генетическими конструкциями. В результате проведенных исследований показано, что в среднем достоверных отличий в уровне экспрессии и удельной активности рекомбинантной фосфолипазы А2 метилотрофными дрожжами K. Phaffii X-33 при использовании нативного сигнала секреции a-MF и его модифицированного варианта mf4i не обнаружено. Однако использование фактора секреции mf4i позволяет получить более высокую продукцию фосфолипазы А2 у отдельных клонов (трансформантов). Полученные данные указывают на перспективность использования фактора секреции mf4i для создания сверхпродуцентов ферментов на основе дрожжей K. Phaffii X-33.
Фосфолипаза а2, генная инженерия, биотехнология ферментов, экспрессия, aox промотор, сигнальный пептид
Короткий адрес: https://sciup.org/140257332
IDR: 140257332 | УДК: 577.21 | DOI: 10.20914/2310-1202-2021-1-263-269
Comparative expression of recombinant phospholipase A2 in Komagataella phaffii depending on the modification of the alpha-factor signaling peptide
Currently, the Russian market of phospholipase A2 enzyme preparations is represented by commercial preparations of foreign manufacturers: Nagase (Japan) and Maxapal (the Netherlands). However, the growing demand and the need to reduce the cost of production of phospholipase A2 require the development of new super-producers of phospholipase A2. In this connection, the aim of the work is to compare the expression of recombinant phospholipase A2 in Komagataella phaffii depending on the modification of the alpha-factor signaling peptide. The object of the study is the recipient yeast strain Komagataella phaffii X-33. The studies were conducted in accordance with generally accepted norms and approaches. Phospholipase A2 genes from Streptomyces violaceoruber were used for this worK. The target sequences were synthesized in the company "Eurogen" (Russia) and cloned as part of the TE vector pUC57. In the course of the work, the genetic constructs pPICZaA-Pla2 and PPICZmf4iA-Pla2 containing the Streptomyces violaceoruber phospholipase A2 gene were assembled under the native signal a-MF and its modification mf4i. The transformation of the yeast Komagataella phaffii X-33 with the obtained genetic constructs was also carried out. As a result of the conducted studies, it was shown that on average, there were no significant differences in the level of expression and specific activity of recombinant phospholipase A2 in methylotrophic yeast K. Phaffii X-33 when using the native a-MF secretion signal and its modified version mf4i. However, the use of the secretion factor mf4i allows for higher production of phospholipase A2 in individual clones. The obtained data indicate the prospects of using the secretion factor mf4i to create super-producers of enzymes based on yeast K. Phaffii X-33.
Текст научной статьи Сравнительная экспрессия рекомбинантной фосфолипазы А2 в Komagataella phaffii в зависимости от модификации сигнального пептида альфа-фактора
Фосфолипазы А2 (РLА2) – одни из самых изученных фосфолипаз, представляют собой липолитические ферменты, катализирующие гидролиз ацильной связи sn-2 в молекуле гидрофосфолипида, что ведет к освобождению свободных жирных кислот и лизофосфолипидов [1]. В ряде работ у РLА2 доказаны антибактериальные [2], противовирусные [3–5], противопара-зитарные [6, 7], антитромбоцитарные [8], гипотензивные [8], противоопухолевые свойства [9]. Кроме того, РLА2 применяются в одном из важнейших этапов рафинирования масла – его гидратации [10]. Особое место РLА2 занимает в промышленном производстве майонеза при ферментативном гидролизе яичного лецитина до изолецитина. Это обеспечивает более высокую стойкость эмульсии и требуемые реологические характеристики майонеза [11, 12]. В настоящее время на рынке России представлено несколько коммерческих ферментных препаратов рекомбинантной ФЛА2: «Nagase» (Япония), нативный штамм-продуцент Streptomyces violaceoruber ; «Maxapal» (Нидерланды), ФЛА2 поджелудочной железы свиней, штамм-продуцент Aspergillus niger . Однако растущие потребности рынка в производстве продуктов питания требуют разработки новых суперпродуцентов РLА2.
Одним из наиболее перспективных продуцентов РLА2 считается представитель метило-трофных дрожжей Komagataella phaffii (ранее Pichia pastoris ). Вид характеризуется высокой скоростью роста, способностью к оптимальному гликозилированию рекомбинантных белков, наличием механизмов эффективной секреции продуцируемых ферментов в культуральную среду, низкой секрецией протеаз и других собственных белков в культуральную среду, наличием регулируемого AOX-промотора [13, 14].
Ранее Liu et. el. был получен штамм-продуцент рекомбинантной РLА2 на основе K. phaffii GS115 с продукцией РLА2 из St. Viola-ceoruber на уровне 34,7 ± 0,2 ед./мл [15], что выше, чем у прокариотических штаммов-продуцентов РLА2 St. violaceoruber (0,5 ед./мл) и Escherichia coli (0,2 ед./мл) [16], однако все же не является достаточным для рентабельного промышленного производства.
Существует целый ряд факторов, определяющих эффективность экспрессии гетерологичных белков, в частности, оптимизация нуклеотидной последовательности целевого гена и повышение его копийности в геноме, оптимизация промотора, выбор сигнального пептида для секретируемых белков [17]. Для секреции гетерологичных белков в K. phaffii наиболее эффективен пре-про-пептид α-фактора (α-MF).
В настоящее время α-MF является наиболее широко распространенным сигнальным пептидом для секреции рекомбинантных белков и именно с ним удаётся добиться высокой экспрессии. Для улучшения вывода белка в настоящее время используют также разные модификации α-MF, полученные в результате направленной эволюции аминокислотного состава, мутаций, объединения с другими лидерными белками и т. д. Одним из перспективных вариантов α-MF может быть синтетический mf4i, с которым удалось повысить экспрессию рекомбинантной фитазы более чем в 3 раза относительно нативного альфа-фактора.
Цель работы – сравнение экспрессии РLА2 в Komagataella phaffii X-33 при использовании нативного α-MF и модифицированного синтетического сигнального пептида α-MF mf4i.
Материалы и методы
Для работы использованы гены фосфолипазы А2 (Рlа2) из Streptomyces violaceoruber (патент на изобретение RU 26763210), и модифицированного сигнала α – MF mf4i (GeneBank, No АY145833.1). Ген Рlа2 оптимизирован для эффективной экспрессии в K. phaffii в соответствии с частотой встречаемости кодонов [18].
Последовательность гена фосфолипазы А2, в соответствии с патентом на изобретение RU 26763210:
GATCCAGCAGATAAACCTCAAGTTTT GGCATCATTCACCCAGACATCCGCATCAT CCCAGAACGCATGGTTGGCCGCTAACAGA AACCAATCTGCTTGGGCTGCTTACGAATTT GATTGGTCTACTGATTTGTGTACTCAAGCT CCAGATAACCCTTTTGGTTTCCCATTCAAC ACTGCTTGTGCTAGACATGATTTCGGTTAC AGAAACTATAAGGCTGCTGGTTCTTTTGAT GCTAACAAGTCCAGAATTGATTCTGCTTTC TATGAGGATATGAAGAGAGTCTGCACTGG TTATACCGGAGAGAAGAACACTGCCTGTA ATTCCACTGCCTGGACCTACTATCAAGCCG TAAAAATTTTTGGT.
Целевые последовательности синтезированы в компании «Евроген» (Россия) и заклонированы в составе ТЕ-вектора рUС57.
Далее рестрикционно-лигазным методом проводили вставку гена Рlа2 в состав векторов экспрессии рРIСZаlрhаА и рРIСZА (Invitrogen, USA). Для этого с плазмиды рUС57-Рlа2 амплифицировали фрагмент ДНК, соответствующий гену Рlа2, праймерами Рlа2 for 5’ – ATATGAATTCGCTCCAGCAGATAAACC-3’ и Рlа2 rev 5’ – ATATGTCGACTCAACCAAA AATCTTTACG-3’ на амплификаторе Т100 (BioRad, USA) с помощью полимеразы Phusion (NEB, England). Полученный фрагмент длиной 366 п.о. клонировали в состав векторов рРIСZаА и рРIСZА по сайтам ЕсоRI и NоtI. Продуктами лигирования трансформировали химически компетентные клетки Escherichia coli Xl10Gold (Stratagen, USA). Корректность нуклеотидной последовательности гена Рlа2 в составе полученных конструкций рРIСZаlрhаА-Рlа2 и рРIСZА-Рlа2 выросших на селективных средах с зеоцином (25 мкг/мл) была подтверждена картированием и секвенированием ДНК в компании Евроген (Россия).
Для сборки конструкции рРIСZmf4iА-рlа2 TA-вектор, содержащий часть гена mf4i, и полученную конструкцию рРIСZА-Рlа2, обрабатывали эндонуклеазами рестрикции ВstВI и ХhоI (СибЭнзим, Россия). Очистку целевых фрагментов ДНК проводили в 1% агарозном геле с последующей элюцией набором CleanUp Mini (Евроген, Россия) и лигированием с использованием Т4 ДНК-лигазы (СибЭнзим, Россия). Продуктами лигирования трансформированы химически компетентные клетки E. coli Xl10Gold (Stratagen). Корректность нуклеотидной последовательности гена mf4i в составе полученной плазмиды рРIСZmf4iА-Рlа2 подтверждали секвенированием.
Генетическая трансформация K. phaffii . Далее собранные генетические конструкции рРIСZаА-Рlа2 и рРIСZmf4iА-Рlа2 использовали для генетической трансформации штамма K. phaffii X-33 (Invitrogen, USA). На каждую трансформацию использовали по 10 мкг плазмид рРIСZаlрhаА-Рlа2 и рРIСZmf4iА-Рlа2, линеаризованных по сайту ВstХI в области AOX-промотора. Трансформация линеаризованными плазмидами штамма K. phaffii X-33 осуществлялась согласно протоколу Invitrogen [19]. Отбор трансформантов проводился на среде YPD с зеоцином (250 мкг/мл). Экспрессионная кассета, интегрируемая в геном K. phaffii представлена на рисунке 1.
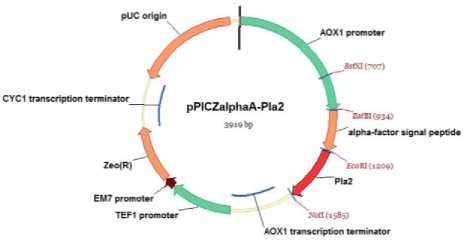
Рисунок 1. Карта вектора экспрессии рРIСZаlрhаА-Рlа2
Figure 1. Map of the рРIСZаlрhаА-Рlа2 expression vector
Экспрессия РLА2 в K. phaffii X-33 . Полученные в результате трансформации K. phaffii X-33 векторами рРIСZаlрhаА-Рlа2 и рРIСZmf4iА-Рlа2 клоны культивировали в колбах Эрленмейера объемом 100 мл, содержащих по 20 мл среде
YPGM. Культивирование осуществляли в орбитальном термошейкере (BioSan, Латвия) при + 30 °C, 250 об/мин. Каждые 24 часа в среду вносили 1% метанола от объема среды. После культивирования клетки осаждали центрифугированием при 4200 g в течение 5 мин. Супернатант отбирали и использовали для анализа активности фосфолипазы А2. Всего проанализировано по 30 клонов K. phaffii с каждым типом сигнала секреции.
Анализ активности РLА2 проводился с использованием кислотно-щелочного метода титрования [15]. Активность РLА2 определялась как количество фермента, требуемое для высвобождения 1 мкг свободной жирной кислоты [20].
Далее образцы культуральной жидкости анализировали методом SDS-электрофореза в 15% ПААГ, а также качественным методом путем нативного электрофореза с последующей инкубацией пластин геля в агаризованном лецитине. по Леммли.
Для определения удельной активности рекомбинантной РLА2 и ферментного препарата «Nagase» проводили очистку фермента на препаративном хроматографе BUCHI на колонке Bio-Rad UNОsрhеrе Q (5 мл). В качестве буфера использовался 40 мМ Трис (рН = 10), в качестве элюента 1 М хлорид натрия в 40 мМ Трис буфере (рН = 10). Оценку активности фосфолипазы А2 в элюате проводили методом кислотнощелочного титрования, содержание белка определяли по Бредфорду.
Результаты и обсуждение
Получены конструкции рРIСZаlрhаА-Рlа2 и рРIСZmf4iА-Рlа2, проверенные секвенированием на корректность вставки и отсутствие мутаций в генах фосфолипазы А2 и модифицированного сигнала секреции mf4i. Линеаризованными конструкциями проведены трансформации компетентных клеток K. phaffii X-33 . По 30 выросших на среде YPD c 250 мкг/мл зеоцина клонов с каждой конструкцией проиндуцированы при культивировании в жидкой питательной среде YPGM. Полученная культуральная жидкость от клонов проанализирована на наличие РLА2 методом гель-электрофореза в ПААГ (рисунок 2). Исходя из полученных данных, клоны с конструкциями рРIСZаlрhаА-Рlа2 и рРIСZmf4iА-Рlа2 продуцируют РLА2. Как и в работе Liu et. el. [18], нами установлено, что K. phaffii экспрессирует три формы РLА2 размером около 13 (А), 16 (В) и 20 (С) кДа. Лишь одна из них соответствует ожидаемому размеру целевой РLА2 в 13,6 кДа. Остальные, вероятно, являются гликозилированными вариантами фермента.
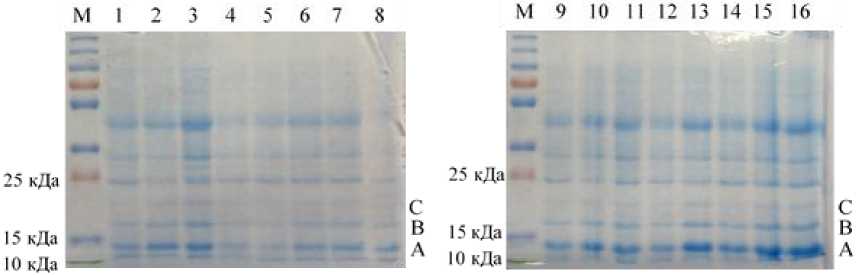
Рисунок 2. Электрофореграмма белков культуральной жидкости клонов с разными вариантами сигнала α-MF. 1–8 – клоны рРIСZаlрhаА-Рlа2; 9–16 – клоны рРIСZmf4i-Рlа2; АВС – формы фосфолипазы А2; М – маркер размера белка
Figure 2. Electrophoregram of proteins of the culture fluid of clones with different signal variants α-MF. 1–8-clones of рРIСZаlрhаА-Рlа2; 9–16-clones of рРIСZmf4i-Рlа2; ABC-forms of phospholipase А2; M-marker of protein size
При этом нативный электрофорез образцов культуральной жидкости с последующим качественным проявлением РLА2 в среде с лецитином показал наличие двух активных форм РLА2 у всех полученных клонов (рисунок 3). Таким образом, одна гликозилированная форма РLА2 является интактной.

Рисунок 3. Результат нативного электрофореза белков культуральной жидкости клонов с разными вариантами сигнала α-MF. 1–4 – клоны рРIСZаlрhаА-Рlа2; 5–7 – клоны рРIСZmf4i-Рlа2
Figure 3. The result of native electrophoresis of proteins of the culture fluid of clones with different signal variants α-MF. 1–4 – clones рРIСZаlрhаА-Рlа2; 5–7-clones рРIСZmf4i-Рlа2
Результаты определения фосфолипазной активности в культуральной жидкости скульти-вированных клонов K. phaffii с разными вариантами генетической конструкции приведены в таблице 1. Средний уровень экспрессии РLА2 под фактором mf4i достоверно не отличается от такового в случае нативного сигнала α – MF. Однако экспрессия единичных клонов K. phaffii оказалась выше при использовании модифицированного сигнала mf4i, что показано на рисунке 4.
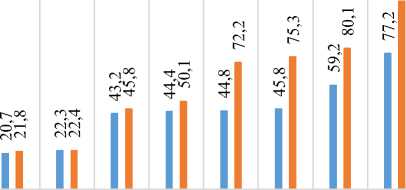
12345678 ■ Активность фосфолипазы (клоны alpha-MF), ед/мл ■ Активность фосфолипазы (клоны mf4i), ед/мл
Рисунок 4. Активность фосфолипазы А2 в культуральной жидкости клонов с различными факторами секреции
Figure 4. Phospholipase А2 activity in the culture fluid of clones with different secretion factors
Таблица 1.
Активность фосфолипазы А2 в культуральной жидкости в зависимости от типа конструкции
Table 1.
Phospholipase А2 activity in the culture fluid, depending on the type of construction
|
Тип конструкции, трансформированной в K. Phaffii Type of construct transformed in K. phaffii |
Средние значения активности РLА2 в культуральной жидкости, ед./мл Average values of РLА2 activity in culture liquid, units/mL |
Максимальная активность РLА2 в культуральной жидкости клонов, ед./мл Maximum activity of РLА2 in culture liquid of clones, units/mL |
|
рРIСZаlрhаА-Рlа2 |
44,7 ± 16,2 |
77,2 |
|
рРIСZmf4iА-Рlа2 |
59,3 ± 3,6 |
106,7 |
Далее была проведена хромотографическая очистка рекомбинантной РLА2 из культуральной жидкости клонов с разными вариантами генетической конструкции, а также ферментного препарата «Nagase». По нашим данным, удельная активность рекомбинантной РLА2, экспрессируемой различными клонами K. phaffii , достоверно не различается и составляет 4650 ед./мг. При этом удельная активность РLА2 из ферментного препарата «Nagase», экспрессируемого St. violaceoruber , составила 5220 ед./мг.
Таким образом, метилотрофные дрожжи K. phaffii вне зависимости от типа сигнала экспрессируют рекомбинантные РLА2 со схожей активностью, сопоставимой с нативным ферментом St. violaceoruber .
Заключение
В результате проведенных исследований показано, что в среднем достоверных отличий в экспрессии, удельной активности рекомбинантной РLА2 метилотрофными дрожжами K. phaffii X-33 при использовании нативного сигнала секреции α – MF и его модифицированного варианта mf4i не обнаружено. Однако использование фактора секреции mf4i позволяет получить более высокую продукцию РLА2 у отдельных клонов K. phaffii .
Модифицированный фактор секреции mf4i имеет более высокий потенциал для экспрессии различных ферментов, что позволяет рассматривать его как перспективный фактор секреции для создания коммерческих экспрессионных систем на основе K. phaffii для синтеза гетерологичных белков.
Список литературы Сравнительная экспрессия рекомбинантной фосфолипазы А2 в Komagataella phaffii в зависимости от модификации сигнального пептида альфа-фактора
- Dennis E.A., Cao J., Hsu V.I.I., Magrioti V. et al. Phospholipase A2 enzymes: physical structure, biological function, disease implication, chemical inhibition, and therapeutic intervention // Chem Rev. 2011. V. 111. P. 6130-6185. doi: 10.1021/cr200085w
- Samy R.P., Gopalakrishnakone P., Stiles B.G., Girish K.S. et al. Snake venom phospholipases A(2): a novel tool against bacterial diseases//Curr Med Chem. 2012. V. 19. P. 6150-6162. doi: 10.2174/092986712804485791
- Muller V.D., Russo R.R., Cintra A.C., Sartim M.A. et al. Crotoxin and phospholipases A2 from Crotalus durissus terrificus showed antiviral activity against dengue and yellow fever viruses // Toxicon. 2012. V. 59. P. 507-515. doi: 10.1016/j.toxicon.2011.05.021
- Muller V.D., Soares R.O., dos Santos N.N., Trabuco A.C. et al. Phospholipase A2 isolated from the venom of Crotalus durissus terrificus inactivates dengue virus and other enveloped viruses by disrupting the viral envelope // PLoS One. 2014. V. 9. №. 11. P. el 12351. doi: 10.1371/journal.pone.0112351
- Russo R.R., Müller V.D.M., Cintra A.C.O., Figueiredo L.T.M. et al. Phospholipase A2 crotoxin B isolated from the venom of Crotalus durissus terrificus exert antiviral effect against dengue virus and yellow fever virus through its catalytic activity//J Virol Antivir Res. 2014. V. 3. P. 1. doi: 10.1016/j.toxicon.2011.05.021
- Castillo J.C., Vargas L.J., Segura C., Gutiérrez J.M. et al. In vitro antiplasmodial activity of phospholipases A2 and a phospholipase homologue isolated from the venom of the snake Bothrops asper // Toxins (Basel). 2012. V. 4. P. 1500-1516. doi: 10.3390/toxins4121500
- Nunes D.C., Figueira M.M., Lopes D.S., De Souza D.L. et al. BnSP-7 toxin, a basic phospholipase A2 from Bothrops pauloensis snake venom, interferes with proliferation, ultrastructure and infectivity of Leishmania (Leishmania) amazonensis // Parasitology. 2013. V. 140. P. 844-854. doi: 10.1017/S0031182013000012
- Silveira L.B., Marchi-Salvador D.P., Santos-Filho N.A., Silva F.P. et al. Isolation and expression of a hypotensive and anti-platelet acidic phospholipase A2 from Bothrops mooj eni snake venom // J Pharm Biomed Anal. 2013. V. 73. P. 3 5-43. doi: 10.1016/j.jpba.2012.04.008
- Rodrigues R.S., Izidoro L.F., de Oliveira R.J., Sampaio S.V. et al. Snake venom phospholipases A2: a new class of antitumor agents//Protein Pept Lett. 2009. V. 16. P. 894-898. doi: 10.2174/092986609788923266
- Borrelli G.M., Trono D. Recombinant lipases and phospholipases and their use as biocatalysts for industrial applications // Int. J.N. Sei. 2015. V. 16. P. 20774-20840. doi: 10.3390/ijmsl60920774
- Murakami M., Sato H., Miki Y., Yamamoto K. et al. A new era of secreted phospholipase A2 (sPLA2) // J Lipid Res. 2015. V. 56. P. 1248-1261. doi: 10.1194/jlr.R058123
- Quach N.D., Arnold R.D., Cummings B.S. Secretory phospholipase A2 enzymes as pharmacological targets for treatment of disease. //Biochem Pharmacol. 2014. V. 90. P. 338-348. doi: 10.1016/j.bcp.2014.05.022
- Ahmad M., Hirtz M., Pitcher H., Schwab H. Protein expression in Pichia pastoris: recent achievements and perspectives for heterologous production//Appl Microbiol Biotechnol. 2014. V. 98. P. 5301-5317. doi: 10.1007/s00253-014-5732-5
- Kang Z., Huang H., Zhang Y., Du G. et al. Recent advances of molecular toolbox construction expand Pichia pastoris m synthetic biology applications //World J Mcrobiol Biotechnol. 2017. V. 33. №. 1. P. 1-8. doi: 10.1007/sl 1274-016-2185-2
- Liu A., Yu X.-W., Sha C., Xu Y. Streptomyces violaceoruber Phospholipase A2: expression in Pichia pastoris, properties, and application in oil degumming // Appl Biochem Biotechnol. 2015. V. 175. №. 6. P. 3195-3206. doi: 10.1007/s12010-015-1492-7
- Takemori D., Yoshino K., Eba C., Nakano H. et al. Extracellular production of phospholipase A 2 from Streptomyces violaceoruber by recombinant Escherichia coli // Protein Expression and Purification. 2012. V. 81. №. 2. P. 145-150. doi: 10.1016/j.pep.20ll.10.002
- Yu X.W., Sun W.H., Wang Y.Z., Xu Y. Identification of novel factors enhancing recombinant protein production in multi-copy Komagataella phaffii based on transcriptomic analysis of overexpression effects // Sci. Rep. 2017. V. 7. №. 1. P. 1-12. doi: 10.1038/s41598-017-16577-x
- Codon Usage Database. URL: http://www.kazusa.or.jp/codon/index.html.
- EasySelect Pichia Expression Kit. For Expression of Recombinant Proteins Using pPICZ and pPICZa in Pichia pastoris. User manual // Invitrogen. 2010. 86 p.
- Valli M., Tatto N.E., Peymann A., Gruber C. et al. Curation of the genome annotation of Pichia pastoris (Komagataella phaffii) CBS7435 from gene level to protein function // FEMS yeast research. 2016. V. 16. №. 6. doi: 10.1093/femsyr/fow051


