Сравнительная макроскопическая характеристика почек крыс при различных способах фиксации
Автор: Смирнов А.В., Гуров Д.Ю., Гучигова Э.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Морфология
Статья в выпуске: 3 (51), 2016 года.
Бесплатный доступ
Представлены результаты качественного и количественного анализа данных, полученных при проведении макроскопического исследования почек крыс при различных способах фиксации. Проведена сравнительная характеристика ряда морфологических параметров почек крыс под воздействием различных сроков экспозиции в фиксирующих растворах, используемых при изготовлении макропрепаратов.
Макропрепарат, формалин, глиоксаль, бальзамирование органов
Короткий адрес: https://sciup.org/142149189
IDR: 142149189 | УДК: 616-091.7
Comparative macroscopic profile of rat kidneys using different fixation methods
The results of qualitative and quantitative analysis of the data obtained during a macroscopic study of rat kidneys using different methods of fixation are presented. The comparative profile of morphological parameters of rat kidneys exposed to fixing solutions used to produce macropreparations for different periods of time was developed.
Текст научной статьи Сравнительная макроскопическая характеристика почек крыс при различных способах фиксации
Изучение макропрепаратов является неотъемлемой частью обучения студентов и слушателей медицинских, фармацевтических, биологических и сельскохозяйственных вузов на морфологических дисциплинах согласно рабочим программам в соответствие с ФГОС 3. Фиксирующий раствор, применяемый при консервации макропрепаратов и бальзамировании, должен отвечать ряду условий [4].
Во-первых, это обеспечение безопасности обучающихся при осуществлении образовательной деятельности. Согласно федеральному закону РФ «Об образовании в Российской Федерации» (№ 273-ФЗ от 29.12.2012, ст. 41, п. 8), «охрана безопасности обучающихся включает в себя: … 8) обеспечение безопасности обучающихся во время пребывания в организации, осуществляющей образовательную деятельность» [11].
Во-вторых, это сохранение прижизненных визуальных характеристик тканей макропрепарата, поскольку вскоре после наступления биологической смерти или удаления органов из организма появляются посмертные изменения [8]. Фиксатор необходим для предотвращения аутолиза и сохранения материала в нативном виде с целью последующего изучения [5].
Кроме того, при выборе фиксатора или бальзамирующего раствора желательно учитывать экономический аспект, т. е. оптимальное соотношение цены раствора с его низкой токсичностью и способностью вызывать минимальные макроскопические изменения в тканях при длительном хранении объектов [7].
Наиболее часто для сохранения макропрепаратов используются растворы на основе формалина [7], который относится ко 2-му классу опасности по ГОСТ 12.1.1007 – высокоопасные вещества.
В продаже в Российской Федерации имеется фиксирующая смесь «Альдофикс» на основе глиоксаля, отечественного производства, не содержащая формальдегида и относящаяся к 4-му классу опасности (вещества малоопасные), т. е. более безвредная в применении [10].
Однако информации о результатах влияния глиоксаля на морфологические параметры органов и тканей в процессе изготовления макропрепаратов при различных сроках фиксации и сравнительной характеристики макропрепаратов, изготовленных с применением других фиксаторов на основе формалина, в доступной научной литературе нами не обнаружено.
ЦЕЛЬ РАБОТЫ
Сопоставление результатов качественного и количественного макроскопического исследования почек крыс при различных способах и длительности фиксации.
МЕТОДИКА ИССЛЕДОВАНИЯ
Исследования были проведены на 12 образцах почек белых крыс линии Wistar [2, 9]. В качестве фиксирующего раствора были использованы смеси на основе нейтрального за-буференного формалина (Ф) и глиоксаля (А) (коммерческое название «Альдофикс»).
Почки продольным разрезом разделяли на 2 половины и проводили измерения поперечного и продольного диаметров. 6 образцов (1-я группа) были помещены в раствор 10 % формалина; 6 образцов (2-я группа) были помещены в раствор «Альдофикса», представляющего собой раствор глиоксаля (альдегида муравьиной кислоты).
Через 1, 3 и 10 суток образцы извлекали, исследовали их качественные (форму, характер поверхности и разреза, определяли изменение цвета и консистенции), количественные (измеряли продольный и поперечный диаметры почек) характеристики, производили фотосъёмку исследуемого биоматериала с заранее определённой освещенностью рабочего места с использованием фотоаппарата Nikon D3000 kit.
Затем образец помещали в марлевый мешочек, который в дальнейшем маркировали цветной нитью и погружали в соответствующий фиксатор.
Через трое суток была произведена перезаливка растворов. Образцы 1-й группы помещали в раствор, состоящий из 50 мл 10 % формалина, 25 мл 96 ° этилового спирта и 25 мл проточной воды.
Образцы 2-й группы помещали в раствор, состоящий из 50 мл альдофикса, 25 мл 96 ° этилового спирта, 25 мл проточной воды.
Полученные в ходе фотосъёмок изображения макропрепаратов открывали в программе Adobe Photoshop CS5, содержащей таблицу цветовой гаммы HSL [1, 3].
На цифровых фотографиях почек, выполненных через 1, 3 и 10 суток фиксации, определяли цифровые значения насыщенности в 6 различных участках, заносили данные в таблицу, проводили статистическую обработку с построением графика.
Полученные количественные данные были подвергнуты статистической обработке с использованием U-критерий Манна–Уитни [6].
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
При качественном изучении макропрепаратов почек крыс отмечалось прогрессивное изменение цвета поверхности и среза органа с приобретением серого оттенка. При этом более выраженные изменения были выявлены при фиксации альдофиксом уже после первых суток (рис. 1).
Таблица HSL представлена показателями: H – оттенок, S – насыщенность и L – свет.
Значения оттенка «H» повышались тем больше, чем больше обесцвечивались (серели) почки после воздействия на них фиксирующей смеси.
Свет «L» имел фиксированный показатель (L = 14), что достигалось путём сохранения одинаковых условий освещённости рабочего места при каждой фотосъёмке.
В данной методике мы пренебрегли значением насыщенности (S).
При проведении анализа с использованием таблицы цветовой гаммы, выявили, что на 1-е сутки оттенок почки, не подвергшейся влиянию фиксаторов, имел H = 5 [ДИ 3,7; 6,3] усл. ед. На 3-и сутки органы, фиксированные в растворе на основе глиоксаля, имели H = 42 [ДИ 41,07; 42,93] усл. ед., в растворе на основе формалина H = 31 [ДИ 29,7; 32,3] усл. ед. На 10-е сутки у почек, находившихся в глиоксале H = 50 [ДИ 47,7; 52,3] усл. ед., в формалине H = 40 [ДИ 38,8; 41,2] усл. ед.
Следовательно, значение показателя оттенка (H) у почек из формалина на 10-е сутки ниже на 20 %, по сравнению с показателем H почек из смеси содержащей глиоксаль (p < 0,05), что говорит о лучшей сохранности цвета под действием фиксатора на основе формалина (рис. 2), так как насыщенность цвета пропорционально уменьшается с повышением значения H (значения оттенка) в цветовой гамме.
Левая почка

Рис. 1. Качественный анализ цвета органов после фиксации
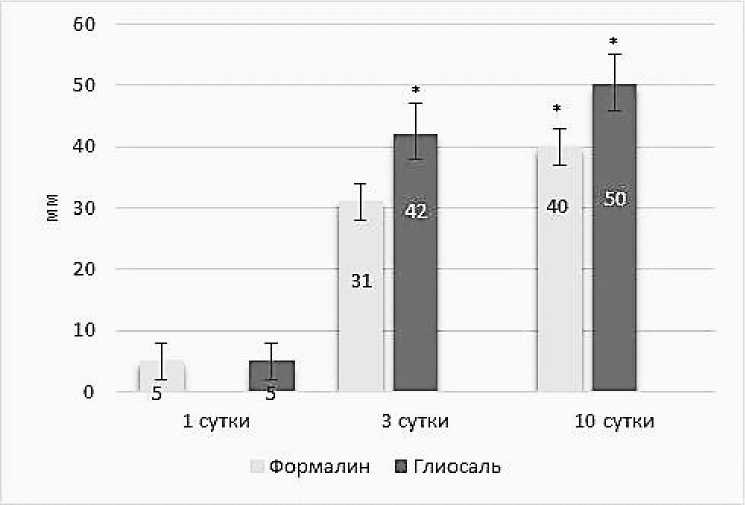
Рис. 2. Изменение H при различных методах фиксации
– различия достоверны относительно контрольной группы при p < 0,05 (использован непараметрический критерий Манна–Уитни;
тест Колмагорова–Смирнова с поправкой Лиллиефорса)
Изменение диаметра почек крыс при различных методах фиксации
|
Номер группы |
Время исследования, в сут. |
||
|
1-е |
3-и |
10-е |
|
|
Продольный диаметр, мм |
|||
|
1-я (Ф) |
13,0 ± 0,26 |
12,8 ± 0,31 |
11,7 ± 0,21 |
|
2-я (А) |
13,0 ± 0,26 |
11,2 ± 0,31* |
8,8 ± 0,31* |
|
Поперечный диаметр, мм |
|||
|
1-я (Ф) |
9,2 ± 0,31 |
9,3 ± 0,21 |
8,0 ± 0,26 |
|
2-я (А) |
9,2 ± 0,31 |
7,7 ± 0,21* |
5,7 ± 0,21* |
– p < 0,05 по сравнению с 1-й группой (двухфакторный дисперсионный анализ с постобработкой тестом Бонферрони).
Отмечено различие в значениях диаметров исследуемых органов различных групп. На 3-и сутки исследования продольный диаметр почек, фиксированных в растворе на основе глиоксаля, уменьшается на 12,5 % (p < 0,05) по сравнению с фиксацией в растворе на основе формалина. На 10-е сутки разница возросла до 24 % (p < 0,05).
Почки, находившиеся в альдофиксе, оказались более сморщенными и значительно меньше в сравнении с почками, фиксированными в растворе на основе формалина, что можно наблюдать на фотографии представляющей две изначально идентичные половины, различающиеся между собой после фиксации по форме и размеру (рис. 3).
Правая почка
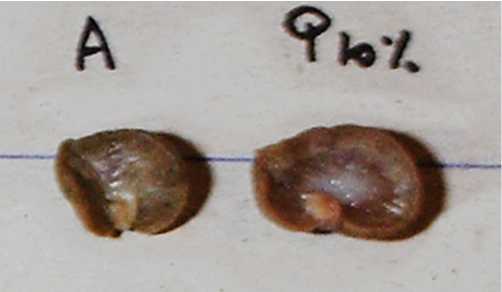
Рис. 3. Изменение формы почек под воздействием различных фиксаторов
ЗАКЛЮЧЕНИЕ
На основании проведенного количественного макроскопического исследования с последующим статистическим анализом, установлено, что поперечный диаметр почки крысы под действием фиксирующего раствора на основе глиоксаля (2-я группа), на 3-и сутки исследования уменьшилcя на 17 % (p < 0,05), на 10-е сутки – на 28 % (p < 0,05) по сравнению с почками, находившимися в фиксаторе на основе формалина (1-я группа).
Продольный диаметр почки крысы под действием фиксирующего раствора на основе глиоксаля (2-я группа) на 3-и сутки исследования уменьшился 12,5 % (p < 0,05) по сравнению с фиксацией в растворе на основе формалина (1-я группа). На 10-е сутки разница возросла до 24 % (p < 0,05).
Анализ изменения цвета, проведённый в таблице цветовой гаммы HSL, и последующая статистическая обработка показали, что более эффективную сохранность цветового оттенка органов обеспечивает фиксация в растворе на основе формалина, о чём свидетельствуют полученные в ходе исследований данные.
Почки, фиксированные в формалине, имели числовое значение оттенка (H) на 10-е сутки ниже на 20 % (p < 0,05) по сравнению с органами, фиксированными в глиоксале.
Проведённые исследования демонстрируют большую сохранность качественных и количественных макроскопических параметров почек крыс под воздействием различных сроков экспозиции в фиксирующем растворе на основе формалина по сравнению с использованием менее токсичного фиксатора на основе глиоксаля.
Является перспективным продолжение поиска новых фиксаторов, обладающих меньшей токсичностью, что соответствует закону РФ (Ф3 № 273) «Об образовании в Российской Федерации», но обеспечивающих лучшую сохранность органов и тканей при бальзамировании.
Список литературы Сравнительная макроскопическая характеристика почек крыс при различных способах фиксации
- Жулькова Е. С., Ильясова Н. Ю., Куприянов А. В. Технология выделения лейкоцитов на изображениях препаратов крови//Компьютерная оптика. -2007. -Т. 31, № 2. -С. 77-81.
- Количественная характеристика патоморфологических изменений в эндокринной части поджелудочной железы крыс при моделировании экспериментального стрептозотоцин-индуцированного сахарного диабета/А. В. Смирнов, Г. Л. Снигур, А. Т. Яковлев и др.//Волгоградский научно-медицинский журнал. -2015. -№ 4 (48). -С. 21-24.
- Кузнецов А. В., Куприянов А. В., Ильясова Н. Ю. Анализ изображения радужной оболочки глаза с использованием преобразования радона//Вестн. Самарского гос. Аэрокосмического ун-та -2008. -№ 2 (15). -С. 240-244.
- Меркулов Г. А. Курс патогистологической техники/Под ред. Д. Н. Чистовича. -Л.: МЕДГИЗ Ленинградское отделение. -1961. -323 с.
- Пикалюк В. С., Мороз Г. А., Кутя С. А. Методическое пособие по изготовлению анатомических препаратов. -Изд-во Крым. гос. мед. ун-та, 2004. -C. 76.
- Реброва О. Ю. Статистический анализ медицинских данных. -2006. -С. 104-108.
- Саркисов Д. С., Перов Ю. Л. Микроскопическая техника: Руководство/Под ред. Д. С. Саркисова и Ю. Л. Перова. -М.: Медицина, 1996. -535 с.
- Сафин Р. Я. Применение иммунологических методов исследования для определения давности наступления смерти//Сибирский мед. журн. -2007. -Т. 73, № 6. -С. 18-20.
- Экспериментальная модель диабетической нефропатии у крыс/А. А. Спасов и др.//Вестник Волгоградского государственного медицинского университета. -2015. -№ 3 (35). -С. 36-40.
- http://aldofix. ru/#application
- http://www.zakonrf.info/zakon-ob-obrazovanii-v-rf/41/


