Сравнительная оценка эффективности термических инструментов в хирургии неспецифической эмпиемы плевры
Автор: Шулутко А.М., Качикин А.С., Ясногородский О.О., Талдыкин М.В., Кернер Д.В., Винарская В.А., Мороз Н.Г.
Журнал: Московский хирургический журнал @mossj
Рубрика: Новые технологии
Статья в выпуске: 1 (35), 2014 года.
Бесплатный доступ
В эксперименте проводилось сравнение результатов коагуляции легочной ткани ПП и электрохирургическими инструментами, определялась зависимость результатов воздействия испытуемых инструментов от экспозиции, изучались особенности репаративных процессов. В зоне воздействия электрохирургических инструментов образуются коагуляционные внутрисосудистые тромбы в глубоких слоях зоны циркуляторных расстройств, что приводит к ишемии некоагулированных тканей и увеличению размеров некроза. Это создает угрозу отторжения струпа и условия для замедленной регенерации с образованием массивного грубого рубца. В ОТИ паренхимы легкого, формирующихся под влиянием ПП, отсутствует некроз некоагулированных тканей, поэтому нет угрозы отторжения коагуляционного струпа, и заживление происходит с образованием тонкого эластичного рубца. При использовании электрохирургических методов с увеличением продолжительности воздействия значительно увеличивается глубина ОТИ. Под воздействием ПП глубина ОТИ существенно не меняется с увеличением экспозиции. В отделении торакальной хирургии ГКБ № 61 в период с 1996 г. по 2012 г. по поводу НЭП с применением ТХИ выполнено 64 оперативных вмешательств. Большинство больных (49), перенесших ВТС-санацию полости эмпиемы, выписаны с полным выздоровлением, 6 - с санированными остаточными полостями небольших размеров. После декортикации легкого как из традиционного, так и из мини-доступа с видеосопровождением все пациенты выписаны с выздоровлением.
Эмпиема плевры, электрохирургические инструменты, торакоскопическая хирургия, плазменнная коагуляция
Короткий адрес: https://sciup.org/142211136
IDR: 142211136 | УДК: 616-089:
Текст научной статьи Сравнительная оценка эффективности термических инструментов в хирургии неспецифической эмпиемы плевры
Введение Вместе с тем, развивающиеся малоинвазивные техно-
В публикациях отечественных и зарубежных авторов отмечается продолжающийся рост заболеваемости неспецифической эмпиемой плевры (НЭП) [1–8].
При этом результаты лечения больных НЭП нельзя считать в полной мере удовлетворительными: травматичные традиционные вмешательства, от торакостомии до плев-рэктомии с декортикацией легкого сопровождаются высокой частотой послеоперационных осложнений [4, 8–10,], летальность при НЭП остается достаточно высокой – 4–6% [11–13] и даже достигает 29% [1, 4, 8, 9].
логии имеют существенные преимущества перед традиционными операциями: малая травматичность операционного доступа и манипуляций; хороший обзор и визуальный контроль всех этапов операции благодаря специальному освещению и увеличению [14, 15]; раннее восстановление нарушенных функций организма и физиологической активности пациента [13, 16, 17]; низкая частота послеоперационных осложнений [18, 19]; сокращение сроков пребывания в стационаре; хороший косметический результат [20, 21]. Менее выраженные нарушения показателей дыхатель- ной функции легких после торакоскопических операций позволяют выполнять эти операции больным пожилого и старческого возраста, у которых торакотомия представляет большой риск [22–25].
Многие авторы сообщают о высокой эффективности лечения НЭП с использованием малоинвазивных технологий (ВТС) [6, 26–28,].
Разработка новых хирургических устройств, использующих тепловую энергию, – термических хирургических инструментов (ТХИ), привела к активному применению их в хирургии легких и плевры [29–31]. В ряде публикаций отмечается высокая эффективность санации полости неспецифической эмпиемы плевры новыми физическими факторами [32– 35].
Материалы и методы
Эксперимент проведен на шести беспородных собаках. В ходе эксперимента проводилось сравнение результатов коагуляции легочной ткани ПП и электрохирургическими инструментами после краевой резекции легкого с визуальной оценкой аэрогемостаза и образовавшегося термического струпа и с последующим забором проб для морфологического исследования. Были взяты образцы размером 1 см3 в виде кубиков ткани с коагуляционным некрозом, которые фиксировались 10% формалином, готовились срезы, препараты окрашивались гематоксилином и эозином.
Тем же животным перед краевой резекцией производилось точечное воздействие на неповрежденную ткань легкого сравниваемыми инструментами на одном уровне мощности в 100 Вт продолжительностью 1, 5, 10, 30 секунд. Пробы для гистологического исследования брались сразу после обработки. Таким образом определялась зависимость результатов воздействия испытуемых инструментов от экспозиции.
Три собаки после краевой резекции легкого с коагуляцией раневой поверхности оставлены в хроническом опыте для изучения особенностей репаративных процессов. Животные выводились из эксперимента на 10-е 21-е сутки после вмешательства.
В эксперименте использовались следующие ТХИ: плазменная система «PlasmaJet®», оснащенная микроплазмотронами диаметром 5 мм и 10 мм, система аргоноплазменной электрокоагуляции – аргонусиленной коагуляции (электро-хирургический генератор «Valleylab Force 4» и аргонный коагулятор) и метод монополярной радиочастотной коагуляции в водной среде (генератор «Valleylab Force 4», оснащенный манипулятором «TissueLink» на соляном растворе).
В отделении торакальной хирургии ГКБ № 61 в период с 1996 г. по 2012 г. по поводу НЭП с применением ТХИ выполнено 64 оперативных вмешательств: 4 плеврэктомии с декортикацией легкого из традиционного доступа, 5 декортикаций легкого из мини-доступа с видеоассистенцией, 55 видеотора-коскопических (ВТС) санаций полости эмпиемы.
В клинике применялись следующие ТХИ: плазменная система «PlasmaJet®», оснащенная микроплазмотронами ди-


Рис.1.Плазменнаясистема«PlasmaJet®», одноразовый микроплазмотрон
диаметром 5 мм


Рис. 2. Аппарат аргонусиленной коагуляции «Фотек ЕА 142», активные электроды для эндоскопического применения
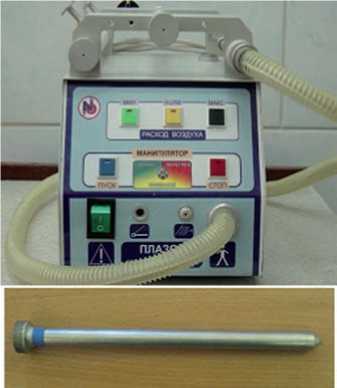
Рис. 3. Плазменная хирургическая установка «Плазон-N» с плазматроном для эндоскопического применения

Рис. 5. Инструменты-маниуляторы различных ТХИ, адаптированные к эндоскопичесому применению

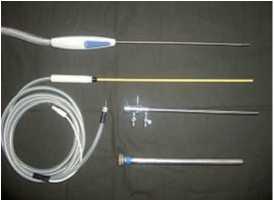
аметром 5мм и 10мм, аппарат аргонусиленной коагуляции (АУК) «Фотек ЕА 142», плазменная хирургическая установка «Плазон-N» с плазматроном для эндоскопического применения, СО2-лазер «Sharplan1080S» с энодоскопическим световодом (рис. 1–5).
ТХИ применялись для ВТС-санации НЭП и для коагуляции девплевризированной поверхности легкого с аэро-гемостатической целью после декортикации легкого как из мини-доступа с видеоассистенцией, так и из традиционной торакотомии.
Основными целями применения ТХИ при ВТС-санации эмпиемы плевры являются:
– вапоризация фибринных наложений и гнойно-некротических масс;
– вапоризация фиброзно измененной висцеральной плевры;
– частичный пневмолиз;
– коагуляция мелких бронхиальных и бронхиоло-альеолярных свищей;
– гермитизация деплевризированной поверхности легкого после механической декортикации;
– стерилизация плевральной полости.
Этапы ВТС-санации полости эмпиемы с помощью различных ТХИ (рис. 6–12).
При плеврэктомии с декортикацией легкого из традиционного и мини-доступа ТХИ использовались для аэрогемостаза раневой поверхности легкого.
Результаты
Сразу после операции «плазменная рана» представляет собой зону коагуляционного некроза глубиной 1,2–1,3 мм с поверхностным обугливанием и зону расстройств кровообращения (зона циркуляторных расстройств – ЗЦР) в виде гиперемии сосудов, стаза капилляров, очаговых кровоизлияний, встречающихся на глубине до 1,5 см.
Расстройства кровообращения носят обратимый характер. Некроз имеет характерное строение: карбонизированный слой (карбонизированный слой – КС), состоящий из угля; губчатый слой, представленный бесструктурными белковыми массами (губчатый слой некроза – ГСН) и компактный слой (КСН), образованный погибшими клетками. Толщина ГСН составляет 200–250 мкм.
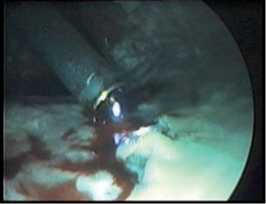
Рис. 6. Вапоризация фибринных наложений и гнойно-некротических масс («PlasmaJet®»)
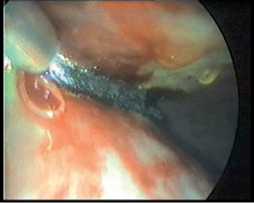
Рис. 7. Бескровный пневмолиз («PlasmaJet®»)
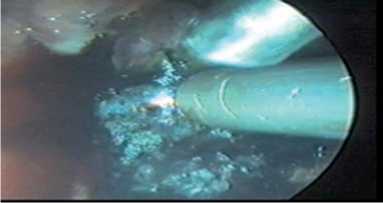
Рис. 8. Коагуляция бронхиального свища («PlasmaJet®»)
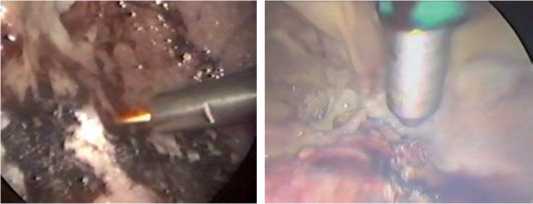
Рис. 9. Вапоризация висцераль- Рис. 10. Вапоризация фибринных ной плевры («PlasmaJet®»)
наложений («Плазон-N»)
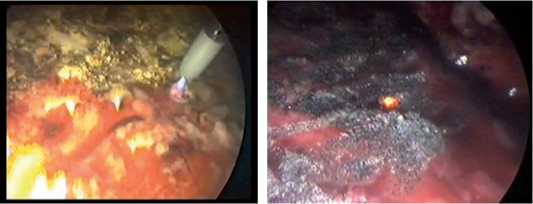
Рис. 12. Вапоризация висцеральной плевры СО2-лазер «Sharplan 1080S»
Рис. 11. Вапоризация висцеральной плевры Аппарат АУК «Фотек ЕА 142»
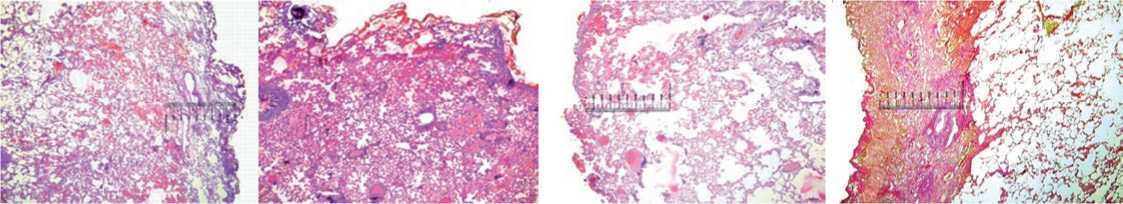
Рис. 13. Биоптат из зоны коагуляции сразу после воздействия ПП. Область термических изменений (ОТИ) паренхимы легкого: равномерная тонкая пленка коагуляционного некроза с одноразмерными порами в губчатом слое, расстройства кровообращения незначительны. Окраска гематоксилином и эозином. Ув. 400 х
Рис. 14. Биоптат из зоны AУК сразу после воздействия. ОТИ паренхимы легкого: неравномерный по толщине и диаметру пор губчатый слой некроза, выраженные циркуляторные расстройства. Окраска гематоксилином и эозином. Ув. 400 х
Рис. 15. Биоптат из зоны использования метода «TL» сразу после воздействия. ОТИ паренхимы легкого: широкая зона некроза без губчатого слоя, прилежащие ткани имбибированы кровью, коагуляционные внутрисосудистые тромбы в глубоких слоях паренхимы. Окраска гематоксилином и эозином. Ув. 400 х
Рис. 16. Биоптат из зоны коагуляции ПП через 21 сутки после воздействия. Формирующийся рубец: тонкий равномерный по толщине слой молодой соединительной ткани без некротических включений. Окраска гематоксилином и эозином. Ув. 400 х
В просвете кровеносных сосудов, находящихся в зоне некроза, коагуляционные тромбы, стенки мелких бронхов сближены, просветы их не определяются. В зоне расстройства кровообращения в просвете альвеол и бронхов серозно-геморрагический транссудат (рис. 13).
При морфологическом исследовании ОТИ, развивающихся в ткани легкого под влиянием электрохирургических инструментов (Argon Biam Coagulation – ABC или аргону-силенная коагуляция – АУК, TissueLink – TL) отмечается образование коагуляционных внутрисосудистых тромбов в глубоких слоях зоны циркуляторных расстройств – до 15 мм (рис. 14, 15).
Проведено сравнение морфологии заживления ран легкого, обработанных разными методами.
Плазменный струп трансформируется в эластичный тонкий рубец за счет активной перестройки его в процессе регенерации, заключающейся в уменьшении общей массы соединительной ткани и в наиболее короткие сроки. К концу третьей недели рубец сформирован. Толщина рубца около 1,5–1,8 мм (рис. 16).
После АУК некроз замещается медленнее с формированием грубого рубца, толщиной до 8–10 мм. Через 21 сутки в рубцовой ткани встречаются фрагменты коагуляционного некроза (рис. 17).
При использовании метода «TL» на месте струпа образуется наиболее массивный грубый рубец, глубиной до 12 мм, в толще которого на 21-е сутки сохраняются участки некроза (рис. 18).
Морфологически установлено, что под влиянием ПП при увеличении экспозиции от 1 секунды до 30 секунд глубина термического повреждения мала и меняется незначительно: ≈ от 1 мм до 2 мм; при использовании методов AУК и «TL» с увеличением продолжительности воздействия от 1 секунды до 30 секунд значительно увеличивается глубина ОТИ: при AУК от 4 мм до 10 мм, при использовании метода «TL» – от 6 мм до 14 мм.
После ВТС-санации полости эмпиемы с применением ТХИ для полного расправления легкого почти в половине случаев (27) потребовалась временная эндобронхиальная окклюзия бронха (ВЭОБ) несущего свищ (дренирующего бронха).
Большинство больных (49), перенесших ВТС-
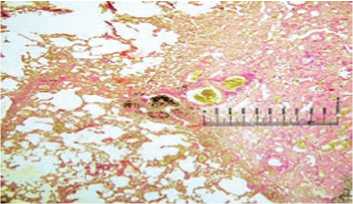
Рис. 17. Биоптат из зоны АУК через 21 сутки после воздействия. Массивный рубец: видны участки коагуляционного некроза в толще соединительной ткани. Окраска гематоксилином и эозином. Ув. 400 х
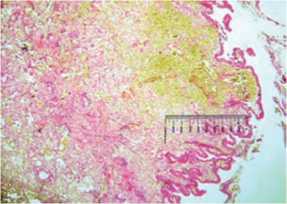
Рис. 18. Биоптат из зоны использования метода «TL» через 21 сутки. Формирование рубца: обширные поля некроза в массе молодой соединительной ткани. Окраска гематоксилином и эозином. Ув. 400 х
санацию полости эмпиемы, выписаны с полным выздоровлением, 6 – с санированными остаточными полостями небольших размеров. Следует отметить, что ВТС-санации выполнялись в наиболее тяжелых случаях, когда дренирование плевральной полости с активной аспирацией и фракционным лаважом оказывались не эффективными.
После декортикации легкого как из традиционного, так и из мини-доступа с видеосопровождением все пациенты выписаны с выздоровлением. Во всех случаях расправление легкого наступало в первые сутки после операции, активного поступления воздуха по дренажам не наблюдалось.
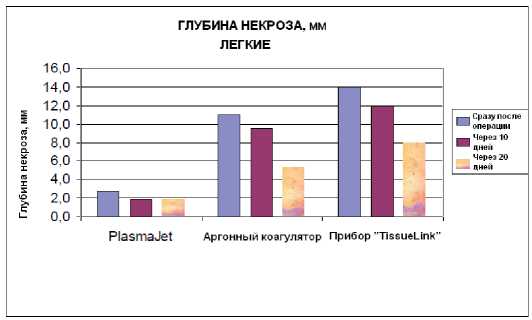
Рис. 19. Динамика заживления зоны воздействия ПП и электрохирургических методов
Отмечено одно нагноение послеоперационной раны при использовании традиционной торакотомии.
Обсуждение
Морфологическое исследование ОТИ ткани легкого в зоне воздействия электрохирургических инструментов (AУК, TissueLink ) показало образование коагуляционных внутрисосудистых тромбов в глубоких слоях зоны циркуляторных расстройств (до 15 мм), что приводит к ишемии некоагули-рованных тканей и увеличению размеров некроза до 15 мм. Увеличение объема некроза и усиление воспалительной реакции создает угрозу отторжения струпа и условия для замедленной регенерации с образованием массивного грубого рубца (рис. 19).
В ОТИ паренхимы легкого, формирующихся под влиянием ПП, отсутствует некроз некоагулированных тканей, поэтому нет угрозы отторжения коагуляционного струпа, и заживление происходит с образованием тонкого эластичного рубца.
При использовании электрохирургических методов с увеличением продолжительности воздействия от 1 сек. до
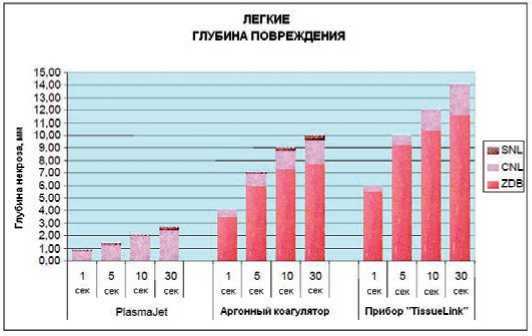
Рис. 20. Зависимость глубины термического повреждения ткани легкого от экспозиции под воздействием ПП и электрохирургических методов
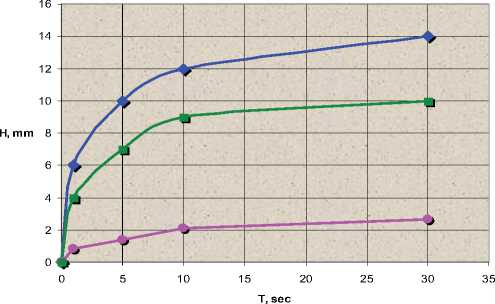
Рис. 21. Графики зависимости глубины термического повреждения ткани легкого от экспозиции под воздействием ПП и электрохирургических методов
30 сек. значительно увеличивается глубина ОТИ: при АУК – от 4 мм до 10 мм, «TL» – от 6 мм до 14 мм (рис. 20).
Под воздействием ПП глубина ОТИ существенно не меняется с увеличением экспозиции. Эта особенность обеспечивает безопасность метода плазменной коагуляции и может быть использована в хирургии легких, в частности, для вапоризации фиброзно измененной висцеральной плевры при операциях по поводу эмпиемы плевры (рис. 21).
С помощью электрохирургических методов возможна только коагуляция, ПП способны не только коагулировать, но разделять (рассекать) и вапоризировать биоткани.
С помощью СО2-лазера достигается вапоризация ткани, но толщина губчатого слоя некроза может быть не достаточной для надежного азрогемостаза, возможно повреждение тонкого коагуляционного струпа в процессе расправления легкого [36, 37].
При использовании даже расфокусированного луча СО2-лазера возможно только точечное воздействие, кровь экранирует углекислотный лазерный луч, дальнодействие луча создает опасность повреждения тканевых структур, находящихся за пределами зоны предполагаемого воздействия, невозможен плавный подвод энергии к объекту, процессы абляции превосходят коагуляцию.
При аргонусиленной коагуляции невозможно точечное воздействие, т.к. при активации инструмента тотчас образуется пятно коагуляции, неосуществим плавный подвод тепла к ткани, распространение электрического тока по кровеносным сосудам не прогнозируемо, поэтому возможно повреждение ткани на большей, чем предполагается, глубине, невозможна вапоризация ткани, необходимо включение в электрическую цепь пациента.
При использовании плазменного потока возможно как точечное, так и рассеянное воздействие, кровь не является экраном для плазменного потока, обеспечивается плавный подвод тепловой энергии к объекту с изменением расстоя- ния от плазменной струи до объекта воздействия, глубина коагуляции хорошо контролируется, при увеличении мощности плазменной струи и изменении расстояния до обрабатываемой поверхности достигается деструкция тканей, что позволяет не только коагулировать их, но и рассекать и испарять, плазменный факел обладает выраженным бактерицидным действием за счет высокой температуры, ультрафиолетового излучения и озона, образующегося в процессе ионизации газа.
Вследствие особенностей характера взаимодействия ПП с биологической тканью, наибольшей универсальностью и большей эффективностью преимущество для ВТС-санации НЭП среди ТХИ имеют плазменные аппараты [3].
Система «PJ» выгодно отличается от других плазменных аппаратов высокой аэрогемостатической эффективностью и универсальностью: одним и тем же инструментом можно не только коагулировать, но и вапоризировать и рассекать ткани.
Уникальные возможности системы «PlasmaJet®», определяются генерацией ПП очень высокой температуры (до 12000–15000 оС), при низком расходе плазмообразующего газа (0,25 л/мин) и широким диапазоном параметров.
Система «PlasmaJet®» снабжена плазматронами, имеющими конструктивные преимущества, – инструменты адаптированы к эндоскопическому применению, удобны при выполнении видеоторакоскопических вмешательств (рис. 22, 23).
Выводы
-
1. Высокоэнергетические термические хирургические инструменты могут эффективно применяться для видео-
- Рис. 22. Плазматроны: «PlasmaJet®» 5мм и «Плазон» – имеется существенное отличие в диаметре манипуляторов
-
2. Плазменные хирургические аппараты имеют существенные преимущества перед другими ТХИ.
-
3. Система «PlasmaJet®» отличается универсальностью – коагуляция, рассечение, испарение биологических тканей; безопасностью, за счет низкого расхода плазмообразующего газа (0,25–0,4 л/мин) и удобством применения благодаря наибольшей адаптации плазматронов-манипуляторов к эндоскопическому применению.
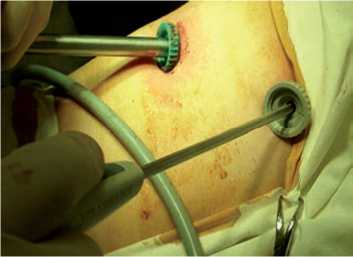
Рис. 23. Малый диаметр плазмоторона обеспечивает свободу перемещения его в различные торакопорты, что создает условия для лучшего обзора и манипулирования торакоскопической санации неспецифической эмпиемы плевры.
Список литературы Сравнительная оценка эффективности термических инструментов в хирургии неспецифической эмпиемы плевры
- Левин А.В., Самуйленков А.М., Цеймах Е.А., Зимонин П.Е. Эмпиема плевры: консервативная терапия, экстракорпоральные методы детоксикации, эндоскопические методы//Туберкулез и болезни легких. 2009. №9. С. 3-11.
- Шулутко А.М., Овчинников А.А., Ясногородский О.О., Мотус И.Я. Эндоскопическая торакальная хирургия. М.: Медицина, 2006. 390 с.
- Ясногородский О.О. Видеосопровождаемые интратора-кальные вмешательства: Автореф. дис..д-ра мед. наук. М., 2000. 31 с.
- Achmed A.E., Yacoub T.E. Empyema thoracic//Clin. Med. Insights. Circ. Respir. Pulm. Med. 2010. Jun. 17. Vol. 4. P. 1-8.
- Renner H., Gabor S. et al. Is aggressive surgery in pleural empyema justified?//Europ. J. cardiothorac. Surg. 1998. Vol. 14. P. 117-122.
- Панюшкин П.В. Торакоскопические вмешательства и операции из минидоступа с видеосопровождением в комплексном лечении неспецифических эмпием плевры. Дис..к.м.н. М., 2005. 97 с.
- Шулутко А.М., Талдыкин М.В., Качикин А.С. Диагностика и хирургическая тактика лечения неспецифической эмпиемы плевры//III хирургический конгресс: «Научные исследования в реализации программы «Здоровье населения России». М., 2008.
- Сигал Е.И., Жестков К.Г., Бурмистров М.В., Пикин О.В. Торакоскопическая хирургия. М., 2012. 352 с.
- Grijalva C.G., Zhu Y., Nuorti J.P., Griffin M.R. Emergence of parapneumonic emryema in the USA//Thorax. 2011. Aug. Vol. 66(8). P. 649-650.
- Wait M. A., Bechles D.L., Hotze M. Thoracoscopic management of empyema thoracis//J. Minim. Access. Surg. 2007. Okt. -Dec. Vol. 3(4). P. 141-148.
- Евтихов P.M., Горохов Г. А., Ланцухова Л.И. и др. Результаты хирургического лечения больных с нагноительными заболеваниями легких//Сборник научных трудов под редакцией проф. Ю.Н. Левашова. Ленинград, 1986. С. 28-31.
- Порханов В.А., Бодня В.Н., Кононенко В.Б. и др. Видеоторакоскопия в лечении эмпиемы плевры//Хирургия. 1999. №11. С. 40-43.
- Mavroudis C., Symmonds J.B., Minagi H., Thomas A.N. Improved survival in management of empyema thoracis//J. Thorac. Cardiovasc. Surg. 1981. Vol. 82. P. 49-57.
- Порханов В.А. Видеоторакоскопия в лечении торакальной патологии: Автореф. дис.. док. мед. наук. М., 1996. 38 с.
- Потапенков М.А., Шипулин П.П. Эндоскопические методы лечения эмпиемы плевры и пиопневмоторакса//Грудная и сердечно-сосудистая хирургия. 1995. №1. С. 56-59.
- Перепелицин В.Н. Малоинвазивные способы хирургического лечения неспецифической эмпиемы плевры: Автореф. дис.. докт. мед. наук. Пермь, 1996.28 с.
- Thurer R. Video-assisted thoracic surgery//Ann. Thorac. Surg. 1993. Vol. 56, P. 199-200.
- Boutin C., Rey F. Complications of thoracoscopy and preventive measures./In: Brown W. Atlas of VATS. -W.B. Saunders Co., 1994. P. 138-153.
- Furrer M., Rechsteiner R., Eigenmann V. et al. Thoracotomy and thoracoscopy: postoperative pulmonary function, pain and chest wall complaints//Eur. J. Cardiothor. Surg., 1997. Vol. 12. P. 82-87.
- Capov I., Jedlicka V. Videothoracoscopy and video-assisted thoracic procedures in the diagnosis and therapy of diseases of the thoracic cavity//Rozhl. Chir. 1999. Vol. 78(1). P. 9-12.
- Schwarz C., Schonfeld N. et al. Medical thoracoscopy//IBES. 1998. Vol. 160. P. 125.
- Гаипов Р.Г. Диагностические и лечебные возможности торакоскопии при плевритах и эмпиемах плевры//Здравоохранение Киргизии. 1984. №3. С. 13-15.
- Горшков Ю.И. и др. Ранняя плеврэктомия по поводу острого гнойного плеврита у больных с повышенным риском//Вестник хирургии им. Грекова. 1981. Т. 127, №10. С. 17-18.
- Massard G., Dabbagh A., Wihlm JM., Kessler R., Barsotti P., Roeslin N., Morand G. Pneumonectomy for chronic infection is a high risk procedure//Ann. Thorac. Surg. 1996. Vol. 62. P. 1033-1038.
- Walker W., Craig S. Video-assisted thoracoscopic pulmonary surgery -current status and potential evolution//Eur. J. Cardiothorac. Surg. 1996. Vol. 10. P. 161-167.
- Solaini L., Prusciano F., Di Francesco F. et al. Video thoracoscopic treatment in pleural empyema//J. Minerva Chir. 2000, Dec. Vol. 55(12). P. 829-833.
- Cassina P.C., Hauser M. Видеоторакоскопия в лечении эмпиемы плевры: подходы в зависимости от стадии и результаты//J. Thorac. Cardiovasc. Surg. 1999, Feb. Vol. 117(2). P. 234-238.
- Merry C.M., Bufo A.J. Ранняя торакоскопическая интервенция при эмпиеме плевры у детей//J. Pediatr. Surg. 1999, Jan. Vol. 34(1). P. 178-180.
- Бирюков Ю.В. Перспективы применения плазменного потока в легочной хирургии//Грудная и сердечно-сосудистая хирургия. 1992. №7-8. С. 47-49.
- Доценко А.П. и др. Применение неодимового ИАГ-лазера для эндоскопического гемостаза в грудной хирургии//Грудная и сердечно-сосудистая хирургия. -1991. -№10. -С. 47-49.
- Кабанов А.Н., Козлов К.К., Домбровский Д.Р. Использование плазменной установки в хирургии легких и плевры//Грудная хирургия. 1989. №5. С. 44-48.
- Кабанов А.Н., Козлов К.К., Котов И.И., Гальперин A.M. Торакоскопическое применение СО2-лазера в комплексном лечении эмпием плевры//Грудная и сердечно-сосудистая хирургия. 1991. №5. С. 47-49.
- Наумов В.Н., Добкин В.Г., Демидов Б.С., Назаров Ч. Особенности применения излучения различных типов лазеров при хирургическом лечении больных с эмпиемами плевры//Грудная хирургия. 1989. №5. С. 53-57.
- Ситко Л.А Ультразвуковая торакоскопическая санация полости эмпиемы плевры//Вестник хирургии им. Грекова. 1984. Т. 132, №2. С. 48-50.
- Шулутко А.М., Саакян Н.А., Ясногородский О.О., Качи-кин А.С., Кузнецов А.Н. Применение термических хирургических инструментов в лечении неспецифической эмпиемы плевры с использованием видеосопровождения и малоинвазивных доступов»//Материалы III научно-практической конференции хирургов Северо-Запада России и XXIV конференция хирургов Республики Карелия, Санкт-Петербург, 2001. С. 134-135.
- Качикин А.С. Применение плазменных потоков для аэрогемостаза в хирургии легких. Дис..к.м.н. М., 2005. 184 с.
- Суслов Н.И. Физико-технические основы плазмодинами-ческих и радиационных методов в хирургии. Дис..д.т.н. М., 1989. 231 с.


