Сравнительный анализ клеток с тканевыми общими маркерами, участвующими в регуляции апоптоза и пролиферации, их диагностическая эффективность у больных фолликулярными аденомами щитовидной железы
Автор: Казаков Сергей Петрович, Заботина Т.Н., Кушлинский Н.Е.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.5, 2010 года.
Бесплатный доступ
В статье представлены новые данные по исследованию методом проточной цитометрии фенотипов клеток в тканях фолликулярных аденом щитовидной железы (АЩЖ) общих маркеров CD95, CD95L, p53 (р53bright, р53*т), bcl-2 (bcl-2bright, bcl-2dim), Ki-67, участвующих в регуляции апоптоза и пролиферации, а также экспрессии мембранных и внутриклеточных белков/рецепторов в/на клетках ткани ШЖ, их диагностическая эффективность. Выявлены два типа АЩЖ, различающиеся по фенотипу. Основным отличием от основной группы доброкачественных опухолей (аденомы I типа) аденом II типа явилось наличие повышенного количества клеток с мембранным рецептором FAS-L. По данным настоящего исследования, частота выявления аденом II типа составила 19,35%. В аденомах II типа отмечались более высокие значения клеток общих маркеров, регулирующих апоптоз и пролиферацию, CD95L, p53, p53dim, p53bright, Ki-67, bcl-2, bcl-2dim, bcl-2bright, имевших отличные показателями диагностической эффективности. Таким образом, АЩЖ отличались по фенотипу клеток ткани, II тип аденом был более агрессивен и имел более худший прогноз.
Аденома, щитовидная железа, апоптоз, пролиферация
Короткий адрес: https://sciup.org/140187851
IDR: 140187851 | УДК: 616.4410006.55-07-018
Proliferation regulations, their diagnostics efficacy in patients with thyroid adenoma
The article features new research data on phenolypes flow cylomelry in thyroid gland follicular adenoma tissue of general markers CD95, CD95L, p53(р53bright, р53dim), bcl-2 (bcl-2bright, bcl-2dim), Ki-67, participating in apoplosis regulation and proliferation, as well as in expression of membranous and intracellular protein/ receptors in thyroid adenoma tissue and their diagnostic efficacy. 2 types of TGA were identified, different in phenolype. The key difference of Type II Adenoma from main group of benign tumors (Type I Adenoma) was increased number of cells with membranous receptor FAS-L. According to the research data, diagnostic frequency of Type II Adenoma was 19,35%. Type II Adenoma was marked by high amount of general markers cells, regulating apoplosis and proliferation, CD95L, p53, p53dim, p53brightl, Ki-67, bcl-2, bcl-2dim, bcl-2bright, which had different diagnostic efficacy characteristics. Thus TGAs differed in tissue cells phenolype; Type II Adenoma was more aggressive with less successful treatment perspectives.
Текст научной статьи Сравнительный анализ клеток с тканевыми общими маркерами, участвующими в регуляции апоптоза и пролиферации, их диагностическая эффективность у больных фолликулярными аденомами щитовидной железы
Исследованию маркеров апоптоза и пролиферации и их вклада в развитие опухолевого процесса у больных доброкачественными и злокачественными новообразованиями щитовидной железы (ЩЖ) в последние годы уделяют все большее внимание [3, 6, 10, 11, 12]. В то же время отсутствие достаточного количества знаний о процессах бластомогенеза, прежде всего о патогенетических механизмах нарушения апоптоза и пролиферации у больных с онкологическими заболеваниями ЩЖ, сдерживает развитие высокоинформативных методов диагностики и мониторинга за лечением этих нозологий [4, 5, 7, 13, 14]. До сих пор у врачей-онкологов, врачей-патоморфологов, иммунологов возникают трудности с диагностикой разных форм новообразований ЩЖ, поэтому большое количество исследований посвящено этому вопросу [1, 15].
Было проведено исследование у 31 больных фолликулярными аденомами ЩЖ (АЩЖ), подтвержденными морфологически. Среди больных было 25 (80,65%) женщины и 6 (19,35%) мужчин (средний возраст 57±14 лет).
Образцы тканей ЩЖ забирались во время операции с последующим приготовлением суспезии клеток общепринятыми методами (0,25% раствор трипсина и ЭДТА 1 ммоль в ФСБ), доведением до конечной концентрации
1–2 106 клеток в мкл и окрашиванием мембранных и внутриклеточных рецепторов (белков) моноклональными антителами фирмы «CALTAG» (Австрия): Bcl-2-FITS, CD95-PE-Cy5, CD95L-PE-Cy5 и фирм «DAKO» (Дания) и «BD» (США) – p53-FITS, Ki-67-РЕ. Полученную суспензию анализировали в трехцветных протоколах на проточном цитофлуориметре COULTER EPICS XL-MCL фирмы «Beckman Coulter» (США) с подсчетом не менее 100 000 событий в зоне гейтирования (12 000 клеток). Полученные цифровые данные в виде файлов (LMD) анализировались в специальной аналитической программе CXP ver.2.2 cо снятием результатов проведенных исследований. Определяли относительное количество клеток с общими маркерами CD95, CD95L, p53 (р53bright, р53dim), bcl-2 (bcl-2bright, bcl-2dim), Кi-67, а также плотность экспрессии мембранных (внутриклеточных) рецепторов (белков) в этих клетках. Плотность экспрессии мембранных (внутриклеточных) рецепторов (белков) оценивали в условных единицах по средней интенсивности свечения флуоресценции (MFI), пропорциональной номеру канала, измеренного в логарифмическом режиме.
Статистическую обработку данных проводили с использованием непараметрических методов по Манну – Уитни. Различия считались достоверными при уровне значимости p<0,05. Для расчета диагностической эффективности (величины порогового значения, показателей чувствительности, специфичности) применяли ROC-анализ.
Были исследованы образцы тканей фолликулярных аденом ЩЖ в целях сравнительного анализа общих маркеров, регулирующих апоптоз и пролиферацию, и их оценке их диагностической эффективности.
При анализе белков, регулирующих апоптоз и пролиферацию, выявлено, что в 19,35% наблюдений определяется иной фенотип аденомы, обозначенный нами как аденома II типа. Основным фенотипическим отличительным признаком аденомы II типа было наличие большого количества клеток в тканях ЩЖ, экспрессирующих маркер FAS-L (CD95L).
Результаты сравнительного исследования общих маркеров, регулирующих апоптоз и пролиферацию в тканях ЩЖ у больных с разными вариантами АЩЖ, представлены в табл. 1.
Изучены показатели количества CD95-клеток в тканях ЩЖ с разными вариантами доброкачественных новообразований (аденом) ЩЖ. Большое количество CD95-клеток выявлено у пациентов с аденомами II типа (3,22±1,08%), минимальное – у больных с основным видом АЩЖ (2,17±1,68%).
Анализ количества CD95L-клеток, содержащихся в суспензии, приготовленной из АЩЖ, показал, что число CD178+-клеток было очень высоким (рис. 1) у больных аденомой II типа и составило 54,54±12,84%, статистиче-
Табл. 1. Общие показатели клеток, содержащих белки, участвующие в регуляции апоптоза и пролиферации в тканях аденом щитовидной железы
|
Показатель |
Группы пациентов |
|
|
I (с аденомами I типа) n=25 |
II (с аденомами II типа) n=6 |
|
|
Количество клеток CD95, % |
2,17±1,68 |
3,22±1,08 |
|
Плотность рецепторов CD95 |
10,17±5,85 |
7,36±2,92 |
|
Количество клеток CD95L, % |
5,96±2,15 |
54,54±12,84* |
|
Плотность рецепторов CD95L |
9,86±5,69 |
3,82±0,46 |
|
Общее количество клеток р53, % |
64,72±15,2 |
93,74±4,98* |
|
Плотность белка р53 (общая) |
4,79±2,09 |
13,56±3,08* |
|
Количество клеток р53 dim, % |
38,73±16,22 |
8,5±2,67* |
|
Плотность белка р53 dim |
1,55±0,08 |
1,77±0,07* |
|
Количество клеток р53 bright, % |
21,82±19,84 |
83,25±9,8* |
|
Плотность белка р53 bright |
10,93±2,21 |
14,84±1,34* |
|
Количество клеток Ki-67, % |
1,45±0,77 |
60,12±18,1* |
|
Плотность белка Ki-67 |
3,26±3,68 |
4,83±0,73 |
|
Общее количество клеток bcl-2, % |
71,47±10,36 |
95,47±4,2* |
|
Плотность белка bcl-2 (общая) |
4,51±1,65 |
16,22±2,23* |
|
Количество клеток bcl-2 dim, % |
48,47±12,83 |
5,24±3,32* |
|
Плотность белка bcl-2 dim |
1,51±0,1 |
1,73±0,06* |
|
Количество клеток bcl-2 bright, % |
18,12±15,29 |
89,85±8,44* |
|
Плотность белка bcl-2 bright |
13,66±2,79 |
16,67±0,93 |
* Статистическая достоверность между группами II и I (р<0,05).
ски достоверно отличаясь (р=0,002) от этого показателя у больных аденомой I типа, где этот показатель был равен 5,96±2,15%. Показатель плотности распределения рецептора CD95L имел тенденцию к 3-кратному снижению в аденомах II типа (3,82±0,46), а в группе пациентов с основным типом АЩЖ это значение было равно 9,86±5,69. В дифференциальной диагностике аденом разных типов нами предлагается использовать показатель количества CD95L-клеток более 28,76%, превышение значения которого свидетельствовало о наличии АЩЖ II типа при диагностической эффективности 99,9% по параметрам чувствительности, специфичности и точности.
В диагностике аденом разных типов могли помочь и показатели количества клеток с белком р53 и плотности распределения белка р53 в исследуемой группе р53-по-зитивных клеток. Значимыми оказались показатели количества р53-клеток, которые были наиболее высокими (93,74±4,98%) в аденомах II типа, достоверно отличаясь (р=0,002) от этого показателя в аденомах I типа (64,72±15,2%). Значение плотности экспрессии белка р53 в этой группе клеток было наибольшим (13,56±3,08) в аденомах II типа, статистически отличаясь (р=0,002) от этого показателя (4,79±2,09) в аденомах I типа. В дифференциальной диагностике АЩЖ разных типов достаточно высока вероятность выявления АЩЖ II типа при показателях количества р53-клеток более 88,82% и значении плотности экспрессии р53-белка более 11,02 (чувствительность и специфичность метода составляли 99,9%).
Наибольшее количество р53dim-клеток клеток отмечено в аденомах
I типа – 38,73±16,22%, в аденомах II типа – 8,5±2,67% (р=0,002) (рис. 1). Плотность распределения белка р53 в р53dim-позитивных клетках изучаемых групп больных была достоверно большей в аденомах II типа (1,77±0,07), статистически достоверно отличаясь (р=0,005) от значения этого же показателя (1,55±0,08) в аденомах I типа.
В диагностике АЩЖ разных типов с высокими показателями чувствительности и специфичности метода 99,9% можно также использовать значение количества р53dim-клеток менее 11,91%, а также величину плотности р53-белка в р53dim-позитивных клетках более 1,68 при чувствительности метода 99,9%, специфичности 93,7% и точности метода 96,8%, которые следует считать критическими значениями при выявлении АЩЖ II типа.
Подобные достоверные различия (р=0,002) выявлены и при сравнении количества р53bright-клеток (см. рис. 1), которое было значительно повышено у больных с аденомой II типа (83,25±9,8%), в то время как у больных с аденомой I типа было намного ниже (21,82±19,84%). Обнаружены также статистически значимые различия (р=0,011) в величинах плотностей распределения белка р53 в р53bright-клетках у больных с аденомой I типа (10,93±2,21) в сравнении с аденомами II типа (14,84±1,34).
Обнаружение количества р53bright-клеток при значениях более 75,21% и величине плотности экспрессии
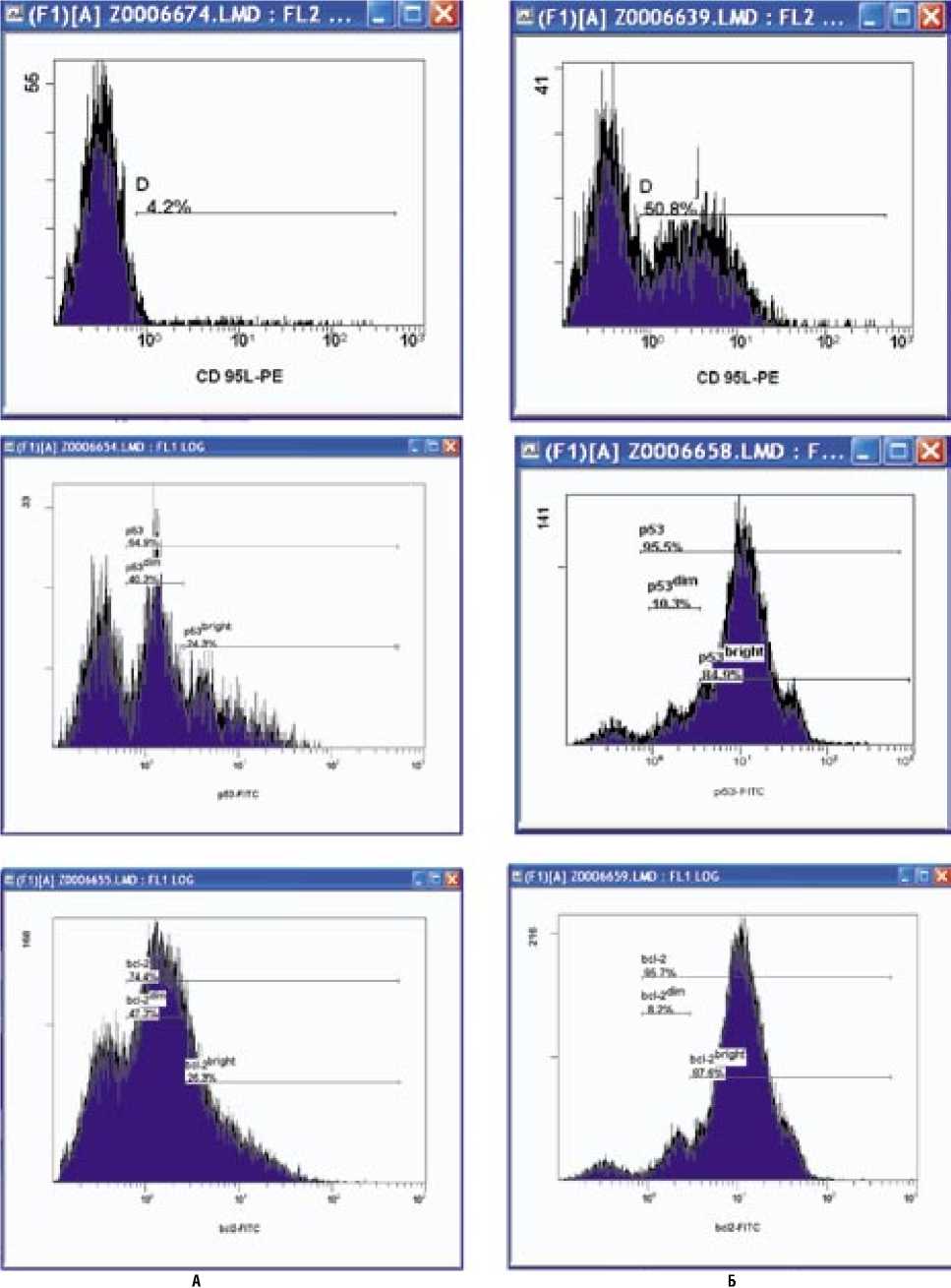
Рис. 1. Гистограммы общего количества клеток с маркерами, регулирующими апоптоз CD95L, р53, р53dim, р53bright, bcl-2, bcl-23dim, bcl-2bright у больных с разными типами аденомы щитовидной железы: А – аденома I типа; Б – аденома II типа

Казаков С.П., Заботина Т.Н., Кушлинский Н.Е.
СРАВНИТЕЛЬНЫЙ АНАЛИЗ КЛЕТОК С ТКАНЕВЫМИ ОБЩИМИ МАРКЕРАМИ, УЧАСТВУЮЩИМИ В РЕГУЛЯЦИИ АПОПТОЗА И ПРОЛИФЕРАЦИИ, ИХ ДИАГНОСТИЧЕСКАЯ ЭФФЕКТИВНОСТЬ У БОЛЬНЫХ ФОЛЛИКУЛЯРНЫМИ АДЕНОМАМИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ белка р53 в р53bright-позитивных клетках более 12,8 позволило предполагать наличие АЩЖ II типа. При этом чувствительность данных методов составила 99,9%, специфичность – 99,9 и 81,2%, а точность метода – 99,9 и 82,8% соответственно.
Выявлено статистически значимое (р=0,002) более чем 40-кратное повышение количества клеток, экспрессирующих маркер Ki-67 (рис. 2), в группе пациентов с аденомой II типа – до 60,12±18,1% по сравнению с аденомой I типа, где этот показатель составил 1,45±0,77%. При этом если показатель превышал 26,35% для значений количества Ki-67-клеток, то имело место АЩЖ II типа с показателями диагностической информативности метода 99,9%. Высокий показатель плотности распределения белка Ki-67 обнаружен в аденомах II типа (4,83±0,73) против 3,26±3,68 в аденомах I типа без достоверно значимых различий.
Число bcl-2-клеток в аденомах II типа было значительно достоверно выше (р=0,002) (95,47±4,2%) по сравнению с аденомами I типа (71,47±10,36%). Обнаружены статистически значимые различия (р=0,002) по величинам плотности распределения белка bcl-2 в bcl-2-по-зитивных клетках между аденомами II типа (16,22±2,23) и I типа (4,51±1,65). Диагностическая эффективность показателей количества bcl-2-клеток и плотности его (bcl-2-белка) распределения достаточно высока и составила по чувствительности и специфичности методов 99,9%. Показатель количества bcl-2-клеток более 88,28% и величина плотности распределения белка bcl-2 более 11,64 считались критическими значениями, которые с высокой достоверностью позволяют выявить АЩЖ II типа.
Показатели количества bcl-2dim-клеток (см. рис. 1) также достоверно (р=0,002) повышены (48,47±12,83%) в аденомах I типа и значительно снижены в аденомах II типа (5,24±3,32%). Величина плотности распределения bcl-2-белка в исследуемой группе bcl-2dim-клеток была повышена в аденомах II типа и составила 1,73±0,06, достоверно отличаясь (р=0,006) от этого показателя при аденомах II типа, где он был достоверно ниже и составил 1,51±0,1. Высокую дифференциально-диагностическую эффективность, достигающую по показателям чувствительности 99,9%, специфичности 99,9 и 93,7% и точности метода 99,9 и 96,8%, выявили значения количества bcl-2dim-клеток и плотность распределения bcl-2-белка на этих клетках. Так, значения количества bcl-2dim-клеток менее 17,43% и показателя плотности экспрессии белка bcl-2 на bcl-2dim-клетках более 1,65 подтверждали наличие АЩЖ II типа.
Иная динамика отмечена при сравнительном анализе показателей количества bcl-2bright-клеток в группах сравнения (см. рис. 1). Количество bcl-2bright-клеток было значительно достоверно (р=0,002) выше в аденомах II типа (89,85±8,44%), чем в аденомах I типа (18,12±15,29%). Дополнительным диагностическим критерием с высокой эффективностью в 99,9% может использоваться этот показатель (количества bcl-2bright-клеток), при значении более 63,33% которого выявляли аденому II типа.
Согласно литературным данным [2, 8, 9], повышенная экспрессия на опухолевых клетках FAS-L, во-первых, создает условия для избегания опухолевыми клетками цитотоксического действия Т-лимфоцитов (CD8+-лим-фоцитов) и натуральных киллерных клеток, а также индукции в них процесса апоптоза, что создает бреши в Т-клеточном репертуаре, убивая любые активные Т-хелперы, в том числе способные распознать опухолевые антигены. Во-вторых, экспрессия FAS-L на опухолевых клетках за счет дефектов в путях апоптозной сигнальной трансдукции блокирует аутокринный путь апоптоза между опухолевыми клетками. В-третьих, повышенная экспрессия FAS-L может быть основным способом ми-
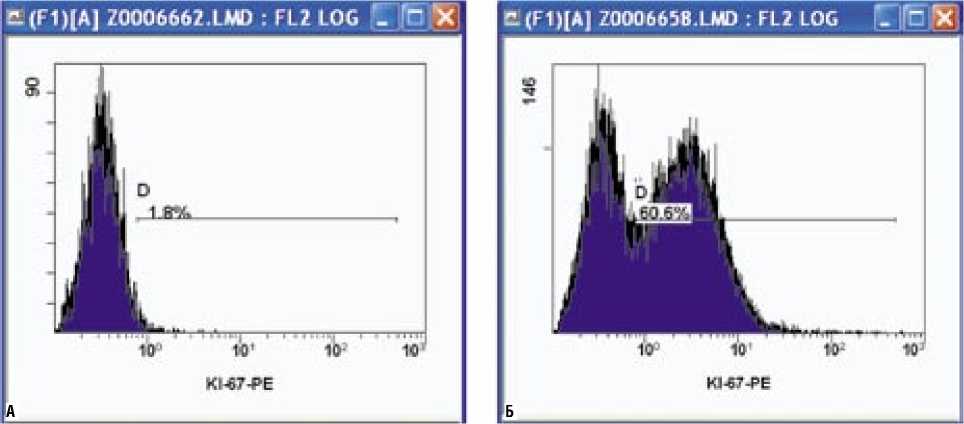
Рис. 2. Гистограммы общего количества клеток с маркером, регулирующим пролиферацию (Ki-67), у больных аденомами I (А) и II (Б) типа щитовидной железы

Казаков С.П., Заботина Т.Н., Кушлинский Н.Е.
СРАВНИТЕЛЬНЫЙ АНАЛИЗ КЛЕТОК С ТКАНЕВЫМИ ОБЩИМИ МАРКЕРАМИ, УЧАСТВУЮЩИМИ В РЕГУЛЯЦИИ АПОПТОЗА И ПРОЛИФЕРАЦИИ, ИХ ДИАГНОСТИЧЕСКАЯ ЭФФЕКТИВНОСТЬ У БОЛЬНЫХ ФОЛЛИКУЛЯРНЫМИ АДЕНОМАМИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ грирующих опухолевых клеток расчистить себе путь от нормальных клеток, отправляя их в апоптоз в процессе инвазии и метастазирования.
Повышенная экспрессия FAS-L в АЩЖ может служить фактором плохого прогноза опухоли с возможным ее быстрым ростом и способностью трансформироваться в злокачественную опухоль. Поэтому выделение АЩЖ с повышенной экспрессией FAS-L в отдельную группу и изучение фенотипа этих новообразований представляет определенную научную, практическую и прогностическую значимость.
Сравнительный анализ разных типов АЩЖ выявил повышение почти в 10 раз количества клеток в изучаемой нами суспензии ткани ЩЖ с маркером СD95L в АЩЖ II типа по сравнению с АЩЖ I типа. Также отмечено 3-кратное снижение плотности экспрессии СD95L-ре-цепторов в СD95L-положительных клетках в группе аденом II типа.
Выявленное значительное повышение количества FAS-L в аденомах II типа может быть плохим прогностическим признаком при проведении химиотерапии, так как считается, что в некоторых типах опухолевых клеток цитостатики индуцируют апоптоз, усиливая экспрессию лигандов и рецепторов семейства TNF. Следовательно, изначально повышенное количество СD95L-положи-тельных клеток в аденомах II типа на фоне химиотерапии может приводить к еще большей концентрации FAS-L на изначально резистентных к сигналам рецепторов смерти аденоматозных клетках, содержащих химиорезистентный невосприимчивый фенотип [2].
В АЩЖ II типа выявлено резкое повышение почти до максимального уровня количества клеток, содержащих белок р53, а также 3-кратное увеличение плотности экспрессии этого белка в р53-позитивных клетках. Исследованиями структуры повышенного содержания р53-поло-жительных клеток доказано, что такое увеличение связано как с 4-кратным ростом субпопуляции р53bright-клеток, так и с повышенной экспрессией белка р53 в р53bright-позитив-ных клетках на фоне характерного снижения выработки этого белка в р53dim-положительных клетках.
Аналогичные изменения обнаружены при исследовании количества клеток с ингибирующим апоптоз белком bcl-2 в аденомах II типа. Отмечено повышенное количество клеток с белком bcl-2, почти 4-кратное увеличение экспрессии этого белка на bcl-2-позитивных клетках прежде всего за счет увеличенного содержания количества bcl-2bright-клеток и повышенной экспрессии bcl-2 белка в bcl-2bright-позитивных клетках на фоне снижения количества bcl-2dim-клеток.
Для АЩЖ II типа характерна повышенная пролиферативная активность суспензии исследуемых клеток по всей ткани аденомы, что подтверждается значительным 40-кратным увеличением количества клеток с внутриклеточным пролиферативным белком Ki-67 и незначительным повышением плотности экспрессии этого белка в Ki-67-позитивных клетках. Такое сочетание значительного повышения количества Ki-67-позитивных клеток с почти 2-кратным повышением плотности распределения этого маркера по Ki-67-позитивным клеткам, нехарактерное для злокачественных и доброкачественных новообразований ЩЖ, которые в основном отличаются невысокой и сниженной пролиферацией, может быть начальным этапом трансформации доброкачественного процесса в злокачественный, например в фолликулярный РЩЖ, обладающий сходными фенотипическими особенностями. Именно поэтому для аденом II типа может быть характерен неблагоприятный прогноз развития за счет использования механизмов повышенного роста в измененных аденоматозных клетках и выраженной апоп-тозной агрессивности, что требует ее систематического динамического наблюдения.
Согласно литературным данным морфологическая граница между фолликулярной аденомой и карциномой ЩЖ нечеткая и возможно выявленная аденома II типа является карциномой ЩЖ. Нами не проводилось сравнительных исследований карцином и выявленных нами аденом II типа в связи с трудностями дополнительных морфологических исследований, однако данное исследование было бы достаточно интересным и позволило бы охарактеризовать выявленную нами аденому II типа.
Так же изучены диагностическая информативность и пороговые значения показателей маркеров, регулирующих апоптоз и пролиферацию, в дифференциальной диагностике аденом I и II типов. Выявлены критические значения по всем исследуемым параметрам белков, регулирующих апоптоз и пролиферацию, с очень хорошими и отличными параметрами диагностической эффективности значений количеств клеток ЩЖ и большинства показателей плотности распределения рецепторов и белков в/на клетках ЩЖ. Среди них отметим лишь группы клеток общих тканевых маркеров, регулирующих апоптоз и пролиферацию, с отличными показателями диагностической эффективности: CD95L, p53, p53dim, p53bright, Ki-67, bcl-2, bcl-2dim, bcl-2bright.
Вывод
В процессе исследования выявлено два типа АЩЖ, различающихся по фенотипу. Основным отличием от основной группы доброкачественных опухолей (аденомы I типа) аденом II типа явилось наличие повышенного количества клеток с мембранным рецептором FAS-L. По данным настоящего исследования, частота выявления аденом II типа составила около 19,35%.
Для врачей клиницистов (хирургов, онкологов, эндокринологов) важным является знание и умение использовать маркеры апоптоза и пролиферации в дополнительной диагностике аденом щитовидной железы, а при выявлении аденом II типа более внимательное наблюдение за этими пациентами и при неблагоприятном прогнозе, перерождении доброкачественного процесса в злокачественный выполнение оперативного вмешательства по показаниям.
Казаков С.П., Заботина Т.Н., Кушлинский Н.Е.
СРАВНИТЕЛЬНЫЙ АНАЛИЗ КЛЕТОК С ТКАНЕВЫМИ ОБЩИМИ МАРКЕРАМИ, УЧАСТВУЮЩИМИ В РЕГУЛЯЦИИ АПОПТОЗА И ПРОЛИФЕРАЦИИ, ИХ ДИАГНОСТИЧЕСКАЯ ЭФФЕКТИВНОСТЬ У БОЛЬНЫХ ФОЛЛИКУЛЯРНЫМИ АДЕНОМАМИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
Результаты исследования показывают, что необходимо совместно с морфологами более подробно изучить выявленную нами аденому II типа ЩЖ и провести более глубокий морфологический анализ на предмет выявления карцином ЩЖ или иного типа фолликулярной аденомы.
Представленные результаты по изучению фенотипа АЩЖ II типа и более подробного морфологического их изучения могут быть полезны при разработке новых препаратов для таргетной терапии, но с иными механизмами запуска в этих опухолевых клетках процессов апоптоза.
Список литературы Сравнительный анализ клеток с тканевыми общими маркерами, участвующими в регуляции апоптоза и пролиферации, их диагностическая эффективность у больных фолликулярными аденомами щитовидной железы
- Дедов И.И., Балаболкин М.И., Марова Е.И. Болезни органов эндокринной системы: Руководство для врачей. М.: Медицина, 2000. 568 с.
- Князкин И.В., Цыган В.Н. Апоптоз в онкоурологии. СПб: Наука, 2007. 240 с.
- Кушлинский Н.Е., Трапезников Н.Н. Современные возможности клинической биохимии в онкологии. Последние факты и новые концепции//Клин. лаб. диагн. 2000. № 9. С. 3-5.
- Лукьянова Н.Ю., Кулик Г.И., Чехун В.Ф. Роль генов р53 и bc-2 в апоптозе и лекарственной резистентности опухолей//Вопр. онкол. 2000. Т. 46, № 2. С. 121-128.
- Марченко И.А. Исследование диагностической значимости теломеразы и других маркеров злокачественной трансформации при новообразованиях щитовидной железы человека: Автореф. дис.... канд. биол. наук. М., 2009. 24 с.
- Соколова О.В. Дифференциально-диагностические критерии фолликулярных опухолей щитовидной железы разной степени злокачественности: Автореф. дис.... канд. мед. наук. СПб, 2009. 22 с.
- Соколова О.В. Особенности экспрессии галектина-3 в фолликулярных опухолях щитовидной железы разной степени злокачественности//Современные проблемы клинической цитоморфологии: Тез. всерос. конф. с межд. участ., науч. чтения, посвящ. памяти чл.-корр. РАМН, з.д.н. РФ проф. О.К. Хмельницкого и 25-летию курса цитол. каф. патол. анат. СПб: МАПО, 2007. С. 104-105.
- Цыган В.Н. Актуальные проблемы иммунологии. СПб: Гуманистика, 2004. 47 с.
- Basolo F., Fiore L., Baldanzi A. el al. Suppression of Fas expression and down-regulation of Fas ligand in highly aggressive human thyroid carcinoma//Lab. Invest. 2000. Vol. 80, № 9. P.1413-1419.
- Erdogan M., Karadeniz M., Berdeli A. et al. Fas/Fas ligand gene polymorphism in patients with papillary thyroid cancer in the Turkish population//J. Endocrinol. Invest. 2007. Vol. 30, № 5. P. 411-116.
- Kotomecki K., Maciaszczyk P., Stepien H. el al. Evaluation of p53 and soluble Fas ligand (sFas-L) serum level concentration as indicators of apoplosis in serum of patients with benign and malignant primary follicular thyroid tumors//Endokrynol. Pol. 2006. Vol. 57, № 4. P. 320-325.
- Mitsiades C.S., Poulaki V., Fanourakis G. Fas signaling in thyroid carcinomas is diverted from apoptosis to proliferation//Clin. Cancer Res. 2006. Vol. 12, № 12. P. 3705-3712.
- Rzeszutko M., Rzeszutko W., Dziegiel P. el al. Expression of FAS/APO 1/CD 95 in thyroid tumors//Folia Hislochem. Cylobiol. 2007. Vol. 45, № 2. Р. 87-91.
- Segev D.L., Umbricht C., Zeiger M.A. Molecular pathogenesis of thyroid cancer//Surg. Oncol. 2003. Vol. 12, N 2. P. 69-90.
- Suster S. Thyroid tumors with a follicular growth pattern: problems in differential diagnosis//Arch. Pathol. Lab. Med. 2006. Vol. 130, № 7. P. 984-988.


