Сравнительный анализ лечения больных метастатическим колоректальным раком с применением локальных методов деструкции
Автор: Трандофилов М.М., Праздников Э.Н., Терясов С.Г., Синявин Д.Ю., Шевченко В.П., Манчуров В.Н., Сизова А.Н., Кошелев И.А., Вахромкин В.С., Шкильнюк П.Г.
Журнал: Московский хирургический журнал @mossj
Рубрика: Онкология
Статья в выпуске: 1 (95), 2026 года.
Бесплатный доступ
Введение. Около 90 % опухолей печени являются метастатическими, преимущественно от колоректального рака (КРР). Лишь 10–25 % таких метастазов являются резектабельными. Без лечения средняя выживаемость составляет менее года, а даже на фоне химиотерапии не превышает 18 месяцев. Цель исследования заключалась в повышении эффективности лечения пациентов с метастазами колоректального рака в печень с применением миниинвазивных методов локальной деструкции. Материалы и методы исследования. В исследовании участвовало 257 пациентов с метастазами КРР в печень (2002–2024 гг.). Всем пациентам проводили УЗИ, МРТ/КТ с контрастом, ПЭТ-КТ и 3D-моделирование (MYRIAN XP-Liver) для планирования тактики. Все пациенты получали комбинированную терапию: ПХТ по схемам FOLFOX/XELOX/FOLFIRI ± таргетная терапия. Трансартериальная химиоэмболизация (ТАХЭ): 34 пациентам (для уменьшения опухоли >4 см). Радиочастотная абляция (РЧА):121 пациенту (опухоли 1–5 см). Микроволновая абляция (МВА): 57 пациентам (опухоли 1–3,5 см). Лазерная абляция (ЛА): 45 пациентам (опухоли 1–3,3 см). Результаты лечения. Выживаемость в группе РЧА: 1 год – 73,5 %, 2 года – 53,3 %, 3 года – 32,1 %. МВА: 1 год – 78,5 %, 2 года – 63,3 %, 3 года – 58,3 %. ЛА: 1 год – 88 %, 2 года – 71 %, 3 года – 43,5 %. Медиана безрецидивной выживаемости – 8,5 месяцев. Годовая выживаемость в подгруппе из 12 пациентов составила 84 %. Летальность составила 0,6 % (2 случая в группе РЧА). Средний койко-день – 7 суток. Заключение. Применение миниинвазивных методов термодеструкции (РЧА, МВА, ЛА) в рамках мультидисциплинарного подхода позволяет значительно расширить показания к лечению для нерезектабельных пациентов (с тяжелой сопутствующей патологией, билобарным поражением, малым функциональным резервом печени). Это повышает общую резектабельность до 35–40 %, снижает операционные риски и количество осложнений, сокращает сроки госпитализации и улучшает показатели выживаемости.
Лазерная абляция, микроволновая абляция, радиочастотная абляция, трансартериальная химиоэмболизация.
Короткий адрес: https://sciup.org/142247248
IDR: 142247248 | УДК: 006.617-089 | DOI: 10.17238/2072-3180-2026-1-116-122
Comparative analysis of treatment of patients with metastatic colorectal cancer using local destruction methods
Introduction. Approximately 90 % of liver tumors are metastatic, predominantly from colorectal cancer (CRC). Only 10–25 % of such metastases are resectable. The median survival is less than a year without treatment and even with chemotherapy it does not exceed 18 months. The aim of the study to improve the effectiveness of treatment for patients with colorectal cancer liver metastases using minimally invasive local destruction methods. Materials and methods of research. The study included 257 patients with CRC liver metastases (2002–2024). All patients underwent ultrasound, contrast-enhanced MRI/CT, PET-CT, and 3D modeling (MYRIAN XP-Liver) for treatment planning. All patients received combined therapy: chemotherapy according to FOLFOX/XELOX/FOLFIRI regimens ± targeted therapy. Transarterial chemoembolization (TACE): 34 patients (to shrink tumors >4 cm). Radiofrequency ablation (RFA): 121 patients (tumors 1–5 cm). Microwave ablation (MWA): 57 patients (tumors 1–3,5 cm). Laser ablation (LA): 45 patients (tumors 1–3,3 cm). Treatment results. Survival in the RFA group: 1 year – 73,5 %, 2 years – 53,3 %, 3 years – 32,1 %. MWA: 1 year – 78,5 %, 2 years – 63,3 %, 3 years – 58,3 %. LA: 1 year – 88 %, 2 years – 71 %, 3 years – 43,5 %. Median relapse-free survival is 8,5 months. The 1-year survival rate in the subgroup of 12 patients was 84 %. Mortality was 0,6 % (2 cases in the RFA group). The average hospital stay was 7 days. Conclusion. The use of minimally invasive thermodestruction methods (RFA, MWA, LA) within a multidisciplinary approach significantly expands treatment indications for non-resectable patients (with severe comorbidities, bilobar involvement, low functional liver reserve). This increases overall resectability to 35–40 %, reduces surgical risks and the number of complications, shortens hospitalization times, and improves survival rates.
Текст научной статьи Сравнительный анализ лечения больных метастатическим колоректальным раком с применением локальных методов деструкции
В структуре онкозаболеваемости 90 % опухолей печени имеют метастатический характер. Основной источник метастазов – колоректальный рак (до 70 %), что обусловлено анатомо-физиологическими особенностями органа [1, 2, 3]. Несмотря на многообразную симптоматику, до 80 % пациентов госпитализируют с III–IV стадиями. Среди радикально пролеченных больных без рецидива почти у 50 % выявляют печеночные метастазы. Их резектабельность, по разным данным, составляет лишь 10– 25 %. Причинами неоперабельности служат внепеченочные метастазы, поражение магистральных сосудов, множественное билобарное распространение, недостаточный функциональный резерв печени и тяжелые сопутствующие патологии [2, 4].
Средняя выживаемость пациентов с метастазами колоректального рака в печень не превышает двух лет. Без лечения продолжительность жизни на IV стадии составляет менее одного года. Даже системная полихимиотерапия обеспечивает лишь небольшое увеличение выживаемости – в среднем до 18 месяцев.
В настоящее время основным хирургическим методом лечения метастазов КРР в печени остается резекция. Однако, значительной группе пациентов она не показана (малый функциональный резерв, сопутствующие заболевания). Для них применяются методы локальной деструкции (радиочастотная, микроволновая, лазерная, ультразвуковая абляция), которые минимизируют послеоперационные осложнения и объем повреждения тканей [5, 6, 7, 8, 9, 10]. В настоящее время имеется мало работ, посвященных сравнительному анализу данных методов лечения. В нашей статье мы хотим отразить данную проблему.
Материалы и методы
В исследование включили 257 пациентов с метастазами колоректального рака в печень, лечившихся в период с 2002 по 2024 год. По нозологиям распределение было следующим: рак ободочной кишки – 220 (69 %) пациентов, прямой кишки – 99 (31 %). По классификации Gennari объем поражения печени составил: I стадия – 127 (40 %) больных, II – 154 (48 %), III – 38 (12 %). Мужчин – 113, женщин – 144. Средний возраст – 68 ± 7,6 лет. Всем пациентам до опе- рации выполняли УЗИ брюшной полости, МРТ и/или КТ с контрастированием, ПЭТ-КТ для точного определения размеров, локализации, количества опухолей и их метаболической активности. С помощью программного обеспечения (MYRIAN XP-Liver) производилась постобработка полученных изображений с построением трехмерных реконструкций и волюметрического анализа, что позволило определиться с дальнейшей хирургической тактикой. Все больные получали комбинированное лечение. Полихимиотерапию проводили по схемам FOLFOX4/XELOX или FOLFIRI с добавлением таргетной терапии (в зависимости от мутаций в генах RAS и BRAF). Предоперационное лечение включало 4–6 курсов, с контролем эффективности по КТ/МРТ и УЗИ каждые три месяца. Терапию продолжали до прогрессирования, развития выраженной токсичности или отказа пациента от дальнейшего лечения.
В рамках лекарственной терапии также применяли трансартериальную химиоэмболизацию (ТАХЭ). Перед процедурой на основе СКТ выполняли реконструкцию сосудов печени. Все операции проводили трансрадиальным доступом (через лучевую артерию) для снижения риска осложнений и ранней активизации пациентов. Использовали методику суперселективной катетеризации питающих артерий микрокатетерами. Этот подход обеспечивает точную доставку взвеси микроэмболов в опухоль, минимизируя риск окклюзии сосуда и нецелевой эмболии. Применяли калиброванные эмболы Hepasphere 50–250 мкм (25 мг), насыщенные концентрированным раствором доксорубицина. Взвесь вводили на скорости 1 мл/мин до достижения стойкого эффекта «стоп-контраст» в течение 7–8 сердечных циклов.
Хирургическое лечение заключалось в использовании локальных методов термодеструкции (радиочастотная, микроволновая абляции, лазерной абляции), а также их сочетание.
Для радиочастотной абляции применяли аппарат Cool-tip (Covidien, Ирландия) мощностью 200 Вт с набором электродов диаметром 1,2–2,0 мм и длиной 10–25 мм. Время экспозиции варьировало от 4 до 10 минут в зависимости от размера опухоли, температура в очаге достигала 100°C. Для микроволновой абляции использовали системы AveCure MWG881 (MedWaves, США) мощностью 32±2 Вт с частотой 902–928 МГц и Surblate (Vision Medicals, Китай) мощностью 90 Вт с частотой 2,45 ГГц и набором антенн (толщина 14– 16 G, активная зона 2–4 см). Время воздействия составляло 5–10 минут, температура достигала 120°C. Для лазерной абляции применяли систему Echolaser X4, сочетающую УЗ-аппарат и четырёхканальный лазер с длиной волны 1064 нм, мощностью 5,0 Вт и энергией 1800 Дж на волокно. Установку аппликаторов выполняли под УЗ- (рис. 1) или видеолапаро-скопическим контролем при чрескожном чреспеченочном доступе либо интраоперационно во время лапаротомии.
Контроль эффективности осуществляли с помощью динамического ультразвукового исследования, компьютерной или магнитно-резонансной томографии.
Все пациенты получали комбинированную терапию, включавшую хирургические и химиотерапевтические методы. Объем хирургического вмешательства представлен в таблице 1.
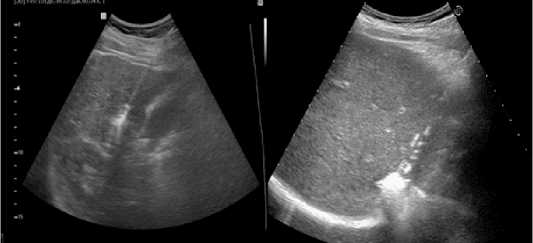
Рис. 1. Выполнение лазерной абляции
Fig. 1. Performing laser ablation
Таблица 1
Объем хирургического вмешательства
Table 1
Extent of surgical intervention
|
Хирургическое лечение Surgical treatment |
Количество больных Number of patients |
||
|
Вид лечения / Type of treatment |
Объем /Extent |
abs |
% |
|
РЧА / RFA |
открыто / laparotomy |
16 |
6 |
|
чрескожно чреспеченочно / percutaneous transhepatic |
89 |
35 |
|
|
видеолапароскопически / laparoscopic access |
16 |
6 |
|
|
всего / total |
121 |
47 |
|
|
МВА / MWA |
открыто / laparotomy |
5 |
2 |
|
чрескожно чреспеченочно / percutaneous transhepatic |
52 |
20 |
|
|
всего / total |
57 |
24 |
|
|
ТАХЭ / TACE |
34 |
13 |
|
|
ЛА / LA |
Открыто |
5 |
2 |
|
чреcкожно чреспеченочно |
40 |
15 |
|
|
Всего |
45 |
17 |
|
|
Всего / Total |
257 |
100 |
|
На предоперационном этапе пациентам выполняли трансартериальную химиоэмболизацию (ТАХЭ) для уменьшения размеров опухоли и повышения безопасности последующего вмешательства. С 2015 по 2025 гг. процедуру провели 34 пациентам (средний возраст 59,26±3,21 года; 13 мужчин, 21 женщина) с опухолями более 4 см (рис. 2).
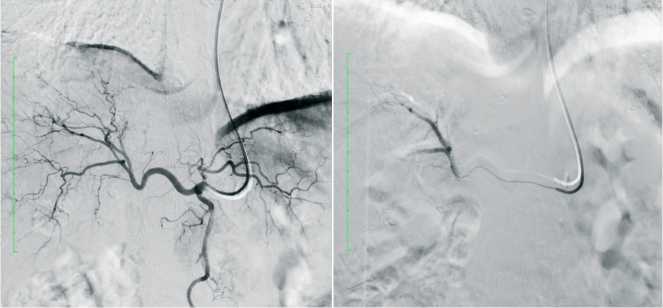
Рис. 2. ТАХЭ S5 образования печени Fig. 2 TACE S5 liver lesions
Пациентам, которым резекция печени была невозможна из-за билобарного поражения, недостаточного функционального резерва или тяжелой сопутствующей патологии, выполняли методы термодеструкции: радиочастотную (РЧА) или микроволновую абляцию (МВА). Перед процедурой проводили УЗИ для планирования доступа. РЧА выполнена 121 пациенту (средний возраст 67,12±1,76 лет; 56 мужчин, 65 женщин) с образованиями 1–5 см. В 16 случаях процедуру проводили интраоперационно при синхронных метастазах вместе с удалением первичной опухоли, в 12 – при контралатеральных метастазах вместе с резекцией печени. В 16 случаях РЧА выполняли под видеолапароскопическим контролем, что позволило абляции крупных метастазов (до 6,5 см) и до 5 узлов за сеанс. В 89 случаях при синхронных и метахронных метастазах РЧА выполняли чрескожно. Параметры воздействия варьировали в зависимости от размера метастаза.
С 2013 года применяли МВА, которая имеет преимущества: большая зона деструкции за меньшее время, проще использование, лучше визуализация. МВА выполнена 57 пациентам (средний возраст 56,32±2,65 года; 27 мужчин, 30 женщин) с опухолями 1–3,5 см. В 5 случаях – интраоперационно с резекцией, в 52 – чрескожно. Температура в очаге достигала 120°C.
Контроль эффективности проводили с помощью УЗИ, КТ и МРТ на 1, 5, 30 сутки и далее каждые 3 месяца.
С 2017 года применяли лазерную абляцию на аппарате Echolaser X4. 45 пациентов получили лечение (средний возраст 56,32±2,65 года; 25 мужчин, 20 женщин) с опухолями 1–3,3см. Преимущества: малый диаметр аппликаторов (17– 21G), возможность использования нескольких световодов, абляция множественных метастазов, полная совместимость с МРТ, безопасность при кардиостимуляторах. Метод эффективен в случаях, когда опухоли находятся вблизи крупных сосудов. Риск повреждения сосудов минимизирован в связи с тем, что при выполнении операции формируется небольшая и четкая зона абляции без вовлечения в сосудистые структуры.
Результаты
Совершенствование КТ с 3D-моделированием сделало её ключевым методом предоперационной визуализации, определяющим резектабельность и тактику (рис. 3). ТАХЭ с гепосферами и доксорубицином выполнена 34 пациентам, что позволило уменьшить опухоли и провести абляцию. Послеоперационные осложнения были минимальными (субфебрилитет, повышение трансаминаз в течение 3 дней). Годовая выживаемость в группе из 12 пациентов составила 84 % (10 больных). Средний койко-день – 4 суток.
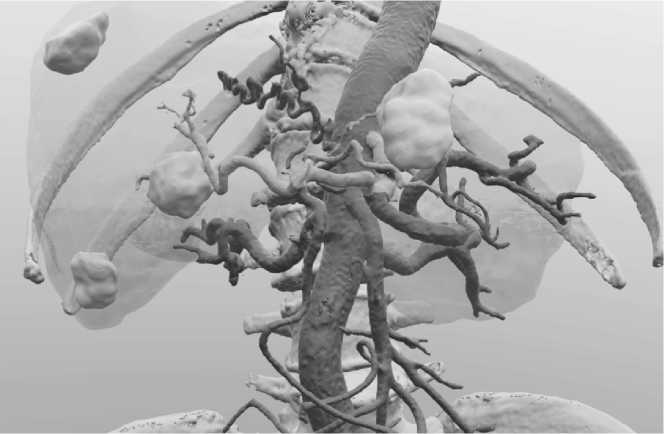
Рис. 3. 3D визуализация Fig. 3. 3D visualization
Несмотря на успехи лекарственной терапии метастатического поражения печени, основным методом лечения, позволяющим увеличить продолжительность жизни пациентов, остается хирургический, заключающийся в резекции пораженного участка печени при сохранении жизнеспособного функционального резерва органа свыше 30 %, удовлетворительном физическом статусе пациента, отсутствие билобарного поражения печени. В данную группу пациентов попадают всего лишь от 10 до 25 %. Интраоперационная термоабляция расширила показания к хирургическому лечению билобарных поражений печени. Среднее время воздействия при РЧА составило 9±3 мин, при МВА – 6±2 мин. Наблюдались следующие осложнения, отраженные в таблице 2.
Таблица 2
Осложнения после применения локальных методов термодеструкции
Сomplications after applying local methods of thermal destruction
Table 2
|
Послеоперационные осложнения Complications |
РЧA / RFA |
МВА / MWA |
ЛА / LA |
|
Летальный исход / Death |
2 |
0 |
0 |
|
Кровотечение из места вкола игольчатого электрода / bleeding from the needle applicator injection site |
3 |
1 |
1 |
|
Острая печеночная недостаточность / Acute liver failure |
2 |
0 |
1 |
|
Желчеистечение из места введения игольчатого электрода / Bile leakage from the needle electrode injection site |
1 |
0 |
0 |
|
Формирование остаточной полости / Residual cavity |
3 |
1 |
2 |
|
Внутрипеченочная гематома / Intrahepatic hematoma |
2 |
1 |
1 |
|
Некроз стенки толстой кишки / Wall necrosis of the colon |
0 |
1 |
0 |
Метастазы печени при РЧА демонстрируют выживаемость: однолетнюю – 73,5 %, двухлетнюю – 53,3 %, трехлетнюю – 32,1 %. При МВА показатели составили 78,5 %, 63,3 % и 58,3 % соответственно (рис. 4, 5). Для ЛА медиана безрецидивной выживаемости достигла 8,5 месяцев, а общая выживаемость – 88 %, 71 % и 43,5 % за один, два и три года.
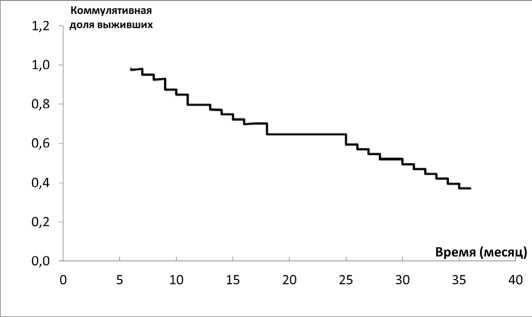
Рис. 4. Общая выживаемость при лазерной абляции
Fig. 4. Overall survival (laser ablation)
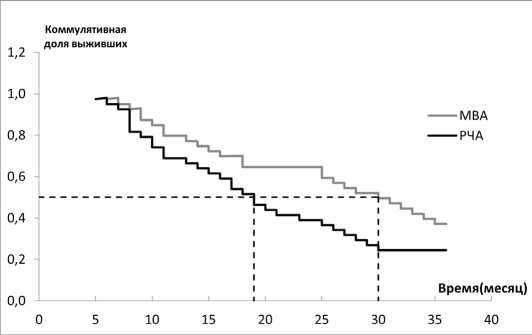
Рис. 5. Общая выживаемость при РЧА, МВА
Fig. 5. Overall survival (RFA, MWA)
Выводы
Применение методик локальной термодеструкции метастазов колоректального рака позволяет снизить операционно-анестезиологические риски и количество осложнений благодаря малотравматичности и миниинвазивности и увеличить общую выживаемость.


