Сравнительный анализ показателей криоконсервированной и свежеполученной спермы баранов-производителей романовской породы
Автор: Лариса Александровна Гнездилова, Сеидфатима Мировна Борунова, Анаида Арутюновна Кочконян
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Ветеринария и зоотехния
Статья в выпуске: 10, 2021 года.
Бесплатный доступ
Был проведен системный анализ нативной и криоконсервированной спермы, полученной от баранов-производителей романовской породы. Опыт проводился на базе ФГБУ «ВГНКИ» в 2020–2021 гг. Всего было проанализировано 20 спермопроб от 10 баранов-производителей. В статье изучены такие параметры идентификации морфофункциональных отклонений спермиев баранов-производителей, как подвижность (нормокинезис, гипокинезис), аномальная акросома, патологические и аномальные формы сперматозоидов, индекс фрагментации ДНК. Взятие генетического материала проводилось согласно требованиям нормативных документов. В сравнительном анализе по показателю подвижности сперматозоидов установили отклонение от нормы только в криоконсервированной сперме, ППД = 13,2 %. При оценке морфологии в криоконсервированной сперме в 7 спермопробах было выявлено более 20 % аномальных сперматозоидов. Установлено что, в криоконсервированной сперме 9 спермопроб с фрагментированной ядерной и митохондриальной ДНК сперматозоидов. Выявлено уменьшение количества спермиев (олигоспермия), снижение их общей и поступательной подвижности (астеноспермия), появление большого количества спермиев с различными аномальными формами (тератозооспермия). Достаточно часто наблюдалось единовременное наличие сочетанных нарушений (олигоастеноспермия, олигоастенотератозооспермия). Обзорные данные по методологии ветеринарно-санитарного контроля спермы баранов не дают нам расширенной интерпретации исследуемых данных. Метод окрашивания по Романовскому с красителем эозин, азур-эозин, указанный в нормативном документе, затрудняет проводить исследования на выявление поврежденной акросомы и патологических форм спермиев. Предложенный метод окраски с помощью тест набора «Диффквик» позволяет ускорить время на окрашивании и более быстро получать результаты. Методика окрашивания акридин-оранжевым позволит выявить фрагментированную ядерную и митохондриальную ДНК.
ДНК, акросома, сперматозоид, баран-производитель, подвижность.
Короткий адрес: https://sciup.org/140257846
IDR: 140257846 | УДК: 636.32:636.082.451 | DOI: 10.36718/1819-4036-2021-10-135-143
Comparative analysis of the Romanov breed rams-producers' cryopreserved and freshly obtained sperm indicators
A systematic analysis of native and cryopreserved sperm obtained from breeders of the Romanov breed was carried out. The experiment was conducted on the basis of the Federal State Budgetary Institution "VGNKI" in 2020–2021. A total of 20 semen samples from 10 breeder rams were analyzed. The paper studies such parameters of identification of morphofunctional abnormalities of sperm of rams-producers, such as: mobility (normokinesis, hypokinesis), abnormal acrosome, pathological and abnormal forms of spermatozoa, DNA fragmentation index. The collection of genetic material was carried out in accordance with the requirements of regulatory documents. In a comparative analysis in terms of sperm motility, a deviation from the norm was found only in cryopreserved sperm, PPD = 13.2 %. When assessing morphology in cryopreserved semen in 7 sperm samples, more than 20 % of abnormal spermatozoa were detected. It was found that cryopreserved sperm contains 9 sperm samples with fragmented nuclear and mitochondrial DNA of spermatozoa. A decrease in the number of spermatozoa (oligospermia), a decrease in their general and translational mobility (asthenospermia), the appearance of a large number of spermatozoa with various abnormal forms (teratozoospermia) were revealed. The simultaneous presence of combined disorders (oligoasthenospermia, oligoastenoteratozoospermia) was quite often observed. Survey data on the methodology of veterinary and sanitary control of sheep semen do not give us an extended interpretation of the data under study. The Romanovsky staining method with eosin, azure-eosin, specified in the regulatory document, makes it difficult to conduct studies to identify damaged acrosomes and pathological forms of sperm. The proposed staining method using the "Diff-Quick" test kit makes it possible to speed up the staining time and get results more quickly. The acridine orange staining technique will reveal fragmented nuclear and mitochondrial DNA.
Текст научной статьи Сравнительный анализ показателей криоконсервированной и свежеполученной спермы баранов-производителей романовской породы
Введение. Важным направлением научнопрактических и научно-исследовательских работ для овцеводства в Российской Федерации является создание современных, продуктивных типов овец, которые соответствуют лучшим породам мирового уровня [1].
Согласно определению В.В. Абонеева, искусственное осеменение – целенаправленное усовершенствование породных и продуктивных качеств в овцеводстве за счет активного использования наиболее ценных баранов-производителей [2]. Результативность искусственного осеменения, а это и высокая оплодотворяемость и плодовитость маток, эффективна лишь тогда, когда правильно проведена работа по подготовке к случке маток баранов-производителей, а самое главное – когда проведены скрининговые мероприятия по проверке генетического материала по всем актуализированным методикам [1].
Оплодотворяющая способность баранов-производителей зависит от комплекса различных бифакторов [3]. Необходимо, чтобы биологическое качество эякулята соответствовало определенным критериям [4]. В результате этого обязательное проведение комплексной оценки спермопродукции необходимо для последующего использования высопродуктивных сельскохозяйственных животных в воспроизводстве [5]. Совместно с классическими методами оценки качества спермы возникает необходимость комплексного подхода к оценке спермопродукции производителей, использования современных методов, а именно определения индекса фрагментации ДНК сперматозоидов и подсчета половых клеток с интактной ак-росомой [6, 7].
Причиной идиопатического бесплодия является содержание большого количества сперми-ев с аномальной акросомой в полученном эякуляте, в случае если в спермограмме диагносци-руется положительные параметры. P. Gottardo объясняет это тем, что в акросоме уменьшается проницаемость плазматической мембраны для ионов кальция, что отражается на их способности прикрепляться к мембране ооцита [8]. В поврежденной дегенеративной акросоме часто наблюдаются выраженные разрушения плазматической мембраны, впоследствии они приводят к низкой оплодотворящей способности сперми-ев баранов-производителей [9]. Отсутствие или повреждение апикального тельца у спермокле-ток проявляется нарушением различных процессов в сперматогенезе.
Митохондриальная дисфункция приводит к нарушению синтеза АТФ и гиперпродукции АФК в сперме, в настоящее время данная патология пополняет группу патологических отклонений у спермиев, которые выражаются чаще всего генетическими, структурными биохимическими дефектами в митохондриях [10, 11].
По данным, представленным С.М. Боруновой (2018 г.), флагманом передовых методов контроля морфофункциональных качеств спермиев является изучение их подвижности и индекса фрагментации ДНК как в головной части, так и в срединной.
Цель исследования. Проведение сравнительной оценки криоконсервированной и свеже-полученной спермы баранов-производителей по морфофункциональным показателям качества семени (подвижность, патологические и ано- мальные формы спермиев, аномальная акро-сома, индекс фрагментации ДНК).
Задачи исследования: провести сравнительную оценку морфологических показателей свежеполученной и криоконсервированной спермы баранов-производителей романовской породы по идентификации аномальных сперматозоидов; установить индекс фрагментации ДНК и митохондриальной дисфункции сперматозоидов в свежеполученной и криоконсервирован-ной сперме баранов-производителей романовской породы.
Материалы и методы. Научные работы исполняли в осенний период 2020 г. на базе кафедры диагностики болезней, терапии, акушерства и репродукции животных МГАВМиБ им. К.И. Скрябина и в лаборатории отдела по контролю качества и стандартизации генетического материала и препаратов, применяемых при воспроизводстве животных ФГБУ «ВГНКИ», по ГОСТ 32277-2013 «Средства воспроизводства. Сперма. Методы испытаний физических свойств и биологического, биохимического, морфологического анализов». Материалом для исследований послужили пробы свежеполученной и крио-консервированной спермы, полученной от баранов-производителей романовской породы. Всего было исследовано 20 спермопроб от 10 баранов-производителей в трехкратной повторности на определение морфофункциональных показателей спермопродукции. Для изучения качественных характеристик спермы (подвижность, скорость движения, аномальные формы, интактная акросома, индекс фрагментации ДНК) использовали сперму баранов-производителей, замороженную в полипропиленовых соломинках.
Подвижность спермиев изучали визуально в световом микроскопе, увеличение х 180 раз, все образцы при микроскопии помещали на термостолик, который был подогрет до t +38 °С. Этот же образец подвергали исследованию на спер-моанализаторе Andro Vision Minitube, позволяющем фиксировать концентрацию, подвижность и скорость движения половых клеток. С помощью микроскопа рассчитывали количественное соотношение прямолинейно-поступательного движения к общему числу спермокле-ток. В исследуемых образцах мы подробно изучили параметры скорости движения спермато- зоидов благодаря расширенной спермаграмме и диаграмме:
-
1. VCL – криволинейная скорость (мик-рон/секунд). Скорость движения спермиев по фактическому пути.
-
2. VSL – прямолинейная скорость (мик-рон/секунд). Скорость перемещения спермиев в прямолинейном направлении.
-
3. VAP – средняя скорость по траектории (микрон/секунд). Скорость в расчете на среднюю длину пути.
-
4. LIN – линейность . Индекс линейности движения реального пути.
-
5. STR – прямолинейность . Индекс прямолинейности движения средней траектории пути.
-
6. BCF – частота колебаний (бие-ний/секунд). Средняя частота, с которой реальная траектория спермоклетки пересекает усредненную траекторию.
-
7. ALH – амплитуда бокового смещения головки . Отклонение головки относительно средней траектории.
-
8. WOB – колебание . Величина, описывающая колебание реальной траектории относительно усредненной, VAP/VCL.
В зависимости от направления движения все половые клетки, по рекомендациям ВОЗ, делят на 3 категории.
-
1. Прогрессивно-подвижные сперматозоиды (PR) (когда клетки осуществляют движение по прямой).
-
2. Непрогрессивно-подвижные сперматозоиды (NP) (когда клетки двигаются по кругу и имеют малый радиус перемещения).
-
3. Неподвижные сперматозоиды (IM).
Интактную акросому и аномальные формы спермиев выявляли с помощью тест-набора «Дифф-Квик». Экспресс-метод основан на минимально затраченном времени. Приготовленные мазки из разбавленной спермы фиксировали буферным раствором. После остатки раствора сливали на фильтровальную бумагу и переходили к красителю № 1 (розовый), используя дозатор на 1–2 мл и равномерно покрывая каждое предметное стекло биожидкостью. Для прокраски требуется 10 мин, далее остатки красителя сливаем на фильтровальную бумагу. На прокрашенную основу наносим краситель № 2 (синий), полностью покрывая розовую зону, даем прокраситься 10 мин и смываем, окуная в емкость с дистиллированной водой два-три раза. Спермии считали морфологически нормальными, если все структурные элементы его сохранены и соответствовали известным нормам. Расчет производили высчитывая от процента общего числа нормальных спермиев число поврежденных по различным критериям и категориям повреждений, таких как аномальные головки, склоненная головка, скрученные и сломанные хвосты, оторвавшиеся головки.
Состояние дизоксирибонуклеиновой кислоты в ядре и митохондриях изучали методом акри-дин-оранжевого теста. Микроскопирование проводили с использованием флуоресцентного микроскопа. Этот метод считают одним из современных в системе биологической экспертизы племенной продукции, так как он является одним из технологически усовершенствованных маркеров апотоза (играет особую роль в регуляции фертильности), что необходимо учитывать при искусственном и естественном осеменении сельскохозяйственных животных. В каждом препарате насчитывают от 100 до 200 сперматозоидов, сначала подсчитывали сперматозоиды с неповрежденной, далее с фрагментированной ДНК. Сперматозоиды с фрагментированной ДНК окрашиваются в оттенки красного цвета, а целые в зеленый. Подсчет ведется по формуле, указанной в МУ «Определение индекса фрагментации ДНК в замороженной сперме у животных-производителей».
Результаты исследования и их обсуждение. При оценке качества семени мы провели исследования полученного эякулята во всех образцах. Сперма, сохраняемая более 25–30 мин после взятия, по физическим показателям соответствовала требованиям и нормам ГОСТ 322002013. Сперма баранов-производителей однородная, молочно-белая с желтым оттенком, вязкая, без примеси крови, гноя и мочи.
Оценку спермы по густоте проводили на микроскопе при увеличении в 180 раз. Степень насыщения спермы спермиями – густая (Г).
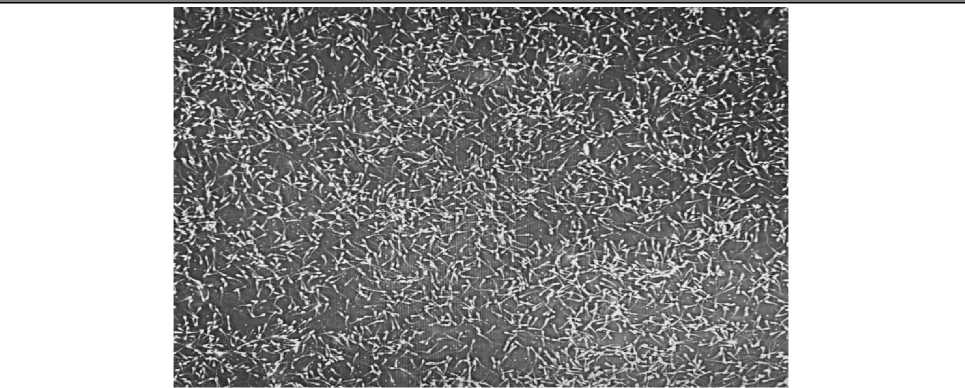
Рис.1. Оценка спермы по густоте. Область с незначительными промежутками (Ув. х 180)
При определении подвижности сперматозоидов в результате проведенных нами исследований все полученные показатели были включены в следующие категории:
^ PR (прогрессивно-подвижные (нормоки-незис) – быстрая прямолинейно-поступательная подвижность, медленная прямолинейнопоступательная подвижность);
^ NP (непрогрессивно-подвижные (гипоки-незис) – круговая подвижность, локальная подвижность);
^ IM (неподвижные (акинезис) - мертвые).
Таблица 1
Показатели подвижности свежеполученной и криоконсервированной спермы, %
|
Общее кол-во проанализ, спермы |
1 802,00 |
|
|
Количество полей |
2.00 |
|
|
Концентрация |
[107мл] |
352,31 |
|
Общая подвижность |
(%) |
98,06 |
|
Поступательная подвижность |
с%> |
92,73 |
|
■ Быстрая поступ. подв-ть |
W |
63,65 |
|
Медл. поступ. подв-ть |
W |
27,86 |
|
■ Круговая подвижность |
(%) |
1,22 |
|
Локальная подвижность |
(%) |
5,33 |
|
■ неподвижный |
(%) |
1,94 |
|
Общ. кол-во сперм/доза |
[13Т |
528,46 |
|
Критерий |
Свежеполученная сперма |
Криоконсервированная сперма |
|
PR |
92,4 – соотв. норме |
13,2 – не соотв. норме |
|
PR+NP |
97,1 – соотв норме |
58,89 – соотв. норме |
|
VCL (pm,'сек) |
VSL (ртАсек) |
VAP (рт/сек) |
DCL [рт] |
DSL ftim] |
DAP (pm] |
ALH [pm] |
BCF (Hz) |
НАС (рад) |
WOB (VAP/VCL) |
LIN (VSL/VCL |
STR (VSL/VAP) |
|
|
Сред.зн.переж, |
172,71 |
68,99 |
89,24 |
37,02 |
13,12 |
18,08 |
1,76 |
12,03 |
0,43 |
0,52 |
0,40 |
0,77 |
Рис. 2. Анализ свежеполученного эякулята
|
VCL (рт/сек) |
VSL (рт/сек) |
VAP (р т/сек) |
DCL [Щп] |
DSL [Мт] |
DAP &ип] |
ALH [рт] |
BCF (Hz) |
НАС (рад) |
WOB LIN (VAP/VCL) (VSUVCL |
STR (VSUVAP) |
|
|
Сред.зн.переж, |
55,30 |
36,75 |
39.93 |
7,39 |
2,76 |
3,56 |
0,40 |
0,90 |
0,17 |
0,72 0,66 |
0,92 |
Рис. 3. Анализ криоконсервированной спермы

|
Общее кол-во проанализ. спермы |
6 528.00 |
|
|
Количество полей |
3,00 |
|
|
Концентрация |
[107мл] |
425,43 |
|
Общая подвижность |
W |
54,78 |
|
Поступательная подвижность |
W |
15,46 |
|
■ Быстрая лоступ. подв-ть |
W |
10,22 |
|
Медл. лоступ. подв-ть |
(%) |
5,13 |
|
■ Круговая подвижность |
(%) |
0,11 |
|
Локальная подвижность |
(%) |
39,32 |
|
■ неподвижный |
(%) |
45,22 |
|
Общ. кол-во слерм/доза |
[«п |
425,43 |
По показателям подвижности были проведены исследования 20 спермопроб от 10 баранов-производителей. Показатель ППД в криоконсер-вированной сперме варьировал от 10,27 до 15,46 %, что не соответствует нормам ГОСТ 32200-2013 (не менее 40 %), показатель ло- кальной подвижности варьировал от 39,32 до 55,00 %. Показатель ППД в свежеполученной сперме варьировал от 88,12 до 96,23 %, что соответствует нормам ГОСТ 32200-2013 (не менее 80 %), показатель локальной подвижности варьировал от 1,89 до 6,9 %.
Таблица 2
Морфологические показатели свежеполученной и криоконсервированной спермы, %
|
Показатель |
Свежеполученная сперма |
Криоконсервированная сперма |
|
Поврежденная акросома |
5,9 (норма не более 10 %) |
11,21 (норма не более 40 %) – соотв. норме |
|
Аномальные формы |
6,5 (норма не более 18 %) |
16,36 (норма не более 20 %) – соотв норме |
Были выявлены 5 спермопроб в свежеполу-ченном эякуляте с поврежденной акросомой более 10 %, которые не соответствовали нормам ГОСТ 32200-2013, – от 3 до 10 %. Средние показатели всех спермпороб: оторвавшиеся головки – 3,4 %; аномальные головки – 4,25; согнутые хвосты – 4,66; закрученные – 4,1 %. Были выявлены 7 спермопроб в замороженном эякуляте с аномальной морфологией более 20 %, которые не соответствовали нормам ГОСТ 32200-2013, – не более 20 %. Показатель интакной акросомы соответствовал нормам и составлял от 3,3 до 25 %, при норме не более 40 %.
Таким образом, морфологические нарушения спермиев выражают изменения в двигательной активности спермоклеток, снижают фертильную способность и их функциональную полноценность в процессе оплодотворения.
Состояние ДНК в сперматозоидах изучали методом SCSA. Измеряли процент сперматозоидов с высокой чувствительностью к pH-индуци-рованной денатурации, который обозначается как индекс фрагментации ДНК – DFI (этот параметр отражает уровень разрывов в ДНК).
Показатель индекса фрагментации ДНК (DFI) свежеполученной и криоконсервированной спермы, %
Таблица 3
|
Показатель |
Свежеполученная сперма |
Криоконсервированная сперма |
|
DFI |
7 |
29 |
Средний показатель количества сперматозоидов с фрагментацией ДНК составил в свеже-полученном эякуляте DFI < 7 %, в замороженооттаянном DFI 29 %. Оба показателя находятся в пределах нормы (не более 30 % с фрагменти- рованной ДНК). В нескольких свежеполученных и криоконсервированных спермопробах нами была выявлена фрагментация ядерной и митохондриальной ДНК более 30 % – DFIi 30 %.
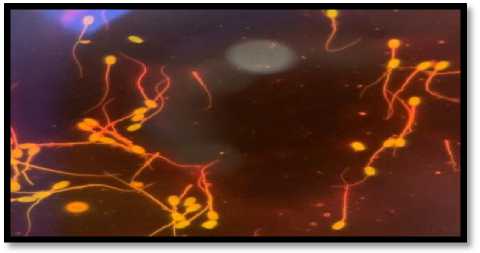
Рис. 4. Большое количество спермиев, окрашенных в оранжевый цвет, свечение в хвостовой части, т.е. митохондриальная дисфункция. Ув. × 40
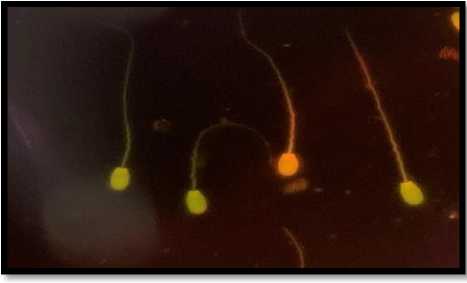
Рис. 5. Фрагментированная ядерная ДНК и митохондриальная ДНК сперматозоида. Ув. × 100
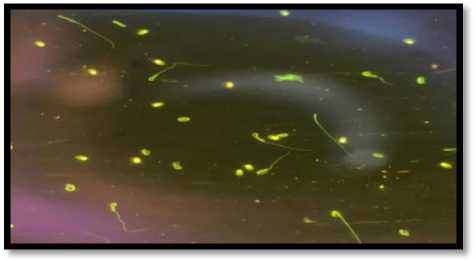
Рис. 6. Большое количество сперматозоидов с аномальной морфологией, несколько головок с незрелым ядром, имеющим аномальную структуру хроматина (HDS).
Заключение. Интерпретируя полученные результаты, можно сделать выводы по сравнительной оценке свежеполученной и криоконсер-вированной спермы. Установлено, что по показателю подвижности сперматозоидов имело место отклонение от нормы только в криокон-сервированной сперме, ППД = 13,204±0,1 %. При оценке морфологических показателей наибольшее количество поврежденных сперматозоидов было обнаружено в 7 криоконсервиро-ванных спермопробах с общей аномалий спер-миев, их среднее значение составляло 25,3 %, что не соответствует нормам ГОСТа. Также было выявлено в криоконсервированной сперме: оторвавшиеся головки – 15,85 %; дефектные головки – 10,2; согнутые хвосты – 6,97; закрученные – 5,55 %. Интактная акросома в крио-консервирванной сперме во всех спермопробах в пределах нормативных данных – ГОСТ не менее 90 %, но в свежеполученном эякуляте было выявлено в 5 спермопробах более 10 % сперматозоидов с поврежденной акросомой более 40 % – ГОСТ не менее 60 %. По показателю индекса фрагментации ДНК выявлено в свежепо-лученной сперме – 3 спермопробы и в криокон-сервированной – 9 спермопроб с фрагментированной ядерной и митохондриальной ДНК сперматозоидов – более 30 % – DFIi 30 % [6]. Определение морфофункциональных параметров спермы баранов-производителей позволяет наиболее полно и расширенно интерпретировать полученные данные спермограммы сельскохозяйственных производителей, установить связь морфофункциональных характеристик и репродуктивных параметров, а также установить критерии, влияющие на оплодотворяющую способность спермы в целом.
Новые методики исследования морфологических показателей позволяют более детально и точно определить биологическую полноценность спермопродукции. Полученные результаты исследований в дальнейшем могут быть стандартизированы, а показатель – индекс фрагментации ДНК включен в ГОСТ 32200-2013 (Средства воспроизводства. Сперма баранов. Технические условия).
Список литературы Сравнительный анализ показателей криоконсервированной и свежеполученной спермы баранов-производителей романовской породы
- Постановление главы администрации Крас-нодарского края о мерах по выводу отрасли овцеводства из кризисного состояния и на-ращиванию поголовью на период 2000–2005 годов. Краснодар, 2002. № 351.
- Абонеев В.В., Гнездилова Л.А., Ранюк В.Т. и др. Воспроизводительная способность ов-цематок и сохранность молодняка различно-го происхождения. 2019; (1): С. 120–125.
- Кидун К.А., Угольник Т.С. Митохондриаль-ная дисфункция сперматозоидов в патоге-незе патоспермий при окислительном стрес-се (обзор литературы) // Проблемы здоро-вья и экологии. 2013. № 2 (36). С. 20–24.
- Иолчиев Б.С., Багиров В.А., Кленовиц-кий П.М. Индекс фрагментации ДНК хрома-тина в сперматозоидах при оценке качества семени у быков-производителей // Сельско-хозяйственная биология. 2012. Т. 47. № 4. С. 31–35.
- Засемчук И.В., Кириченко И.С. Воспроизво-дительные качества баранов породы со-ветский меринос // Вестник Донского госу-дарственного аграрного университета. 2019. № 33. Ч. 1. С. 5–6.
- Evenson D.P. The sperm chromatin structure assay (SCSA) and other sperm DNA fragmen-tation tests for evaluation of sperm nuclear DNA integrity as related to fertility. Anim. Reprod. Sci. 2016; 169: P. 56–75.
- Ushakova I.V., Volodyaeva T.O., Volodin M.A., Pyataeva S.V., Vysokikh M.U., Abubaki-rov A.N.. Prospect for using the evaluation test mitochondrial membrane potential spermatozo-ids in art programs. Materials of the ХХVI inter-national conference Russian association Hu-man reproduction. 2016; 136.
- A strategy to exploit surrogate sire technology in livestock breeding programs / P. Gottardo, G. Gorjanc, M. Battagin et al. // G3: Genes, ge-nomes, genetics. 2019. Vol. 9. No. 1. P. 203–215. DOI: 10.1534/g3.118.200890.
- Mohammadzadeh S., Hoseini S.A., Kadivar A. Сравнительное изучение семени баранов романовской породы и породы Lori Bakhtiari // Сельскохозяйственная биология. 2018. № 2. С. 318–325.
- Борунова С.М., Иолчиев Б.С., Абрамов П.Н. Эффективный метод определения целост-ности акросомы сперматозоида у быков-производителей // Ветеринария, зоотехния и биотехнология. 2017. № 4. С. 29–34.
- Храпко К. Митохондрии, митохондриальная ДНК и соматические митохондриальные мутации: имеют ли они отношение к старе-нию. 2007. С. 54–60.


