Сравнительный анализ повторного ретроградного моно- и бистентирования при злокачественной стриктуре терминального отдела холедоха и дисфункции непокрытого саморасширяющегося металлического стента
Автор: Шабунин А.В., Багателия З.А., Лебедев С.С., Коржева И.Ю., Тавобилов М.М., Карпов A.А., Афанасьева В.А., Ибрагимли З.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Онкология
Статья в выпуске: 3 (77), 2021 года.
Бесплатный доступ
Введение. В настоящее время достаточно хорошо изучен вопрос выбора типа билиарного стента при обструкциях терминального отдела холедоха злокачественного генеза, однако вопрос выбора стента при дисфункциях ранее установленных стентов практически не исследован. При этом непокрытые саморасширяющиеся стенты функционируют в среднем от 4 до 12 месяцев, что обусловливает актуальность изучения данной проблемы.Цель исследования. Целью исследования было сравнение моно- и параллельного бистентирования пластиковыми стентами при дисфункции непокрытого саморасширяющегося стента, установленного с целью декомпрессии при обструкции терминального отдела холедоха злокачественного генеза.Материалы и методы исследования. В основную группу вошли 30 пациентов, которым при рестентировании были установлены 2 параллельных стента по типу «стент-в-стент», группу контроля составили 52 пациента с установленным при рестентировании 1 пластиковым стентом по типу «стент-в-стент».Результаты лечения. Статистически значимым оказалось преимущество основной группы в сравнении с группой контроля по скорости снижения послеоперационных показателей лейкоцитоза, прямого билирубина и диаметра холедоха. Статистически значимого преимущества группы контроля по сравнению с основной группой ни по одному из исследованных показателей выявлено не было.Заключение. По результатам нашего исследования можно сделать предварительные выводы о преимуществе применения метода параллельного бистентирования пластиковыми стентами по сравнению с моностентированием в лечении механической желтухи при дисфункции ранее установленного непокрытого саморасширяющегося металлического стента, что, однако, требует дальнейшего изучения для подтверждения полученных ранее результатов.
Пластиковый билиарный стент, бистентирование, механическая желтуха, эндоскопическая ретроградная холангиопанкреатография, дисфункция
Короткий адрес: https://sciup.org/142231472
IDR: 142231472 | УДК: 006.617-089 | DOI: 10.17238/2072-3180-2021-3-22-28
Comparative analysis of repeated retrograde mono - and bistentation in malignant stricture of the terminal choledochus and dysfunction of an uncovered self-expanding metal stent
Background. At present, the issue of choosing the type of biliary stent in obstructions of the terminal part of the common bile duct of malignant origin has been studied quite well, however, the issue of choosing a stent in case of dysfunctions of previously installed stents has practically not been studied.Study purpose. The aim of the study was to compare mono- and parallel bistenting with plastic stents in case of dysfunction of an uncoated self-expanding stent placed for the purpose of decompression in case of obstruction of the terminal part of the common bile duct of malignant origin.Study material and methods. The main group included 30 patients who received 2 parallel stent-to-stent stents during restentation, the control group consisted of 52 patients with 1 stent-to-stent plastic stent installed during restentation.Outcomes: The advantage of the main group in comparison with the control group was statistically significant in terms of the rate of decrease in postoperative leukocytosis, direct bilirubin and common bile duct diameter. No statistically significant advantage of the control group in comparison with the main group was found for any of the studied parameters.Conclusions. Preliminary conclusions can be drawn about the advantage of using the parallel bistening method with plastic stents compared to monostenting in the treatment of obstructive jaundice with dysfunction of a previously installed uncoated self-expanding metal stent.
Текст научной статьи Сравнительный анализ повторного ретроградного моно- и бистентирования при злокачественной стриктуре терминального отдела холедоха и дисфункции непокрытого саморасширяющегося металлического стента
Эндоскопическое ретроградное стентирование холедоха является на сегодняшний день основным методом билиарной декомпрессии при обтурации терминального отдела холедоха (ТОХ) как доброкачественного, так и злокачественного генеза, при котором значение достижения адекватного и как можно более длительного дренажа билиарного тракта обретает еще большие масштабы вследствие разрешения механической желтухи и холангита как обязательного условия для проведения химиотерапии, способствующей увеличению продолжительности жизни у неоперабельных пациентов, а порой и переходу их в группу возможного хирургического лечения [1, 2]. Как правило, обеспечение оттока желчи у данной группы больных сопряжено с эндоскопической установкой того или иного стента, а также с регулярными эндоскопическими санациями и рестентированиями при его закупорке и дисфункции, что обусловливает актуальность поиска оптимального выбора типа стента [1]. Выбор в настоящее время осуществляется среди металлических саморасширяющихся стентов (СРМС) – полностью покрытых (ПП-СРМС), частично покрытых (ЧП-СРМС) либо непокрытых (НП-СРСМС) – и пластиковых стентов, каждый из которых имеет свой ряд преимуществ и недостатков [3]. Если при первичных эндобилиарных вмешательствах при неоперабельных злокачественных стриктурах выбор склоняется в сторону саморасширяющихся металлических стентов, то при повторных вмешательствах при закупорке и дисфункции установленного ранее стента вопрос повторного выбора остается открытым касательно как типа, так и количества стентов [3], в том числе и при дисфункции НП-СРМС, исследованной нами в данной работе. При этом скорость возникновения дисфункции первично установленных НП-СРМС по некоторым данным достигает сроков от 4 до 12 месяцев, что обуславливает актуальность изучения данного вопроса [2]. Нашей задачей в данной работе было сравнение моно- и двойного параллельного стентирования пластиковыми стентами у пациентов с механической желтухой, вызванной обтурацией ТОХ злокачественной этиологии с дисфункцией ранее установленного НП-СРМС.
Материалы и методы
Характеристика групп пациентов
Были изучены две группы пациентов с механической желтухой злокачественного генеза, которым за период с января 2018 г. по декабрь 2019 г. на базе ГКБ им. С.П. Боткина были выполнены повторные эндобилиарные вмешательства в связи с дисфункцией установленного ранее НП-СРМС. Критериями включения приняты: 1) установка стента по показаниям при механической желтухе злокачественной этиологии, 2) стентирование холедоха на уровне терминального отдела без дополнительного стентирования проксимальных отделов желчных протоков или главного панкреатического протока, 3) наличие проведенных ранее ретроградных билиарных стентирований. Критериями исключения явились: 1) наличие первично-множественных злокачественных новообразований, 2) наличие ранее и установка в момент исследования стентов в любые отделы желчевыводящей системы, помимо терминального отдела холедоха, а также в двенадцатиперстную кишку и панкреатический проток, 3) отсутствие ранее установленного стента/стентов в ТОХ, 4) наличие ранее / одномоментно перенесенного антеградного чрескожного чреспеченочного дренирования желчных протоков, 5) наличие в анамнезе хирургических вмешательств на органах гепатобилиарной системы, 6) наличие одномоментного назобилиарного дренирования, 7) наличие сопутствующих заболеваний в стадии суб- и декомпенсации, 8) выполнение стентирования у пациентов с операбельными новообразованиями и запланированным последующим хирургическим лечением.
Диагностическими признаками дисфункции стента были желтушность кожных покровов и склер, гипербилирубинемия, преимущественно за счет прямой фракции, билиарная гипертензия, а также в ряде случаев лейкоцитоз, лихорадочный синдром и/или болевой синдром в верхних отделах живота.
В основную группу вошли 30 пациентов, которым при рестентировании были установлены 2 параллельных стента. Из них 6 пациентов были мужчинами, а 24 пациента – женщинами. Средний возраст составил 70,5 (от 55 до 81 года). Причинами первоначального стентирования были: злокачественное образование головки поджелудочной железы (ПЖ) (26 пациентов) и аденокарцинома большого дуоденального сосочка (БДС) (4 пациента). Причинами дисфункции первичного стента – первичное прорастание ранее установленного НП-СРМС опухолью (21 пациентов) или билиарный сладж НП-СРМС (9 пациентов).
Группу контроля составили 52 пациента с установленным при рестентировании 1 пластиковым стентом в ТОХ. Средний возраст был 69,2 лет (от 44 до 89 лет), количество мужчин – 18, женщин – 34. Причины первоначального стентирования: злокачественное образование головки ПЖ (40 пациентов), аденокарцинома БДС (5 пациентов), воротная холангиокар-цинома (4 пациента) и хронический лимфоцитарный лейкоз с поражением лимфоузлов гепатодуоденальной связки (ГДС)
(3 пациента). Причины дисфункции первичного стента: прорастание ранее установленного НП-СРМС опухолевой тканью (38 пациентов) и билиарный сладж НП-СРМС (14 пациентов).
Cравнительная характеристика основной и контрольной групп представлена в таблице 1. Характеристика групп по однородности исходных лабораторных и инструментальных параметров представлена в таблице 2.
Таблица 1
Сравнительная характеристика основной и контрольной групп
Table 1
Comparative characteristics of the main and control groups
|
Признак Sign |
Основная группа, Main group, n=30 |
Группа контроля, Control group, n=52 |
р |
|
Пол: муж/жен Gender: male / female |
6/24 |
18/34 |
0,16 |
|
Средний возраст, лет Average age, years |
70,5 (от 55 до 81 года, from 55 to 81 years old) |
69,2 (от 44 до 89 лет, from 44 to 89 years old) |
0,26 |
|
Причина первоначального стентирования: Reason for initial stenting: |
0,21 |
||
|
1) злокачественное образование головки ПЖ, malignant formation of the head of the pancreas |
26 |
40 |
|
|
2) аденокарцинома БДС, adenocarcinoma of the papilla |
4 |
5 |
|
|
3) воротная холангиокарцинома, portal cholangiocarcinoma |
0 |
4 |
|
|
4) лейкоз с поражением лимфоузлов ГДС, leukemia with damage to the lymph nodes of the hepatoduodenal ligament |
0 |
3 |
|
|
Причина дисфункции стента: Cause of stent dysfunction: |
0,77 |
||
|
1) прорастание НП-СРМС, germination of an uncoated stent |
21 |
38 |
|
|
2) билиарный сладж НП-СРМС, biliary sludge of uncoated stent |
9 |
14 |
|
Таблица 2
Статистический анализ
Характеристика групп по исходным лабораторным и инструментальным параметрам
Table 2
Characteristics of groups by initial laboratory and instrumental parameters
|
Признак, средняя величина в группе, Sign, average value in the group |
Основная группа, Main group, n=30 |
Группа контроля, Control group, n=52 |
р |
|
лейкоцитоз, *10^9/л, leukocytosis, *10^9/l |
7,9 (±4,9) |
10,3 (±6,4) |
0,07 |
|
прямой билирубин, мкмоль/л, direct bilirubin, μmol / l |
78,8 (±73,4) |
57,36 (±50,9) |
0,32 |
|
альфа-амилаза, Ед/л, alpha-amylase, U / L |
62,2 (±56,9) |
58,02 (±106,8) |
0,1 |
|
диаметр холедоха, мм, diameter of the common bile duct, mm |
16,37 (±5,9) |
13,00 (±5,6) |
0,06 |
Характеристика алгоритма лечения
Эндоскопическое вмешательство включало удаление установленного ранее стента, ретроградную холангиографию (РХГ) с применением контрастного йодсодержащего препарата, ревизию и санацию холедоха и повторное стентирование двумя стентами (длина первого стента от 5 до 9 см, размер 8,5 Fr, длина второго стента от 5 до 9 см, размер 10 Fr) либо одним (длина 7 см, размер 10 Fr) типа Амстердам.
Все вмешательства осуществлялись под общей внутривенной анестезией двумя эндоскопистами с количеством выполняемых РХПГ не менее 200 в год и стажем работы более 10 лет. Лекарственная терапия в послеоперационном периоде включала инфузионно-спазмолитическую, противоязвенную и системную антибактериальную терапию защищенным ингибиторами бета-лактамаз цефалоспорином III поколения длительностью 7 суток, а также антисекреторную терапию синтетическими аналогами соматостатина при гиперами-лаземии. Контроль инструментальных (УЗИ органов гепатобилиарной системы) и лабораторных (общего и прямого билирубинов, альфа-амилазы, общего анализа крови) показателей стандартно проводился перед вмешательством и на первые сутки после вмешательства, а также дополнительно при выявлении отрицательной динамики показателей либо выявлении осложнений. Наблюдение за пациентами осуществлялось до момента следующего эпизода рестентирования либо удаления стента.
Для проведения статистического анализа использовались U-критерий Манна-Уитни и Хи-квадрат Пирсона со статистически значимым значением Р<0,05. Оценка результатов проводилась по показателям отношения значений лабораторных (прямой билирубин, альфа-амилаза и лейкоцитоз) и инструментальных (диаметр холедоха) показателей на второй день после операции к значениям показателей до вмешательства, а также по количеству дней до выписки из стационара, количеству осложнений, выявленных в каждой группе и продолжительности бессимптомного периода до следующего эндобилиарного вмешательства.
Результаты
Частота технического успеха в обеих группах составила 100%. Среднее количество дней до выписки в основной группе 5,64 (от 1 до 15 дней), в группе контроля – 7,19 (от 1 до 28 дней), при сравнении групп статистической разницы выявлено не было (р=0,516). Аналогичные результаты получились и при сравнении количества дней до следующего вмешательства – без статистически значимой разницы между группами (р=0,451) при среднем количестве дней 55,53 (от 3 до 183) в основной группе и среднем количестве дней 43,67 (от 3 до 119) в группе контроля. Также статистически значимой разницы не было получено при сравнении результатов отношения показателей альфа-амилазы на первые сутки после вмешательства к показателям до вмешательства (р=0,07, среднее отношение в основной группе 0,97, в группе контроля 0,86) и сравнении количества осложнений (р=0,41 при применении критерия Хи-квадрата Пирсона).
Всего в основной группе было выявлено 2 осложнения, в обоих случаях – дисфункция стента в пределах одной госпитализации вследствие билиарного сладжа, которая была разрешена путем повторного эндобилиарного вмешательства с санацией билиарного дерева и заменой стентов с последующей положительной динамикой и выпиской на 3 и 5 сутки после операции. Также в основной группе был 1 летальный исход вследствие прогрессирования онкопатологии без признаков дисфункции стента, холангита и нарастания билиарной гипертензии.
В группе контроля выявлено всего 12 осложнений, из которых 10 случаев дисфункций стента (9 вследствие билиарного сладжа и 1 вследствие дислокации стента), успешно разрешенных при повторном вмешательстве с санацией желчных путей и заменой стента, 1 случай гемобилии, купированной консервативной гемостатической терапией, а также 1 случай возникновения холангиогенного абсцесса с последующим дренированием его под УЗ наведением и успешным ведением с положительной динамикой и выпиской пациента на 8-е сутки после дренирования (рис. 1). Из 10 случаев дисфункции стента в
4 при повторных эндобилиарных вмешательствах был выявлен гнойный холангит, не повлиявший, однако, на положительные исходы лечения.
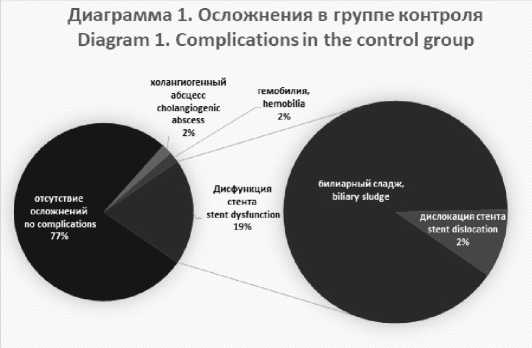
Дисфункция
Диаграмма 1. Осложнения в группе контроля Diagram 1, Complications in the control group холангиогенный абсцесс cholangiogenic abscess гемобил ия, hemobilia отсутствие осложнений no complications билиарный сладж, biliary sludge
Рис. 1. Диаграмма осложнений в группе контроля
Fig. 1. Diagram of complications in the control group
Статистически значимым оказалось преимущество основной группы по данным отношения послеоперационных показателей (Х2) лейкоцитоза, прямого билирубина и диаметра холедоха к дооперационным (Х1): среднее отношение лейкоцитоза в основной группе составило 0,21, в группе контроля – 0,97 (р=0,02), среднее отношение прямого билирубина – 0,75 в основной группе и 0,83 в группе контроля (р=0,03) и среднее отношение диаметра холедоха – в основной группе 0,69 и в группе контроля 0,83 (р=0,04) (рис. 2).
Диаграмма 2. Отношение послеоперационных показателей к дооперационным в основной группе и группе контроля, Х2/Х1
Diagram 2 The ratio of postoperative to preoperative indicators in the main group and the control group, X2/X1
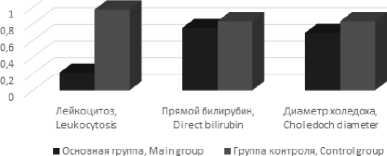
Рис. 2. Диаграмма отношений послеоперационных показателей к дооперационным в основной группе и группе контроля
Fig. 2. Diagram of the ratio of postoperative to preoperative indicators in the main group and the control group
Статистически значимого преимущества группы контроля по сравнению с основной группой ни по одному из исследованных показателей выявлено не было.
Обсуждение
Проблема паллиативного лечения механической желтухи у пациентов с нерезектабельными злокачественными заболеваниями органов гепатобиларной системы на сегодняшний день остается крайне актуальной вследствие неоднократных эпизодов дисфункций стентов у данной группы больных и рецидива механической желтухи, чреватой такими опасными для жизни пациента осложнениями, как холангит и холанги-огенный сепсис [1]. В то же время, если применению разных типов стентов при первичных эндобилиарных вмешательствах на данный момент посвящено множество исследований, то в случае с дисфункциями стентов данных в мировой литературе крайне мало, что обусловливает важность продолжения поисков наиболее оптимальных по срокам продолжительности безрецидивного периода, количеству осложнений, скорости восстановления пациента и финансовой составляющей видов стентов [3]. Согласно рекомендациям Европейского общества гастроинтестинальной эндоскопии, основанных на результатах ряда мета-анализов, первично при злокачественной билиарной обструкции наиболее оптимальным является установка СРМС, ассоциированная с более длительной выживаемостью пациентов, меньшим риском несостоятельности стента и меньшим количеством повторных вмешательств [4, 5, 6, 7, 8], однако выбор стента при дисфункции первично установленного СРМС остается неопределенным [3]. Кроме того, некоторые публикации говорят о возможно сопоставимых по срокам состоятельности стентов результатах в случае применения множественного параллельного стентирования [9, 10]. При сравнении затрат в случае применения СРМС и пластиковых стентов литературные данные разнятся: одни авторы отмечают превышение стоимости установки СРМС в 10–18 раз в сравнении с пластиковыми стентами [9], другие указывают на сопоставимые затраты при использовании пластиковых и металлических стентов [11]. Некоторые исследования демонстрируют отсутствие различий между применением саморас-ширяющихся металлических стентов (СРМС) и пластиковых стентов (по типу «стент-в-стент» как в первом, так и во втором случае) при окклюзии ранее установленного СРМС у пациентов со злокачественной билиарной обструкцией [12], однако работ, сравнивающих моно- и двойное параллельное стентирование с установкой пластиковых стентов в ранее установленный СРМС при его дисфункции найти не удалось. Ряд авторов указывает на снижение продолжительности бессимптомного периода функционирования пластиковых стентов (до момента следующего вмешательства) с 66 дней при установке минимум двух стентов непосредственно в холедох до 40 при установке их в СРМС по типу «стент-в-стент» [1], но в нашем исследовании среднее количество дней 43,67 наблюдалось только при установке одного стента, сохраняясь при параллельном множественном стентировании на уровне среднего количества дней 55,53. Тем не менее, статистически значимой разницы по количеству дней ни до следующего стентирования, ни до выписки пациентов выявлено нами не было. Также статистически значимой разницы не было получено при сравнении количества осложнений и результатов отношения показателей альфа-амилазы на первые сутки после вмешательства к показателям до вмешательства. Однако статистически значимое преимущество двойного параллельного стентирования по показателям снижения в послеоперационном периоде лейкоцитоза, прямого билирубина и диаметра холедоха в совокупности с отсутствием значимого преимущества контрольной группы с моностентированием позволяет сделать предварительный вывод о лучших результатах применения двойного параллельного стентирования в сравнении с моностентированием пластиковым стентом у пациентов с дисфункцией ранее установленного НП-СРМС, что, однако, требует дальнейшего изучения проблемы в силу таких ограничений нашего исследования как относительно небольшая выборка пациентов и ретроспективный характер исследования.
Выводы
Первоначальные данные как мировой литературы, так и нашего исследования позволяют делать предварительные выводы о преимуществе применения метода множественного (от 2 и более стентов) параллельного стентирования пластиковыми стентами по сравнению с моностентированием пластиковым стентом в лечении механической желтухи при дисфункции ранее установленного непокрытого саморасширяющегося металлического стента, что, однако, требует дальнейшего изучения для подтверждения полученных ранее результатов.
Список литературы Сравнительный анализ повторного ретроградного моно- и бистентирования при злокачественной стриктуре терминального отдела холедоха и дисфункции непокрытого саморасширяющегося металлического стента
- Iwasaki A., Kubota K., Kurita Y. et al. The placement of multiple plastic stents still has important roles in candidates for chemotherapy for unresectable perihilar cholangiocarcinoma. J Hepatobiliary Pancreat Sci., 2020, Oct; № 27(10), рр. 700–711. https://doi.org/10.1002/jhbp.804
- Radwana M., Emarab M., Zaghloulb M. et al. Double plastic stenting for inoperable malignant biliary stricture among cirrhotic patients as a possible cost-effective treatment: a pilot study. European Journal of Gastroenterology & Hepatology, 2019, № 31, рр. 1057–1063. https://doi.org/10.1097/MEG.000000000000142
- Dumonceau J., Tringali A., Papanikolaou I. et al. Endoscopic biliary stenting: indications, choice of stents and results: European Society of Gastrointestinal Endoscopy (ESGE) clinical Guideline – Updated October 2017. Endoscopy, 2018, № 50, рр. 910–930. https://doi.org/10.1055/a-0659-9864
- Moole H., Jaeger A., Cashman M. et al. Are self-expandable metal stents superior to plastic stents in palliating malignant distal biliary strictures? A meta-analysis and systematic review. Medical Journal Armed Forces India, 2017, № 73(1), рр. 42–48. http://dx.doi.org/10.1016/j.mjafi.2016.08.014
- Pu L., Hourneaux de Moura E., Bernardo W. et al. Endoscopic stenting for inoperable malignant biliary obstruction: A systematic review and meta-analysis. World J Gastroenterol, 2015, December 21, № 21(47), рр. 13374–13385. https://doi.org/10.3748/wjg.v21.i47.13374
- Hong W., Chen X., Wu W. et al. Metal versus plastic stents for malignant biliary obstruction: An update meta-analysis. Clinics and Research in Hepatology and Gastroenterology, 2013, № 37(5), рр. 496–500. https://doi.org/10.1016/j.clinre.2012.12.002
- Almadi M., Barkun., Martel M. Plastic vs. Self-Expandable Metal Stents for Palliation in Malignant Biliary Obstruction: A Series of Meta-Analyses. American Journal of Gastroenterology, 2017, № 112(2), рр. 260–273. https://doi.org/10.1038/ajg.2016.512
- Sawas T., Al Halabi Sh., Parsi M. et al. Self-expandable metal stents versus plastic stents for malignant biliary obstruction: a meta-analysis. Gastrointestinal Endoscopy, 2015, № 82(2), рр. 256–267. https://doi.org/10.1016/j.gie.2015.03.1980
- Lawrence C. and Romagnuolo J. Double Plastic Stents for Distal Malignant Biliary Obstruction: Preliminary Evidence for a Novel Cost-Effective Alternative to Metal Stenting. The American Journal of Gastroenterology, 2014, № 109, рр. 295–297. https://doi.org/10.1038/ajg.2013.409
- Cabral J., Taglieri E., Pelosof A. et al. Comparative Study between Plastic and Metallic Stents for Biliary Decompression in Patients with Distal Biliary Obstruction. Gastroenterology Research and Practice, 2017, Volume 2017. https://doi.org/10.1155/2017/7621821
- Walter D., van Boeckel P., Groenen M. et al. Cost Efficacy of Metal Stents for Palliation of Extrahepatic Bile Duct Obstruction in a Randomized Controlled Trial. Gastroenterology, 2015, № 149(1), рр. 130–138. https://doi.org/10.1053/j.gastro.2015.03.012
- Shah T., Desai S., Haque M. et al. Management of occluded metal stents in malignant biliary obstruction: similar outcomes with second metal stents compared to plastic stents. Dig Dis Sci., 2012, № 57(11), рр. 2765–2773. https://doi.org/10.1007/s10620-012-2272-7


