Сравнительный анализ реконструкции поясничного отдела позвоночника с применением имплантатов из аддитивно-производимых метаматериалов на основе ячеек периодичности с различной топологией
Автор: Шошева О.П., Жмайло М.А., Маслов Л.Б., Иванов С.Д., Боровков А.И., Заборовский Н.С., Пташников Д.А.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 1 т.30, 2026 года.
Бесплатный доступ
Несмотря на существенный прогресс в области нейрохирургии, стабильная реконструкция позвоночника после тотальной спондилэктомии единым блоком по-прежнему является сложной задачей. Зачастую для этого проводится замена тела позвонка имплантатом и транспедикулярная фиксация. Однако применяемые стандартные имплантаты не всегда способны обеспечить необходимую поддержку и естественное распределение нагрузки, что увеличивает вероятность возникновения нестабильности и проседания имплантата. Этим обусловлена актуальность создания персонализированных имплантатов с применением аддитивных технологий. В настоящем исследовании было рассмотрено пять имплантатов: один из полимера и четыре из метаматериалов, близких по свойствам к кортикальной костной ткани позвонков. Среди них было два решетчатых (Body-centered Cube и Diamond) и два ТПМП-метаматериала (Fischer-Koch и Gyroid). Для каждого имплантата был выполнен расчет напряженно-деформированного состояния реконструированного позвоночника при шести основных его движениях: наклонах вперед, назад, вправо и влево и поворотах вправо и влево. Полученные результаты привели к выводу, что с точки зрения прочности рассмотренные имплантаты из метаматериалов оказывают почти идентичное влияние на биомеханику поясничного отдела позвоночника. А также, несмотря на то что их использование вызывает более высокий уровень напряжений в системе, оно предпочтительнее из-за способности метаматериалов стимулировать прорастание в имплантат костной ткани.
Замена тела позвонка, транспедикулярная фиксация, индивидуальный имплантат, решетчатые метаматериалы, ТПМП-метаматериалы, конечно-элементный анализ, напряженно-деформированное состояние
Короткий адрес: https://sciup.org/146283276
IDR: 146283276 | УДК: 531/534: [57+61] | DOI: 10.15593/RZhBiomeh/2026.1.05
Comparative analysis of lumbar spine reconstruction using implants made of additively manufactured metamaterials based on unit cells with different topologies
Despite great progress made in neurosurgery, stable spinal reconstruction after total en bloc spondylectomy remains a challenge. While the common tactic is to replace the vertebral body with an implant and perform transpedicular fixation, the standard implants do not always provide the necessary support and natural load distribution, increasing the risks of instability and subsidence of the implant. It is therefore of utmost importance to construct customized implants based on additive technologies. Our study considers five implants: one made of polymer and four made of metamaterials similar in properties to cortical tissue of the vertebrae. Two of the implants were made of lattice metamaterials (Body-centered Cube and Diamond) and two of TPMS metamaterials (Fischer–Koch and Gyroid). Stress–strain analysis of the reconstructed spine was carried out for each implant for six basic movements: flexion, extension, right bending, left bending, right rotation and left rotation. Our findings led us to conclude that the metamaterial implants have an almost identical influence on the biomechanics of the lumbar spine in terms of strength. Furthermore, even though higher stresses were observed in the system in this case, metamaterials can still be recommended for use in implants as they stimulate ingrowth of bone tissue into the implant.
Текст научной статьи Сравнительный анализ реконструкции поясничного отдела позвоночника с применением имплантатов из аддитивно-производимых метаматериалов на основе ячеек периодичности с различной топологией
RUSSIAN JOURNAL OF BIOMECHANICS
В общей статистике первичных новообразований скелета на опухоли позвоночного столба приходится менее 5 % случаев [1]. В то же время осевой скелет является наиболее уязвимой зоной для метастатического поражения: в этой области локализуется порядка 39 % всех случаев вторичного новообразования костных структур [2]. Несмотря на существенное развитие методов клинической онкологии и совершенствование нейрохирургических техник, лечение пациентов с новообразованиями подобного характера остается сложной задачей, требующей дальнейшего поиска оптимальных стратегий лечения [3].
Тотальная спондилэктомия единым блоком, известная как TES (total en bloc spondylectomy), представляет собой сложную хирургическую процедуру. Она подразумевает полное удаление пораженного позвонка вкупе с окружающими его опорными мышечно-связочными структурами и прилегающими межпозвонковыми дисками. Применение данной методики доказало эффективность при лечении первичных и метастатических злокачественных новообразований позвоночного столба. Радикальная резекция позволяет значительно минимизировать риск рецидива, что способствует существенному увеличению выживаемости и повышению качества жизни пациентов в долгосрочной перспективе [4-6]. Финальным этапом TES является замещение удаленного тела позвонка имплантатом и реализация многоуровневой инструментальной фиксации для обеспечения стабильности реконструированного отдела. Данная система фиксации состоит из металлических стержней и транспедикулярных винтов. Ключевым условием успешного исхода операции является прецизионная стабилизация имплантата, необходимая для обеспечения достаточных прочностных характеристик позвоночного столба после операции, восстановления его опорной функции и создания благоприятных условий для остеоинтеграции [7]. Однако применение стандартных серийных изделий зачастую не позволяет добиться конгруэнтности контактных поверхностей «имплантат -кость», что препятствует физиологичному распределению нагрузки. Подобное несоответствие существенно увеличивает риски миграции конструкции, возникновения необратимых деформаций и проседания имплантата в тела смежных позвонков [8-11]. Проседание является одним из наиболее распространенных осложнений, возникающих после TES [12-14]. Зачастую это связано с ключевым недостатком серийных конструкций имплантатов, а именно со сложностью их адаптации к уникальной анатомии отдельного пациента. Вследствие этого переход к проектированию персонализированных конструкций на основе технологий аддитивного производства является одним из наиболее многообещающих векторов развития вертебрологии. Внедрение таких решений открывает новые возможности для улучшения результатов хирургического лечения, особенно в клинических случаях, связанных с онкологическими поражениями позвоночного столба [15]. Более того, аддитивное производство расширяет возможности проектирования, позволяя интегрировать в структуру имплантата дополнительные фиксирующие элементы, что существенно повышает общую механическую стабильность системы.
Метод конечных элементов (МКЭ) в сочетании с комплексным биомеханическим анализом напряженно-деформированного состояния (НДС) является подходом, исключительная польза которого признана в травматологии, ортопедии и, в частности, вертебрологии [16-25]. Данный вычислительный метод доказал эффективность при изучении особенностей распределения нагрузок в структурах позвоночника в условиях различных функциональных сценариев: от физиологически нормальных или патологических состояний до оценки результатов хирургического вмешательства [26-34]. Кроме того, МКЭ широко применяется для изучения биомеханических характеристик межпозвонковых дисков и прогнозирования влияния их эндопротезов на двигательную функцию позвоночного столба [35-41]. Несмотря на обширную базу исследований, число работ, посвященных анализу НДС позвоночника в условиях сочетания замены тела позвонка и транспедикулярной фиксации, остается недостаточным. В ряде исследований МКЭ применялся для осуществления сравнительной оценки влияния различных подходов к фиксации реконструированного поясничного отдела на выполнение основных движений позвоночника [42-45]. В других работах с помощью МКЭ сопоставлялись результаты замены тела позвонка различными стандартными имплантатами, включая полимерные и металлические [46-49]. Также существуют публикации, где методом МКЭ осуществлялся сравнительный анализ обычных серийных имплантатов с теми, что были созданы посредством аддитивного производства [15; 50]. Однако при тщательном изучении литературы не было обнаружено исследований, где конечно-элементный анализ использовался бы для сравнения имплантатов на основе метаматериалов с различной топологией.
Настоящая работа является продолжением исследования, направленного на анализ биомеханического состояния поясничного отдела позвоночника после реконструкции с применением транспедикулярной системы фиксации и персонализированных имплантатов в условиях действия физиологичных нагрузок [51]. Следовательно, набор имплантатов из метаматериалов, отобранных для настоящего сравнительного анализа, базируется на выводах предыдущего этапа исследований. Работа по-прежнему сфокусирована не только на поиске наиболее эффективных конструкций для улучшения результатов хирургических операций, но и на расширении теоретической базы знаний о механизмах взаимодействия имплантатов с костными структурами.
Материалы и методы
Объект исследования
В качестве объекта данного исследования выступает биомеханическая система, включающая два сегмента поясничного отдела: L 1 –L 2 и L 4 –L 5. В структуру модели входят соответствующие костные структуры, межпозвонковые диски и комплекс из семи основных связок, формирующих связочный аппарат. Объединение указанных сегментов в единую систему реализовано посредством имплантата, замещающего тело позвонка L3 , и задней фиксирующей конструкции. Последняя включает в себя два продольных стержня и систему из десяти транспедикулярных винтов (рис. 1).
Объем исследования
В предшествующей работе [51] был выполнен сравнительный анализ трех конфигураций искусственного позвонка поясничного отдела: двух полимерных конструкций с латеральным и задним типами крепления, а также металлического имплантата аддитивного производства с решетчатой структурой и латеральной фиксацией. Полученные результаты позволили установить, что с точки зрения прочностных характеристик оптимальным решением является использование полимерного изделия с задним типом крепления. Кроме того, была обнаружена проблема надежности фиксации имплантата из метаматериала, вызванная появлением локальных пластических деформаций в основании его фланцев. В связи с этим и с учетом вышесказанного было выдвинуто предположение, что задняя фиксация данного имплантата может быть решением указанной проблемы.
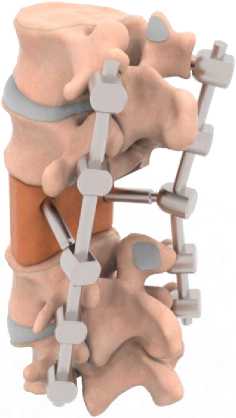
а
Рис. 1. Компоненты объекта исследования:
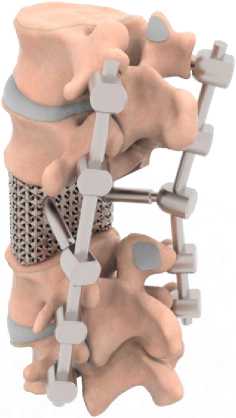
б
а – с имплантатом из полимера;
б – с имплантатом из метаматериала
В настоящем исследовании анализируются два типа имплантатов с задним типом крепления. К первому типу относится цельная полимерная конструкция, ко второму – изделия из металлических биометаматериалов, изготовленные методом аддитивного производства. Последние представлены двумя вариантами топологии: на основе регулярных решеток и на основе трижды периодических минимальных поверхностей (ТПМП). Материал для полимерного имплантата такой же, как в предыдущем исследовании – полиэфирэфиркетон ( PEEK ). Для металлических же имплантатов было отобрано по два различных метаматериала каждого вида. Внешний вид их ячеек периодичности представлен на рис. 2, а их характеристики приведены в табл. 1. Характерный размер элементарной ячейки каждого рассмотренного метаматериала составляет 5 мм.
Таким образом, в настоящей работе рассматриваются пять имплантатов, представленных на рис. 3. Канал в центре каждого имплантата предназначен для заполнения костным алло- или аутотрансплантатом. В дальнейшем для краткости обозначения определенного метаматериала будет использоваться лишь название типа его ячейки периодичности: например, имплантат из метаматериала Body-centered Cube .

в г
Рис. 2. Фрагмент метаматериала с элементарной ячейкой: а – Body-centered Cube – решетчатого типа; б – Diamond – решетчатого типа; в – Fischer-Koch – типа ТПМП; г – Gyroid – типа ТПМП
Таблица 1
Характеристики метаматериалов, рассматриваемых в исследовании
|
Параметр |
Тип ячейки периодичности |
Пористость, % |
|
Решетчатые |
Body-centered Cube |
54 |
|
метаматериалы |
Diamond |
50 |
|
ТПМП- |
Fischer-Koch |
60 |
|
метаматериалы |
Gyroid |
58 |

а

б

в


д
Рис. 3. Имплантат: а – полимерный; б – из метаматериала с элементарной ячейкой Body-centered Cube ; в – из метаматериала с элементарной ячейкой Diamond ; г – из метаматериала с элементарной ячейкой Fischer-Koch ; д – из метаматериала с элементарной ячейкой Gyroid
Выбор метаматериалов для исследования осуществлен на основе анализа зависимости эффективных физико-механических свойств метаматериалов с различными типами элементарных ячеек от значений их пористости [52; 53] . Все представленные выше метаматериалы обладают свойствами, наиболее близкими к свойствам кортикальной костной ткани поясничных позвонков. Подобные материалы представляют особый интерес, поскольку изготовленные из них имплантаты, предположительно, обеспечивают наиболее естественное распределение нагрузок в позвоночнике.
В сравнении с серийными аналогами, все представленные в работе имплантаты спроектированы с полной конгруэнтностью поверхностям замыкательных пластинок смежных позвонков. Такая геометрия призвана обеспечить более равномерное распределение механических напряжений. Еще одной конструктивной особенностью является наличие элементов дополнительной фиксации. Согласно имеющимся данным [44], даже персонализированные изделия не гарантируют точного прилегания из-за риска интраоперационного смещения или дестабилизации при высокоамплитудных движениях в постхирургическом периоде. Внедрение вспомогательных фиксирующих элементов в структуру имплантата позволяет повысить стабильность системы, ослабить воздействие на костные пластинки и минимизировать вероятность проседания изделия.
Помимо всего прочего, пористая структура метаматериалов стимулирует процессы остеоинтеграции [54–56], что ведет к формированию биокомпозита. Данный фактор значительно повышает стабильность фиксации имплантируемых изделий в долгосрочной перспективе.
Подготовка геометрических моделей
Основой для построения анатомически достоверной CAD (Computer-Aided Design) модели костных структур (рис. 4, а) послужили данные КТ-сканирования пациента с новообразованием в теле L3-позвонка (рис. 4, б). Это позволило учесть анатомические особенности костных структур, необходимые для последующего биомеханического анализа. На первом этапе в среде 3D Slicer 5.6.2 была выполнена сегментация снимков, результатом которой стала сеточная STL-модель. Последующая обработка в Autodesk Meshmixer 3.5.474 позволила нивелировать погрешности сегментирования и произвести дифференциацию костных тканей на слои с различными механическими характеристиками.
В рамках подготовки модели было проведено удаление пораженного позвонка L 3 и остистого отростка L 2, а также создание отверстий под транспедикулярные винты. Финальная детализация геометрии в Autodesk Meshmixer включала построение межпозвонковых дисков, суставных хрящей, а также хрящевых и субхондральных замыкательных пластинок. Толщина последних была задана неравномерной согласно морфометрическим данным из литературы [57; 58].
Проектирование остальных компонентов системы – стержней, винтов и самих тел имплантатов – осуществлялось методами твердотельного моделирования в программном комплексе ANSYS SpaceClaim 2019.2.
Свойства материалов
В настоящем исследовании все используемые материалы рассматриваются как гомогенные среды с изотропными эффективными характеристиками.
Материалом для стержней и транспедикулярных винтов, а также основой для всех метаматериалов служит титановый сплав Ti -6 Al -4 V . В качестве альтернативного материала для монолитного имплантата выбран полиэфирэфиркетон ( PEEK ), пригодный для аддитивного производства. Данный материал распространен в вертебрологии, что обусловлено его биоинертностью, высокой усталостной выносливостью и способностью обеспечивать необходимую прочность фиксирующей системы [59; 60].
В разработанной модели анатомическая структура позвонков включает компактный слой, трабекулярную или губчатую ткань, хрящи фасеточных суставов и субхондральные концевые пластинки (рис. 5). Во внутренней структуре межпозвонковых дисков же выделяются пульпозное ядро и окружающее его в горизонтальной плоскости фиброзное кольцо, заключенные между хрящевыми замыкательными пластинками (рис. 6).
Физико-механические свойства всех используемых в данном исследовании материалов приведены в табл. 2.
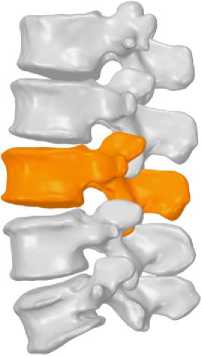
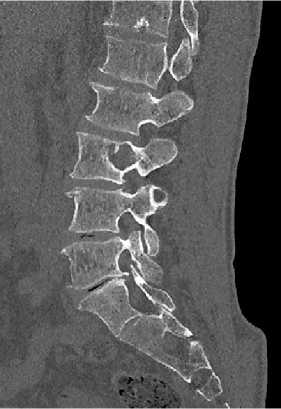
б
Рис. 4. Геометрическая модель костных структур поясничного отдела позвоночника ( а ); КТ-снимок пояснично-крестцового отдела позвоночника пациента ( б )
а
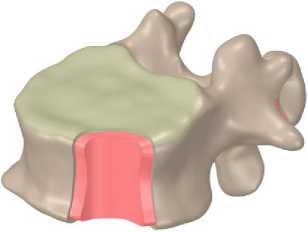
Рис. 5. Структура позвонка

Рис. 6. Структура межпозвонкового диска
Таблица 2
Физико-механические характеристики компонентов расчетной модели
|
Материал |
Математическая модель |
Модуль Юнга, МПа |
Коэффициент Пуассона |
Предел текучести, МПа |
|
Кортикальная костная ткань [61] |
Идеально упругопластическая |
18 439 |
0,28 |
189,8 |
|
Губчатая костная ткань [62; 62] |
67 |
0,2 |
1,84 |
|
|
Субхондральная замыкательная пластинка [64] |
193 |
0,29 |
3,94 |
|
|
Хрящевая замыкательная пластинка [65] |
Линейно-упругая |
5,9 |
0,42 |
– |
|
Хрящ фасеточного сустава [45] |
Гиперупругая модель Нео-Гука |
C io = 5,36; D 1 =0,04 |
||
|
Вещество фиброзного кольца [45] |
Гиперупругая модель Муни – Ривлина |
C io = O,18; C 01 = 0,045 |
||
|
Пульпозное ядро [45] |
C io = O,12; C 01 =0,03 |
|||
|
PEEK [66] |
Идеально упругопластическая |
4 000 |
0,38 |
110 |
|
Титановый сплав Ti -6 Al -4 V [19] |
113 800 |
0,34 |
950 |
|
Связочный комплекс поясничного отдела позвоночника представлен в модели семью ключевыми структурами: желтой связкой ( LF ), надостистой ( SSL ) и межостистой ( ISL ) связками, образующими капсулу связками фасеточных суставов ( FCL ), а также межпоперечной ( ITL ), задней продольной ( PLL ) и передней продольной ( ALL ) связками. Моделирование связочного аппарата реализовано посредством одномерных соединительных элементов, работающих по принципу линейных пружин растяжения [67]. Их физико-механические параметры представлены в табл. 3.
Взаимодействие компонентов модели
В созданной конечно-элементной модели связь стержней с головками транспедикулярных винтов, а также фиксация резьбовой части винтов в костной ткани позвонков, описаны как линейные соединения. В свою очередь, взаимодействие суставных отростков позвонков в фасеточных суставах и имплантата с поверхностями субхондральных замыкательных пластинок соседних позвонков моделируется как нелинейный контакт (рис. 7). В обеих контактных парах установлено условие трения с коэффициентом, равным 0,1.
Граничные условия и нагрузки
В рамках настоящей конечно-элементной постановки граничное условие моделирует опирание нижнего поясничного позвонка ( L 5) на крестцовый отдел (рис. 8, а ). Внешние силовые факторы же приложены к верхнему позвонку L 1 (рис. 8, б ).
Данная схема разработана для адекватного воспроизведения работы связочного аппарата, в действительности соединяющего поясничный отдел позвоночника с соседними ему отделами. Узлы соединительных элементов, моделирующих связочный аппарат, находятся на плоскостях иссечения поясничного отдела из позвоночного столба. Для обеспечения точной передачи усилий данные узлы жестко связаны с управляющими точками на замыкательных пластинках верхнего и нижнего позвонков. Именно в этих точках заданы кинематические граничные условия и векторы внешних силовых воздействий.
Таблица 3
Свойства связок
|
Связка |
ALL |
PLL |
ITL |
LF |
ISL |
SSL |
FCL |
|
Жесткость, ⋅103 Н/м |
347 |
29,5 |
1,4 |
7,7 |
0,3 |
2,5 |
36 |

в
а б
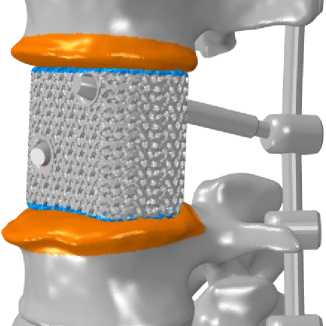
г
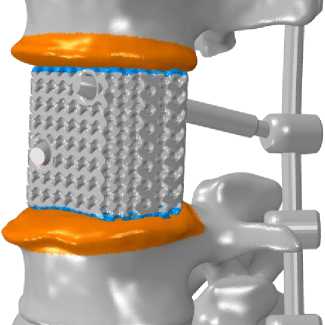
д
Рис. 7. Визуализация контактного взаимодействия между телом имплантата и замыкательными пластинками в случае с имплантатом из: а – монолитного полимера; б – метаматериала Body-centered Cube ; в – метаматериала Diamond ; г – метаматериала Fischer-Koch ; д – метаматериала Gyroid
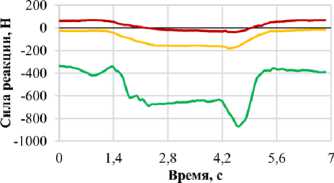
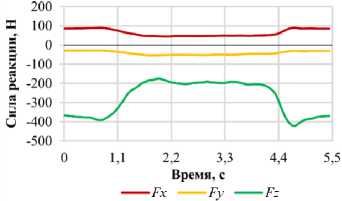
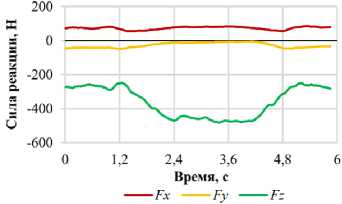
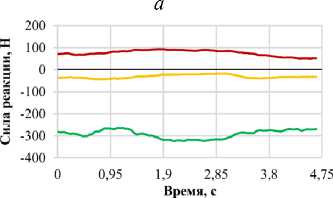
Количественные параметры силовых воздействий были определены на основе верифицированных данных базы OrthoLoad [68] и представлены на рис. 9 и 10. Данный репозиторий содержит результаты натурных измерений усилий, действующих на имплантаты в ходе реализации различных биомеханических сценариев. Таким образом, обеспечена высокая достоверность входных параметров моделирования. В настоящем исследовании моделируются шесть базовых сценариев: сагиттальные наклоны вперед и назад, латеральные наклоны в левую и правую стороны, а также повороты в обоих направлениях.
Конечно-элементное разбиение
Построение конечно-элементных сеток позвоночнодвигательных сегментов и имплантатов выполнялось в программной среде Altair SimLab (рис. 11 и 12). Генерация же сеток для стержней и транспедикулярных винтов была реализована средствами SIMULIA Abaqus 2021 (рис. 13). Параметры конечно-элементных сеток, включая количество и типы элементов, а также количество узлов, для каждого компонента сборки представлены в табл. 4.
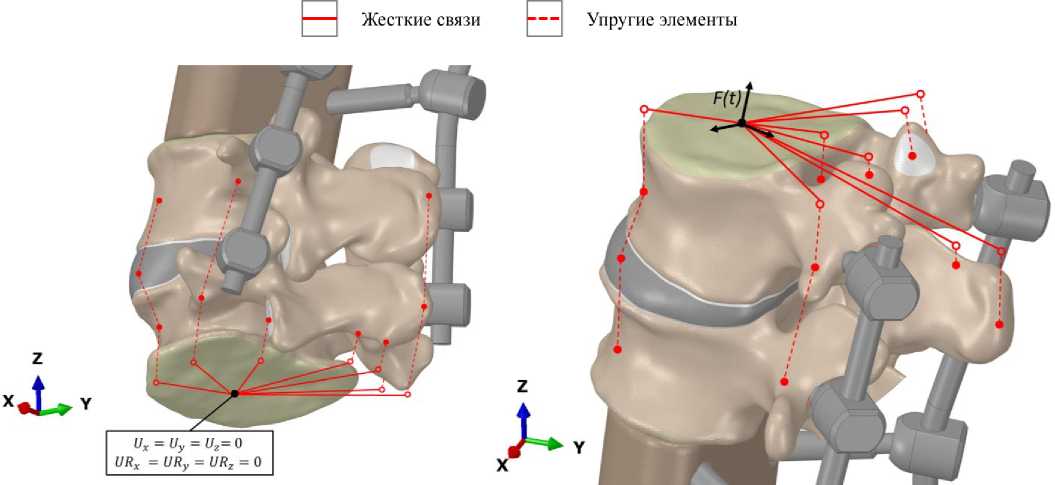
Рис. 8. Схема приложения граничных условий и нагрузок: а – жесткая фиксация нижнего опорного позвонка L 5; б – приложение расчетного вектора нагрузки к краниальной поверхности верхнего позвонка L 1
•Fx ----Fy ----Fz
б
в
■Fx ----Fy ----Fz
г
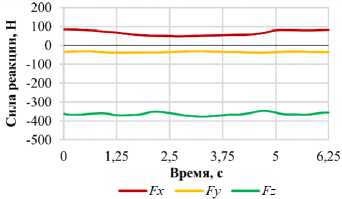
д
Рис. 9. Графики зависимости проекций силы реакции позвонка L 1 от фазы нагружения для различных видов двигательной активности: а – наклон вперед; б – наклон назад; в – наклон вправо; г – наклон влево;
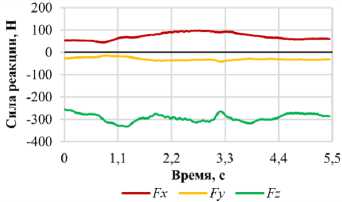
е
д – поворот вправо; е – поворот влево
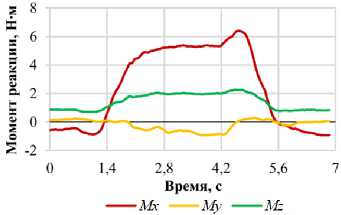
а
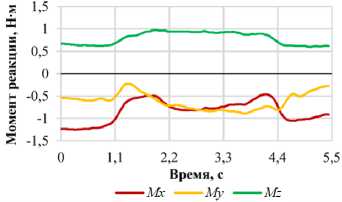
г
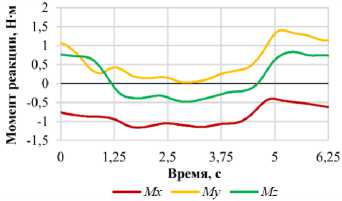
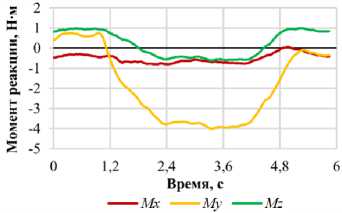
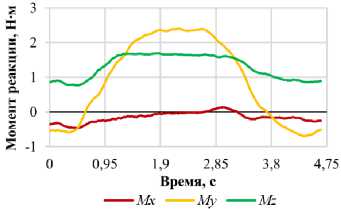
Рис. 10. Графики зависимости проекций момента реакции позвонка L 1 от фазы нагружения для различных видов двигательной активности: а – наклон вперед; б – наклон назад; в – наклон вправо; г – наклон влево; д – повороте вправо; е – поворот влево
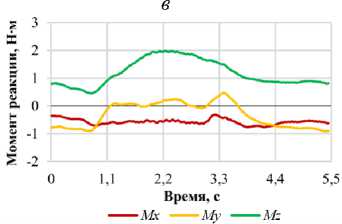
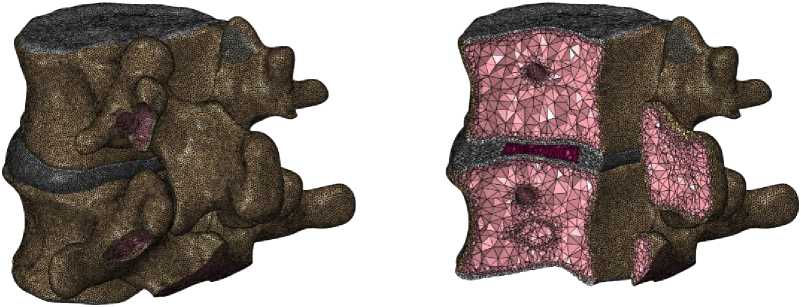
Рис. 11. Конечно-элементное разбиение позвоночно-двигательного сегмента L 1– L 2



в г д
Рис. 12. Конечно-элементное разбиение имплантата, выполненного из: а – полимера; б – метаматериала Body-centered Cube ; в – метаматериала Diamond ; г – метаматериала Fischer-Koch ; д – метаматериала Gyroid
а б

Рис. 13. Конечно-элементное разбиение стержней и ортопедических винтов
Таблица 4
Характеристики конечно-элементных сеток компонентов расчетной модели
|
Компонент |
Количество элементов |
Количество узлов |
Тип элемента |
|
|
Позвоночник |
4 238 840 |
819 826 |
Линейные твердотельные тетраэдральные элементы с четырьмя узлами типа C 3 D 4 - 3 843 508 элементов. Линейные твердотельные тетраэдральные элементы с четырьмя узлами типа C 3 D 4 H ( Hybrid formulation ) - 395 332 элементов |
|
|
Имплантат |
Из полимера |
273 522 |
62 482 |
Линейные твердотельные тетраэдральные элементы с четырьмя узлами типа C 3 D 4 |
|
Из метаматериала Body-centered Cube |
1 026 743 |
279 728 |
||
|
Из метаматериала Diamond |
1 018 161 |
265 577 |
||
|
Из метаматериала Fischer-Koch |
953 881 |
284 519 |
||
|
Из метаматериала Gyroid |
768 060 |
201 215 |
||
|
Стержни |
Стержень 1 |
5 934 |
7 367 |
Линейные твердотельные гексаэдральные элементы с восемью узлами типа C 3 D 8 R ( Reduced integration ) |
|
Стержень 2 |
6 109 |
7 650 |
||
|
Винты задней системы фиксации |
Винт 1 |
18 654 |
4 081 |
Линейные твердотельные тетраэдральные элементы с четырьмя узлами типа C 3 D 4 |
|
Винт 2 |
18 438 |
4 035 |
||
|
Винт 3 |
18 865 |
4 117 |
||
|
Винт 4 |
18 608 |
4 071 |
||
|
Винт 5 |
22 077 |
33 726 |
Квадратичные твердотельные тетраэдральные элементы с десятью узлами типа C 3 D 10 |
|
|
Винт 6 |
22 139 |
33 895 |
||
|
Винт 7 |
18 728 |
4 094 |
Линейные твердотельные тетраэдральные элементы с четырьмя узлами типа C 3 D 4 |
|
|
Винт 8 |
18 478 |
4 043 |
||
|
Винт 9 |
18 752 |
4 098 |
||
|
Винт 10 |
18 571 |
4 057 |
||
|
Всего: |
Полимерный имплантат |
4 711 606 |
997 542 |
C 3 D 4, C 3 D 4 H , C 3 D 8 R , C 3 D 10 |
|
Имплантат из метаматериала Bodycentered Cube |
5 470 936 |
1 214 788 |
||
|
Имплантат из метаматериала Diamond |
5 462 354 |
1 200 637 |
||
|
Имплантат из метаматериала Fischer-Koch |
5 398 074 |
1 219 579 |
||
|
Имплантат из метаматериала Gyroid |
5 212 253 |
1 136 275 |
||
Проведение расчетов
Все расчеты в рамках данной работы производились в программном комплексе SIMULIA Abaqus 2021. Вычислительный этап исследования реализован на базе ресурсов кластерной вычислительной системы, архитектура которой включает расчетные узлы с процессорами Intel Xeon Silver 4210R и оперативной памятью объемом 128 Гб на каждый узел. Мониторинг и диспетчеризация расчетных процессов осуществлялись в среде SPDM-системы (Simulation Process and Data Management) CML-Bench [69], что обеспечило эффективное управление инженерными данными и прослеживаемость всех этапов численного моделирования. Для каждого из рассматриваемых движений позвоночника продолжительность расчетов составляла до 12 ч, что характерно для всех исследуемых имплантатов.
Результаты и обсуждение
Оценка надежности реконструкции позвоночника
В качестве критериев оценки надежности реконструированного отдела позвоночника в данной работе приняты характер распределения и значения эквивалентных напряжений по Мизесу. Оценка перечисленных параметров и показателей проводилась в наиболее нагруженных участках модели: в области соприкосновения субхондральных пластинок с имплантатом, в элементах задней фиксирующей конструкции, а также в костных тканях, окружающих ортопедические винты [42–46; 70]. Высокие значения напряжений в перечисленных зонах указывают на повышенную вероятность проседания имплантата, разрушения металлоконструкции или дестабилизацию всей системы фиксации. Все вышеуказанные факторы вызывают нарушение стабильности реконструированного позвоночника.
Субхондральные замыкательные пластинки
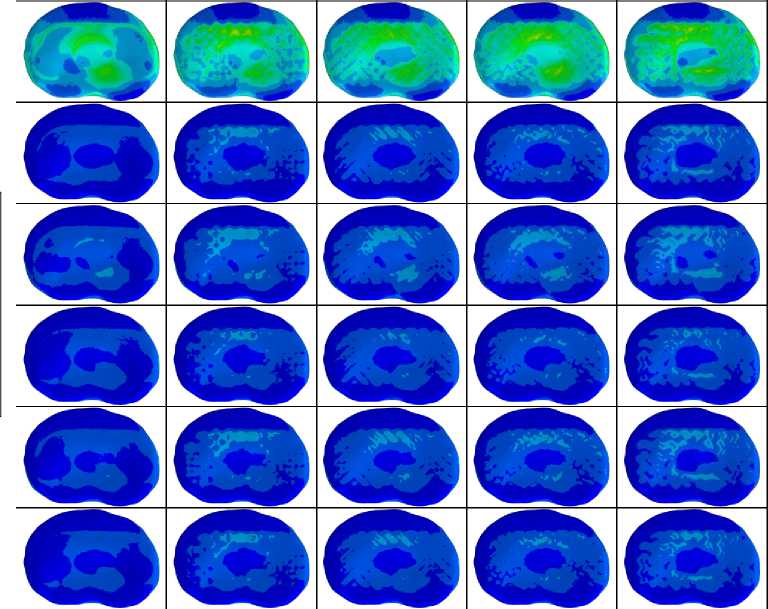
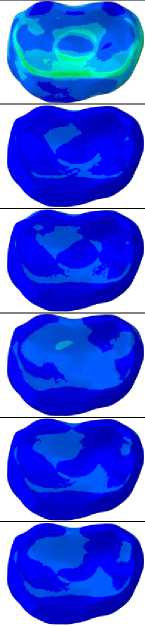
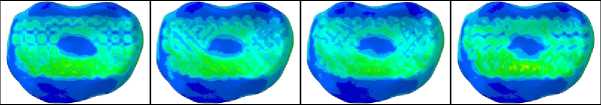
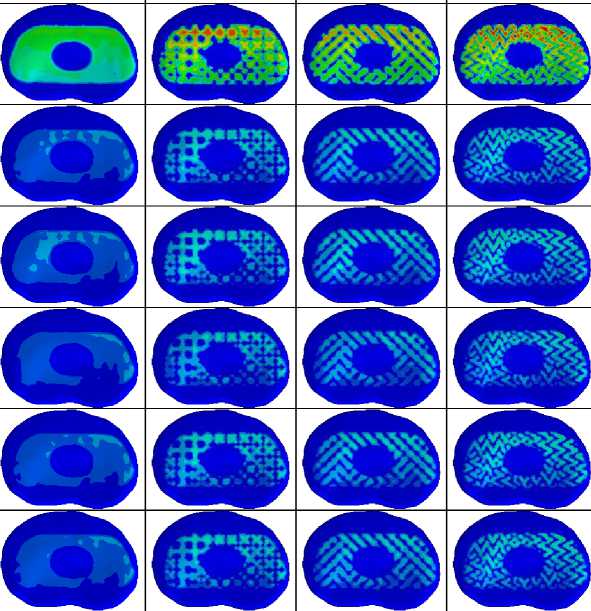
В данной работе особое значение придается анализу биомеханического взаимодействия искусственного позвонка с примыкающими субхондральными пластинками. Визуализация распределения эквивалентных напряжений по Мизесу в структуре субхондральных концевых пластинок представлена на рис. 14 и 15. Для повышения удобства и обеспечения корректности сравнительного анализа при отображении напряжений в замыкательных пластинках была использована унифицированная цветовая шкала. Следует отметить, что на всех полях величин в настоящем исследовании для каждого конечного элемента отображено максимальное значение величины за время действия соответствующей нагрузки. Пиковые значения напряжений, зафиксированные в субхондральных пластинках, прилегающих к имплантату сверху и снизу, приведены в табл. 5 и 6.
Все рассмотренные в данной работе имплантаты, включая полимерный, вызывают в субхондральных замыкательных пластинках распределение напряжений чрезвычайно схожего характера. Наибольший уровень напряжений наблюдается при выполнении наклона вперед. Напряжения при этом охватывают большую часть поверхности пластинок, но в области действия передней части имплантата их значения немного выше. Напряжения же, вызванные выполнением остальных характерных движений позвоночника, в обеих замыкательных пластинках имеют малые значения и относительно равномерно распределены в области контакта с имплантатом.
Случай с полимерным имплантатом
Случай с имплантатом из метаматериала Body-centered Cube
Случай с имплантатом из метаматериала Diamond
Случай с имплантатом из метаматериала Fischer-Koch
Случай с имплантатом из метаматериала Gyroid
S_max, Mises
+2.511e+06 +2.302e+06 +2,093e+06 + 1.883e+06 + 1.674e+06 + 1.465e+06 +1.256e+O6 + 1.046e+06 +8.371e+05 +6.2786 + 05 +4.186e+05 +2.093e+05 +0.000e+00 Наклон вперед Наклон назад Наклон вправо Наклон влево Поворот вправо Поворот влево Рис. 14. Распределения эквивалентных напряжений по Мизесу в субхондральном слое замыкательной пластинки, контактирующей с верхним торцом имплантата, Па Случай с полимерным имплантатом Случай с имплантатом из
метаматериала
Body-centered Cube
Случай с имплантатом из
метаматериала
Diamond
Случай с имплантатом из
метаматериала
Fischer-Koch
Случай с имплантатом из
метаматериала
Gyroid
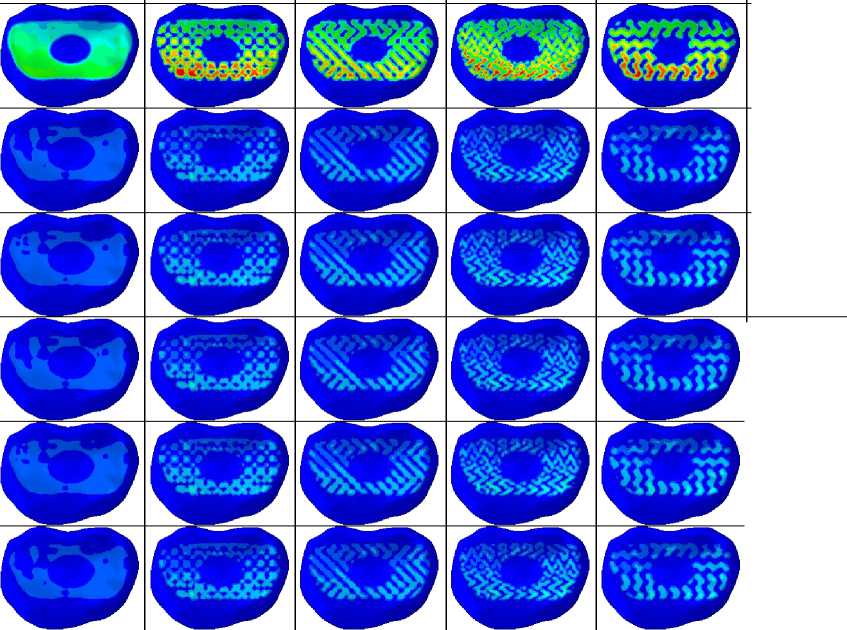
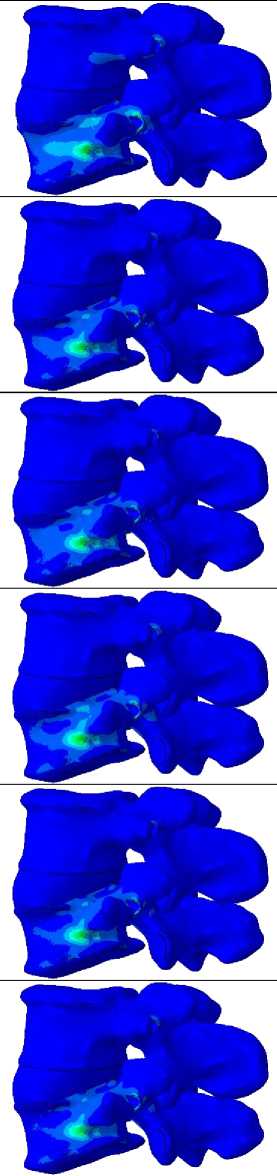
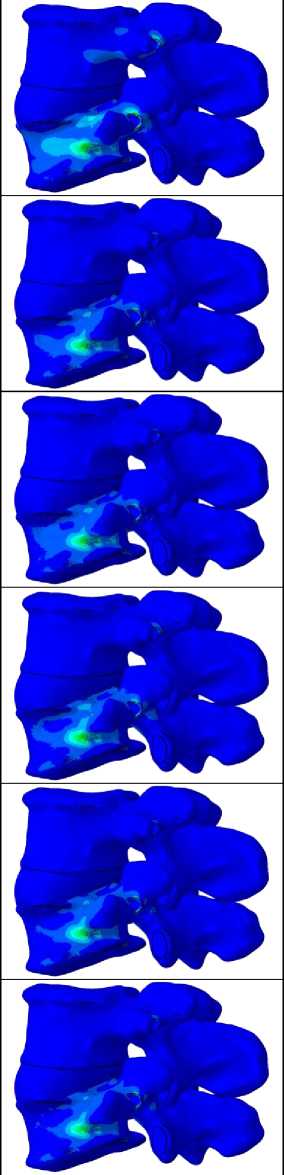
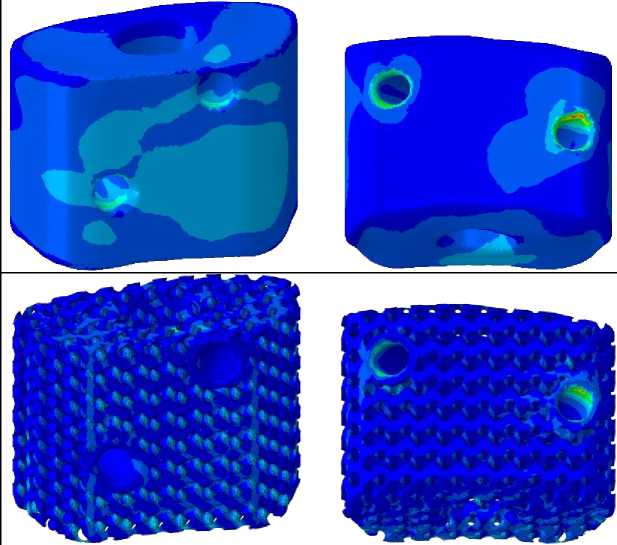
S_max, Mises Наклон вперед □□□□ Наклон назад Наклон вправо Наклон влево Поворот вправо Поворот влево Рис. 15. Распределения эквивалентных напряжений по Мизесу в субхондральном слое замыкательной пластинки, контактирующей с нижним торцом имплантата, Па Таблица 5 Максимальные значения эквивалентных напряжений по Мизесу в верхней субхондральной замыкательной пластинке, МПа Вид движения позвоночника Случай с полимерным имплантатом Случай с имплантатом из метаматериала Body-centered Cube Случай с имплантатом из метаматериала Diamond Случай с имплантатом из метаматериала Fischer-Koch Случай с имплантатом из метаматериала Gyroid Наклон вперед 2,295 2,511 2,162 2,177 2,291 Наклон назад 0,825 0,776 0,652 0,734 0,618 Наклон вправо 0,775 0,719 0,618 0,683 0,716 Наклон влево 0,890 0,784 0,648 0,724 0,574 Поворот вправо 0,843 0,781 0,682 0,748 0,630 Поворот влево 0,817 0,758 0,638 0,721 0,608 Описанные результаты отличаются от полученного ранее для конструкции из метаматериала с латеральным типом крепления [51]. Для случая с названным имплантатом во всех расчетных сценариях была характерна выраженная неравномерность распределения напряжений в нижней замыкательной пластинке, что проявлялось в локализации зоны повышенных напряжений преимущественно в задней части системы «имплантат – пластинка». То же наблюдалось и при сагиттальном наклоне вперед для верхней субхондральной пластинки. Также следует указать, что во всех изученных случаях максимальные значения напряжений сосредоточены по периферии замыкательных пластинок. Данное явление, вероятно, обусловлено градиентом жесткости, вызванным соседством в данных областях материалов, обладающих существенно различными физико-механическими характеристиками. Важно подчеркнуть, что зафиксированные пиковые значения напряжений не превышают 67 % от предела текучести костной ткани. Данный запас прочности указывает на низкую вероятность возникновения необратимых деформаций замыкательных пластинок и, как следствие, минимизирует риск проседания имплантата во всех изученных случаях. При анализе распределения напряжений в обеих замыкательных пластинках вне краевых зон было установлено, что использование имплантатов из различных метаматериалов при выполнении всех исследованных движений приводит к близким уровням напряжений, несколько превышающим показатели для полимерной конструкции. Подобное различие, по-видимому, продиктовано меньшей эффективной площадью контакта решетчатых и ТПМП-метаматериалов c поверхностью субхондральных пластинок в сравнении с монолитным полимером. Данные выводы совпадают с теми, что были сделаны в работе Pokorni et al. [46], а также Zhangui et al. [48], в которых исследовалось влияние площади соответствующих поверхностей имплантатов на биомеханику позвоночника. Визуализация распределений контактного давления в парах «субхондральная пластинка – имплантат» при варьировании условий нагружения представлена на рис. 16 и 17. Для повышения удобства и обеспечения корректности сравнительного анализа при отображении давлений на поверхностях замыкательных пластинок была использована унифицированная цветовая шкала. Данные о пиковых значениях контактных давлений в названных зонах приведены в табл. 7 и 8. Все рассмотренные в данной работе имплантаты, включая полимерный, вызывают в каждой из замыкательных пластинок практически идентичные распределения контактного давления. При этом распределения эти неравномерны, и в области передней части имплантата значения этих давлений значительно выше. Это обстоятельство согласуется с данными из предыдущего исследования для имплантата из метаматериала с латеральным типом крепления, где большие давления также наблюдались на удалении от места фиксации изделия. Максимальные значения контактного давления в каждой из замыкательных пластинок для всех типов исследуемых конструкций достигаются в сценарии с сагиттальным наклоном вперед. Вместе с тем в большинстве расчетных случаев величина давления в зоне контакта для имплантатов из металлических метаматериалов более чем в 1,5 раза превосходит соответствующие значения для полимерного изделия. Как упоминалось ранее, ключевым фактором здесь выступает меньшая эффективная площадь контакта с пластинками у пористых структур в сравнении со сплошным полимером. Кроме того, в ходе сравнительного анализа выявлено, что ТПМП-метаматериалы вызывают в субхондральных пластинках несколько более высокие уровни давления, чем решетчатые метаматериалы. Если рассматривать только группу металлических имплантатов аддитивного производства, то наиболее благоприятное распределение контактного давления наблюдается при использовании структуры Diamond. Применение же метаматериала Fischer-Koch, напротив, приводит к возникновению наиболее интенсивных давлений на поверхностях замыкательных пластинок. Таблица 6 Максимальные значения эквивалентных напряжений по Мизесу в нижней субхондральной замыкательной пластинке, МПа Вид движения позвоночника Случай с полимерным имплантатом Случай с имплантатом из метаматериала Body-centered Cube Случай с имплантатом из метаматериала Diamond Случай с имплантатом из метаматериала Fischer-Koch Случай с имплантатом из метаматериала Gyroid Наклон вперед 2,230 2,367 2,408 2,338 2,604 Наклон назад 0,425 0,449 0,419 0,458 0,479 Наклон вправо 0,489 0,487 0,455 0,466 0,500 Наклон влево 0,492 0,522 0,523 0,563 0,559 Поворот вправо 0,461 0,477 0,435 0,495 0,505 Поворот влево 0,443 0,470 0,462 0,515 0,509 CPRESS_max +2.383e+06 +2.184e+06 +1.986e+06 + 1.787e+06 + 1.589e+06 + 1.390e+06 +1.192e+06 +9.929e+05 +7.943e+05 +5.958e+05 +3.972e+05 + 1.986e+05 +0.000e+00 Случай с полимерным имплантатом Случай с имплантатом из метаматериала Body-centered Cube Случай с имплантатом из метаматериала Diamond Случай с имплантатом из метаматериала Fischer-Koch Случай с имплантатом из метаматериала Gyroid Наклон вперед Наклон назад Наклон вправо Наклон влево Поворот вправо Поворот влево Рис. 16. Распределения контактного давления на поверхности субхондральной замыкательной пластинки, контактирующей с верхним торцом имплантата, Па Позвоночник В позвоночно-двигательном сегменте L1–L2 области эквивалентных напряжений по Мизесу локализованы вблизи каналов транспедикулярных винтов, а уровень напряжений незначителен. Кроме того, характер распределения напряжений в костной ткани при использовании различных металлических метаматериалов практически идентичен для каждого из рассмотренных типов нагрузки. В связи с этим на рис. 18 представлены распределения напряжений только для сегмента L4–L5 и только для двух случаев: с полимерным имплантатом и имплантатом из метаматериала Fischer-Koch. Для повышения удобства и обеспечения корректности сравнительного анализа при отображении напряжений в костных тканях позвонков была использована унифицированная цветовая шкала, а зафиксированные пиковые значения напряжений приведены в табл. 9. Независимо от сценария двигательной активности, поля распределения напряжений в позвоночном столбе обладают высокой степенью сходства при использовании как полимерных, так и металлических имплантатов. Повышенные напряжения сосредоточены в костной ткани вокруг винтов и в теле нижнего позвонка. Высокие значения напряжений в данном позвонке являются следствием принятой математической модели граничных условий, а именно жесткого закрепления, и лишь частично отражают реальную биомеханику взаимодействия с крестцом. Однако данное допущение не искажает общую картину, так как область задания граничного условия удалена от зоны, представляющей наибольший интерес. Наиболее нагруженным состоянием позвоночника является сагиттальный наклон вперед. При выполнении же остальных наклонов уровни напряжений в позвоночнике близки и несколько выше, чем при выполнении поворотов. Анализ показал, что во всех исследуемых сценариях зоны максимальных значений напряжений расположены в области перехода от компактного слоя кости к губчатой ткани вблизи каналов ортопедических винтов в нижнем позвонке. Такое локальное распределение напряжений обусловлено градиентом жесткости на границе этих двух различных по свойствам сред. В то же время в остальных участках кости, взаимодействующих с элементами системы фиксации, значения напряжений не превышают предела текучести. Это позволяет сделать вывод о достаточном запасе прочности позвонков и стабильности транспедикулярной фиксирующей системы [70]. Настоящие результаты соответствуют тем, что были получены в предыдущем исследовании [51] и в работе Dong et al. [42]. Результаты сравнительного анализа свидетельствуют, что для случаев с имплантатами из метаматериалов характерны несколько более высокие напряжения в позвоночнике, чем для случая с полимерным аналогом. При этом ТПМП-структуры вызывают незначительно большую нагрузку на кость по сравнению с решетчатыми структурами. Тем не менее общий анализ НДС позволяет заключить, что все протестированные варианты имплантатов оказывают практически эквивалентное влияние на биомеханику поясничного отдела позвоночного столба. Случай с полимерным имплантатом Случай с имплантатом из метаматериала Body-centered Cube Наклон вперед Наклон вправо Наклон влево Поворот вправо Случай с имплантатом из метаматериала Diamond Случай с имплантатом из метаматериала Fischer-Koch Случай с имплантатом из метаматериала Gyroid CPRESS_max +2.495e+06 +2.287e+06 +2.079e+06 + 1.871e+06 + 1.663e+06 + 1.455e+06 + 1.248e+06 + 1.0406+06 +8.3176+05 +6.238e+05 +4.158e+05 +2.079e+05 +0.0006+00 Рис. 17. Распределения контактного давления на поверхности субхондральной замыкательной пластинки, контактирующей с нижним торцом имплантата, Па Таблица 7 Максимальные значения контактного давления на поверхности верхней субхондральной замыкательной пластинки, МПа Вид движения позвоночника Случай с полимерным имплантатом Случай с имплантатом из метаматериала Body-centered Cube Случай с имплантатом из метаматериала Diamond Случай с имплантатом из метаматериала Fischer-Koch Случай с имплантатом из метаматериала Gyroid Наклон вперед 1,283 2,031 2,020 2,383 2,289 Наклон назад 0,499 0,803 0,760 0,917 0,883 Наклон вправо 0,477 0,780 0,749 0,914 0,837 Наклон влево 0,521 0,766 0,723 0,863 0,823 Поворот вправо 0,502 0,788 0,748 0,897 0,874 Поворот влево 0,495 0,773 0,731 0,879 0,843 Таблица 8 Максимальные значения контактного давления на поверхности нижней субхондральной замыкательной пластинки, МПа Вид движения позвоночника Случай с полимерным имплантатом Случай с имплантатом из метаматериала Bodycentered Cube Случай с имплантатом из метаматериала Diamond Случай с имплантатом из метаматериала Fischer-Koch Случай с имплантатом из метаматериала Gyroid Наклон вперед 1,395 2,359 2,188 2,495 2,432 Наклон назад 0,405 0,667 0,648 0,770 0,696 Наклон вправо 0,427 0,698 0,683 0,809 0,741 Наклон влево 0,410 0,669 0,656 0,758 0,695 Поворот вправо 0,424 0,707 0,678 0,803 0,737 Поворот влево 0,413 0,687 0,644 0,780 0,715 Имплантаты Характер распределения эквивалентных напряжений по Мизесу внутри имплантатов демонстрирует единообразие для всех моделируемых типов физической активности. Аналогичная схожесть НДС наблюдается и при сравнении конструкций из различных метаматериалов. В связи с этим на рис. 19 представлены результаты только для двух репрезентативных случаев: со сплошным полимерным изделием и с имплантатом из ТПМП-метаматериала Gyroid. Сводные данные по пиковым значениям напряжений, возникающих в теле каждого имплантата при различных сценариях нагружения, приведены в систематизированном виде в табл. 10. Во всех исследуемых изделиях напряжения сосредоточены преимущественно в передней части, в то время как в задней части наблюдаются лишь области повышенных напряжений вблизи отверстий для винтов. В имплантатах из металлических метаматериалов также имеет место локализация повышенных напряжений в областях с тонкими структурами, возникшими при обрезке геометрии в ходе построения моделей. Сагиттальный наклон вперед вызывает во всех рассмотренных имплантатах наибольшие напряжения. При выполнении остальных движений уровни напряжений в большинстве случаев достаточно близки. Подобная схожесть в значениях напряжений наблюдается и при сравнении между собой результатов для конструкций из различных метаматериалов. Исключение составляет лишь имплантат из метаматериала на основе ячейки Body-centered Cube. В данном случае при наклонах вперед и вправо значения напряжений существенно выше показателей для других типов движений, а также значений, фиксируемых в остальных изделиях. Это может быть обусловлено наличием зоны повышенных напряжений в области с особо тонкими структурами на внешней границе, где тетраэдральные конечные элементы чрезвычайно искажены и практически вырождены в плоскость. Помимо всего прочего, следует отметить, что уровень напряжений во всех рассмотренных имплантатах из метаматериалов крайне низок и составляет менее 10 % от значения предела текучести. Данное обстоятельство подтверждает выдвинутую в предыдущем исследовании [51] гипотезу о том, что использование для имплантатов из метаматериалов заднего типа крепления эффективно нивелирует риски, связанные с надежностью их фиксации. Задняя фиксирующая система Во всех расчетных сценариях зоны повышенных напряжений в системе задней фиксации локализуются в области шеек и головок транспедикулярных винтов вблизи функциональных отверстий, а также на участках стержней между зонами крепления винтов. Характер распределения напряжений в стержнях обусловлен выбранной моделью взаимодействия компонентов системы фиксации, а именно линейным соединением, что находит подтверждение в работе Gu et al. [48]. Наибольший уровень напряжений зафиксирован в области шеек винтов. Аналогичная его локализация описывалась в работе Han et al. [43] при анализе различных вариантов стабилизации грудопоясничного отдела позвоночного столба. Количественные данные по упомянутым пиковым значениям напряжений приведены для каждого сценария в табл. 11. Сагиттальный наклон вперед является наиболее рискованным видом двигательной активности для фиксирующей системы. Кроме того, уровни напряжений в случаях с изделиями из метаматериалов близки и заметно превышают значения, полученные для полимерного имплантата. Тем не менее в среднем наиболее интенсивное нагружение системы фиксации отмечается при использовании метаматериала с ячейкой периодичности Fischer-Koch, тогда как структура Diamond обеспечивает наименьшие напряжения в системе. Вместе с тем из анализа результатов следует, что напряжения в компонентах транспедикулярной фиксирующей системы остаются в безопасном диапазоне, составляя менее 40 % от предела текучести материала. Столь существенный запас прочности согласуется с результатами исследования Pokorni et al. [46], а также нашего предыдущего исследования [51]. Таким образом, прочность системы фиксации обеспечивается при применении любого из предложенных типов имплантатов вне зависимости от сценария двигательной активности. Случай с полимерным имплантатом Smax, Mises (Avg: 100%) — + 1.893e+08 +1.735e+08 --+1.578e+08 --+ 1.420e+08 --+ 1.262e+08 — - +1.104e+08 --+9.465e+07 --+7.888e+07 --+6.310e+07 --+4.733e+07 -- + 3.155e+07 ■ - +1.578e+07 ■ +0.000e+00 Случай с имплантатом из метаматериала Fischer-Koch Наклон вперед Наклон назад Наклон вправо Наклон влево Поворот вправо Поворот влево Рис. 18. Распределения эквивалентных напряжений по Мизесу в позвоночно-двигательном сегменте L4–L5, Па Таблица 9 Максимальные значения эквивалентных напряжений по Мизесу в костных тканях позвоночника, МПа Вид движения позвоночника Случай с полимерным имплантатом Случай с имплантатом из метаматериала Body-centered Cube Случай с имплантатом из метаматериала Diamond Случай с имплантатом из метаматериала Fischer-Koch Случай с имплантатом из метаматериала Gyroid Наклон вперед 176,7 187,9 186,5 189,3 188,4 Наклон назад 127,8 138,6 136,3 142,0 139,5 Наклон вправо 137,5 146,6 143,1 151,3 146,9 Наклон влево 138,4 149,1 146,7 151,7 149,9 Поворот вправо 116,9 126,9 124,6 129,3 127,6 Поворот влево 115,4 125,5 123,2 128,1 126,4 Полимерный имплантат Имплантат из метаматериала «Gyroid» S_max, Mises (Avg: 100%) —- +6.474e+06 +5.934e + 06 --+ 5.395e + 06 --+4.855e + 06 — +4.316e + 06 --+3.776e+06 --+3.237e+06 --+ 2.697e + 06 --+2.158e+O6 --+1.618e+06 E+1.079e+06 + 5.395e + 05 +0.000e+00 S_max, Mises (Avg: 100%) —- +4.167e+07 +3.820e + 07 --+3.473e+07 --+3.126e + 07 --+2.7786 + 07 --+2.4316 + 07 --+2.084e + 07 --+1.736e+07 --+1.3896+07 --+1.042e+07 E+6.946e+06 + 3.473e + 06 +0.000e+00 Рис. 19. Распределения эквивалентных напряжений по Мизесу в имплантатах, Па Обобщение результатов Анализ напряженно-деформированного состояния поясничного отдела позвоночника после реконструкции при действии различных нагрузок позволил установить высокую степень сходства биомеханического отклика системы для всех рассмотренных вариантов имплантатов. Отличаются лишь значения напряжений, которые во всех компонентах системы для случаев с имплантатами из метаматериалов имеют несколько более высокий уровень, чем в случае с полимерным изделием. Сравнение же результатов, полученных для имплантатов из разных метаматериалов, выявляет лишь незначительные отличия, зачастую не имеющие закономерности. Уровень напряжений в субхондральных замыкательных пластинках во всех рассмотренных случаях не достигает предела текучести, что сводит к минимуму риск проседания исследуемых конструкций. Наряду с этим совокупность полученных данных свидетельствует о высокой конструкционной прочности самих имплантатов, а также о стабильности транспедикулярной фиксации. Подобная механическая безопасность обусловлена тем, что напряжения в теле имплантатов, в элементах задней системы фиксации и в периимплантатной костной ткани находятся на уровнях, значительно более низких, чем пределы текучести соответствующих материалов. Данный факт верифицирует гипотезу, выдвинутую в предыдущей работе: использование для имплантатов из метаматериалов заднего типа крепления, полностью решает вопрос надежности их фиксации в позвоночнике. Резюмируя все вышеизложенное, можно заключить, что с точки зрения прочности рассмотренные имплантаты из метаматериалов оказывают практически идентичное влияние на биомеханику поясничного отдела позвоночника. Таким образом, для осуществления выбора оптимального метаматериала для имплантата, заменяющего позвонок, необходимо провести сравнение метаматериалов с точки зрения стимулирования ими прорастания в имплантат костной ткани. Несмотря на то что применение полимерного имплантата обеспечивает более низкие показатели напряжений в системе, он не является предпочтительным вариантом. Данный вывод основывается на том, что уровни напряжений, зафиксированные для конструкций из метаматериалов, превышают значения, наблюдаемые для полимера, лишь незначительно. К тому же во всех случаях эти значения остаются в пределах, соответствующих упругой деформации, и не достигают предела текучести, что подтверждает эффективность и безопасность использования передовых метаматериалов для создания позвоночных имплантатов. Также важно учитывать, что структура метаматериалов способствует остеоинтеграции, а следовательно, и увеличению стабильности фиксации имплантатов [55]. Ограничения исследования Настоящее исследование обладает некоторыми ограничениями. Во-первых, конечно-элементные модели основаны на данных только одного пациента, что не позволяет распространить сделанные выводы на пациентов с отличными анатомическими особенностями. Во-вторых, в рамках разработанной конечноэлементной модели не учитывалось влияние мышечного аппарата и окружающих мягких тканей. Поскольку данные структуры вносят существенный вклад в распределение биомеханических нагрузок, их Таблица 10 Максимальные значения эквивалентных напряжений по Мизесу в имплантатах, МПа Вид движения позвоночника Полимерный имплантат Имплантат из метаматериала Body-centered Cube Имплантат из метаматериала Diamond Имплантат из метаматериала Fischer-Koch Имплантат из метаматериала Gyroid Наклон вперед 6,5 86,0 39,5 38,6 41,7 Наклон назад 3,2 28,2 16,4 15,6 16,0 Наклон вправо 5,0 52,4 21,8 22,0 23,2 Наклон влево 4,0 23,1 23,8 23,4 23,5 Поворот вправо 4,1 28,3 19,1 18,5 18,4 Поворот влево 4,1 26,4 21,9 20,3 21,3 Таблица 11 Максимальные эквивалентные напряжения по Мизесу в задней фиксирующей системе, МПа Наконец, за рамками настоящей работы осталось воздействие циклических динамических нагрузок, характерных для естественной двигательной активности человека. Анализ усталостной прочности и изменения напряженно-деформированного состояния системы в условиях циклического нагружения в будущем позволят более точно оценить эксплуатационный ресурс и долговечность предложенных имплантатов. Заключение В настоящем исследовании реализован анализ биомеханического поведения поясничного отдела позвоночника после выполнения реконструктивного вмешательства по установке различных изделий, заменяющих позвонок. Оценка параметров напряженно-деформированного состояния осуществлялась в условиях действия физиологических нагрузок, соответствующих распространенным видам двигательной активности человека. Необходимо подчеркнуть, что даже при текущем уровне развития нейрохирургической техники достижение надежной стабилизации позвоночника после тотальной спондилэктомии единым блоком по-прежнему представляет собой одну из наиболее сложных клинических задач. Производственные ограничения серийных имплантатов часто не позволяют достичь физиологичного распределения нагрузок и обеспечить достаточную поддержку, что в условиях динамических нагрузок повышает риск миграции и проседания



Вид движения позвоночника
Случай с полимерным имплантатом
Случай с имплантатом из метаматериала Bodycentered Cube
Случай с имплантатом из метаматериала Diamond
Случай с имплантатом из метаматериала Fischer-Koch
Случай с имплантатом из метаматериала Gyroid
Наклон вперед
324,2
356,4
349,2
369,3
359,3
Наклон назад
159,4
246,4
245,0
249,0
245,2
Наклон вправо
150,9
234,0
234,4
236,9
233,1
Наклон влево
194,5
292,2
291,3
296,1
292,0
Поворот вправо
158,5
238,0
237,2
241,6
237,6
Поворот влево
178,4
271,6
270,4
276,0
271,6
включение в расчетную схему представляет собой перспективное направление для дальнейших исследований.


