Сравнительный анализ результатов резекции ободочной кишки по поводу колоректального рака в зависимости от стороны гемиколэктомии: данные Ульяновского областного клинического диспансера
Автор: Тонеев Е.А., Прохоров Д.Д., Корымасов Е.А., Белоногов Н.И., Асанов Б.М., Шагаева А.И.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 1, 2026 года.
Бесплатный доступ
Колоректальный рак (КРР) является одной из ведущих причин онкологической заболеваемости и смертности. В России КРР формирует около 10 % всей онкопатологии и занимает 3-е место в структуре онкологической смертности, что подчеркивает приоритет совершенствования радикального хирургического лечения. Несостоятельность межкишечного анастомоза (НМА) остается ключевым исходом гемиколэктомии по поводу колоректального рака и напрямую влияет на прогноз. Цель. Провести сравнительный анализ частоты развития несостоятельности межкишечного анастомоза и структуры послеоперационных осложнений после правосторонней и левосторонней гемиколэктомии у пациентов с колоректальным раком. Материалы и методы. В ретроспективное исследование включены 354 пациента, оперированные в ГУЗ Ульяновский областной клинический онкологический диспансер в 2019–2024 гг. Пациенты распределены на 2 группы: с правосторонней (n=278) и левосторонней гемиколэктомией (n=76). Анализ факторов риска развития несостоятельности анастомоза проводился с использованием многофакторной логистической регрессии. Результаты. По нашим данным, частота мультивисцеральных резекций в группах была сопоставимой: при левосторонней гемиколэктомии – 8 из 76 случаев (10,5 %), при правосторонних – 26 из 278 (9,4 %). Подавляющее большинство операций в обеих группах выполнялось без мультиорганного компонента – 68 из 76 (89,5 %) и 252 из 278 (90,6 %) соответственно. Различия не имели статистической значимости (χ2, p=0,930). Несостоятельность межкишечного анастомоза отмечена у 2,2 % пациентов после правосторонней гемиколэктомии и у 6,6 % после левосторонней (p=0,033). Независимыми предикторами данного осложнения стали низкий предоперационный уровень альбумина (OR 0,84; p=0,023) и сторона операции (OR 0,30; p=0,033). ROC-анализ модели показал высокую прогностическую точность (AUC=0,879). Выводы. Правосторонняя гемиколэктомия характеризуется меньшей частотой развития несостоятельности анастомоза по сравнению с левосторонней. Низкий уровень сывороточного альбумина является значимым предиктором осложнений, что подчеркивает важность предоперационной оценки и коррекции нутритивного статуса.
Колоректальный рак, гемиколэктомия, несостоятельность анастомоза, альбумин, хирургические осложнения, логистическая регрессия, ROC-анализ
Короткий адрес: https://sciup.org/14134854
IDR: 14134854 | УДК: 616.348-006.6-089.87 | DOI: 10.34014/2227-1848-2026-1-60-72
Comparative analysis of colon resection results for colorectal cancer depending on the side of hemicolectomy: data from the Ulyanovsk Regional Clinical Dispensary
Colorectal cancer (CRC) is one of the leading causes of cancer morbidity and mortality. In Russia, CRC accounts for approximately 10 % of all cancer cases and ranks third in the structure of cancer-related mortality, highlighting the priority of improving radical surgical treatment. Anastomotic leak (AL) remains a key complication of hemicolectomy for colorectal cancer directly affecting the clinical outcome. Objective. The aim of the study is to conduct a comparative analysis of the incidence of anastomotic leak and the structure of postoperative complications after right and left hemicolectomy in patients with colorectal cancer. Materials and Methods. The retrospective study included 354 patients who underwent surgery at the Ulyanovsk Regional Clinical Oncology Dispensary in 2019-2024. The patients were divided into two groups: those with right hemicolectomy (n=278) and those with left hemicolectomy (n=76). Risk factors for anastomotic leak were analyzed using multivariable logistic regression. Results. According to our data, the frequency of multivisceral resections was comparable between the groups: 8 of 76 cases (10.5 %) for left hemicolectomy and 26 of 278 (9.4 %) for right hemicolectomy. The vast majority of operations in both groups were performed without a multiorgan component: 68 of 76 (89.5 %) and 252 of 278 (90.6 %), respectively. The differences were not statistically significant (χ2, p=0,930). Anastomotic leak was noted in 2.2 % of patients after right hemicolectomy and in 6.6 % after left hemicolectomy (p=0.033). Low preoperative albumin levels (OR 0.84; p=0.023) and the side of surgery (OR 0.30; p=0.033) were identified as independent predictors of the complication. ROC analysis demonstrated high predictive accuracy of the model (AUC=0.879). Conclusion. Right hemicolectomy is characterized by a lower incidence of anastomotic leak compared to left hemicolectomy. A low serum albumin level is a significant predictor of complications. This fact highlights the importance of preoperative assessment and correction of the patient's nutritional status.
Текст научной статьи Сравнительный анализ результатов резекции ободочной кишки по поводу колоректального рака в зависимости от стороны гемиколэктомии: данные Ульяновского областного клинического диспансера
Введение. Колоректальный рак (КРР) является одной из ведущих причин онкологической заболеваемости и смертности. В России КРР формирует около 10 % всей онкопатологии и занимает третье место в структуре онко- логической смертности, что подчеркивает приоритет совершенствования радикального хирургического лечения. Это подтверждается национальными сводками по онкостатистике и профильными российскими публикациями [1].
Несостоятельность межкишечного анастомоза (НМА) остается ключевым исходом гемиколэктомии по поводу колоректального рака и напрямую влияет на прогноз. При этом ряд работ показывает, что профили риска могут отличаться в зависимости от стороны оперативного вмешательства. По результатам многоцентрового исследования, включившего 1750 плановых колэктомий, частота развития несостоятельности после правосторонних резекций (1,35 %) была ниже, чем после левосторонних (5,20 %), что задает клинически значимую гипотезу для сравнения этих двух типов операций [2].
В крупных популяционных исследованиях доля правосторонних гемиколэктомий превышает долю левосторонних. Так, по данным анализа Nationwide Inpatient Sample, в США в 2007 г. из 50 799 онкологических колэктомий 63,5 % были правосторонними, а 36,5 % – левосторонними [3]. Схожая картина описана в европейских исследованиях. С 2010 по 2021 г. правосторонняя локализация рака встречалась у 58,7 % оперированных больных, что отражает «сдвиг вправо» при оперативном пособии [4].
Цель исследования. Сравнение частоты развития несостоятельности межкишечного анастомоза и структуры послеоперационных осложнений после правосторонней и левосторонней гемиколэктомии, а также определение независимых предикторов НМА у пациентов с колоректальным раком.
Материалы и методы. Было проведено ретроспективное исследование историй болезни 582 пациентов с КРР, проходивших лечение с 01.01.2019 по 01.12.2024 в хирургическом отделении абдоминальной онкологии ГУЗ Областной клинический онкологический диспансер (г. Ульяновск) [5].
Анализ медицинской документации проводился по единому разработанному протоколу.
В исследование включали пациентов с морфологически верифицированным злокачественным новообразованием толстой кишки, которым в плановом порядке выполняли левостороннюю или правостороннюю гемиколэк- томию либо резекцию сигмовидной кишки путем срединной лапаротомии с обязательной установкой брюшного дренажа для контроля состояния послеоперационной раны и раннего выявления осложнений.
Стадирование выполняли по 8-й редакции классификации TNM, а предоперационное обследование и периоперационное ведение осуществляли в соответствии с действующими клиническими рекомендациями Минздрава России [6].
В итоговый анализ включены 354 пациента, соответствующие критериям отбора. Участники были распределены на 2 группы по типу вмешательства: правосторонняя (n=278) и левосторонняя гемиколэктомия (n=76).
При поступлении всем больным выполняли антропометрию с расчетом ИМТ и осуществляли комплексную предоперационную оценку функционального статуса с помощью ЭКГ, эхокардиографии, спирометрии; при наличии сопутствующей патологии проводили консультации профильных специалистов, консультация кардиолога назначалась всем в целях стратификации кардиориска. При сниженной фракции выброса или аритмии назначали ХМ-ЭКГ, по клиническим показаниям – нагрузочные пробы (велоэргометрию). Для стратификации коморбидности рассчитывали индекс Charlson, послеоперационные осложнения оценивали по классификации Clavien – Dindo. Все пациенты проходили предоперационную консультацию анестезиолога. К операции допускались после достижения компенсации сопутствующих заболеваний.
Активизацию после хирургического вмешательства начинали с первых суток; питание – с жидкостей в первые сутки с последующим расширением по мере восстановления моторики. Дренаж удаляли на 3–4-е сут при минимальном отделяемом. Переливание крови или ее компонентов проводили строго по показаниям. НМА верифицировали по выделению кишечного содержимого по дренажу, лабораторным признакам воспаления и данным КТ брюшной полости. По показаниям выполняли повторное вмешательство в объеме, определяемом интраоперационно.
Оценка факторов, влияющих на риск раз- дели из анализа исключались предикторы с вития несостоятельности анастомоза, осу- корреляцией больше 0,75.
ществлялась с использованием многоуровне- Статистический анализ данных прово-вой логистической регрессии. Для предвари- дился с использованием программного обес-тельного анализа взаимосвязей между предик- печения R 4.2.2. и StatTech 4.1.2 (ООО «Стат-торами использовалась тепловая карта муль- тех», Россия).
тиколлинеарности. Она позволяет выявить Результаты. В анализ включены данные высокую корреляцию между переменными, 354 пациентов, перенесших правостороннюю которая может негативно сказаться на интер- (n=278) и левостороннюю (n=76) гемиколэкто-претации модели из-за эффекта мультиколли- мию. Остальные клинико-демографические неарности. Для повышения стабильности мо- показатели участников представлены в табл. 1.
Таблица 1 Table 1 Основные клинико-демографические показатели пациентов
Key Clinical and Demographic Parameters
|
Правосторонняя Левосторонняя Показатель Категория гемиколэктомия, n=278 гемиколэктомия, n=76 arame er a egory Right hemicolectomy, n=278 Left hemicolectomy, n=76 |
p |
|
Женский 175 (62,9) 45 (59,2) Пол, абс. (%) Female Sex, abs, (%) МMaуlжeской 103 (37,1) 31 (40,8) |
0,644 |
|
B И M М I Т , , k к g г / / m м 2 2,,MМeе((QQ11––QQ33)) 26,46 (23,46–30,10) 26,41 (23,29–30,71) |
0,803 |
|
СД, абс. (%) Нет / No 228 (82,0) 67 (88,2) DM, abs. (%) Да / Yes 50 (18,0) 9 (11,8) |
0,271 |
|
ГБ, абс. (%) Нет / No 145 (52,2) 44 (57,9) HT, abs. (%) Да / Yes 133 (47,8) 32 (42,1) |
0,448 |
|
ИБС, абс. (%) Нет / No 188 (67,6) 56 (73,7) CAD, abs. (%) Да / Yes 88 (31,7) 20 (26,3) |
0,429 |
|
ХСН, абс. (%) Нет / No 200 (71,9) 57 (75,0) CHF, abs. (%) Да / Yes 78 (28,1) 19 (25,0) |
0,701 |
Примечание. ИМТ – индекс массы тела, СД – сахарный диабет, ГБ – гипертоническая болезнь, ИБС – ишемическая болезнь сердца, ХСН – хроническая сердечная недостаточность.
Note. BMI – body mass index, DM – diabetes mellitus, HT – hypertension, CAD – coronary artery disease, CHF – chronic heart failure.
При межгрупповом сравнении исходных Значимые различия параметров опухоли клинико-демографических показателей стати- также не обнаружены (табл. 2).
стически значимых различий не выявлено.
Таблица 2
Table 2
Tumor Parameters
|
Показатель Parameter |
Категория Category |
Правосторонняя гемиколэктомия, n=278 Right hemicolectomy, n=278 |
Левосторонняя гемиколэктомия, n=76 Left hemicolectomy, n=76 |
p |
|
Стадия, n (%) Stage, n (%) |
I (T1N0M0) |
23 (8,3) |
6 (7,9) |
0,873 |
|
I (T2N0M0) |
21 (7,6) |
8 (10,5) |
||
|
IIA |
30 (10,8) |
7 (9,2) |
0,742 |
|
|
IIB |
12 (4,3) |
4 (5,3) |
||
|
IIC |
7 (2,5) |
4 (5,3) |
||
|
IIIA |
22 (7,9) |
7 (9,2) |
0,658 |
|
|
IIIB |
69 (24,8) |
18 (23,7) |
||
|
IIIC |
33 (11,9) |
8 (10,5) |
||
|
IVA |
38 (13,7) |
7 (9,2) |
0,911 |
|
|
IVB |
15 (5,4) |
5 (6,6) |
||
|
IVC |
8 (2,9) |
2 (2,6) |
||
|
Число удаленных лимфатических узлов, n, Ме (Q1–Q3) Number of removed lymph nodes, n, Me (Q1–Q3) |
19 (13–27) |
12 (8–19) |
0,287 |
|
Параметры опухоли
По нашим данным, частота мультивисце-ральных резекций в группах была сопоставимой: при левосторонней гемиколэктомии – 8 из 76 случаев (10,5 %), при правосторонней – 26 из 278 (9,4 %). Подавляющее большинство операций в обеих группах выполня-
лось без мультиорганного компонента – 68 из 76 (89,5 %) и 252 из 278 (90,6 %) соответственно. Различия не имели статистической значимости (χ2, p=0,930).
Анализ хирургических параметров представлен в табл. 3.
Таблица 3
Table 3
Surgical Parameters
|
Показатель Parameter |
Категория Category |
Правосторонняя гемиколэктомия, n=278 Right hemicolectomy, n=278 |
Левосторонняя гемиколэктомия, n=76 Left hemicolectomy, n=76 |
p |
|
Срок госпитализации, дней, Ме (Q₁–Q₃) Duration of hospitalization, days, Me (Q₁–Q₃) |
14 (11,00–16,00) |
14 (12,00–17,00) |
0,064 |
|
|
Время операции, мин, Ме (Q 1 –Q 3 ) Operation time, min, Me (Q1–Q3) |
120 (90,00–150,00) |
120 (90,00–142,50) |
0,666 |
|
|
Объем кровопотери, мл, Ме (Q 1 –Q 3 ) Volume of blood loss, ml, Me (Q1–Q3) |
200 (100,00–300,00) |
175 (100,00–325,00) |
0,639 |
|
|
Гемотрансфузия, абс. (%) Hemotransfusion, abs. (%) |
Нет / No |
245 (88,1) |
71 (93,4) |
0,266 |
|
Да / Yes |
33 (11,9) |
5 (6,6) |
||
Продолжительность госпитализации была сопоставимой, отмечалась лишь пограничная тенденция к большей длительности при левосторонних вмешательствах: 14 (12,00–17,00) против 14 (11,00–16,00) дней (p=0,064). По остальным ключевым хирургическим харак-
теристикам статистически значимых различий также не выявлено.
Распределение пациентов по степеням послеоперационных осложнений согласно классификации Clavien – Dindo представлено в табл. 4.
Таблица 4
Table 4
Оценка хирургических осложнений по классификации Clavien – Dindo Assessment of surgical complications according to the Clavien – Dindo classification
Несостоятельность межкишечного анастомоза была зарегистрирована в 6,6 % случаев после левосторонней гемиколэктомии (5 из 76) и в 2,2 % наблюдений после правостороннего вмешательства (6 из 278) (p=0,033; OR 0,30 (95 % ДИ 0,10–0,91)).
Анализ влияния стороны оперативного лечения как независимого фактора риска развития несостоятельности анастомоза осуществляли с применением многоуровневой логистической регрессии.
Предикторы для построения модели были отобраны по итогам оценки мультиколлинеарности с помощью тепловой карты на основе матрицы корреляций (рис. 1).
Бинарные показатели включены в анализ для оценки их влияния на количественные и категориальные. Исключение этих переменных может привести к потере значимой информации, особенно в случаях, когда их влияние взаимосвязано с другими предикторами (например нейтрофильно-лимфоцитарный индекс (NLR), альбумин или срок госпитализации).
Благодаря включению бинарных показателей карта мультиколлинеарности стала более полной и отражает их потенциальное взаимодействие с ключевыми физиологическими и клиническими параметрами.
|
Значение Value |
Правосторонняя гемиколэктомия, n=278 Right hemicolectomy, n=278 |
Левосторонняя гемиколэктомия, n=76 Left hemicolectomy, n=76 |
p |
|
Grade 0–I, абс. (%) |
228 (82,0) |
61 (80,3) |
0,986 |
|
Grade II, абс. (%) |
19 (6,8) |
6 (7,9) |
|
|
Grade IIIA, абс. (%) |
14 (5,0) |
5 (6,6) |
|
|
Grade IIIB, абс. (%) |
8 (2,9) |
2 (2,6) |
|
|
Grade IVA, абс. (%) |
6 (2,2) |
1 (1,3) |
|
|
Grade IVB, абс. (%) |
0 (0,0) |
0 (0,0) |
|
|
Grade V, абс. (%) |
3 (1,1) |
1 (1,3) |
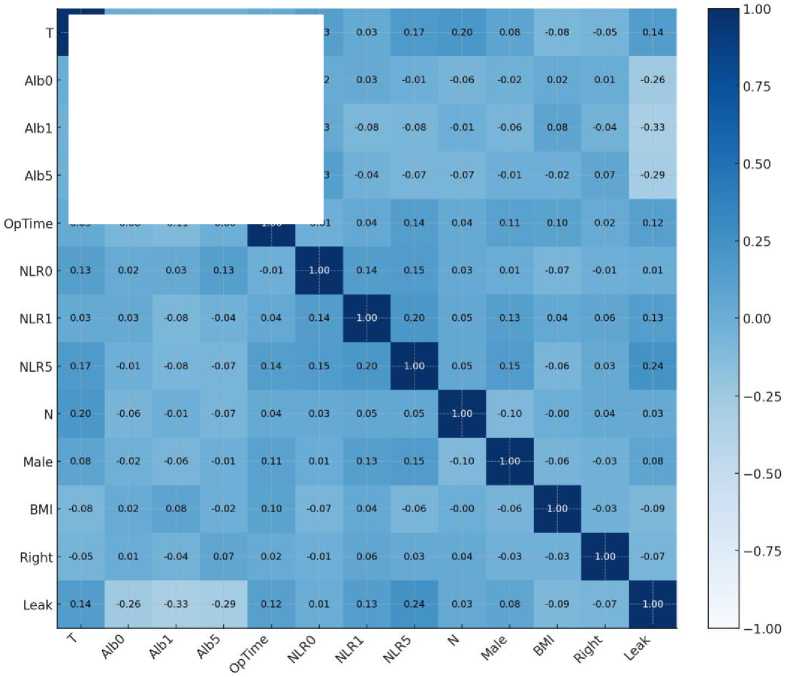
Рис. 1. Тепловая карта на основе матрицы корреляций
(T, N – категории по системе TNM (большее значение T соответствует большей глубине инвазии); Alb0, Alb1, Alb5 – уровни сывороточного альбумина (г/л) до операции, на 1-е и 5-е сут соответственно; OpTime – длительность операции (мин); NLR0, NLR1, NLR5 – нейтрофильно-лимфоцитарный индекс до операции, на 1-е и 5-е сут; Male – пол (1 – мужчина, 0 – женщина); BMI – индекс массы тела (кг/м2);
Right – сторона операции (1 – правосторонняя гемиколэктомия, 0 – левосторонняя гемиколэктомия); Leak – несостоятельность анастомоза (1 – да, 0 – нет); коэффициенты – парные корреляции Пирсона, рассчитанные по принципу pairwise complete observations (для каждой пары признаков использовались все доступные непустые наблюдения); знак коэффициента указывает направление связи, модуль – ее силу)
-
Fig. 1. Correlation matrix heatmap
(T, N – categories according to the TNM staging system (higher T values indicate greater depth of invasion); Alb0, Alb1, Alb5 – serum albumin levels (g/L): preoperative, postoperative day 1 (POD1), and postoperative day 5 (POD5), respectively; OpTime – operation time (min); NLR0, NLR1, NLR5 – neutrophil-to-lymphocyte ratio: preoperative, POD1, and POD5 respectively; Male – gender (1 – male, 0 – female); BMI – body mass index (kg/m2); Right – surgical site (1 – right hemicolectomy, 0 – left hemicolectomy); Leak – anastomotic leakage (1 – yes, 0 – no); coefficients represent Pearson pairwise correlation coefficients calculated using the pairwise complete observations method (all available non-empty observations were used for each pair of features); the sign of the coefficient indicates the direction of the relationship, while its absolute value represents its strength)
Табл. 5 представляет результаты многоуровневого логистического регрессионного анализа, проведенного для оценки факторов, влияющих на риск развития несостоятельности анастомоза.
Основной целью модели было выявление значимых предикторов осложнений с учетом возможных случайных эффектов возрастной
категории. В их числе оказались низкий до-операционный уровень альбумина: на каждый 1 г/л риск снижался (OR 0,84; 95 % ДИ 0,72–0,98; p=0,023)), и сторона операции: правосторонняя гемиколэктомия ассоциировалась с меньшей вероятностью несостоятельности по сравнению с левосторонней (OR 0,30; 95 % ДИ 0,10–0,91; p=0,033). Отме-
Таблица 5
Table 5
|
Показатель Parameter |
Coefficient |
Std. Error |
OR |
95 % ДИ (low –high) 95 % CI |
p-value |
|
T (категория) T (category) |
0,99 |
0,511 |
2,69 |
0,99–7,33 |
0,053 |
|
Альбумин до операции, г/л Albumin before surgery, g/l |
-0,173 |
0,076 |
0,84 |
0,72–0,98 |
0,023 |
|
Альбумин на 5 сут, г/л Albumin, Day 5, g/l |
-0,041 |
0,054 |
0,96 |
0,86–1,07 |
0,448 |
|
Время операции, мин Operation time, min |
0,005 |
0,005 |
1,0 |
1,00–1,01 |
0,322 |
|
NLR на 5-е сут NLR, Day 5 |
0,049 |
0,042 |
1,05 |
0,97–1,14 |
0,242 |
|
Альбумин на 1-е сут, г/л Albumin, Day 1, g/l |
-0,111 |
0,063 |
0,9 |
0,79–1,01 |
0,078 |
|
N (категория) N (category) |
-0,288 |
0,36 |
0,75 |
0,37–1,52 |
0,423 |
|
Пол (муж.) Sex (male) |
0,635 |
0,493 |
1,89 |
0,72–4,96 |
0,198 |
|
NLR на 1-е сут NLR, Day 1 |
0,037 |
0,021 |
1,04 |
1,00–1,08 |
0,081 |
|
NLR до операции NLR, before surgery |
-0,052 |
0,123 |
0,95 |
0,75–1,21 |
0,675 |
|
ИМТ, кг/м2 BMI, kg/m2 |
-0,054 |
0,053 |
0,95 |
0,85–1,05 |
0,309 |
|
Правосторонняя vs Левосторонняя Left vs Right |
-1,219 |
0,571 |
0,3 |
0,10–0,91 |
0,033 |
Хирургические параметры
чена пограничная тенденция к росту риска при увеличении категории T (OR 2,69; 95 % ДИ 0,99–7,33; p=0,053), а также для альбу-
мина на 1-е сут (p=0,078) и NLR на 1-е сут (p=0,081). Прочие переменные статистически значимого лияния не показали.
Результаты многомерной логистической регрессии
Results of Multivariate Logistic Regression
Для оценки качества модели была построена ROC-кривая (рис. 2).
Площадь под кривой (AUC) составила 0,879, что свидетельствует о хорошей предсказательной способности модели.
Таким образом, выявлена независимая связь: правосторонняя гемиколэктомия ассоциировалась с меньшей вероятностью развития
НМА по сравнению с левосторонней (OR 0,30; 95 % ДИ 0,10–0,91; p=0,033), как и более высокий дооперационный альбумин (OR 0,84 на 1 г/л; 95 % ДИ 0,72–0,98; p=0,023). Отмечены пограничные тенденции для более высокой категории T (p=0,053), альбумина на 1-е сут (p=0,078) и NLR на 1-е сут (p=0,081).
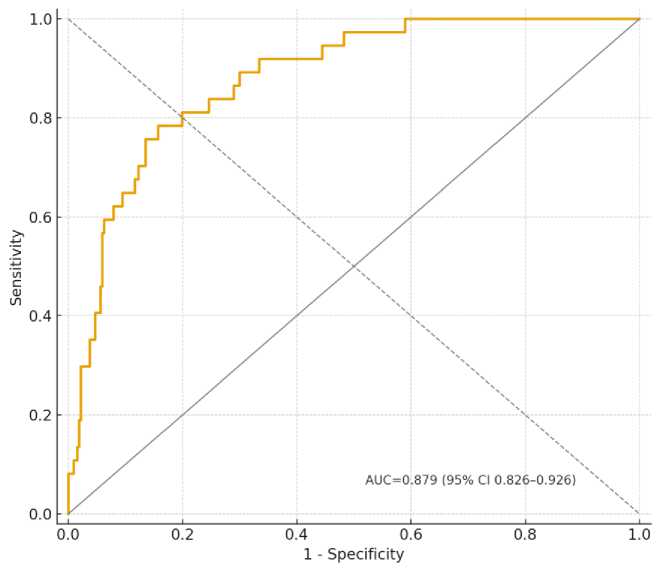
Рис. 2 . ROC-анализ модели
-
Fig. 2 . ROC analysis
Обсуждение. В наше исследование включены 354 пациента: правосторонняя гемиколэктомия выполнена у 278 (78,5 %) чел., левосторонняя – у 76 (21,5 %) чел. Такое распределение соответствует текущим эпидемиологическим трендам. В ретроспективных когортных исследованиях и обзорах последних доля правосторонних вмешательств стабильно выше, чем левосторонних. Это подтверждается свежими исследованиями иностранных коллег [7].
Данные литературы о связи стороны резекции и частоты несостоятельности межкишечного анастомоза неоднозначны. Так, Veyrie et al. на основе многоцентрового исследования, включившего 1 750 случаев, показали, что частота НМА была существенно ниже при правосторонней колэктомии (1,35 %, 7 из 520), чем при левосторонней (5,20 %, 64 из 1 230; p<0,0001) [2]. Однако другие работы демонстрируют более сбалансированные результаты. Например, австралийские коллеги заявляют, что частота НМА после правосторонней гемиколэктомии сопоставима с показателями при левосторонних резекциях и не выделяется как однозначно меньшая [8].
По нашим данным, частота развития несостоятельности межкишечного анастомоза зависела от стороны вмешательства: НМА была зарегистрирована у 6,6 % пациентов после левосторонней гемиколэктомии и у 2,2 % после правосторонней (p=0,033; OR 0,30 (95 % ДИ 0,10–0,91)).
30-дневная послеоперационная смертность была низкой и статистически не различалась между группами: 1,1 % (3 из 278) после правосторонней и 1,3 % (1 из 76) после левосторонней гемиколэктомии (p>0,05). Тяжелые осложнения (по классификации Clavien – Dindo – IVА–V) отмечены в 9 (3,2 %) случаях после правосторонних резекций и в 3 (3,9 %) случаях после левосторонних. Основными причинами тяжелых исходов являлись послеоперационная пневмония, острый коронарный синдром и септические осложнения, в т.ч. связанные с несостоятельностью анастомоза [9]. Стоит отметить, что развитие сепсиса остается одним из ключевых факторов неблагоприятных исходов у пожилых больных. В то же время стандартизированная диагностика и градация НМА, ранняя лабораторная стратификация и своевременное выявление НМА
способствуют снижению летальности при плановых операциях по поводу КРР [10].
Современные статистические подходы и методы проектирования клинических исследований позволяют более четко разграничить влияние стороны оперативного вмешательства и нутритивного статуса на результат лечения и влияние сопутствующих факторов, обеспечивая тем самым выявление действительно независимых предикторов несостоятельности анастомоза и неблагоприятных исходов [11]. В нашей многофакторной модели такими предикторами оказались низкий до-операционный уровень альбумина и левая сторона операции, что согласуется с данными современных исследований, где оба этих параметра рассматриваются как ключевые факторы риска развития НМА и повышения летальности [12].
В данной работе мы осознанно ограничили сравнение двумя основными типами гемиколэктомий – правосторонней и левосторонней. Такой подход позволяет исключить влияние анатомо-технических различий между сегментами ободочной кишки и обеспечить сопоставимость по объему и онкологической радикальности вмешательства. Включение сегментарных резекций или тотальных колэктомий привело бы к гетерогенности выборки: эти операции отличаются не только длиной резецируемого участка и васкуляриза-
цией, но и частотой формирования колоректального анастомоза, который имеет существенно более высокий риск развития несостоятельности. Сопоставление именно правой и левой гемиколэктомии позволяет анализировать пациентов с близкими показаниями и техниками вмешательства, что снижает селекционное смещение и делает группы более однородными по хирургическим параметрам, условиям анастомозирования и послеоперационному ведению.
Заключение. Правосторонняя гемиколэктомия сопровождалась достоверно меньшей частотой развития несостоятельности межкишечного анастомоза по сравнению с левосторонней (2,2 % против 6,6 %; p=0,033). Независимыми предикторами несостоятельности в многофакторной модели стали низкий доопе-рационный уровень сывороточного альбумина и левая сторона вмешательства. ROC-анализ показал высокую дискриминационную способность модели (AUC=0,879), что подтверждает надежность полученных результатов. Частота тяжелых осложнений и 30-дневная летальность оставались низкими и сопоставимыми между группами. Полученные данные подчеркивают значение оценки нутритивного статуса в предоперационном периоде и подтверждают более благоприятный профиль безопасности правосторонней гемиколэктомии при колоректальном раке.


