Сравнительный анализ результатов стереотаксической радиотерапии и резекции печени при солитарных метастазах рака толстой кишки в печени
Автор: Москаленко А.Н., Черных М.В., Сагайдак И.В., Малинина К.А., Магомедов М.М., Лядов В.К.
Журнал: Московский хирургический журнал @mossj
Рубрика: Онкология
Статья в выпуске: 2 (88), 2024 года.
Бесплатный доступ
Актуальность. Современный стандарт лечения при солитарных метастазах колоректального рака в печени - комбинация резекции печени и полихимиотерапии. При невозможности проведения хирургического лечения возможно применение стереотаксической радиотерапии (СРТ).Цель. Оценить результаты применения СРТ и резекции печени у пациентов с солитарными метастазами рака толстой кишки в печени.Материалы и методы. Выполнена ретро-проспективная оценка локального контроля (ЛК), общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП), частоты осложнений в группах хирургического и лучевого лечения. В группу СРТ вошло 26 больных, которым проводилась СРТ с медианой дозы 54 Гр. в 3 фракции. Резекции печени были выполнены 32 пациентам. Группы не имели статистически значимых различий по основным показателям.Результаты. Медиана наблюдения составила 33,6 мес. в группе СРТ и 30,5 мес. в группе хирургического лечения (p>0,05). Токсичности 2 степени и выше не отмечено. Показатель трехлетнего ЛК в группе СРТ достиг 64,2 % (95 %ДИ = 46-89,6 %) и 72,8 % (95 %ДИ = 56,7-93,6 %) в группе хирургии (р=0,53), медиана ЛК не была достигнута. Трехлетняя ОВ в группе СРТ составила 67,9 % (95 %ДИ = 50,8-90,7 %) и 64,4 % (95 % ДИ = 44,5-93,2 %) в группе хирургического лечения (р=0,85). Трехлетняя ВБП для группы СРТ составила 5,8 % (95 %ДИ = 3,9-8,7 %) с медианой 9,2 мес. и 15,6 % (95 %ДИ = 5,9-40,8 %) в группе хирургии с медианой 16,5 мес. (р=0,44). Статистически значимых различий между СРТ и резекцией печени в ЛК и ОВ не было.Заключение. При неоперабельных солитарных метастазах рака толстой кишки в печени СРТ может обеспечить ЛК и ОВ, сопоставимые с результатами хирургического лечения, при соблюдении режима гипофракционирования и СОД ≥ 51 Гр.
Стереотаксическая радиотерапия, рак толстой кишки, олигометастатическое поражение, солитарный метастаз, резекция печени
Короткий адрес: https://sciup.org/142241731
IDR: 142241731 | УДК: 616-006.66 | DOI: 10.17238/2072-3180-2024-2-44-51
Stereotactic body radiotherapy vs surgery in solitary colorectal cancer metastastases
Introduction. The standard of treatment for solitary metastases of colorectal cancer in the liver is a combination of liver resection and polychemotherapy. If surgery is not possible, stereotactic radiotherapy (SBRT) may be used.The purpose of the study. To evaluate the results of SBRT and liver resection in patients with solitary metastases of colon cancer in the liver.Materials and methods of research. Local control (LC), overall survival (OS), and progression-free survival (PFS), and the incidence of complications in the liver resection (n = 32) and SBRT (n = 26) groups were retrospectively assessed. The median dose was 54 Gy into 3 factions.Results. Median follow-up - 33.6 months. in the SBRT group and 30,5 months in the surgery group (p>0,05). No grade 3 toxicity was noted. Three-year LC in the CRT group reached 64,2 % (95 % CI = 46-89,6 %) and 72,8 % (95 % CI = 56,7-93,6 %) in the surgery group (p = 0,53), the median LC has not been reached. Three-year OS in the SBRT group was 67,9 % (95 % CI = 50,8-90,7 %) and 64,4 % (95 % CI = 44,5-93,2 %) in the surgical group (p = 0,85). The 3-year PFS for SBRT was 5,8 % with a median of 9,2 months and 15,6 % in the surgery group with a median of 16,5 months (p=0,44). There were no statistically significant differences between SBRT and liver resection in LC and OS.Conclusion. For solitary metastases of colon cancer in the liver, SBRT can provide results comparable to those of surgical treatment.
Текст научной статьи Сравнительный анализ результатов стереотаксической радиотерапии и резекции печени при солитарных метастазах рака толстой кишки в печени
Рак толстой кишки занимает 3 место (9,8 %) в структуре онкологической заболеваемости и 2 (9,2 %) место по смертности: в 2022 г. в мире выявлено более 1,85 млн пациентов и отмечено более 850 тысяч летальных исходов [1]. Отдаленные метастазы при этом заболевании диагностируют у 20–50 % пациентов, чаще всего в печени [2]. Больным с олигометастатическим поражением (1–5 метастазов в 1 или нескольких органах) показано применение комбинированного подхода к лечению, сочетающего локальные методы воздействия и проведение системной лекарственной терапии [3].
Комбинированное лечение в виде резекции печени в сочетании с системным противоопухолевым лечением позволяет достичь 5-летней общей выживаемости (ОВ) более чем у 40 % пациентов с олигометастатическим процессом и 71 % при наличии солитарного метастаза [4]. В то же время проведение радикальной резекции печени возможно лишь у 10–25 % пациентов в связи с особенностями расположения очагов, функциональным состоянием паренхимы или ее дефицитом после ранее выполненных операций, наличием тяжелых сопутствующих заболеваний [5]. В связи с этим активно развиваются различные варианты обеспечения локального контроля (ЛК) метастатических очагов в печени, одним из которых является стереотаксическая радиотерапия (СРТ). У большинства пациентов СРТ проводится в связи с невозможностью выполнения резекции печени, что делает затруднительным прямое срав- нение результатов этих методов лечения. Нами предпринята попытка сравнительной оценки онкологических результатов СРТ и резекции печени у отобранных по наиболее значимым клиническим параметрам пациентов. Учитывая ключевое значение числа опухолевых очагов для выживаемости пациентов [7], нами было принято решение оценить результаты лечения лишь у пациентов с солитарными метастазами в печени.
Материалы и методы
В ретро-проспективное исследование включено 58 пациентов с верифицированной аденокарциномой толстой кишки с солитарными синхронными или метахронными метастазами в печени. В группу лучевой терапии было включено 26 пациентов, которым проводилось лечение на базе ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России (n=14) и клиники ООО «ПЭТ-Технолоджи Подольск» (n=12) в 2018–2022 гг. В группу хирургического лечения вошли 32 пациента, которым выполнялись резекции печени на базе ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России (n=21) и ГБУЗ «ГКОБ1 ДЗМ» (n=11) в 2019–2020 гг.
В данное исследование были включены пациенты, прошедшие не более 2 линий ПХТ и не имевшие неконтролируемых внепеченочных метастазов. Ограничение по числу полученных линий ПХТ позволило исключить из исследования пациентов, имевших множественные эпизоды прогрессирования заболевания и, следовательно, имеющих худший прогноз по показа- телям выживаемости, с целью обеспечения сопоставимости групп сравнения.
Все больные в данном исследовании были предварительно обсуждены на междисциплинарном консилиуме. Пациенты, вошедшие в группу СРТ, были признаны неоперабельными в силу малого объема остатка печени после проведенного ранее оперативного лечения (n=17) или особенностей расположения метастатических очагов (n=9). Пациентам, соответствовавшим критериям операбельности и резектабельности, было проведено хирургическое лечение. Статистически значимых различий между группами пациентов в данном исследовании по ключевым клиническим параметрам не было (табл. 1).
Таблица 1
Основные клинико-эпидемиологические характеристики изученной группы пациентов
Patient characteristics
Table 1
|
Показатель/ Indicator |
СРТ / SBRT (n=26) |
Резекция печени / liver resection (n=32) |
p-value |
|
Пол: мужской / женский, (%) / Gender: male/female, (%) |
16/10 (61,5/38,5) |
12/20 (37,5/62,5) |
0,112 |
|
Средний возраст, лет ± стандартное отклонение (минимум-максимум) / Age, mean ± standart deviation (minimum-maximum) |
61,9±13,6 (30-84) |
63,9±8,8 (47-82) |
0,778 |
|
ECOG, n (%) |
0,891 |
||
|
0 |
1 (3,8) |
3 (9,4) |
|
|
1 |
21 (80,8) |
24 (75) |
|
|
2 |
4 (15,4) |
5 (15,6) |
|
|
Число линий ПХТ до начала лечения (%) / Сhemotherapy lines before treatment (%) |
|||
|
1 |
22 (84,6) |
21 (65,6) |
0,135 |
|
2 |
4 (15,4) |
11 (34,4) |
|
|
Т первичной опухоли (%) / T of primary tumor (%) |
|||
|
3 |
17 (65,4) |
21 (65,6) |
1 |
|
4 |
9 (34,6) |
11 (34,4) |
|
|
N первичной опухоли (%) / N of primary tumor (%) |
|||
|
0 |
10 (38,5) |
13 (40,6) |
0,839 |
|
1 |
11 (42,3) |
11 (34,4) |
|
|
2 |
5 (19,2) |
8 (25,0) |
|
|
Степень дифференцировки первичной опухоли (%) / Grаde of primary tumor (%) |
0,581 |
||
|
1 |
2 (7,7) |
5 (15,6) |
|
|
2 |
19 (73,1) |
23 (71,9) |
|
|
3 |
5 (19,2) |
4 (12,5) |
|
|
Наличие мутации в генах системы RAS (%) / RAS mutation (%) |
|||
|
нет/ no |
18 (69,2) |
18 (56,2) |
0,416 |
|
да/ yes |
8 (30,8) |
14 (43,2) |
|
|
Средний размер очага, см (минимум-максимум) / Average lesion size, sm (minimum-maximum) |
2,7±1,4 (1 – 6,5) |
3,1±1,7 (0,9-6,8) |
0,429 |
Продолжение Таблицы 1
|
Предшествовавшее локальное лечение метастаза/ов в печени, да/нет (%) / Previous local treatment of liver metastases, yes/no (%) |
15/11 (57,7/42,3) |
14/18 (43,8/56,2) |
0,428 |
|
Внепеченочные метастазы в анамнезе, да/нет (%) / Extrahepatic metastases, yes/no (%) |
7/19 (26,9 /73,1) |
10/22 (31,2/68,8) |
0,778 |
|
Синхронные / метахронные метастазы на момент дебюта болезни (%) / initially synchronous / metachronous metastases (%) |
14/12 (53,8/46,2) |
18/14 (56,3/43,7) |
0,9 |
У всех пациентов, включенных в данное исследование, первичная опухоль была удалена в объеме R0 до начала лечения метастазов.
Все больные в данном исследовании получили как минимум 1 линию ПХТ. Резекции печени на предыдущих этапах лечения проводились 15 (57,7 %) больным в группе СРТ и 14 (43,8 %) пациентам в группе хирургического лечения.
В группе СРТ внепеченочные очаги имелись у 7 (26,9 %) пациентов: у 4 больных ранее были проведены резекции легкого по поводу солитарных метастазов, у 3 пациентов отмечалась стабилизация после СРТ солитарных очагов в легком, забрюшинном лимфатическом узле, теле 5 поясничного позвонка, соответственно. В группе хирургического лечения у 10 (31,2 %) пациентов ранее были выполнены резекции легкого по поводу солитарного метастаза.
СРТ проводилась в режиме гипофракционирования с достижением СОД от 40 до 60 Гр. на очаг в 1–5 фракций с медианой 54 Гр. в 3 фракциях.
СРТ проводилась на ускорителе электронов Varian Clinac 2300 iX с применением трёхмерного планирования, многолепесткового коллиматора Milenium 120 и динамических клиновидных фильтров энергией фотонов 6 МэВ. Для исключения влияния дыхательных движений применялась технология проведения лучевой терапии с задержкой дыхания на вдохе под контролем системы RPM (Real-time Position Management). Предлучевая подготовка проводилась на спиральном компьютерном томографе GE Light Speed с последующим совмещением данных топометрической компьютерной томографии и магнитно-резонансной томографии с применением технологии Fusion для выбора объёмов облучения. Верификация плана дистанционной лучевой терапии проводилась с использованием технологии компьютерной томографии в коническом пучке и рентгеновских снимков в киловольтном пучке на ускорителе Clinac 2300iX. Укладка пациента производилась с помощью индивидуального фиксирующего средства.
Объем резекции печени определялся на основании данных предоперационного КТ или МРТ органов брюшной полости с внутривенным болюсным контрастированием и окончательно утверждался в соответствии с данными интраоперационной ревизии и интраоперационного ультразвукового исследования печени. Было выполнено 24 (75 %) атипичных резекции печени, 3 (9,3 %) сегментэктомии и 5 (15,7 %) гемигепатэктомий. У 12
(28 %) пациентов операция выполнялась лапароскопическим доступом.
Конечными точками исследования были: частота осложнений, постлучевая токсичность, ЛК, ОВ, выживаемость без прогрессирования (ВБП). После проведения локального воздействия на метастазы пациентам проводилось динамическое наблюдение: КТ или МРТ органов брюшной полости с внутривенным болюсным контрастированием 1 раз в 3 месяца. ЛК оценивался согласно критериям EORTC-RECIST 1.1[6]. Токсичность оценивалась согласно общим терминологическим критериям для нежелательных явлений (CTCAE) 5.0 [7]. Послеоперационные осложнения оценивались согласно критериям Dindo-Clavien [8].
При отсутствии прогрессирования пациентам продолжалось динамическое наблюдение, при прогрессировании проводили ПХТ, реже при олигопрогрессировании рассматривались варианты локального воздействия.
Оценка ЛК, ОВ и ВБП проведена методом Каплана-Майера. Для анализа влияния клинических факторов на ЛК, ОВ и ВБП использована модель пропорциональных рисков Кокса. Уровень значимости равнялся 0,05.
Статистическая обработка результатов проведена в программной среде R (версия 4.1.1) с использованием пакетов survival, survminer и ggplot2.
Результаты
В группе лучевой терапии у 3 (17 %) больных наблюдалась токсичность 1 степени по CTCAE 5.0, проявлявшаяся в виде тошноты и общего недомогания. Токсичности 2 степени и выше отмечено не было.
В группе хирургического лечения средняя продолжительность операции составила 197±24 минут при средней кровопотере 404±30 мл. Осложнения в послеоперационном периоде развились у 5 (15,6 %) пациентов: внутрибрюшные жидкостные скопления, потребовавшие пункционного дренирования у 4 (12,5 %) больных, раневая инфекция у 1 (3,1 %) больного. Летальности в послеоперационном периоде не было. Резекция R1 по данным гистологического исследования была выполнена у 1 (3,1%) больного.
Медиана наблюдения составила 33,6 мес. в группе лучевой терапии и 30,5 мес. в группе хирургического лечения (р>0,05).
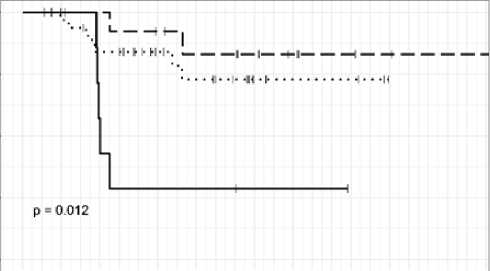
Показатель трехлетнего ЛК в группе СРТ достиг 64,2 % (95 % ДИ = 46–89,6 %) и 72,8 % (95 % ДИ = 56,7–93,6 %) в группе хирургического лечения, медиана ЛК не была достигнута, различие не было статистически значимым (р=0,53). Исходя из анализа кривых Каплана-Майера, можно отметить, что локальные рецидивы опухоли происходили на протяжении первого года после проведения лечения и уровень ЛК в обеих группах вышел на плато на втором году наблюдения. При исключении из анализа 12 пациентов, получивших СД ≤ 50 Гр, показатель ЛК в группе СРТ достигает 86,2 % (рис. 1).
1«'
— СРТ £50Гр Ч- СРТ, 251 Гр «һ Хирургия
075'
050'
0 2 4 • е 10 12 14 15 18 20 22 24 26 2« 30 32 М 36 М 40 42 *4 46 48
Орсын, месяцы
Рис. 1. Уровень ЛК при солитарных метастазах
Fig. 1. LC level in solitary metastases
Показатель трехлетней ОВ в группе СРТ составил 67,9 % (95 % ДИ = 50,8–90,7 %) и 64,4% (95 % ДИ = 44,5–93,2 %) в группе хирургического лечения. Показатель трехлетней ВБП для группы СРТ составил 5,8 % (95 % ДИ = 3,9–8,7 %) с медианой 9,2 мес. и 15,6 % (95 % ДИ = 5,9–40,8 %) в группе хирургического лечения с медианой 16,5 мес. Статистически значимых различий за период наблюдения по показателям ОВ и ВБП выявлено не было (рис. 3–4), хотя и отмечена тенденция к более раннему системному прогрессированию в группе СРТ.
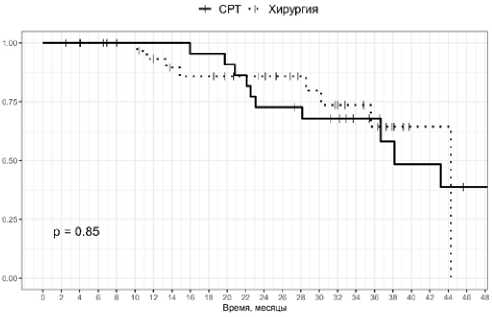
Рис. 2. ОВ для солитарных метастазов
Fig. 2. OS in solitary metastases
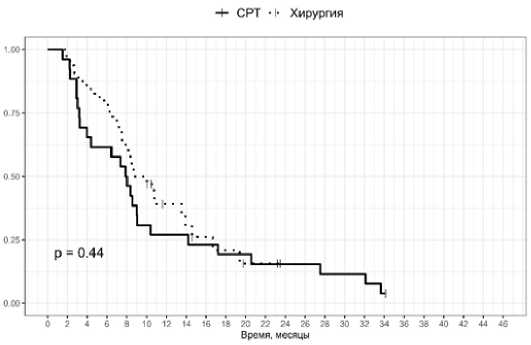
Рис. 3. ВБП для солитарных метастазов Fig. 3. DFS in solitary metastases
При проведении однофакторного анализа с целью поиска предикторов показателей ЛК, ОВ и ВБП установлено повышение вероятности нарушения ЛК у пациентов, ранее перенесших резекцию печени: ОШ 1,47 (95 % ДИ 0,65–2,268), р=0,023. Также было установлено повышение вероятности прогрессирования у пациентов с метастатическим поражением регионарных лимфатических узлов первичной опухоли (N1–2 против N0): ОШ 2,19 (95 % ДИ 1,06–4,5), р=0,03. Дальнейший многофакторный анализ не проводился в связи с отсутствием достаточного количества наблюдений.
Обсуждение
Комбинированная терапия, включающая резекцию печени и ПХТ, является наиболее эффективным лечебным подходом у больных с резектабельными и потенциально резектабельными метастазами рака толстой кишки в печени [2, 3]. При невозможности проведения хирургического лечения СРТ может применяться в качестве метода локального контроля.
Нами в 2023 г. был проведен анализ результатов применения СРТ (n=62) и резекции печени (n=83) у пациентов с олигометастазами рака толстой кишки в печени, показавший преимущество хирургического метода лечения перед лучевой терапией у данной группы больных. Показатель двухлетнего ЛК составил 62 % в группе СРТ и 80 % в группе хирургии (p=0,019), а двухлетняя OВ составила 69,5 % в группе СРТ и 84,7 % в группе хирургии (p=0,03). Однако группы исследования статистически значимо различались по числу предшествующих линий ПХТ, количеству и размерам метастазов, наличию внепеченочных метастазов [9]. Тем не менее были выявлены некоторые прогностические предикторы. Так, суммарная доза облучения ≥ 51 Гр. явилась значимым фактором улучшения ЛК, в то время как размер метастаза более 3 см служил негативным фактором для ОВ. С целью дальнейшей оценки возможностей СРТ метастазов рака толстой кишки в печени и индивидуализации показаний к ее проведению было принято решение провести сравнительный анализ данного метода и резекции печени у сопоставимых групп пациентов с солитарными метастазами колоректального рака в печени, прошедших не более 2 линий ПХТ.
В доступной нам литературе удалось найти единственное зарубежное исследование, в котором напрямую сравнивалась СРТ и резекция печени. Исследование Roman и соавт. 2019 г. [10] включало 90 больных, которые были разделены на группы хирургии (n=55) и СРТ (n=45). Анализ показал отсутствие достоверных различий в однолетней ОВ в группе СРТ (86,1 %) и хирургии (88,7 %). Однако при сроке наблюдения в 3 года ОВ в группе СРТ составила 21,2 % против 60,9 % в группе хирургии. Стоит отметить, что в данном исследовании не была выделена группа солитарных метастазов и не оценивался показатель ЛК, а также не представлены данные по различиям между группами по степени предлеченности пациентов.
Наиболее актуальный на данный момент мета-анализ за авторством Petrelli включал 18 исследований и 656 больных, которым проводилась СРТ по поводу олигометастазов колоректального рака в печени. Однолетняя ОВ составила 67 % (95 % ДИ = 42,1 – 92,2 %), медиана ОВ – 31,5 месяцев. Показатель однолетнего локального контроля составил 67 % (95 % ДИ = 43,8 –90,2 %). Частота токсических реакций 3 степени и выше по CTCAE составила 8,5 % [11]. Данные нашего исследования соответствуют этим результатам. Обращает на себя внимание, что в исследуемой нами группе пациентов не было отмечено тяжелых постлучевых реакций несмотря на высокую медиану СОД 54 Гр. в 3 фракциях.
Нами не было найдено отдельных исследований, посвященных применению СРТ при солитарных очагах в печени, однако многие авторы, включая крупное исследование Mahadevan и соавт. (213 больных), отмечают статистически значимое улучшение результатов СРТ при уменьшении числа очагов [12]. В определенной степени можно рассматривать в качестве сопоставимых по дизайну исследования, посвященные сравнению результатов радиочастотной абляции и резекции печени. Так, Meijerink и соавт. [13] в 2018 г. провели систематический обзор и мета-анализ данных 48 сравнительных исследований у пациентов с различным числом метастазов. Было показано преимущество резекции печени по выживаемости, однако у отобранной категории больных с небольшими единичными метастатическими очагами в печени при достижении А0 статуса показатели выживаемости могли быть сопоставимы с результатами хирургии.
При анализе полученных результатов обращают на себя внимание отличия нашей группы пациентов от больных, изученных в зарубежных исследованиях СРТ метастазов в печени. Так, в большинстве опубликованных работ пациенты до проведения СРТ получали несколько линий лекарственной терапии. Например, по данным Clerici и соавт., более 2 линий химиотерапии получили 55 % больных [14]. Частота предшествующего хирургического лечения в зарубежных исследованиях составляет 10–60 % против 70,6 % в нашей когорте пациентов [15]. Мы считаем, что отсутствие статистически значимых различий показателей выживаемости в нашем исследовании при достаточной медиане наблюдения (33,6 мес. в группе СРТ и 30,5 мес. в группе хирургии) может быть обусловлено именно тем, что для сравнения были отобраны сопоставимые по степени предлеченности пациенты.
За время наблюдения локальный рост опухоли после СРТ произошел у 7 пациентов. С нашей точки зрения у 5 больных это связано преимущественно с недостаточно интенсивным режимом СРТ, при котором не было достигнуто БЭД 100 Гр. Данное значение рассматривается Petrelli и соавт. в качестве порогового показателя, определяющего высокую вероятность эффективного ЛК [11]. У оставшихся 2 пациентов предикторами развития локального рецидива были размер метастаза более 3 см и наличие мутации в генах системы RAS.
В группе хирургического лечения локорегионарный рецидив за время наблюдения отмечен у 4 пациентов. У 2 из них размер метастатического очага превышал 5 см. Следует отметить, что несмотря на выполение значительной по объему резекции печени (в первом случае гемигепатэктомия справа, во втором – анатомическая резекция 2 и 3 сегментов печени) и отрицательный край резекции, расстояние от опухолевого узла до линии резекции у обоих пациентов составляло менее 5 мм. Еще у 2 пациентов, перенесших атипичные резекции 7 и 8 сегментов печени, соответственно, хирургический край резекции также составил < 1 см. У 2 из 4 пациентов также были выявлены мутации в генах системы RAS.
Очевидными недостатками нашего исследования являются его ретроспективный характер и малый объем выборки, однако мы считаем, что полученные данные все же позволяют сформировать мнение о высокой безопасности и значительной эффективности СРТ у больных с солитарными метастазами колоректального рака в печени, не подлежащих хирургическому лечению.
Заключение
При неоперабельных солитарных метастазах рака толстой кишки в печени СРТ может обеспечить показатели локального контроля и выживаемости, сопоставимые с результатами хирургического лечения, при соблюдении режима гипофракционирования и СОД ≥ 51 гр.
Список литературы Сравнительный анализ результатов стереотаксической радиотерапии и резекции печени при солитарных метастазах рака толстой кишки в печени
- Chhikara B.S. and Parang K. Global Cancer Statistics 2022: the trends projection analysis. Chemical Biology Letters, 2023, № 10, рр. 451.
- Adam R., De Gramont A., Figueras J. et al. The oncosurgery approach to managing liver metastases from colorectal cancer: a multidisciplinary international consensus. The Oncologist, 2012, № 17, рр. 1225-1239.
- Nordlinger B., Van Cutsem E., Rougier P. et al. Does chemotherapy prior to liver resection increase the potential for cure in patients with metastatic colorectal cancer? A report from the European Colorectal Metastases Treatment Group. Eur J Cancer, 2007, № 43, рр. 2037-2045.
- Aloia T.A., Vauthey J.N., Loyer E.M. et al. Solitary colorectal liver metastasis: resection determines outcome. ArchSurg, 2006, May, № 141(5), рр. 460-466.
- Adam R., De Gramont A., Figueras J. et al. Managing synchronous liver metastases from colorectal cancer: a multidisciplinary international consensus. Cancer Treatment Reviews, 2015, № 41, рр. 729-741
- Guenther L.M., Rowe R.G., Acharya P.T. et al. Response Evaluation Criteria in Solid Tumors (RECIST) following neoadjuvant chemotherapy in osteosarcoma. Pediatr Blood Cancer, 2018, Apr; № 65(4).
- Freites-Martinez A., Santana N., Arias-Santiago S., Viera A. Using the Common Terminology Criteria for Adverse Events (CTCAE - Version 5.0) to Evaluate the Severity of Adverse Events of Anticancer Therapies. ActasDermosifiliogr (Engl Ed), 2021, Jan; № 112(1), рр. 90-92.
- ClavienP.A., BarkunJ., DindoD. TheClavien-Dindo classification of surgical complications: five-yearexperience. Ann Surg., 2009, Aug; № 250(2), рр. 187-196.
- Москаленко А.Н., Лядов В.К., Черных М.В., Сагайдак И.В., Ищанов Д.Г., Гарипов М.Р., Галкин. Сравнительный анализ применения стереотаксической лучевой терапии и хирургического лечения при олигометастазах рака толстой кишки в печени. Практическая онкология, 2023. Т. 24, № 1. С. 48-58.
- Roman J., Vávra P., Ekrtová T. Comparison of surgical intervention to Cyberknife radiotherapy in the treatment of liver malignancies. RozhlChir., 2019, № 98(10), рр. 408-413.
- Petrelli F., Comito T., Barni. SBRT for CRC liver metastases. Stereotactic body radiotherapy for colorectal cancer liver metastases: A systematic review. RadiotherOncol., 2018, Dec; № 129(3),427-434.
- Mahadevan A., Andrew M. Gaya, Rachelle Marie Lanciano. Stereotactic body radiotherapy (SBRT) for colorectal liver metastasis: Clinical outcomes from the international multi-institutional RSSearch Patient Registry. Mahadevan. Journal of ClinicalOncology, 2019, № 37, рр. 15
- Meijerink M.R., Puijk R.S., van Tilborg A.A.J.M. Radiofrequency and Microwave Ablation Compared to Systemic Chemotherapy and to Partial Hepatectomy in the Treatment of Colorectal Liver Metastases: A Systematic Review and Meta-Analysis. Cardiovasc Intervent Radiol., 2018, № 41(8), рр. 1189-1204.
- Clerici E., Comito T., Franzese C. Role of stereotactic body radiation therapy in the treatment of liver metastases: clinical results and prognostic factors. Strahlenther Onkol., 2020, Apr; № 196(4), рр. 325-333.
- Scorsetti M., Comito T., Tozzi A. Final results of a phase II trial for stereotactic body radiation therapy for patients with inoperable liver metastases from colorectal cancer. J Cancer Res Clin Oncol., 2015, Mar; № 141(3), рр. 543-553.


