Стабилизация сино-тубулярного соединения как эффективный способ коррекции аортальной недостаточности у пациентов с аневризмой восходящей аорты
Автор: Панфилов Д.С., Софронов А.В., Козлов Б.Н.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 2 т.39, 2024 года.
Бесплатный доступ
Введение. Аортальная недостаточность, обусловленная дилатацией зоны сино-тубулярного соединения как результат аневризмы восходящего отдела аорты, требует сочетанной хирургической коррекции. Недостаточное количество исследований, посвященных этой проблеме, побуждает к проведению анализа данных.Цель исследования: оценка ранних и среднесрочных результатов стабилизации сино-тубулярного соединения в ходе протезирования восходящей аорты у пациентов с аневризмой восходящей аорты и умеренной аортальной недостаточностью.Материал и методы. В ретроспективной анализ были включены 57 пациентов с аневризмой восходящей аорты и аортальной недостаточностью, оперированных в период с января 2011 по январь 2024 гг. Пациенты были разделены на 2 группы в зависимости от степени аортальной регургитации: группа 1 включила пациентов с аортальной регургитацией 1-й степени («Ао рег 1»), группу 2 сформировали пациенты с аортальной недостаточностью менее 2-й степени («Ао рег 2»). Были проанализированы ранние и отсроченные послеоперационные результаты обсуждаемых пациентов.Результаты. В течение госпитального периода не отмечено значимых межгрупповых различий по частоте необратимого и преходящего неврологического дефицита, частоте дыхательной недостаточности, острого повреждения почек, кровотечения и летальности. В сроки до 2 лет в группе «Ао рег 1» выживаемость составила 100%, а в группе «Ао рег 2» - 87,4%. В обеих группах зарегистрировано снижение объемных показателей левого желудочка с одновременным уменьшением размеров аорты на всех исследуемых уровнях в послеоперационном периоде. В течение всего периода наблюдения ни в одном случае не было установлено возврата или увеличения степени аортальной регургитации. Не было потребности в повторном вмешательстве на проксимальных отделах аорты.
Аневризма восходящей аорты, аортальная недостаточность, сино-тубулярное соединение
Короткий адрес: https://sciup.org/149145658
IDR: 149145658 | УДК: 616.13-007.64:616.126.32-089.844 | DOI: 10.29001/2073-8552-2024-39-2-69-77
Sino-tubular junction stabilization as an viable approach for aortic insufficiency in ascending aortic aneurysms
Introduction. Aortic insufficiency caused by ascending aortic aneurysm with concomitant dilation of the sino-tubular junction requires combined surgery. To date there is a lack of relevant papers.Aim: To analyze early and mid-term outcomes in patients undergoing ascending aortic replacement with sino-tubular junction stabilization for aortic insufficiency.Methods. The retrospective study included 57 patients with ascending aortic aneurysm and aortic insufficiency who underwent aortic replacement from December 2011 to January 2024. All patients were stratified into 2 groups according to aortic regurgitation (AR) grade: 1st group included patients with 1 grade, 2d group - patients with 2 grade. We analyzed clinical early and mid-term outcomes.Results. There were no significant differences in neurological, pulmonary, renal complications as well as bleeding and mortality in the early postoperative period. Mid-term survival was 100% and 87.4% in the AR 1 grade and AR 2 grade, respectively. In both groups, the volumetric parameters of the left ventricle and size of the aorta at all levels studied were decreased in the postoperative period. There were no patients with recurrent or increased aortic insufficiency. No patient required proximal aortic reoperation.Conclusion. Ascending aortic replacement with concomitant sino-tubular junction stabilization without additional aortic cusp repair and/or aortic root surgery is a safe and durable procedure providing reduce the aortic insufficiency regurgitation grade.
Текст научной статьи Стабилизация сино-тубулярного соединения как эффективный способ коррекции аортальной недостаточности у пациентов с аневризмой восходящей аорты
Аортальная недостаточность встречается в 5–20% случаев и характеризуется нарушением запирательной функции аортального клапана, которая при отсутствии лечения приводит к тяжелой систолической дисфункции [1, 2].
Согласно данным литературы, изолированная аортальная недостаточность зачастую обусловлена структурными изменениями створок (перфорация створок вследствие инфекционного эндокардита, атеросклеротическое поражение) или функциональным состоянием (моно-, би- и квадрикуспидальный аортальный клапан) [3]. В то же время аортальная недостаточность при аневризмах восходящей аорты нередко является следствием дилатации одного из структурно-анатомических компонентов корня аорты: базального кольца, синусов Вальсальвы или сино-тубулярного соединения [4].
Среди вариантов хирургической коррекции аортальной регургитации у пациентов с расширенными синусами Вальсальвы и увеличенным диаметром фиброзного кольца выделяют в первую очередь реимплантацию аортального клапана (процедура David), а также раз- личные клапаносохраняющие операции, предложенные M.H. Yacoub и соавт. [5], E. Lansac и соавт. [6]. Указанные методики хирургической реконструкции корня аорты хорошо зарекомендовали себя и характеризуются устойчивым эффектом в отношении восстановления нормальной функции аортального клапана. При этом крайне недостаточно работ, анализирующих эффективность коррекции аортальной недостаточности, обусловленной дилатацией сино-тубулярного соединения при неизмененном корне аорты и интактных створках аортального клапана.
Цель исследования: анализ ранних и среднесрочных результатов стабилизации сино-тубулярного соединения в ходе протезирования восходящей аорты у пациентов с аневризмой восходящей аорты и умеренной аортальной недостаточностью.
Материал и методы
С января 2011 по январь 2024 гг. были прооперированы 446 пациентов с патологией грудной аорты. Из анализа были исключены пациенты с расслоением аорты любого типа, аневризмой одного или нескольких сину- сов Вальсальвы, пациенты с аортальным стенозом или недостаточностью более 2-й степени, а также повторно оперированные пациенты. Показаниями для стабилизации сино-тубулярного соединения были: нерасширенное фиброзное кольцо аортального клапана (< 27 мм) и синусов Вальсальвы (< 50 мм), центральная аортальная регургитация, отсутствие или минимальные дегенеративные изменения створок аортального клапана (небольшие фенестрации, незначительный фиброз / склероз, отсутствие кальцинатов). Окончательное решение о выборе варианта хирургического вмешательства принималось интраоперационно, исходя из текущей ситуации.
Таким образом, был проведен ретроспективный анализ 57 пациентов, соответствующих критериям включения. Анализируемые пациенты были разделены на 2 группы в зависимости от степени аортальной регургитации: группа 1 включила пациентов с аортальной регургитацией 1-й степени («Ао рег 1»), группу 2 сформировали пациенты с аортальной недостаточностью более 1-й, но менее 2-й степени («Ао рег 2»). Дизайн исследования представлен на рисунке 1.
В ходе исследования было выполнено межгрупповое сравнение данных пациентов на до-, интра- и послеоперационном этапах.
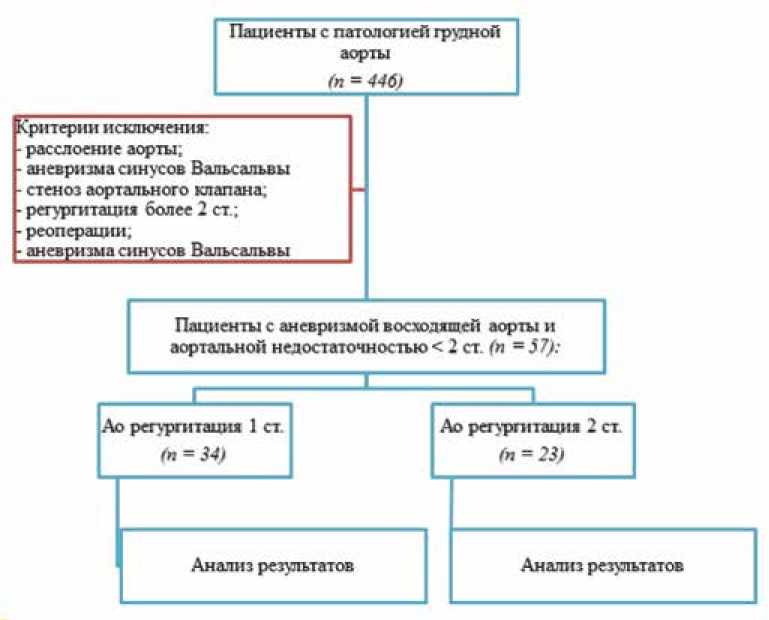
Рис. 1. Дизайн исследования
Fig. 1. Study design
Конечные точки
Первичной комбинированной конечной точкой был возврат исходной аортальной недостаточности или увеличение ее степени. В качестве вторичных конечных точек были выбраны выживаемость и необходимость в повторном вмешательстве на аортальном клапане по поводу аортальной недостаточности.
Хирургическая техника
Во всех случаях операцию проводили через срединную стернотомию в условиях легкой гипотермии (28–30 °C), циркуляторного ареста с антеградной церебральной перфузией через брахиоцефальный ствол. По достижении целевой температуры инициировали циркуляторный арест нижней части тела с антеградной перфузией головного мозга. Дистальный аортальный анастомоз формировали с использованием техники открытого анастомоза с резекци- ей малой кривизны дуги аорты от основания безымянной артерии до проекции устья левой подключичной артерии.
По завершению анастомоза возобновляли искусственное кровообращение с последующим согреванием пациента. Проксимальный аортальный анастомоз формировали на уровне сино-тубулярного соединения. Стабилизацию сино-тубулярного соединения с одновременной его редукцией достигали путем выбора меньшего по диаметру аортального протеза по отношению к диаметру аорты на уровне сино-тубулярного соединения. Размер протеза аорты варьировал в пределах 28–32 мм.
Для формирования аортального анастомоза преимущественно использовали непрерывный обвивной шов. В ряде случаев использовали комбинированную технику сосудистого шва, включающего непрерывный матрасный и обвивной шов. При наличии показаний выполняли аутовенозное и/или аутоартериальное аортокоронарное шунтирование.
Инструментальное обследование
Эхокардиография
Эхокардиографические показатели оценивались трансторакально на ультразвуковых системах «Siemens Acuson Sequoia 512». До и после операции анализировали объемные размеры левого желудочка в систолу и диастолу (конечный диастолический и конечный систолический объемы). Сократительную функцию левого желудочка определяли по значению фракции выброса.
Мультиспиральная компьютерная томография
Измерения проводили с помощью компьютерной томографической ангиографии в ЭКГ-синхронизированном режиме, используя 64-срезовый сканер Discovery NM-CT 570c (GE Healthcare, Милуоки, Висконсин, США) с пространственным разрешением ангиографической фазы в диапазоне от 0,6 до 1,25 мм. Сбор данных осуществляли в бесконтрастном, контрастном режимах и в отсроченной артериальной фазе. Все измерения проводили в плоскости, перпендикулярной центральной линии аорты по внешним контурам стенки аорты. Диаметр корня аорты определяли как максимальный размер между синусами Вальсальвы. Диаметр сино-тубулярного соединения измеряли на уровне вершины створок аортального клапана в зоне комиссур. Максимальный диаметр восходящей аорты определяли на уровне бифуркации легочной артерии. Диаметр дуги аорты измеряли в проксимальном отделе, не доходя 1 см до устья брахиоцефального ствола. Анализ и оценка изображений были основаны на консенсусе двух опытных исследователей.
Наблюдение за пациентами
Все клинические данные были собраны до операции, на интраоперационном этапе, а также в раннем и среднесрочном послеоперационном периодах. В отсроченном периоде наблюдения сбор данных осуществлялся на основании визитов пациентов в стационар с проведением инструментальных обследований, включая трансторакальную эхокардиографию, мультиспиральную компьютерную томографию аорты. При невозможности госпитализации в стационар данные обследования пациентов были получены из копий медицинских обследований, заключений проведенных обследований. Средний период наблюдения за пациентами составил 7,5 [3,5; 11,5] мес. (диапазон 1–95).
Статистический анализ
Статистическую обработку данных проводили с помощью пакетов программ: STATISTICA 13.0, R 3.3.1, Medcalc 14.8.1. Нормальность закона распределения количественных показателей проверяли с помощью критерия Шапиро – Уилка. Параметры, подчиняющиеся нормальному закону распределения, описывали с помощью среднего значения ( М ) и стандартного отклонения ( SD ); не подчиняющиеся нормальному закону распределения – с помощью медианы ( Ме ) и интерквартильного промежутка [ Q1; Q3 ]. В случае нормального распределения количественных показателей в независимых группах для проверки значимости их различий использовали t -критерий Стьюдента; при отсутствии нормального распределения – критерий Манна – Уитни. Сравнение количественных показателей до и после операции выполняли с помощью парного критерия Стьюдента при нормальном распределении показателя на этапах наблюдения, с помощью критерия Уилкоксо-на – при отсутствии нормального распределения. Для сравнения категориальных показателей в группах 1 и 2 применяли χ2 критерий Пирсона и точный критерий Фишера. Анализ выживаемости (свободы от возврата аортальной недостаточности) у оперированных пациентов проводили по методу Каплана – Майера. Сравнение кривых выживаемости в группах 1 и 2 выполняли с использованием лог-рангового теста. Проверку статистических гипотез проводили при критическом уровне значимости р = 0,05.
Результаты
При анализе дооперационных характеристик не было статистически значимых различий по спектру и частоте сопутствующей и фоновой патологии, а также по антропометрическим данным. В то же время были отмечены межгрупповые различия по ряду эхокардиографических параметров. При этом стоит отметить, что оцениваемые параметры не выходили за рамки референсных значений. Размеры аорты на измеряемых уровнях также имели статистически значимые различия, однако в то же время не характеризовались клинически значимыми особенностями. На всех измеряемых уровнях, кроме тубулярной части восходящей аорты, размеры аорты не достигали критериев аневризмы (табл. 1).
Таблица 1. Дооперационные показатели
Table 1. Preoperative data
|
Показатели |
Ао рег 1, n = 34 |
Ао рег 2, n = 23 |
p |
|
Возраст, лет |
62,5 [56; 69] |
63,5 [57; 68,5] |
0,856 |
|
Мужской пол, n ( %) |
21 (58,6) |
17 (76,1) |
0,132 |
|
ИМТ, кг/м2, n ( %) |
30,1 ± 5,9 |
30,5 ± 5,7 |
0,813 |
|
ППТ, м2 |
1,9 ± 0,2 |
2 ± 0,2 |
0,745 |
|
ИБС, n ( %) |
19 (55,8) |
17 (73,9) |
0,456 |
|
Артериальная гипертензия, n ( %) |
28 (82,3) |
20 (87) |
0,244 |
|
ПИКС, n ( %) |
3 (8,8) |
3 (13) |
0,212 |
|
ДАК, n ( %) |
10 (29,4) |
0 |
< 0,001 |
|
Сахарный диабет, n ( %) |
5 (14,7) |
1 (4,3) |
0,125 |
|
ХОБЛ, n ( %) |
1 (2,9) |
3 (13) |
0,342 |
|
Нарушение мозгового кровообращения, n ( %) |
6 (17,6) |
5 (21,7) |
0,765 |
|
Эхокардиография |
|||
|
ФВ ЛЖ, % |
63 [58; 68] |
57 [49; 67] |
< 0,001 |
Окончание табл. 1
End of table 1
|
Показатели |
Ао рег 1, n = 34 |
Ао рег 2, n = 23 |
Р |
|
КДО, мл |
106,5 [97; 124] |
142 [120; 1 85] |
< 0,001 |
|
КСО, мл |
40 [31; 48] |
55 [47; 93] |
< 0,001 |
МСКТ
|
ФК АК, мм |
25 [23; 26] |
26 [23; 27] |
0,023 |
|
Синусы Вальсальвы, мм |
43,2 ± 5,2 |
47,2 ± 5,9 |
0,008 |
|
Сино-тубулярное соединение, мм |
39,2 ± 6 |
43,6 ± 6,2 |
0,027 |
|
Восходящая аорта, мм |
51 [49,75; 54] |
53 [50; 60] |
0,369 |
|
Дуга аорты, мм |
36 [33; 40] |
40 [36; 45] |
0,047 |
Примечание: ДАК – двустворчатый аортальный клапан, ИМТ – индекс массы тела, ИБС – ишемическая болезнь сердца, КСО – конечный систолический объем, КДО – конечный диастолический объем, МСКТ – мультиспиральная компьютерная томография, ППТ – площадь поверхности тела, ПИКС – постинфарктный кардиосклероз, ФВ – фракция выброса, ФК АК – фиброзное кольцо аортального клапана, ХОБЛ – хроническая обструктивная болезнь легких.
Продолжительность искусственного кровообращения, сердечного и циркуляторного ареста была значимо короче в группе с меньшей степенью аортальной недостаточности. Тем не менее, длительность всей операции была сопоставима у пациентов обеих групп ( p = 0,159). Частота выполнения сочетанного аортокоронарного шунтирования не различалась в обеих группах (табл. 2).
В таблице 3 приведены основные осложнения раннего послеоперационного периода. В течение госпитально- го периода не отмечено значимых межгрупповых различий по частоте преходящего неврологического дефицита, инсультов или делирия. Частота острого повреждения почек была сопоставимой у пациентов обеих групп. В то же время дыхательную недостаточность и потребность в рестернотомии по поводу кровотечения отмечали только у пациентов группы с более выраженной аортальной недостаточностью, однако статистически значимых различий установлено не было.
Таблица 2. Интраоперационные данные
Table 2. Intraoperative data
|
Показатели |
Ао рег 1, n = 34 |
Ао рег 2, n = 23 |
Р |
|
Время операции, мин |
250 [220; 300] |
270 [240; 315] |
0,159 |
|
Время ИК, мин |
117 [95,5; 146,5] |
135 [115; 170] |
< 0,001 |
|
Сердечный арест, мин |
65 [57; 75] |
95 [70; 120] |
< 0,001 |
|
Циркуляторный арест, мин |
17 [15; 19] |
18 [17; 25,5] |
0,02 |
|
Коронарное шунтирование, n (%) |
8 (23,5) |
8 (34,7) |
0,721 |
|
Размер аортального протеза, мм |
30 [28; 32] |
30 [28; 32] |
> 0,999 |
Примечание: ИК – искусственное кровообращение.
Таблица 3. Послеоперационные данные
Table 3. Postoperative data
|
Показатели |
Ао рег 1, n = 34 |
Ао рег 2, n = 23 |
Р |
|
Нахождение в реанимации, койко-дни |
2 [1; 10] |
2 [1; 13] |
0,234 |
|
Время ИВЛ, ч |
12 [6; 43] |
18 [9; 40] |
0,06 |
|
Дыхательная недостаточность (трахеостомия), n ( %) |
0 |
1 (4,3) |
0,435 |
|
Делирий, n ( %) |
0 |
3 (13) |
0,239 |
|
Инсульт, n ( %) |
1 (2,9) |
1 (4,3) |
0,765 |
|
Заместительная почечная терапия, n ( %) |
1 (2,9) |
1 (4,3) |
0,765 |
|
Инфаркт миокарда, n ( %) |
0 |
0 |
> 0,999 |
|
Раневые осложнения, n ( %) |
0 |
1 (4,3) |
0,435 |
|
Кровотечение (рестернотомия), n ( %) |
0 |
2 (8,7) |
0,367 |
|
Летальность, n ( %) |
0 |
0 |
> 0,999 |
Примечание: ИВЛ – искусственная вентиляция легких.
Анализ динамики объемных размеров левого желудочка в обеих группах продемонстрировал снижение как систолических, так и диастолических показателей сразу после операции относительно дооперационных данных. Аналогичная картина была отмечена с динамикой фрак- ции выброса левого желудочка в обеих группах. Тем не менее, перечисленные изменения были статистически незначимы (табл. 4). Подобная динамика отмечена и при внутригрупповом анализе в среднесрочном послеоперационном периоде (табл. 5).
Таблица 4. Динамика параметров левого желудочка в раннем послеоперационном периоде (внутригрупповой анализ) Table 4. Dynamics of the left ventricle parameters in the early postoperative period (intragroup analysis)
|
Параметры |
Ао рег 1, n = 34 |
Ао рег 2, n = 23 |
||||
|
До операции |
После операции |
p |
До операции |
После операции |
p |
|
|
ФВ ЛЖ, % |
63 [62; 66] |
64 [62; 67] |
0,427 |
57 [49; 67] |
60 [54; 64] |
0,343 |
|
КДО, мл |
106,5 [97; 124] |
100 [90; 119] |
0,214 |
142 [120; 185] |
137 [106; 170] |
0,162 |
|
КСО, мл |
40 [31; 48] |
37 [30; 45] |
0,167 |
55 [47; 93] |
52,5 [36; 67] |
0,06 |
Примечание: КДО – конечный диастолический объем, КСО – конечный систолический объем, ФВ ЛЖ – фракция выброса левого желудочка.
Таблица 5. Динамика параметров левого желудочка в среднесрочном послеоперационном периоде (внутригрупповой анализ)
Table 5. Dynamics of the left ventricle parameters in the mid-term follow-up (intragroup analysis)
|
Показатели |
Ао рег 1, n = 34 |
p |
Ао рег 2, n = 23 |
p |
||
|
После операции |
1 год |
После операции |
1 год |
|||
|
ФВ ЛЖ, % |
64 [62; 67] |
66 [63; 68] |
0,461 |
137 [106; 170] |
61,5 [57; 67] |
0,476 |
|
КДО, мл |
100 [90; 119] |
97 [88; 113] |
0,753 |
52,5 [36; 67] |
108 [102; 158] |
0,34 |
|
КСО, мл |
37 [30; 45] |
34 [30; 41] |
0,76 |
60 [54; 64] |
40 [35; 68] |
0,565 |
Примечание: КДО – конечный диастолический объем, КСО – конечный систолический объем, ФВ ЛЖ – фракция выброса левого желудочка.
На рисунке 2 отражено изменение степени аортальной регургитации после операции по сравнению с исходными значениями в период наблюдения до 2 лет после хирургического вмешательства. Стоит отметить, что у большинства пациентов в исследуемых группах отмечен регресс аортальной недостаточности.
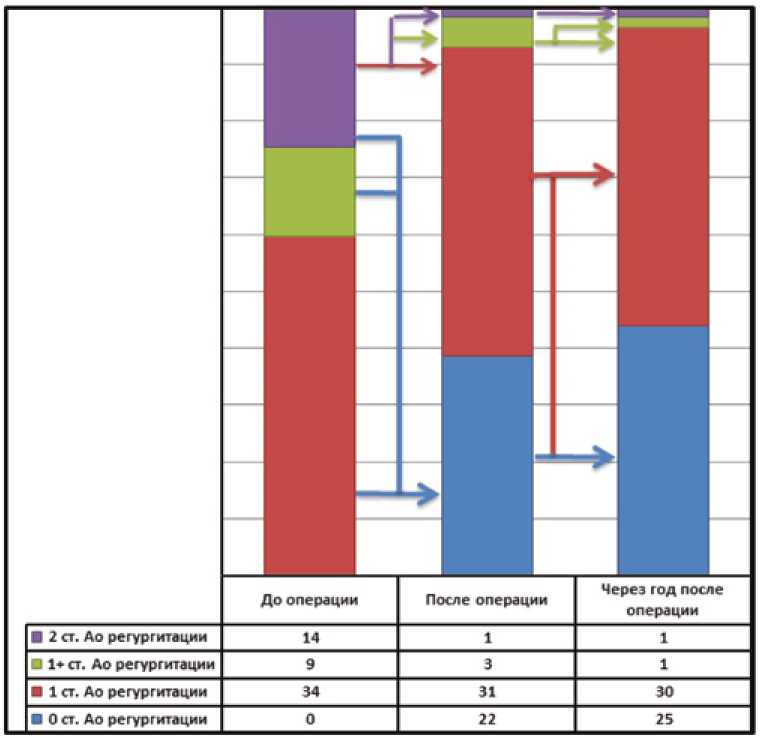
Рис. 2. Динамика степени аортальной недостаточности на до- и послеоперационном этапах
Fig. 2. Dynamics of the of aortic insufficiency grade in the pre- and postoperative periods
Анализ размеров аорты до и после операции показал их уменьшение на всех измеряемых уровнях в обеих обсуждаемых группах после хирургического вмешательства (табл. 6). Стоит отметить, что в группе с легкой степенью аортальной регургитации послеоперационные размеры аорты на уровне синусов Вальсальвы и сино-тубулярного соединения сократились относительно дооперационных значений на 5,6% (p < 0,001) и 16,3% (p = 0,004), а в группе с умеренной недостаточностью – на 6,4% (p = 0,08) и 19,7% (p = 0,017) соответственно.
Таблица 6. Динамика размеров аорты до и после операции
Table 6. Dynamics of aortic size before and after surgery
|
Параметры |
Ао рег 1, n = 34 |
Ао рег 2, n = 23 |
||||
|
До операции |
После операции |
p |
До операции |
После операции |
p |
|
|
ФК АК, мм |
25 [23; 26] |
23 [21; 25] |
0,112 |
26 [23; 27] |
25 [23; 25] |
0,285 |
|
Синусы Вальсальвы, мм |
43,2 ± 5,2 |
40,8 ± 3,9 |
< 0,001 |
47,2 ± 5,9 |
44 ± 4,3 |
0,08 |
|
Сино-тубулярное соединение, мм |
39,2 ± 6 |
32,8 ± 3,2 |
0,004 |
43,6 ± 6,2 |
35 ± 4,1 |
0,017 |
|
Восходящая аорта, мм |
51 [49,75; 54] |
32 [31; 34] |
< 0,001 |
53 [50; 60] |
33 [31; 35] |
< 0,001 |
|
Дуга аорты, мм |
36 [33; 40] |
35 [30; 38] |
0,274 |
40 [36; 45] |
33 [32; 34] |
0,016 |
Примечание: ФК АК – фиброзное кольцо аортального клапана.
При межгрупповом сравнении послеоперационных размеров аорты отмечено статистически значимое различие на уровне синусов Вальсальвы в группах «Ао рег 1» и «Ао рег 2» (40,8 ± 3,9 против 44 ± 4,3 мм, p < 0,001) при сопоставимой редукции размеров аорты на уровне сино-тубулярного соединения (32,8 ± 3,2 против 35 ± 4,1 мм, p = 0,312).
В среднесрочном периоде была проанализирована выживаемость обсуждаемых пациентов (рис. 3).
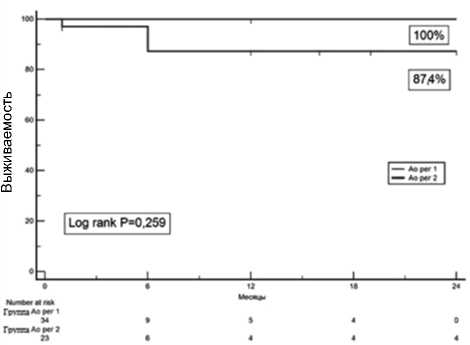
Рис. 3. Кривые выживаемости Каплана – Майера у пациентов с легкой и умеренной аортальной недостаточностью в течение 2 лет после операции
Fig. 3. Kaplan – Meier survival analysis for patients with mild and moderate aortic regurgitation at 2 years after surgery
Так, в сроки до 2 лет в группе с минимальной аортальной регургитацией этот показатель составил 100%, а в группе с умеренной аортальной недостаточностью – 87,4%. Причинами смерти явились острое нарушение мозгового кровообращения через 6 мес. после операции (n = 1) и двусторонняя пневмония, ассоциированная с COVID-19 (n = 1). В течение всего периода наблюдения ни в одном случае не было отмечено возврата или увеличения степени аортальной регургитации, вследствие чего не было потребности в повторном вмешательстве на проксимальных отделах аорты.
Обсуждение
Стремление к выполнению клапаносохраняющих операций основано на исключении протез-обусловлен-ных осложнений, что способствует улучшению качества жизни пациента. Понимание механизма аортальной регургитации является ключевым моментом в выборе вида хирургической коррекции. Пациенты с аортальной недостаточностью, обусловленной расширением корня аорты вследствие ее комплексной природы, требуют сложных вариантов хирургического восстановления структур корня аорты и створок аортального клапана [7, 8].
Одновременно с этим существует категория пациентов, у которых аортальная недостаточность главным образом обусловлена дилатацией сино-тубулярного соединения [9]. Основываясь на теоретических предположениях D.J. Corrigan и соавт. [10], одними из первых R.W. Frater и соавт. [11], представили успешный опыт редукции сино-тубулярного соединения у небольшой когорты больных в качестве варианта коррекции аортальной недостаточности при аневризме восходящей аорты. Позже K. Furukawa и соавт. [12] в экспериментальном исследовании подтвердили важную роль дилатации сино-тубулярного соединения в генезе аортальной регургитации. Авторы, продемонстрировав удовлетворительные результаты редукции сино-тубу-лярного соединения, отметили эффективность данной техники в отношении восстановления нормальной функции аортального клапана без дополнительного вмешательства на створках. M. Moscarelli и соавт. [13], представив собственный подход к стабилизации си-но-тубулярного соединения, также отметили хороший результат этой процедуры.
Таким образом, возможность коррекции аортальной недостаточности без увеличения объема операции до сложной аорто-аннулярной реконструкции является привлекательной альтернативой за счет своей меньшей травматичности и технической сложности, что может быть особенно полезным у пациентов с тяжелым комор-бидным статусом, в клиниках с относительно небольшим опытом аортальной хирургии и т. д. [4].
Анализируемые в данном исследовании результаты раннего послеоперационного периода, включающие неврологический дефицит, дыхательную недостаточность, острое почечное повреждение, а также кардиальные, инфекционные и геморрагические осложнения, были зарегистрированы в единичных случаях без статистически значимых различий между группами. Необходимо подчеркнуть, что в обеих группах ранней летальности не было зарегистрировано.
Полученные в настоящем исследовании клинические результаты согласуются с данными, опубликованными N. Morimoto и соавт. [4]. В своем исследовании авторы также не отметили случаев послеоперационной летальности. При этом частота церебральных инсультов составила 6,9%. В другом исследовании M. Asano и соавт. [14] после выполнения протезирования тубулярной части восходящей аорты в сочетании с разными вариантами пластики створок аортального клапана сообщили об уровне послеоперационной летальности 2,1%. По мнению авторов, летальные случаи были обусловлены не усложнением уровня вмешательства на аортальном клапане, а сопутствующими кардиохирургическими вмешательствами (аортокоронарное шунтирование – 16%, вмешательство на дуге аорты – 22,2%).
В нашей серии 28% пациентов потребовалось сочетанное аортокоронарное шунтирование. При этом всем пациентам была выполнена реконструкция дуги аорты (hemiarch-процедура). Несмотря на это, в настоящем исследовании не было отмечено негативного влияния сочетанных вмешательств на исход хирургического лечения.
При комплексном анализе ранних и среднесрочных результатов было установлено, что стабилизация си-но-тубулярного соединения, являясь эффективной процедурой в отношении уменьшения аортальной регургитации, ассоциирована со стабильно удовлетворительным результатом в отношении свободы от реоперации как в раннем послеоперационном периоде, так и в двухлетние сроки после операции. С. Tataroglu и соавт. [15] в своем исследовании также продемонстрировали удовлетворительные долгосрочные результаты даже у пациентов с расслоением аорты. Однако T.E. David и соавт. [16], проведя анализ послеоперационных результатов, отметили субоптимальные показатели выживаемости в сроки до 10 лет, которые были обусловлены повторными аортальными операциями по поводу аневризматической болезни грудной аорты. Согласно данным литературы, одним из главных факторов, ответственных за увеличенную вероятность повторных вмешательств, является сложная пластика створок аортального клапана [4, 17]. Высокий уровень свободы от реопераций в нашей серии наблюдений, по всей видимости, связан с полным отсутствием подобных вмешательств.
Ряд авторов статистически обосновали, что двустворчатый аортальный клапан per se является предиктором повторного вмешательства на аортальном клапане в среднесрочном послеоперационном периоде [14]. Однако в своем исследовании мы не смогли подтвердить данную гипотезу, вероятно, из-за относительно небольшой выборки пациентов.
У обсуждаемых пациентов редукция сино-тубулярной зоны аорты также позволила достичь клинически значимого уменьшения размеров корня аорты, отмечавшегося в течение всего периода наблюдения. Полученные данные соотносятся с результатами, представленными R. De Paulis и соавт. [18], которые выявили аналогичную картину в отношении размеров корня аорты после редукции сино-тубулярного соединения. I. Vendramin и соавт. [19] в своей публикации продемонстрировали, что уменьшение размеров синусов Вальсальвы прямо коррелирует с послеоперационным темпом роста этого сегмента аорты. Отмечаемая динамика позволяет значительным образом снизить не только частоту реопераций на проксимальном отделе аорты, но и риски аорто-ассоциированных осложнений даже у пациентов с двустворчатым аортальным клапаном, несмотря на некоторую тенденцию к увеличению размеров корня в послеоперационном периоде [20].
Заключение
Стабилизация сино-тубулярного соединения при реконструкции аневризмы восходящей аорты без дополнительного вмешательства на створках аортального клапана является эффективным и безопасным вариантом хирургического вмешательства и характеризуется удовлетворительными среднесрочными результатами.
Список литературы Стабилизация сино-тубулярного соединения как эффективный способ коррекции аортальной недостаточности у пациентов с аневризмой восходящей аорты
- Bekeredjian R., Graybur P.A. Valvular heart disease: aortic regurgitation. Circulation. 2005;112(1):125-134. https://doi.org/10.1161/CIRCULATIONAHA.104.488825.
- Weiss R.M., Miller J.D., Heistad D.D. Fibrocalcific aortic valve disease: opportunity to understand disease mechanisms using mouse models. Circ. Res. 2013;113(2):209-222. https://doi.org/10.1161/CIRCRESAHA.113.300153.
- Esmailzadeh M., Alimi H., Maleki M., Hosseini S. Aortic valve injury following blunt chest trauma. Res. Cardiovasc. Med. 2014;3(3):e17319. https://doi.org/10.5812/cardiovascmed.17319.
- Morimoto N., Matsumori M., Tanaka A., Munakata H., Okada K., Okita Y. Adjustment of sinotubular junction for aortic insufficiency secondary to ascending aortic aneurysm. Ann. Thorac. Surg. 2009;88(4):1238-1243. https://doi.org/10.1016/j.athoracsur.2009.05.048.
- Yacoub M.H., Gehle P., Chandrasekaran V., Birks E.J., Child A., Radley-Smith R. Late results of a valve-preserving operation in patients with aneurysms of the ascending aorta and root. J. Thorac. Cardiovasc. Surg. 1998;115(5):1080-1090. https://doi.org/10.1016/S0022-5223(98)70408-8.
- Lansac E., Di Centa I., Sleilaty G., Lejeune S., Khelil N., Berrebi A. et al. Long-term results of external aortic ring annuloplasty for aortic valve repair. Eur. J. Cardiothorac. Surg. 2016;50(2):350-360. https://doi.org/10.1093/ejcts/ezw070.
- Youssefi P., Lansac E., Zacek P., Berrebi A., Czytrom D., Mankoubi L. et al. Aortic valve repair - “Pearls and Pitfalls.” J. Vis. Surg. 2020;6:36. https://doi.org/10.21037/jovs-2019-10.
- Чарчян Э.Р., Тивелев Б.В., Брешенков Д.Г., Попов С.О., Белов Ю.В. Пластика аортального клапана при операции по методике David у пациентов с двустворчатым аортальным клапаном. Кардиология и сердечно-сосудистая хирургия. 2023;16(1):62-67. https://doi.org/10.17116/kardio20231601162.
- Khoury G.El., Glineur D., Rubay J., Verhelst R., d’Udekem d’Acoz Y., Poncelet A. et al. Functional classification of aortic root / valve abnormalities and their correlation with etiologies and surgical procedures. Curr. Opin. Cardiol. 2005;20(2):115-121. https://doi.org/10.1097/01.hco.0000153951.31887.a6.
- Corrigan D.J. Permanent patency of the mouth of the aorta. Edinb. Med. Surg. J. 1832;37:111. URL: https://pubmed.ncbi.nlm.nih.gov/30331470 (14.05.2024).
- Frater R.W. Aortic valve insufficiency due to aortic dilatation: Correction by sinus rim adjustment. Circulation. 1986;74(3_pt_2):I136-142. https://pubmed.ncbi.nlm.nih.gov/3742771 (14.05.2024).
- Furukawa K., Ohteki H., Cao Z.-L., https://doi.org/K., Narita Y., Minato N. et al. Does dilatation of the sinotubular junction cause aortic regurgitation? Ann. Thorac. Surg. 1999;68(3):949-954. URL: https://pubmed.ncbi.nlm. nih.gov/10509990 (14.05.2024).
- Moscarelli M., Bonifazi R., Nasso G., Di Bari N., Speziale G. A modified technique for ascending aorta replacement with sinotubular junction stabilization. Ann. Thorac. Surg. 2020;110:e335-337. https://doi.org/10.1016/j.athoracsur.2020.03.121.
- Asano M., Kunihara T., Aicher D., El Beyrouti H., Rodionycheva S., Schäfers H.-J. Mid-term results after sinutubular junction remodeling with aortic cusp repair. Eur. J. Cardiothorac. Surg. 2012;42(6):1010- 1015. https://doi.org/10.1093/ejcts/ezs120.
- Tataroglu C., Cenal A.R., Tekumit H., Uzun K., Polat A., Akinci E. Reduction of the sinotubular junction in patients undergoing ascending aortic replacement with coexisting aortic insufficiency. J. Card. Surg. 2011;26(1):88-91. https://doi.org/10.1111/j.1540-8191.2010.01181.x.
- David T.E., Feindel C.M., Armstrong S., Maganti M. Replacement of the ascending aorta with reduction of the diameter of the sinotubular junction to treat aortic insufficiency in patients with ascending aortic aneurysm. J. Thorac. Cardiovasc. Surg. 2007;133:414-418. https://doi.org/10.1016/j.jtcvs.2006.09.049.
- Козлов Б.Н., Панфилов Д.С., Базарбекова Б.А., Сондуев Э.Л., Бойко А.М. Непосредственные результаты хирургического лечения аневризмы восходящей аорты в сочетании со стенотическим поражением аортального клапана. Сибирский журнал клинической и экспериментальной медицины. 2023;39(3):135-142. https://doi.org/10.29001/2073-8552-2023-39-3-135-142.
- De Paulis R., Cetrano E., Moscarelli M., Ando G., Bertoldo F., Scaffa R. et al. Effects of ascending aorta replacement on aortic root dilatation. Eur. J. Cardiothorac. Surg. 2005;27:86-89. https://doi.org/10.1016/j. ejcts.2004.10.043.
- Vendramin I., Meneguzzi M., Sponga S., Deroma L., Cimarosti R., Lutman C. et al. Bicuspid aortic valve disease and ascending aortic aneurysm: Should an aortic root replacement be mandatory? Eur. J. Cardiothorac. Surg. 2016;49:103-109. https://doi.org/10.1093/ejcts/ezv069.
- Панфилов Д.С., Базарбекова Б.А., Панфилова Н.О., Саушкин В.В., Сондуев Э.Л., Сазонова С.И. и др. Динамика изменения размеров корня аорты после одномоментной коррекции стенозированного аортального клапана и аневризмы восходящей аорты. Российский кардиологический журнал. 2023;28(1):5198. https://doi.org/10.15829/1560-4071-2023-5198.


