Стенозирующий лигаментит пальцев кисти
Автор: Котельников Г.П., Панкратов А.С., Николаенко А.Н., Борисов А.П., Ключников А.С., Пискун В.В., Князев Н.А., Люкшин Д.В.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Обзор литературы
Статья в выпуске: 6 т.30, 2024 года.
Бесплатный доступ
Введение. Стенозирующий лигаментит пальцев кисти является распространенной причиной инвалидности руки. Несмотря на 174-летнюю историю изучения заболевания, тактика лечения и новые малоинвазивные подходы к оперативному вмешательству вызывают интерес исследователей всего мира.Цель работы - на основании анализа российских и зарубежных литературных источников определить современное состояние проблемы лечения стенозирующего лигаментита.Материалы и методы. Поиск научных публикаций осуществлен в поисковых системах PubMed, MedLine и eLibrary. Отобрано 70 источников, преимущественно за последние 10 лет.Результаты и обсуждение. Лечение стенозирующего лигаментита следует начинать в зависимости от стадии заболевания с учетом его продолжительности, наличия рецидивов или осложнений, сопутствующего состояния пациента. Консервативная терапия должна включать ортопедическую иммобилизацию сустава и/или инъекции кортикостероидов. Несмотря на то, что чрескожное рассечение кольцевидной связки малоинвазивно и имеет ряд преимуществ (меньшую травматизацию тканей, более короткое время восстановления, отсутствие болезненных рубцов), согласно данным большинства исследователей, предпочтительно использовать открытую лигаментотомию, которая способствует минимизации осложнений и рецидивов заболевания.Заключение. Эффективность консервативных методик при лечении стенозирующего лигаментита составляет от 47 до 93 %, хирургического вмешательства - 94-99 %. Хирургическое лечение показано при отсутствии результатов консервативного лечения. Оно является высокоэффективным, имеет малое количество осложнений и рецидивов.
Стенозирующий лигаментит, болезнь нотта, кольцевидная связка
Короткий адрес: https://sciup.org/142243873
IDR: 142243873 | УДК: 616.747.7-009.1-08-039.73:616-089](048.8) | DOI: 10.18019/1028-4427-2024-30-6-906-915
Stenosing tenosynovitis
Introduction Stenosing tenosynovitis or trigger finger is a common cause of hand disability. With the 174year history of the condition, treatment strategy and new minimally invasive surgical approaches are essential for researchers around the world.The objective was to determine the current treatment options of the stenosing tenosynovitis using the Russian and foreign literature.Material and methods The original literature search was conducted on key resources including Scientific Electronic Library (www.elibrary.ru), the National Library of Medicine (www.pubmed.org) and MedLine. Seventy contributions were identified published for the last 10 years.Results and discussion Treatment of stenosing ligamentitis can be initiated depending on the stage of the disease, the duration, relapses or complications, comorbidities. Conservative orthopaedic treatment includes joint immobilization and/or corticosteroid injections. Although percutaneous dissection of the annular ligament is minimally invasive and has advantages of less tissue trauma, shorter recovery time, absence of painful scars open ligamentotomy can help to minimize complications and relapses of the disease.Conclusion Conservative treatment of trigger finger is effective in 47 to 93 % and surgical procedures are practical in 94-99 %. Surgical treatment can be employed with failure of conservative treatment and has been shown to be effective and with a low rate of complications and relapses.
Текст обзорной статьи Стенозирующий лигаментит пальцев кисти
Стенозирующий лигаментит (СЛ) («щелкающий» палец, болезнь Нотта) — распространенное заболевание пальцев кисти, которое вызвано поражением сухожильно-связочного аппарата, приводящим к нарушению двигательной функции [1]. Болезнь щелкающего пальца получила свое название из-за болезненного щелкающего звука, издаваемого при движении пораженного пальца [2]. Заболевание впервые описано в 1850 г. французским хирургом Альфредом Ноттом [2, 3] и характеризуется типичным «защелкиванием» пальца или пальцев при максимальном сгибании в кулак, ограничением движений, болью у основания пальцев при надавливании, утренней скованностью движений в кисти [4]. СЛ нередко приводит к выраженному снижению функции кисти и силы захвата. При прогрессировании болезни может изменяться качество жизни пациента [5, 6].
Цель работы — на основании анализа российских и зарубежных литературных источников определить современное состояние проблемы лечения стенозирующего лигаментита.
МАТЕРИАЛЫ И МЕТОДЫ
Для поиска публикаций использовали электронные базы PubMed, MedLine и электронную библиотеку eLibrary. Поиск осуществляли по ключевым словам и словосочетаниям на русском и английском языках: стенозирующий лигаментит (stenosing ligamentitis), частота встречаемости патологии (incidence of pathology), консервативная терапия (conservative therapy), оперативные методы лечения (operative methods of treatment), отдаленные результаты лечения (long-term treatment results), осложнения (complications).
Критерии включения:
-
— полнотекстовые научные статьи, в которых представлены основополагающие сведения о стенозирующем лигаментите (этиология, патоморфология, классификация);
-
— полнотекстовые научные публикации, содержащие современную информацию о методах лечения СЛ (консервативного и оперативного);
-
— полнотекстовые научные статьи, представляющие результаты многоцентровых когортных исследований, а также конкретные клинические примеры, посвященные лечению СЛ, его осложнений и отдаленным результатам терапии.
Критерии невключения: тезисы научно-практических конференций, статьи без полнотекстовой версии, а также публикации, которые не удовлетворяли в полной мере критериям включения.
Для анализа отобрано 70 публикаций (59 иностранных и 11 отечественных), преимущественно использовали литературу за последние 10 лет.
РЕЗУЛЬТАТЫ
Этиология заболевания . В литературе описано несколько причин возникновения щелкающего пальца, хотя точная этиология до настоящего времени не выяснена. Возможной причиной являются повторные, монотонные движения пальцев и локальная травма [7]. Имеются литературные данные, связывающие щелкающий палец с профессиями, требующими длительного захвата предметов и сгибания руки, такими как использование ножниц или ручных инструментов [7–10]. Помимо этого, развитию болезни Нотта способствуют деформирующий артроз суставов пальцев кисти, теносиновит сухожилий сгибателей и другие воспалительные заболевания кисти [11]. СЛ нередко возникает на фоне системных заболеваний — сахарного диабета, подагры или ревматоидного артрита [12]. Кроме вышеперечисленных в качестве причин болезни упоминаются выполнение однообразных движений руками (печать на клавиатуре, вождение автомобиля); регулярные, интенсивные нагрузки на пальцы; воспалительный процесс, локализованный в кисти; травмы и повреждения; наследственная предрасположенность; атеросклероз; заболевания щитовидной железы; постоянное сдавливание связок; физический труд с нагрузкой на руки [13, 14].
Хотя естественное течение СЛ не изучено полностью, D. McKee et al. определили, что у 52 % пациентов в когорте из 348 человек симптомы заболевания полностью исчезли к 8 мес. без какого-либо лечения [15]. По статистике СЛ встречается у 2–3 % населения, чаще у женщин старше 40 лет [16]. Стоит отметить, что нередко данное поражение встречается у детей [17]. Как правило, СЛ поражает в первую очередь безымянный и большой пальцы: безымянный палец — 44 %, большой палец — 26 %, средний палец — 20 %, мизинец — 7 %, указательный палец — 3 % случаев [18].
Патоморфология . При СЛ воспаление и гипертрофия кольцевидной связки постепенно ограничивают нормальную экскурсию сухожилий сгибателя [19, 20]. Биомеханическая основа эффективного функционирования сухожилий кисти обеспечивается системой, состоящей из кольцевидных и крестообразных блоков в каждом пальце, которые служат для максимизации силы, вырабатываемой сухожилием сгибателя, и эффективности движения (рис. 1) [19].
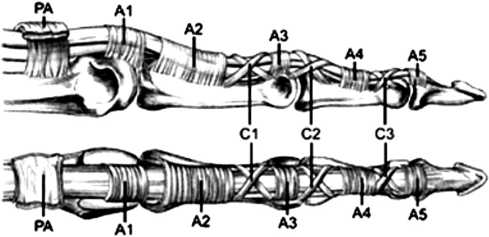
Рис. 1. Схема костно-фиброзного канала:
А — кольцевидные блоки (А1–А5);
С — крестообразные блоки (С1–С3);
РА — ладонный апоневроз [19]
Наиболее часто поражаемым блоком при СЛ является первый кольцевидный блок (A1) на головке пястной кости, хотя известны случаи во втором и третьем кольцевидных блоках (A2 и A3), а также в ладонном апоневрозе [19]. Это связано с тем, что из-за своего расположения блок А1 подвергается воздействию самых высоких сил и градиентов давления как при нормальном, так и при силовом захвате. Болезнь Нотта характеризуется утолщением сухожильного влагалища и связки А1, а иногда и образованием узелков на сухожилии вместе с сужением просвета, что приводит к нарушению связи между сухожилием и его влагалищем на уровне головки пястной кости.
Классификация . Согласно классификации D.P. Green [11] выделяют четыре степени тяжести СЛ (табл. 1).
Таблица 1
Классификация СЛ (D.P. Green)
|
Стадия |
Клинические признаки |
|
|
I (начальная) |
Боль, защемление, сообщаемое пациентом, болезненность над блоком А1 |
|
|
II (активная) |
Фиксация при разгибании пальца при физикальном обследовании |
|
|
III (пассивная) |
III А |
Исправление защемления с помощью пассивного разгибания пальца |
|
III Б |
Потеря активного сгибания |
|
|
IV (контрактура) |
Защемление с фиксированной сгибательной контрактурой проксимального межфалангового сустава |
|
На ранних стадиях заболевания у пациентов может наблюдаться безболезненное щелканье или скованность пораженного пальца (стадия I) [21]. По мере прогрессирования заболевания возникает болезненное защемление или блокировка пальца, что может потребовать пассивного разгибания непораженной руки (стадия II). При осмотре суставы пораженного пальца обычно не опухают и не эритематозны, несмотря на жалобы на боль. При щелкающем пальце утолщенный и болезненный блок A1 можно пропальпировать сразу дистальнее поперечной ладонной складки, что отличает его от других заболеваний рук (ревматоидный артрит, подагра и др.). Наличие этого «болезненного узелка» и отсутствие предшествующей травмы подтверждают подозрение на СЛ III стадии. На поздней стадии заболевания (степень IV) пациенты намеренно стараются избегать активного использования пальца, что приводит к развитию фиксированной контрактуры проксимального межфалангового сустава [21].
Лечение стенозирующего лигаментита . Наиболее эффективный метод терапии болезни Нотта все еще остается предметом дискуссий [23, 24, 25, 26]. В зависимости от степени болезни в медицинской практике используют различные методы, однако, как правило, следует начинать с консервативной терапии [27].
Консервативное лечение. Первоначальное консервативное лечение СЛ включает использование нестероидных противовоспалительных препаратов для купирования болевого синдрома, иммобилизацию пястно-фалангового сустава, инъекции кортикостероидов, физиотерапию и массаж [25, 28, 29].
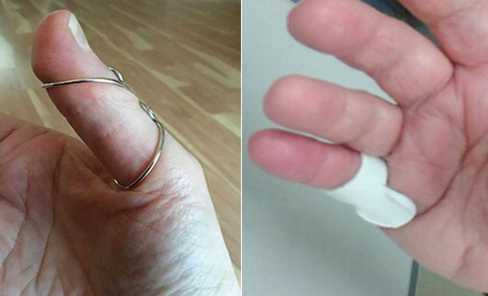
Рис. 2. Варианты шинирования пальцев кисти [29]
Иммобилизация пястно-фалангового сустава . Целью шинирования является предотвращение трения, вызванного движением сухожилия сгибателя через пораженный блок А1, пока воспаление не купируется [29]. Считается, что шинирование является подходящим вариантом лечения для пациентов, которые отказываются от инъекций кортикостероидов [30]. Данный метод менее эффективен у пациентов с тяжелыми триггерами или длительной продолжительностью симптомов. При этом используют различные варианты шин: изготовленные по индивидуальному заказу кольцевые шины, шины из термопластика, металла или готовые шины (рис. 2) [29].
Следует шинировать палец в течение 6 нед. или дольше, если воспаление продолжается. D. Lunsford et al. рекомендуют иммобилизацию сустава на 6–10 нед., при этом эффективность лечения составляет 47–93 % [27]. По мере уменьшения боли и воспаления пациент может самостоятельно накладывать шину на ночь и постепенно возобновлять обычную деятельность руки [29]. Некоторым пациентам может потребоваться до 6 мес. На основе европейского исследования HANDGUIDE сделан вывод, что оптимального режима ортопедии не существует, и продолжительность лечения должна подбираться индивидуально в зависимости от продолжительности симптомов, тяжести и предпочтений каждого пациента [22].
Инъекция кортикостероидов . Инъекция кортикостероидов для лечения щелкающего пальца описана еще в 1953 г. L.D. Howard [30]. В исследованиях ряда авторов указывается достаточно высокая эффективность (до 93 %) на начальных стадиях СЛ при отсутствии сопутствующих эндокринологических заболеваний, продолжительности болезни менее 6 мес., одном пораженном пальце [31, 32, 33, 34]. Многие исследователи подчеркивают, что при болезни Нотта, продолжающейся более 6 мес., происходит хондроидная метаплазия связки A1, следовательно, консервативная терапия не будет эффективна [32, 33]. В доступной литературе указан широкий диапазон эффективности — от 49 до 93 % после первой инъекции [32, 34]. J. Castellanos et al. описывают долгосрочную эффективность кортикостероидной терапии в 69 % (продолжительность наблюдения составила 8 лет, в исследование включен 71 пациент) [35].
Инъекцию традиционно вводят непосредственно в оболочку [36]. Имеются сообщения о внесиновиальной инъекции, которая может быть столь же эффективной, но при этом снижается риск повреждения сухожилия (рис. 3) [29]. Если симптомы не исчезают после первой инъекции или возвращаются после нее, вероятность успеха второй инъекции обычно вдвое ниже, чем при первоначальном лечении [29].

Рис. 3. Место инъекции: А1 — проекция расположения блока А1; NV — проекция сосудисто-нервного пучка [29]
C.S. Polat et al. оценили эффективность кортикостероидной терапии у 43 пациентов, инъекции проводили под контролем УЗИ [37]. Авторы описывают высокую эффективность инъекции глюкокортикостероидов в сочетании с иммобилизацией сустава.
В проспективном анализе 99 щелкающих пальцев K.J. Shultz et al. наблюдали постоянные симптомы после инъекции кортикостероидов в течение одного месяца у пациентов с несколькими щелкающими пальцами в 5,8 раза чаще, чем у пациентов с одним пораженным пальцем [38].
Физиотерапия и массаж включают:
-
— ультразвуковое воздействие на воспаленное сухожилие и влагалище для уменьшения воспаления и рубцовых спаек;
-
— фрикционный массаж сухожилий, который может разрушить и уменьшить спайки, узелки и отеки;
-
— пассивный диапазон движений в пястных и межфаланговых суставах;
-
— пассивное внутреннее и внешнее растяжение кисти и запястья [29].
P.E. Ferrara et al. рекомендуют использование экстракорпоральной ударно-волновой терапии (ESWT) с частотой 15 Гц и плотностью потока от 0,1 до 3 бар [39]. Результаты показали, что ESWT является эффективной и безопасной терапией для консервативного лечения СЛ: значимо купирует болевой синдром, улучшает функциональный уровень и качество жизни.
Хирургическое лечение . При неэффективности консервативного лечения и блокад, а также при наличии поздних стадий заболевания рекомендовано оперативное вмешательство — рассечение кольцевидной связки А1 у основания пальца [40–43].
При болезни Нотта операцию выполняют двумя основными способами:
-
1) открытый метод с небольшим разрезом кожи, наложением швов и последующими повязками (под местной анестезией хирург-ортопед рассекает кольцевидную связку А1, которая ограничивает движение сухожилия) [44, 45];
-
2) малоинвазивный метод, при котором делают лишь небольшие проколы кожи иглой, без наложения швов и повязок [46, 47].
Хирургическое открытое вмешательство является «золотым стандартом» лечения СЛ, поскольку оно позволяет более тщательно осмотреть область операции, является высокоэффективным (эффективность приближается к 100 %) и имеет низкий уровень осложнений [48]. Существует множество техник хирургического открытого лечения СЛ [49, 50, 51].
-
A. Kosiyatrakul и S. Luenam предлагают следующую хирургическую технику [52]. Кисть пациента устанавливают в супинаторном положении, большой палец — в положении радиального отведения. Линию разреза планируют до инъекции местной анестезии. Лучевая борозда находится между блоком А1 и лучевой сесамовидной костью. Длинный сгибатель большого пальца и проксимальную фалангу большого пальца идентифицируют пальпаторно и обозначают маркером (рис. 4). Кожу инфильтрируют 3–4 мл 1 % лидокаина без адреналина, вокруг плеча накладывают жгут. Производят разрез кожи по намеченной линии. При рассечении глубокого дермального слоя кожи проводят мягкую тупую диссекцию для идентификации лучевого пальцевого нерва в подкожном слое. Связку А1 рассекают скальпелем вдоль ее радиального края (рис. 5). Кожу зашивают нейлоновыми швами 4–0.
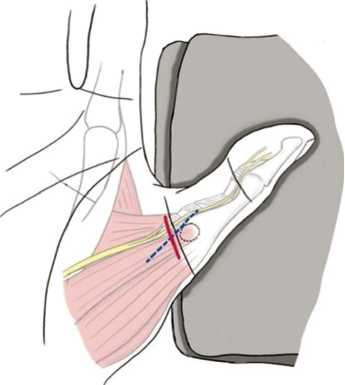
Рис. 4. Иллюстрация разреза кожи (красная линия), радиальной борозды (пунктирная синяя линия) и лучевой сесамовидной кости (пунктирная черная линия) [52]
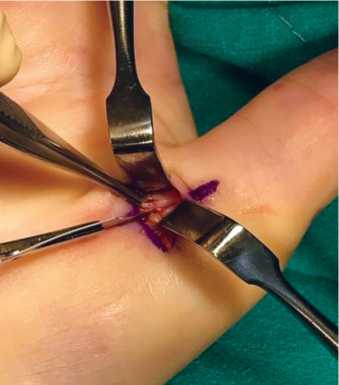
Рис. 5. Рассечение блока А1 большого пальца по его лучевому краю [52]
Осложнения при открытом вмешательстве на блоке А1 могут варьировать от незначительных до значительных [53, 54]. Незначительные осложнения (болезненность в области рубца, в месте локализации блока А1 и небольшое отставание при разгибании) не требуют хирургического лечения. Значительные осложнения вызывают существенные нарушения функций руки, включая постоянное или рецидивирующее срабатывание, натяжение сухожилия сгибателя и повреждение пальцевого нерва [55].
Наиболее уязвимой структурой во время высвобождения блока А1 большого пальца является лучевой пальцевой нерв [56]. Нерв может быть поврежден, если разрез кожи сделан слишком глубоко. Анатомические исследования показали, что нерв расположен на глубине 1,29–2,19 мм в коже. Таким образом, как только будет рассечен самый глубокий дермальный слой кожи, следует провести осторожное тупое рассечение для идентификации и защиты лучевого пальцевого нерва [56].
В ретроспективном исследовании 3428 пациентов, перенесших открытое хирургическое вмешательство на щелкающем пальце, J.E. Koopman et al. сообщили, что у 16 % пациентов возникли осложнения, и только 2 % потребовалось оперативное лечение [57].
A.E. Federer et al. продемонстрировали значительно более высокий показатель осложнений (26,3 % против 13,0 %) у пациентов с сахарным диабетом по сравнению с больными без диабета, что было связано со значительно более высоким показателем ограниченного послеоперационного диапазона движений у пациентов с эндокринологической патологией [58].
Чрескожное вмешательство на кольцевидной связке широко освещается в литературе, при этом эффективность данного метода приближается к 95 % [59, 60]. Чрескожное хирургическое вмешательство на блоке А1 впервые представлено J. Lorthioir в 1958 году [61]. D.M. Eastwood et al. еще в 1992 г. назвали его амбулаторной процедурой, показав эффективность 94 % [62]. При данном вмешательстве пястно-фаланговый сустав гиперэкстензируется ладонью вверх, тем самым растягивая блок А1 и смещая нейроваскулярные структуры дорсально. После инъекции лидокаина для купирования боли игла вводится через кожу в блок А1. Затем ее перемещают, чтобы надрезать блок проксимальнее и дистальнее места инъекции [60]. А.В. Жигало с соавт. разработали новый малоинвазивный способ подкожного рассечения связки A1 с помощью использования специальных игл малого диаметра (0,6–1,2 мм) [63, 64]. При применении данной техники у 215 пациентов в большинстве случаев получены отличные и хорошие результаты (70 % и 20,3 % соответственно); удовлетворительные — в 7,5 %, неудовлетворительные (рецидив заболевания) — в 2,2 % случаев [63].
Китайские исследователи M. Pan et al. оценили у 21 пациента эффективность технологии чрескожного рассечения кольцевидной связки с использованием игольчатого ножа под контролем УЗИ [65], получив эффект при однократном вмешательстве.
-
Р. Xie et al. рандомизировали 76 пациентов в группы при открытом или чрескожном хирургическом вмешательстве и не обнаружили никакой разницы в диапазоне движений пальцев или рецидиве симптомов [60]. Однако некоторые авторы ссылаются на повышенный риск неполного освобождения, образования рубцов, повреждения нервов и рецидива [66]. A. Aksoy указывает на то, что чрескожная декомпрессия — это вмешательство, выполняемое вслепую, и нельзя забывать о возникновении непредвиденных осложнений, таких как повреждения пальцевого нерва (гипестезия), рецидива, болезненного рубца и разрыва сухожилия [66].
Несмотря на выявленную по данным многих авторов высокую эффективность хирургического лечения СЛ, имеются публикации, свидетельствующие о сохраняющемся болевом синдроме при долгосрочном исследовании пациентов. Так, D. Langer et al. показывают, что через год после вмешательства в 37 % случаев больные жаловались на умеренные или сильные боли [67].
Однако не только хирургическое вмешательство чревато последствиями. J. Oh описывает необычный случай разрыва глубокого сгибателя пальцев после однократной инъекции кортикостероидов у 57-летнего гольфиста-мужчины [68]. На подобные осложнения указывают и другие авторы [69, 70].
ОБСУЖДЕНИЕ
Стенозирующий лигаментит — это распространенная причина инвалидности кисти, часто встречается в практической работе профильных специалистов, однако до настоящего времени выбор оптимального метода лечения является предметом дискуссий.
Лечение следует начинать с консервативных методов при наличии показаний (I–III стадии заболевания). Инъекции кортикостероидов уменьшают толщину блока А1 и считаются терапией первой линии. При этом большинство авторов отмечает невысокую эффективность гормональной терапии (43–57 %) [16, 19, 27, 28, 30, 34, 38]. Инъекции кортикостероидов следует предлагать всем пациентам перед хирургическим вмешательством, независимо от сопутствующих заболеваний [12, 41]. Индивидуальные ортопедические шины позволяют уменьшить боль, но требуют длительной иммобилизации сустава. Показатели эффективности ортезов составляют 50–93 %, в случае поражения большого пальца — менее 50 % [22, 29]. Однако анализ литературных данных, включая рандомизированные когортные исследования, показал отсутствие убедительных доказательств эффективности высокого уровня [4, 14, 15].
Большинство авторов отдает предпочтение оперативным методам [6, 26, 40, 41, 43, 60, 66]. Хирургическое лечение СЛ не следует проводить в течение трех месяцев после инъекции кортикостероидов [19, 27]. По данным многих исследователей, показатели эффективности сопоставимы как при открытом, так и при чрескожном доступе [24, 27, 42, 52, 57, 60]. Чрескожный способ считается менее инвазивной операцией, однако присутствует риск ятрогенного повреждения лучевого пальцевого нерва [36, 46, 61, 62, 63]. Открытый метод является предпочтительным, по мнению многих авторов, хотя он и связан с риском инфицирования в краткосрочной перспективе, образованием рубцовой ткани, тем не менее, имеет более высокие показатели эффективности при ретроспективном долгосрочном изучении [1, 45, 52, 53]. Кроме того, данный метод позволяет хирургам идентифицировать редкий случай атравматического разрыва сухожилия глубокого сгибателя пальцев [27].
Мы считаем, что лечение болезни Нотта должно быть индивидуальным. Каждый вариант лечения имеет свои преимущества, риски и ограничения. Перед принятием обоснованного решения необходимо обсудить эти вопросы с пациентом. Мы согласны с тем, что лечение следует начинать с консервативных методов при I–III стадии СЛ. Хирургические методы имеют более высокие показатели эффективности, однако они должны применяться в случае неэффективности консервативной терапии, при рецидиве болезни и IV стадии заболевания (рис. 6).
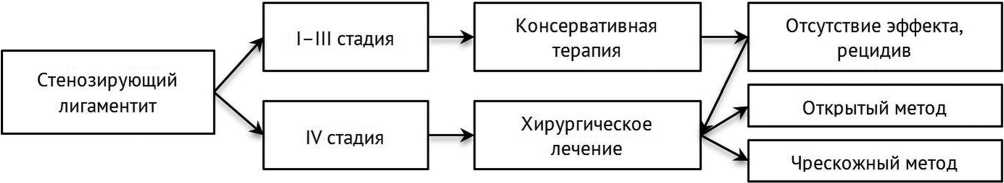
Рис. 6. Алгоритм лечения стенозирующего лигаментита
Дальнейшее изучение этиологии, патогенеза и патоморфологии СЛ поможет разработать новые методы терапии. Отдельный интерес представляет разработка новых малоинвазивных способов лечения болезни Нотта.
ЗАКЛЮЧЕНИЕ
Анализ современной литературы показал, что лечение СЛ следует начинать консервативно с инъекций кортикостероидов и/или ортопедической иммобилизации пястно-фалангового или проксимального межфалангового сустава.
Хирургическое вмешательство (открытый или чрескожный метод) показано при рецидиве после или неэффективности консервативного лечения или изначально в случаях продолжительностью > 6 месяцев. Открытое хирургическое вмешательство на связке A1 считается «золотым стандартом» вследствие минимизации осложнений и рецидивов.
Список литературы Стенозирующий лигаментит пальцев кисти
- Чуловская И.Г., Егиазарян К.А., Бадриев Д.А. и др. Стенозирующий лигаментит кольцевидных связок пальцев кисти (болезнь Нотта). Современный взгляд на диагностику и лечение. Хирургическая практика. 2023; 8(3):73-86. doi: 10.38181/2223-2427-2023-3-6
- Чуловская И.Г., Егиазарян К.А., Лядова М.В. Болезни кисти в пожилом и старческом возрасте. В кн: Гериатрия. Национальное руководство. Под ред. Ткачевой О.Н., Фроловой Е.В., Яхно Н.Н. М.: ГЭОТАР-Медиа. 2018;486-500.
- Clapham PJ, Chung KC. A historical perspective of the Notta's node in trigger fingers. J Hand Surg Am. 2009;34(8):1518-1522. doi: 10.1016/j.jhsa.2009.04.041
- Saldana MJ. Trigger digits: diagnosis and treatment. J Am Acad Orthop Surg. 2001;9(4):246-252. doi: 10.5435/00124635200107000-00004
- Lin YN, Chiu CC, Huang SW, et al. Association Between Manual Loading and Newly Developed Carpal Tunnel Syndrome in Subjects With Physical Disabilities: A Follow-Up Study. Arch Phys MedRehabil. 2017;98(10):2002-2008. doi: 10.1016/j.apmr.2017.02.008
- Hammert WC, Boyer MI, Bozentka DJ, Calfee RP. ASSH Manual of Hand Surgery. Lippincott Williams & Wilkins; 2012:656.
- Волкова А.М. Хирургия кисти. Том 1. Екатеринбург: Средне-Уральское книжное издательство; 1991:123-124.
- Каратеев А.Е., Каратеев Д.Е., Орлова Е.С., Ермакова Ю.А. «Малая» ревматология: несистемная ревматическая патология околосуставных мягких тканей верхней конечности. Часть 1. Современная ревматология. 2015;9(2):4-15. doi: 10.14412/1996-7012-2015-2-4-15
- Sampson SP, Badalamente MA, Hurst LC, Seidman J. Pathobiology of the human A1 pulley in trigger finger. J Hand Surg Am. 1991;16(4):714-21. doi: 10.1016/0363-5023(91)90200-u
- Gorsche R, Wiley JP, Renger R, et al. Prevalence and incidence of stenosing flexor tenosynovitis (trigger finger) in a meat-packing plant. J Occup Environ Med. 1998;40(6):556-560. doi: 10.1097/00043764-199806000-00008
- Wolfe SW. Tendinopathy. In: Wolfe SW, Hotchkiss RN, Pederson WC, Kozin SH, Cohen MS, eds. Green's Operative Hand Surgery. 7th ed. Philadelphia: Elsevier; 2017:1903-1925.
- Kuczmarski AS, Harris AP, Gil JA, Weiss AC. Management of Diabetic Trigger Finger. J Hand SurgAm. 2019;44(2):150-153. doi: 10.1016/j.jhsa.2018.03.045
- Новиков А.В., Щедрина М.А. О критериях оценки эффективности реабилитации больных с патологией кисти. Вестник травматологии и ортопедии им Н.Н. Приорова. 2007;(1):78-83.
- Lee YK, Kam BS, Lee KW, et al. Ten trigger fingers in an adult man: a case report. J Korean Med Sci. 2007;22(1):170-172. doi: 10.3346/jkms.2007.22.1.170
- McKee D, Lalonde J, Lalonde D. How Many Trigger Fingers Resolve Spontaneously Without Any Treatment? Plast Surg(Oakv). 2018;26(1):52-54. doi: 10.1177/2292550317740691
- Gil JA, Hresko AM, Weiss AC. Current Concepts in the Management of Trigger Finger in Adults. J Am Acad Orthop Surg. 2020;28(15):e642-e650. doi: 10.5435/JAA0S-D-19-00614
- Ashmead D 4th, Okada H, Macknin J, et al. Trigger Fingers After Open Carpal Tunnel Release. Plast Surg (Oakv). 2020;28(4):192-195. doi: 10.1177/2292550320928554
- Farr S. Open Release of Pediatric Trigger Thumb. JBJS Essent Surg Tech. 2022;12(2):e21.00053. doi: 10.2106/JBJS. ST.21.00053
- Makkouk AH, Oetgen ME, Swigart CR, Dodds SD. Trigger finger: etiology, evaluation, and treatment. CurrRevMusculoskeletMed. 2008;1(2):92-96. doi: 10.1007/s12178-007-9012-1
- Bayat A, Shaaban H, Giakas G, Lees VC. The pulley system of the thumb: anatomic and biomechanical study. J Hand Surg Am. 2002;27(4):628-635. doi: 10.1053/jhsu.2002.34008
- Ng NYY, Sirisena R, Chua YX. Management of stenosing flexor tenosynovitis in primary care. Singapore Med J. 2023;64(4):255-261. doi: 10.4103/SINGAP0REMEDJ.SMJ-2021-262
- Huisstede BM, Hoogvliet P, Coert JH, et al. Multidisciplinary consensus guideline for managing trigger finger: results from the European HANDGUIDE Study. Phys Ther. 2014;94(10):1421-1433. doi: 10.2522/ptj.20130135
- Flatt AE. Notta's nodules and trigger digits. Proc (Bayl UnivMed Cent). 2007;20(2):143-145. doi: 10.1080/08998280.20 07.11928272
- Ryzewicz M, Wolf JM. Trigger digits: principles, management, and complications. J Hand Surg Am. 2006;31(1):135-146. doi: 10.1016/j.jhsa.2005.10.013
- Golas AR, Marcus LR, Reiffel RS. Management of Stenosing Flexor Tenosynovitis: Maximizing Nonoperative Success without Increasing Morbidity. PlastReconstrSurg. 2016;137(2):557-562. doi: 10.1097/01.prs.0000475789.46608.39
- Huisstede BM, Gladdines S, Randsdorp MS, Koes BW. Effectiveness of Conservative, Surgical, and Postsurgical Interventions for Trigger Finger, Dupuytren Disease, and De Quervain Disease: A Systematic Review. Arch Phys MedRehabil. 2018;99(8):1635-1649.e21. doi: 10.1016/j.apmr.2017.07.014
- Lunsford D, Valdes K, Hengy S. Conservative management of trigger finger: A systematic review. J Hand Ther. 2019;32(2):212-221. doi: 10.1016/j.jht.2017.10.016
- Teo SH, Ng DCL, Wong YKY. Effectiveness of proximal interphalangeal joint-blocking orthosis vs metacarpophalangeal joint-blocking orthosis in trigger digit management: A randomized clinical trial. J Hand Ther. 2019;32(4):444-451. doi: 10.1016/j.jht.2018.02.007
- Mandel C. Conservative Management of Trigger Finger. 2023. Available from: https://www.medbridge.com/blog/2023/01/ conservative-management-of-trigger-finger/. Accessed Sept 5, 2024.
- Howard LD Jr, Pratt DH, Bunnell S. The use of compound F (hydrocortone) in operative and non-operative conditions of the hand. J Bone Joint Surg Am. 1953;35-A(4):994-1002.
- Matthews A, Smith K, Read L, et al. Trigger finger: An overview of the treatment options. JAAPA. 2019;32(1):17-21. doi: 10.1097/01.JAA.0000550281.42592.97
- Dardas AZ, VandenBerg J, Shen T, et al. Long-Term Effectiveness of Repeat Corticosteroid Injections for Trigger Finger. J Hand Surg Am. 2017;42(4):227-235. doi: 10.1016/j.jhsa.2017.02.001
- Clark DD, Ricker JH, MacCollum MS. The efficacy of local steroid injection in the treatment of stenosing tenovaginitis. Plast Reconstr Surg. 1973;51(2):179-180. doi: 10.1097/00006534-197302000-00014
- Wang AA, Hutchinson DT. The effect of corticosteroid injection for trigger finger on blood glucose level in diabetic patients. J Hand Surg Am. 2006;31(6):979-981. doi: 10.1016/j.jhsa.2006.03.022
- Castellanos J, Muñoz-Mahamud E, Domínguez E, et al. Long-term effectiveness of corticosteroid injections for trigger finger and thumb. J Hand Surg Am. 2015;40(1):121-126. doi: 10.1016/j.jhsa.2014.09.006
- Panghate A, Panchal S, Prabhakar A, Jogani A. Outcome of percutaneous trigger finger release technique using a 20-gauge hypodermic needle. J Clin Orthop Trauma. 2020;15:55-59. doi: 10.1016/j.jcot.2020.10.043
- Polat CS, Onat SS, Kulakli F, et al. The effectiveness of ultrasound guided local corticosteroid injection combined with orthosis in the treatment of trigger digit: a randomized controlled study. J PMR Sci. 2023:26(2):125-132. doi: 10.31609/jpmrs.2022-90423
- Shultz KJ, Kittinger JL, Czerwinski WL, Weber RA. Outcomes of Corticosteroid Treatment for Trigger Finger by Stage. Plast Reconstr Surg. 2018 0ct;142(4):983-990. doi: 10.1097/PRS.0000000000004761
- Ferrara PE, Codazza S, Maccauro G, et al. Physical therapies for the conservative treatment of the trigger finger: a narrative review. Orthop Rev (Pavia). 2020;12(Suppl 1):8680. doi: 10.4081/or.2020.8680
- Hansen RL, S0ndergaard M, Lange J. Open Surgery Versus Ultrasound-Guided Corticosteroid Injection for Trigger Finger: A Randomized Controlled Trial With 1-Year Follow-up. J Hand Surg Am. 2017;42(5):359-366. doi: 10.1016/j. jhsa.2017.02.011
- Stirling PHC, Jenkins PJ, Duckworth AD, et al. Functional outcomes of trigger finger release in non-diabetic and diabetic patients. J Hand Surg Eur Vol. 2020;45(10):1078-1082. doi: 10.1177/1753193420925027
- Fiorini HJ, Tamaoki MJ, Lenza M, et al. Surgery for trigger finger. Cochrane Database Syst Rev. 2018;2(2):CD009860. doi: 10.1002/14651858.CD009860.pub2
- Дзацеева Д.В., Титаренко И.В. Стенозирующий лигаментит пальцев кисти. Вестник хирургии им. И.И. Грекова. 2006;165(6):63-68.
- Дейкало В.П., Толстик А.Н., Болобошко К.Б. Клиническая анатомия кисти и хирургические доступы. Витебск: ВГМУ; 2013:123. Доступно по: https://core.ac.uk/download/pdf/53873562.pdf. Ссылка активна на 5.09.2024.
- Ho SWL, Chia CY, Rajaratnam V. Characteristics and Clinical Outcomes of Open Surgery for Trigger Digits in Diabetes. J Hand Microsurg. 2019;11(2):80-83. doi: 10.1055/s-0038-1670927
- Sahu R, Gupta P. Experience of Percutaneous Trigger Finger Release under Local Anesthesia in the Medical College of Mullana, Ambala, Haryana. Ann Med Health Sci Res. 2014;4(5):806-809. doi: 10.4103/2141-9248.141558
- Twu J, Patel N, Wolf JM, Conti Mica M. Impact of Variation of Corticosteroid Dose, Injection Site, and Multiple Injections on Blood Glucose Measurement in Diabetic Patients. J Hand Surg Am. 2018;43(8):738-744. doi: 10.1016/j. jhsa.2018.06.005
- Vasiliadis AV, Itsiopoulos I. Trigger Finger: An Atraumatic Medical Phenomenon. J Hand Surg Asian Pac Vol. 2017;22(2):188-193. doi: 10.1142/S021881041750023X
- Mohd Rashid MZ, Sapuan J, Abdullah S. A randomized controlled trial of trigger finger release under digital anesthesia with (WALANT) and without adrenaline. J Orthop Surg (Hong Kong). 2019;27(1):2309499019833002. doi: 10.1177/2309499019833002
- Дзацеева Д.В.. Титаренко И.В. Способ хирургического лечения стенозирующего лигаментита пальцев кисти. Вестник хирургии им. И.И. Грекова. 2008;167(1):72-74.
- Tyllianakis M, Kasimatis G, Athanaselis S, Melachrinou M. Rice-body formation and tenosynovitis of the wrist: a case report. J Orthop Surg (Hong Kong). 2006;14(2):208-211. doi: 10.1177/230949900601400221
- Kosiyatrakul A, Luenam S. Surgical Treatment for Trigger Thumb Using a Radial Approach. J Hand Microsurg. 2022;15(5):388-394. doi: 10.1055/s-0042-1749421
- Will R, Lubahn J. Complications of open trigger finger release. J Hand Surg Am. 2010;35(4):594-596. doi: 10.1016/j. jhsa.2009.12.040
- Baek JH, Chung DW, Lee JH. Factors Causing Prolonged Postoperative Symptoms Despite Absence of Complications After A1 Pulley Release for Trigger Finger. J Hand Surg Am. 2019;44(4):338.e1-338.e6. doi: 10.1016/j.jhsa.2018.06.023
- Bruijnzeel H, Neuhaus V, Fostvedt S, et al. Adverse events of open A1 pulley release for idiopathic trigger finger. J Hand Surg Am. 2012;37(8):1650-6. doi: 10.1016/j.jhsa.2012.05.014
- Laing TA, Sierakowski A, Elliot D. Management of painful scar-tethered cutaneous nerves of the upper limb. Hand Surg Rehabil. 2017;36(3):208-214. doi: 10.1016/j.hansur.2017.03.001
- Koopman JE, Zweedijk BE, Hundepool CA, et al. Prevalence and Risk Factors for Postoperative Complications Following Open A1 Pulley Release for a Trigger Finger or Thumb. J Hand Surg Am. 2022;47(9):823-833. doi: 10.1016/j. jhsa.2022.04.017
- Federer AE, Baumgartner RE, Cunningham DJ, Mithani SK. Increased Rate of Complications following Trigger Finger Release in Diabetic Patients. Plast Reconstr Surg. 2020;146(4):420e-427e. doi: 10.1097/PRS.0000000000007156
- Шастин Н.П. Десятилетний опыт применения малоинвазивной лигаментотомии при стенозирующем лигамен-тите у детей. Вопросы современной педиатрии. 2006;5(1):659. URL: https://cyberleninka.ru/ article/n/desyatiletniy-opyt-primeneniya-mal0invazivn0y-ligamentotomii-pri-stenoziruyuschem-ligamentite-u-detey/viewer
- Xie P, Zhang OH, Zheng GZ, et al. Stenosing tenosynovitis: Evaluation of percutaneous release with a specially designed needle vs. open surgery. Orthopade. 2019;48(3):202-206. doi: 10.1007/s00132-018-03676-4
- Lorthioir J Jr. Surgical treatment of trigger-finger by a subcutaneous method. J Bone Joint Surg Am. 1958;40-A(4):793-795.
- Eastwood DM, Gupta KJ, Johnson DP. Percutaneous release of the trigger finger: an office procedure. J Hand Surg Am. 1992;17(1):114-117. doi: 10.1016/0363-5023(92)90125-9
- Жигало А.В., Силаев А.К., Почтенко В.В. и др. Новая малоинвазивная методика лечения больных со стенози-рующим лигаментитом. Вопросы реконструктивной и пластической хирургии. 2017;(2(61)):53-60. doi: 10.17223/ 1814147/60/06
- Жигало А.В., Почтенко В.В., Морозов В.В. и др. Особенности выполнения чрескожной лигаментотомии связки А1 на I пальце кисти (наш опыт). Вопросы реконструктивной и пластической хирургии. 2021;24(2):64-73. doi: 10.52581/1814-1471/77/07
- Pan M, Sheng S, Fan Z, et al. Ultrasound-Guided Percutaneous Release of A1 Pulley by Using a Needle Knife: A Prospective Study of 41 Cases. Front Pharmacol. 2019;10:267. doi: 10.3389/fphar.2019.00267
- Aksoy A, Sir E. Complications of Percutaneous Release of the Trigger Finger. Cureus. 2019;11(2):e4132. doi: 10.7759/ cureus.4132
- Langer D, Luria S, Michailevich M, Maeir A. Long-term functional outcome of trigger finger. Disabil Rehabil. 2018;40(1):90-95. doi: 10.1080/09638288.2016.1243161
- Oh J, Jo L, Lee JI. Do not rush to return to sports after trigger finger injection. Am J Phys Med Rehabil. 2015;94(4):e26-30. doi: 10.1097/PHM.0000000000000267
- Tanaka T, Ogawa T, Yanai T, et al. Disruption of Flexor Tendon after Intrasheath Triamcinolone Acetonide Injection for Trigger Digits: Two Case Reports. J Hand Surg Asian Pac Vol. 2017;22(3):380-383. doi: 10.1142/S0218810417720285
- Yamada K, Masuko T, Iwasaki N. Rupture of the flexor digitorum profundus tendon after injections of insoluble steroid for a trigger finger. J Hand Surg Eur Vol. 2011;36(1):77-78. doi: 10.1177/1753193410382377


