Стресс-эхокардиография в определении инотропного резерва левого желудочка на этапах восстановительного лечения пациентов после коронарной хирургии
Автор: Тривоженко Александр Борисович, Ярощук Светлана Александровна, Семенова Юлия Владимировна, Радзивил Татьяна Тимофеевна, Козлов Сергей Вадимович
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 2 т.29, 2014 года.
Бесплатный доступ
Физическая реабилитация пациентов после коронарной хирургии является важной и неотъемлемой частью комплексного восстановительного лечения. При этом сложно оценить ее эффективность, учитывая то, что традиционные ЭКГ-методы не позволяют детализировать состояние инотропного резерва левого желудочка до и после лечения. Для более тщательной экспертизы мы предлагаем использовать велоэргометрическую стресс-ЭхоКГ с расчетом степени максимального увеличения ФВ (ΔФВ) на пике пробы. Исследование с участием 35 человек (средний возраст 51,3+,8 лет) показало, что в группе реконвалесцентов (n=12), прошедшей полный цикл физической реабилитации, значения максимальной фракции выброса (ФВ) при выполнении контрольной стресс-ЭхоКГ оказались самыми высокими (среднее - 89+2%, ΔФВ=48%). Инотропный резерв в результате комплексного хирургического, медикаментозного и восстановительного лечения увеличился на 70%. В группе пациентов (n=15), которые секвестрировали программу тренирующих процедур, отказавшись от динамических нагрузок, данные показатели были заметно ниже. Пиковая ФВ в среднем составила 83+5% (ΔФВ=37%), а итоговое увеличение резервной сократимости левого желудочка оказалось равным 28% по сравнению с исходным значением. В группе обследуемых лиц (n=8), исключивших восстановительную кинетическую терапию, ФВ на пике контрольной стресс-ЭхоКГ, в среднем оказалась равной 82+5% (ΔФВ=36%), а инотропный резерв возрос лишь на 20%.
Ишемическая болезнь сердца, стресс-эхокардиография, физическая реабилитация, инотропный резерв
Короткий адрес: https://sciup.org/14919936
IDR: 14919936 | УДК: 616.1;
Stress-echocardiography in evaluation of left ventricular inotropic reserve at stages of medical rehabilitation in patients after coronary surgery
Physical rehabilitation of patients after coronary surgery is an important part of comprehensive medical rehabilitation. However, it is challenging to evaluate efficacy of the treatment considering that traditional electrocardiographic methods do not provide detailed information about the status of left ventricular inotropic reserve before and after the treatment. To achieve detailed expert evaluation, we proposed to use cycle ergometer stress-echocardiography with calculation of the degree of maximum increase in left ventricular ejection fraction (ΔEF) at test peak. The study included 35 individuals (mean age of 51.3+7.8 years). Data showed that group of convalescents (n=12) who completed the entire program of physical rehabilitation had the highest maximum EF values (89+2%; ΔEF=48%) in control stress-echocardiography. As a result of comprehensive surgical, pharmacological, and rehabilitational treatment, left ventricular inotropic reserve increased by 70%. Group of patients (n=15) who limited the program of training procedures and cancelled dynamic loads showed significantly lower values of EF and ΔEF: peak EF was 83+5% (ΔEF=37%); the total increase in inotropic reserve was 28%. In group of individuals (n=8) who excluded the regenerative kinetic therapy, control stress-echocardiography showed peak EF of 82+5% (ΔEF=36%) and only 20%-increase in inotropic reserve.
Текст научной статьи Стресс-эхокардиография в определении инотропного резерва левого желудочка на этапах восстановительного лечения пациентов после коронарной хирургии
Реабилитация больных после операций на коронарных артериях представляет собой комплекс мероприятий, направленных на быстрое и качественное восстановление здоровья, трудового и психологического статуса реконвалесцентов. Наряду с медикаментозным лечением и физиотерапевтическими процедурами большое значение придается тренирующим программам восстановительной кинетической терапии, которые направлены на повышение толерантности к физической нагрузке [2, 4, 6].
Физическая реабилитация зависит от активности пациентов и включает лечебную физическую культуру, терренкур и дозированные подъемы по ступенькам лестницы [6].
Для оценки эффективности восстановительного лечения обычно проводится инструментальная и лабораторная диагностика наиболее важных показателей деятельности организма [5, 8]. При этом расчет интегральной систолической функции левого желудочка (ЛЖ) в процессе стандартных ультразвуковых исследований выполняется с целью определения динамического изменения общей сократимости сердечной мышцы. В настоящее время доказано, что ФВ является одним из наиболее точных и стандартизированных параметров, характеризующих систолическую функцию ЛЖ. Вместе с тем измерение ФВ в состоянии физического покоя несет весьма ограниченную информацию о резервной контрактильности миокарда [1, 9, 10, 13].
Стандартный расчет инотропного резерва (ИР) в процессе велоэргометрии (ВЭМ) с ЭКГ основан на динамическом измерении артериального давления (АД) и представляет собой разницу исходного и максимального систолического АД, причем в норме он составляет 70–75 мм рт. ст., при ишемической болезни сердца (ИБС) закономерно снижается до 50–60 мм рт. ст. [3, 7]. Значение данного показателя для восстановительной медицины трудно переоценить, так как увеличение инотропного резерва как раз и является конечной целью физической реабилитации [2, 6]. Вместе с тем “слепой” метод оценки нагрузочной сократимости ЛЖ недостаточно точен, так как уровень АД зависит не только от контрактильности миокарда, но и от тонуса периферических артерий и частоты сердечных сокращений (ЧСС). Увеличение ударного объема может сопровождаться параллельной тран-зиторной дилатацией ЛЖ, что является симптомом скрытой сердечной недостаточности [10, 16].
Вышеперечисленные обстоятельства требуют поиска новых, более точных способов определения инотропного резерва ЛЖ для экспертной оценки эффективности восстановительного лечения. Совокупность приведенных аргументов определила цель исследования: изучить возможности стресс-эхокардиографии (стресс-ЭхоКГ) с ВЭМ в определении инотропного резерва ЛЖ у пациентов с ИБС, прошедших физическую реабилитацию после хирургической реваскуляризации миокарда.
Материал и методы
Для достижения поставленной цели были приглашены 35 человек (32 мужчины и 3 женщины) в возрасте от 39 до 65 лет (средний возраст – 51,3±7,8 лет). Эндоваскулярное протезирование одной из коронарных артерии с имплантацией сосудистого стента было выполнено 17 пациентам, 14 мужчинам и трем женщинам в возрасте от 39 до 56 лет (средний возраст – 48,7±10,4 лет). Стентирование двух коронарных артерий состоялось у 5 мужчин в возрасте от 46 до 65 лет (средний возраст – 53,6±7 лет). Коронарное шунтирование маммарными артериями было выполнено 8 мужчинам в возрасте от 46 до 65 лет (средний возраст – 51,5±5 лет), комбинированное аутоартериальное и аутовенозное шунтирование – 5 мужчинам в возрасте от 57 до 65 лет (средний возраст – 59±2 лет). Из общего числа прооперированных пациентов, в 9 случаях было установлено два шунта, в 4 случаях – один.
В исследование не включались пациенты, перенесшие инфаркты миокарда, имеющие сердечную недостаточность с низкой ФВ (менее 50%), клинически значимые нарушения ритма или любые противопоказания для нагрузочных тестирований. Также были исключены пациенты с любыми хирургическими осложнениями или за- тянувшимся периодом ранней послеоперационной ре-конвалесценции (отсроченной стернорегенерацией, плевральными или перикардиальными выпотами).
Абсолютных противопоказаний для проведения активного курса физической реабилитации не было ни у одного человека, и каждому реконвалесценту был предложен амбулаторный 25-дневный цикл лечебной гимнастики, терренкура и дозированных подъемов по ступенькам лестницы.
Лечебная физкультура включала стандартный кардиологический комплекс упражнений, количество повторений каждого упражнения не превосходило 4–5 раз, длительность одного занятия не превышала 30 мин. Методика дозированной ходьбы включала начальный этап, в процессе которого скорость передвижения составляла 60 шагов в мин в течение 30 мин, а пройденное расстояние было в пределах 1–2 км. В дальнейшем темп ходьбы увеличивался и к концу лечения составлял 80–90 шагов в мин, а пройденное расстояние возрастало до 5–6 км. Ежедневные кратковременные подъемы по ступенькам лестницы происходили в медленном темпе, с периодами отдыха после 2-3 лестничных пролетов, общая продолжительность степ-нагрузки не превышала 10 мин [6].
Ультразвуковые исследования в состоянии покоя и стресс-ЭхоКГ проводились каждому обследуемому изначально, а также после завершения восстановительного лечения. Определение ИР выполнялось до операции и после окончания физической реабилитации, сроки между первой и повторной диагностическими процедурами были приблизительно одинаковыми и составляли от 5 до 6 мес. Промежуток времени от выполнения операции до проведения контрольного ультразвукового исследования, совмещенного с ВЭМ, составлял от 50 до 60 дней.
Алгоритм стресс-ЭхоКГ включал исходную тонометрию, ЭКГ, стандартную ЭхоКГ с расчетом ФВ по Teichholz et al. [13], после чего в вертикальном положении пациента на велоэргометре осуществлялся нагрузочный этап пробы в виде ступенчато возрастающего теста. Пробная нагрузка для мужчин моложе 59 лет составляла 50 Вт с последующим увеличением каждые 3 мин на 50 Вт. У всех обследуемых женщин, а также у мужчин старше 59 лет нагрузка инициировалась с 30 Вт и возрастала аналогично [3, 14, 15].
Если состояние “акустических окон” удовлетворяло требованиям полноценной визуализации всех сегментов эндокарда и миокарда ЛЖ, то ультразвуковой мониторинг в процессе физической нагрузки проводился из трансторакального доступа. У троих пациентов с неудовлетворительной визуализацией объекта выполнялась установка чреспищеводного (ЧП) датчика, и динамическое состояние ЛЖ оценивалось из трансгастрального ультразвукового доступа при осуществлении ВЭМ. При этом рвотный рефлекс угнетался внутривенным введением 8 мг ондансетрона, а также местным орошением ротоглотки спреем лидокаина [1].
На каждой ступени нагрузки регистрировались ЧСС и АД, а также измерялись конечно-систолический и конечно-диастолический объемы ЛЖ, после чего вычислялась ФВ по стандартной методике. Для максимально корректного расчета интегральной сократимости, стандар-
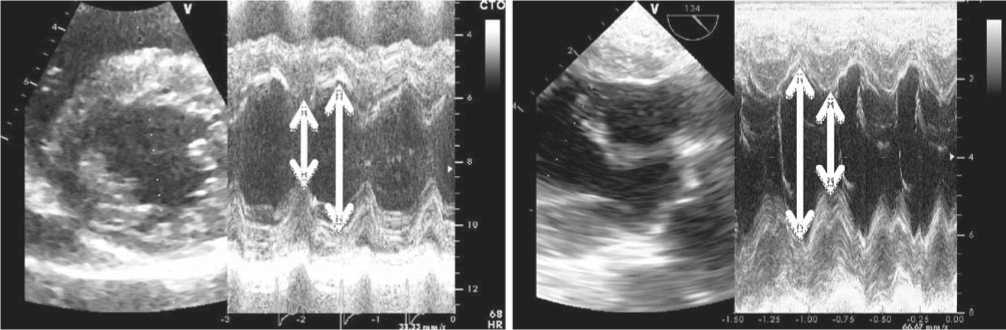
Рис. 1. Идентичные измерения систолических и диастолических размеров основания ЛЖ из парастернального доступа (левая панель) и трансгастрального доступа (правая панель)
тизированные измерения в состоянии покоя и на пике нагрузки у всех пациентов осуществлялись идентично, независимо от способа визуализации (трансторакального или чреспищеводного). С этой целью использовались предельно перпендикулярные дуплексные серошкальные “срезы” основания ЛЖ, полученные из парастернальных или трансгастральных позиций при покадровом просмотре захваченного видео (рис. 1).
В качестве параметра, наиболее точно характеризующего инотропный резерв (предельную сократимость миокарда при обеспечении нагрузочной потребности организма в оксигенации), рассматривалась степень максимального увеличения ФВ ( ∆ ФВ) на пике пробы:
∆ ДФВ = (ФВ на пике ВЭМ – ФВ в покое) / ФВ в покое х 100%.
Все исследования выполнялись в первой половине дня, одним экспертом, аппаратное оснащение включало ультразвуковой сканер GE Vivid E9 с кардиологическими и ЧП датчиками, велоэргометр Tunturi Е40, компьютерный электрокардиограф “Альтоника” и пульсоксиметр.
Права пациентов обеспечивались пунктуальным разъяснением цели и задач исследования, предоставлением подробной информации о возможных осложнениях и рисках, подписанием информированного согласия [7].
Результаты
Полную программу физической реабилитации осуществили лишь 12 чел., которые составили первую группу. Ежедневные упражнения в рамках лечебной физкультуры выполнили 15 реконвалесцентов второй группы, которые отказались заниматься дозированной ходьбой. Третью группу составили 8 чел., полностью исключивших восстановительную кинетическую терапию. Сравнительная оценка показателей, характеризующих ИР, осуществлялась между тремя группами пациентов, которые характеризовались приблизительно одинаковым возрастом и были сопоставимы по соотношению пациентов с “большой” и “малой” хирургией коронарных артерий (табл. 1).
Учитывая относительно небольшое количество наблюдений в выборках, а также отсутствие осложнений стернотомической коронарной хирургии и быстрое послеоперационное восстановление, выделение малочисленных подгрупп пациентов с коронарным шунтированием в каждой из представленных групп, было признано статистически нецелесообразным.
Для сопоставления “визуализирующего” и “слепого” методов изучения резервной сократимости ЛЖ процентное увеличение ФВ ( ∆ ФВ) сравнивалось с процентным увеличением систолического АД ( ∆ САД).
Исходная стресс-ЭхоКГ позволила определить состояние ИР у каждого больного ИБС до проведения операции и последующего восстановительного лечения. В первой группе пациентов преднагрузочная ФВ измерялась в интервале от 55 до 67% (среднее 59±4), на пике пробы – от 69 до 80% (среднее 76±3). Во второй группе изначальная ФВ варьировала в диапазоне от 52 до 62% (среднее 58±4), на пике ВЭМ – от 68 до 80% (среднее 75±5). В третьей группе пациентов исходная ФВ находилась в интервале от 54 до 62% (среднее 57±3), на пике нагрузки – от 70 до 78% (среднее 74±4). Таким образом, инотропный резерв, измеренный предложенным методом, в первой группе в среднем оказался равен 29%, во второй – 29%, а в третьей – 30%.
Таблица 1
Виды оперативного лечения и объемы физической реабилитации
|
Характеристика |
Группы пациентов |
||
|
I II |
III |
||
|
Количество |
12 |
15 |
8 |
|
Средний возраст |
53,6±7 |
51,7±9 |
52±5 |
|
Эндоваскулярное протезирование |
8 (67%) |
9 (60%) |
5 (63%) |
|
Коронарное шунтирование |
4 (33%) |
6 (30%) |
3 (37%) |
|
Вид физической реабилитации |
Количество занятий |
||
|
Лечебная физкультура |
25 (100%) |
25 (100%) |
0 (0%) |
|
Ходьба по ступенькам лестницы |
25 (100%) |
25 (100%) |
0 (0%) |
|
Терренкур |
25 (100%) |
0 (0%) |
0 (0%) |
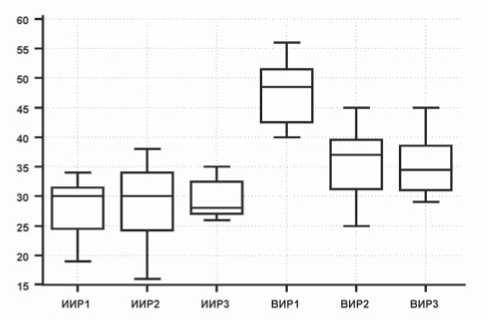
Рис. 2. Исходный инотропный резерв (ИИР%) и возросший инотропный резерв (ВИР%) в группах пациентов, рассчитанный по ∆ ФВ
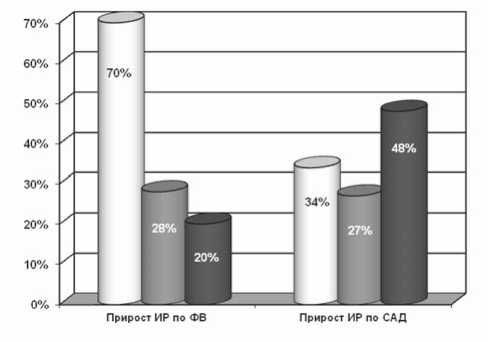
Рис. 3. Итоговый прирост инотропного резерва в группах пациентов, вычисленный “визуализирующим” методом по ∆ ФВ и “слепым” методом по ∆ САД
При расчете ИР классическим способом, по динамическому увеличению САД, было выявлено, что изучаемый показатель оказался выше в каждой из этих групп. Средние значения ДСАД составили 50, 40 и 32% соответственно (табл. 2).
Очевидная диспропорциональность между ∆ САД и ∆ ФВ была обусловлена тем, что у определенного количества пациентов нагрузочное увеличение ударного объема сопровождалось параллельной умеренной транзитор-ной дилатацией ЛЖ.
Повторно проведенное ультразвуковое исследование, совмещенное с ВЭМ, также позволило оценить динамический рост ФВ у каждого из реконвалесцентов.
В первой группе исходная ФВ измерялась в интервале от 57 до 64% (среднее 60±3), на пике ВЭМ – от 86 до 91 (среднее 89±2). Во второй группе реконвалесцентов преднагрузочная ФВ варьировала в пределах от 57 до 65% (среднее 61±4), на пике пробы – от 74 до 88% (среднее 83±5). В третьей группе обследуемых лиц исходная ФВ измерялась в интервале от 57 до 65% (среднее 60±3), на высоте физической нагрузки – от 76 до 87% (среднее 82±5). Таким образом, ИР в первой группе был в среднем равен 48%, во второй – 37%, а в третьей – 36%.
Непараметрический критерий Манна–Уитни продемонстрировал статистически значимые различия в ∆ФВ между группами. В первой группе реконвалесцентов в результате комплексного лечения ИБС (хирургического, медикаментозного, восстановительного) инотропный резерв оказался выше, чем во второй (р=0,0001) и третьей (р=0,0008) группах.
При расчете ИР традиционным методом в 1, 2 и 3-й группах пациентов было обнаружено, что средняя ∆ САД составила 67, 51 и 55% соответственно (табл. 3).
Таким образом, в первой группе реконвалесцентов, выполнивших всестороннюю программу физической реабилитации в виде статических и динамических нагрузок, инотропный резерв, определенный по ∆ ФВ, в среднем, возрос на 70%. Во второй группе, отказавшейся от терренкура, – на 28%, а в третьей группе, полностью исключившей восстановительную кинетическую терапию, – лишь на 20% (рис. 2).
Вполне очевидно, что данное обстоятельство было связано с тем, что пациенты первой группы в процессе восстановительного лечения выполняли длительные динамические нагрузки, тренирующие сердечную мышцу.
Иначе выглядело итоговое увеличение инотропного резерва, рассчитанного традиционным методом по ∆ САД. Данный показатель возрос в первой группе в среднем на 34%, во второй – на 27% и в третьей – на 48%, а данные “слепой” методики не соответствовали данным “визуализирующей” технологии. Динамическое измерение систолического АД в процессе ВЭМ показало, что у пациентов, отказавшихся от физической реабилитации, итоговый рост инотропного резерва оказался парадоксально выше, чем у реконвалесцентов, выполнивших комплекс специализированных тренирующих процедур (рис. 3).
Таблица 2
Динамическое изменение САД и ФВ в группах пациентов в процессе исходной стресс-ЭхоКГ (до проведения коронарной хирургии и комплексного восстановительного лечения)
Таблица 3
Динамическое изменение САД и ФВ в подгруппах пациентов в процессе контрольной стресс-ЭхоКГ (после завершения восстановительного лечения)
|
Группы пациентов |
САД в покое |
САД на пике ВЭМ |
∆ (%) |
ФВ в покое |
ФВ на пике ВЭМ |
∆ (%) |
|
I (n=12) |
120±10 |
180±18 |
+50 |
59±4 |
76±3 |
+29 |
|
II (n=15) |
123±11 |
172±18 |
+40 |
58±4 |
75±5 |
+29 |
|
III (n=8) |
124±14 |
170±20 |
+37 |
57±3 |
74±4 |
+30 |
|
Группы пациентов |
САД в покое |
САД на пике ВЭМ |
∆ (%) |
ФВ в покое |
ФВ на пике ВЭМ |
∆ (%) |
|
I (n=12) |
126±14 |
210±20 |
+67 |
60±3 |
89±2 |
+48 |
|
II (n=15) |
132±22 |
200±20 |
+51 |
61±4 |
83±5 |
+37 |
|
III (n=8) |
129±11 |
200±18 |
+55 |
60±3 |
82±5 |
+36 |
Обсуждение
Общеизвестно, что интеграция визуализирующих технологий в процесс оценки результатов восстановительного лечения существенно повышает ее надежность [1, 5, 8]. Стресс-ЭхоКГ позволила максимально точно определить инотропный резерв и оценить его динамическое увеличение после комплексного хирургического, медикаментозного и восстановительного лечения ИБС.
Приоритет ультразвукового метода изучения резервной сократимости ЛЖ был основан на недостаточной точности классического способа. Как известно, уровень систолического АД определяется не только глобальной систолической функцией, но зависит от ЧСС и состояния сосудистого тонуса. В проведенном исследовании было обнаружено, что увеличение ударного объема нередко сопровождалось параллельной умеренной транзи-торной дилатацией ЛЖ, в результате чего АД возрастало непропорционально увеличению ФВ, искажая истинную характеристику потенциальной контрактильности ЛЖ. Вполне очевидно, что “слепой” метод не учитывал вероятности динамического морфофункционального изменения ЛЖ в ответ на физическую нагрузку. Стресс-ЭхоКГ, напротив, базировалась исключительно на вычислении ФВ, что доказало состоятельность метода в дефиниции инотропного резерва [9–12].
Эндоваскулярное протезирование коронарных артерий и коронарное шунтирование на сегодняшний день признаны самыми эффективными методами лечения ИБС. Реконструкция нормального просвета поврежденных сосудов увеличивает инотропный резерв ЛЖ за счет воссоздания коронарного кровообращения. Однако хирургическая реваскуляризация не ликвидирует основной причины заболевания и не устраняет прогресс коронарного атеросклероза [2].
Важнейшей проблемой, на решение которой должна быть нацелена восстановительная терапия, является тренировка сердечной мышцы, а также внесердечных факторов кровообращения, уменьшающих нагрузку на миокард. Специальные упражнения стимулируют развитие коллатерального кровообращения и снижают содержание в крови холестерина, что ведет к уменьшению риска тромбообразования. При этом достижение клинического эффекта всецело зависит от комплексного подхода к физической реабилитации, недооценка какого-либо из ее разделов может снизить общую результативность восстановительного лечения [4, 6].
Исследование продемонстрировало, что реконвалесценты, прошедшие всесторонний цикл тренирующих процедур, отличались более высокими значениями потенциальной контрактильности ЛЖ. Пациенты, отказавшиеся или секвестрировавшие восстановительную кинетическую терапию, напротив, характеризовались низкими показателями инотропного резерва.
Кроме этого подтвердилась первостепенная роль длительных аэробных динамических нагрузок в укреплении сердечной мышцы, доказано, что терренкур и дозированная ходьба по ступенькам лестницы позитивным образом отразились на функциональном состоянии сердечно-сосудистой системы.
Выводы
-
1. Благодаря точности расчета ФВ ЛЖ, велоэргометри-ческая стресс-ЭхоКГ обладает большей информативностью в определении и детализации инотропного резерва, чем общепринятые нагрузочные электрокардиографические и тонометрические методы.
-
2. Инотропный резерв у кардиохирургических пациентов, прошедших всестороннюю программу восстановительной кинетической терапии, включающей динамические аэробные нагрузки, существенно выше, чем у реконвалесцентов, исключивших или секвестрировавших физическую реабилитацию.
Список литературы Стресс-эхокардиография в определении инотропного резерва левого желудочка на этапах восстановительного лечения пациентов после коронарной хирургии
- Абалмасов В.Г., Тривоженко А.Б., Стручков П.В. Трансторакальная и чреспищеводная стресс-эхокардиография. -М.: ИД Медпрактика-М, 2012. -96 с.
- Аретинский В.Б. Система восстановительного лечения после операций аортокоронарного шунтирования и эндоваскулярного протезирования коронарных артерий: автореф. дис.. докт. мед. наук. -М., 2008. -42 с.
- Аронов Д.М., Лупанов В.П. Функциональные пробы в кардиологии, 3-е изд. перераб. и доп. -М.: МЕДпресс-информ, 2007. -328 с.
- Басов Г.В., Макарова И.Н. Реабилитация пациентов после оперативного лечения ишемической болезни сердца//Физиотерапия, бальнеология и реабилитация. -2010. -№ 1. -С. 30-37.
- Бобровницкий И.П., Павлов В.Н., Разумов А.Н. и др. Диагностические технологии восстановительной медицины//Новые медицинские технологии. -2010. -№ 10. -С. 3943.
- Епифанов В.А. Медицинская реабилитация: руководство для врачей/под ред. В.А. Епифанова. -2-е изд., испр. и доп. -М.: МEДпресс-информ, 2008. -352 с.
- Кужель Д.А., Матюшин Г.В., Савченко Е.А. и др. Нагрузочные пробы в кардиологии: обеспечение безопасности при проведении и интерпретация результатов: учебное пособие для последипломного образования врачей -Красноярск: КрасГМУ, 2009. -114 с.
- Лямина Н.П., Котельникова Е.В., Карпова Э.С. Новые подходы к оценке качества реабилитационно-профилактических мероприятий у пациентов с ишемической болезнью сердца//Кардиология. -2009. -№ 5. -С. 48-52.
- Aboukhoudir F., Rekik S. Left ventricular systolic function deterioration during dobutamine stress echocardiography as an early manifestation of diabetic cardiomyopathy and reversal by optimized therapeutic approach//Int. J. Cardiovasc. Imaging. -2012. -Vol. 28. -Р. 1329-1339.
- Donal E., Thebault1 C., Lund L.H. et al. Heart failure with a preserved ejection fraction additive value of an exercise stress echocardiography//Eur. Heart J. Cardiovasc. Imaging. -2012. -Vol. 13. -Р. 656-665.
- Emmett L., Ng A., Ha L. et al. Comparative assessment of rest and post-stress left ventricular volumes and left ventricular ejection fraction on gated myocardial perfusion imaging and echocardiography in patients with transient ischemic dilation on adenosine MPI: Myocardial stunning or subendocardial hypoperfusion?//J. Nucl. Cardiol. -2012. -Vol. 19. -Р. 735-742.
- Mehrotra P., Labib S.B., Schick E.C. Differential effects of dobutamine versus treadmill exercise on left ventricular volume and wall stress//J. Am. Soc. Echocardiogr. -2012. -Vol. 25. -P. 911-918.
- Nihoyannopoulos P., Kisslo J. Echocardiography. -London: Springer-Verlag, 2009. -667 р.
- Picano E. Stress Echocardiography: 5th, completely revised and updated edition. -Berlin: Springer-Verlag, 2009. -630 р.
- Peteiro J., Bouzas-Mosquera A. Exercise echocardiography//World J. Cardiol. -2010. -Vol. 8. -Р. 223-232.
- Squeri A., Gaibazzi N., Reverberi C. et al. Ejection fraction change and coronary artery disease severity: a vasodilator contrast stress-echocardiography study//J. Am. Soc. Echocardiogr. -2012. -Vol. 25. -P. 454-459.


