Строение Органических и элементоорганических соединений. Сообщение 6
Автор: Шарутин В.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 2 т.17, 2025 года.
Бесплатный доступ
Взаимодействием эквимолярных количеств пентафенилсурьмы с карбоновыми кислотами в бензоле синтезированы и структурно охарактеризованы карбоксилаты тетрафенилсурьмы Ph4SbOC(O)R (R=CНF2 (1), CF2CF2CF3 (2), C6H4Cl-2 (3), C6H4Br-3 (4), C6Н3F2-2,5 (5), C6H3F2-2,3 (6), C6F4H (7), C6F5 (8), в которых атомы сурьмы имеют искаженную тригонально-бипирамидальную координацию с атомом кислорода карбоксигрупп в аксиальном положении. Присутствие координационной связи центрального атома металла с карбонильным атомом кислорода позволяет говорить об увеличении координационного числа атома сурьмы до 6. Анализ структурных данных карбоксилатов тетрафенилсурьмы показывает, что искажение тригонально-бипирамидальной конфигурации молекул проявляется в разной степени. Анализ структурных данных карбоксилатов тетрафенилсурьмы 1-8 показывает, что искажение тригонально-бипирамидальной конфигурации молекул проявляется в разной степени. Длины связей С=О (1,197(3)-1,284(7) Å) короче длин связей С-О (1,196(18)-1,231(8) Å) (длины двойных связей в карбоновых кислотах (1,226-1,229 Å). Расстояния Sb-С в молекулах 1-8 находятся в интервале 2,095(6)-2,167 Å, причем расстояние Sb-Cакс (2,154(3) Å (2) - 2,174(4) Å (5)) выше экваториальных связей Sb-Cэкв. Кроме того, имеются внутримолекулярные контакты между атомом сурьмы и карбонильным кислородом (3,100(5) Å (5) - 3,517(6) Å (2)), что меньше суммы ван-дер-ваальсовых радиусов этих атомов (3,700 Å). Максимальный экваториальный угол со стороны контакта Sb∙∙∙O=C (120,7(2)°-130,67(14)°) меньше двух других экваториальных углов. Величины аксиальных углов CаксSbO варьируют от 171,97° (1) до 179,12(6)° (8). Эффект транс -влияния в ряду карбоксилатов тетрафенилсурьмы (при возрастании длины связи Sb-O расстояние Sb-Сакс укорачивается) в основном выполняется. Длины связей Sb-O в карбоксилатах тетрафенилсурьмы 1-8 изменяются в диапазоне (2,278-2,340 Å), и значительно превышают сумму ковалентных радиусов атомов сурьмы и кислорода (2,07 Å). Минимальное отклонение длины связи Sb-O от суммы ковалентных радиусов атомов сурьмы и кислорода имеет место в соединении 3, максимальное - в соединении 2.
Карбоксилат тетрафенилсурьмы, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147248078
IDR: 147248078 | УДК: 546.865+548.3+548.312.4 | DOI: 10.14529/chem250206
Structure of organic and organoelemental compounds. Part 6
Tetraphenylantimony carboxylates Ph4SbOC(O)R (R=CHF2 (1), CF2CF2CF3 (2), C6H4Cl-2 (3), C6H4Br-3 (4), C6H3F2-2,5 (5), C6H3F2-2,3 (6), C6F4H (7), C6F5 (8) have been synthesized by the interaction of equimolar amounts of pentaphenylantimony with carboxylic acids in benzene; their structures have been characterized. In these carboxylates, the antimony atoms have a distorted trigonal-bipyramidal coordination with the oxygen atom of carboxyl groups in the axial position. The presence of a coordination bond between the central atom and carbonyl oxygen atom suggests an increase in the coordination number of the antimony atom to 6. Analysis of the structural data of tetraphenylantimony carboxylates shows that the distortion of the trigonal-bipyramidal configuration of molecules 1-8 manifests itself to varying degrees. The C=O bond lengths (1.197(3)-1.284(7) Å) are shorter than the C-O bond lengths (1.196(18)-1.231(8) Å), while the lengths of double bonds in carboxylic acids are (1.226-1.229 Å). The Sb-C distances in molecules 1-8 are in the range of 2.095(6)-2.167 Å, and the Sb-Cax distance (2.154(3) Å (2) - 2.174(4) Å (5)) is higher than the Sb-Ceq equatorial bonds. In addition, there are intramolecular contacts between the antimony atom and the carbonyl oxygen (3.100(5) Å (5) - 3.517(6) Å (2)), which is less than the sum of the van der Waals radii of these atoms (3.700 Å). The maximum equatorial angle on the side of the Sb∙∙∙O=C contact (120.7(2)°-130.67(14)°) is less than the other two equatorial angles. Complete tables of atomic coordinates, bond lengths and valence angles have been deposited with the Cambridge Crystallographic Data Centre (No 2115014 (1), 1876829 (2), 2214913 (3), 2214921 (4), 2115013 (5), 2233398 (6), 1919918 (7), 1821410 (8); deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Текст научной статьи Строение Органических и элементоорганических соединений. Сообщение 6
Известно, что во многих комплексах переходных металлов карбоксилатные заместители проявляют бидентатные свойства, играя роль мостиковых или хелатирующих лигандов [1 - 3]. Наличие карбоксилатного лиганда в ацилатах тетраарилсурьмы допускает реализацию дополнительной внутримолекулярной координации атома сурьмы с карбонильным кислородом. Впервые внутримолекулярное взаимодействие Sb∙∙∙O=C обнаружили Боне и Соверби при изучении строения формиата [4] и ацетата тетрафенилсурьмы [5]. Они установили, что расстояния между атомом сурьмы и карбонильным кислородом, формально несвязанными друг с другом, составляют 3,291 и 2,594 Å соответственно при сумме ван-дер-ваальсовых радиусов атомов сурьмы и кислорода равной 3,70 A [6]. Расстояние Sb—O=C во втором комплексе является аномально коротким среди всех известных к настоящему времени карбоксилатов тетрафенилсурьмы [7 - 10] и приближается по своему значению к сумме ковалентных радиусов сурьмы и кислорода (2,05 Å [6]).
С целью исследования строения карбоксилатов тетрафенилсурьмы был синтезирован ряд указанных соединений: Ph 4 SbOC(O)R (R=CНF 2 ( 1 ), CF 2 CF 2 CF 3 ( 2 ), C 6 H 4 Cl-2 ( 3 ), C 6 H 4 Br-3 ( 4 ), C 6 Н 3 F 2 -2,5 ( 5 ), C 6 H 3 F 2 -2,3 ( 6 ), C 6 F 4 H ( 7 ), C 6 F 5 ( 8 ) и изучены особенности их строения.
Экспериментальная часть
Карбоксилаты тетрафенилсурьмы синтезировали по методике, описанной в [9]. В работе использовали карбоновые кислоты производства фирмы Alfa Aesar. Элементный анализ выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
ИК-спектры соединений 1 - 8 записывали на ИК-спектрометре Shimadzu IRAffinity-1S в таблетках KBr в области 4000–400 см–1.
РСА кристаллов 1-8 проведен на дифрактометре D8 Quest фирмы Bruker (MoKa-излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [11]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [12] и OLEX2 [13]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Основные кристаллографические данные и результаты уточнения структур 1-8 приведены в табл. 1. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2115014 (1), 1876829 (2), 2214913 (3), 2214921 (4), 2115013 (5), 2233398 (6), 1919918 (7), 1821410 (8); ; .
|
GO |
Ёл ь 6 о X о |
гч о 'Г |
те я к S о 2 |
7 £ |
гч 40 |
5 00* |
■п сЧ 7 о см |
о о S |
СМ |
о о § |
ос 40 CM |
тГ |
О ОО in |
04 О |
О ос см |
R о X тег о X •п о |
ОО in ос ос 40" |
o’ ф ос V VI VI VI VI VI О С ?? 7 7 1 |
in |
см о ОО |
о ОС о |
tn m о |
00 теГ |
. ©4 СП ГЧ — О tn — °. о ° II II ем - ^ |
. ГЧ о о теГ ГЧ 04 - Чо ° II II ем - ос £ |
ГЧ 04 О 'Я, |
|
Г- |
л и О К о |
40 |
| - |
i |
04 a? |
in ш tn °1 o’ |
о in |
ОС см о ОО |
О г-1 оо |
5 40 |
гч 40 |
см |
2 |
04. о |
°, о см 40 |
см о X тег о X ш *4 о |
^ 40 00 СМ о 40 |
О о" С' — - еМ VI VI VI VI VI Vl 22п 7 1 1 |
О |
04 О о см |
гч 4© с о" |
о о |
да |
. 04 1П 04 теГ О °. О ° II н 7 |
in 2 ос О £5 1! 7 - 00 - в |
4© теГ |
|
© |
7 £ О |
гч 00 tn |
те га о. н |
5 |
40 oo 0- |
o' |
ОС 00 |
ОО А. ос |
□o' ом гм ОО |
СМ О ос 40 |
1 |
см |
ОС |
in ОО о |
о ос мп |
О' о о X *4 о' X те? о' |
С* ОС 40 ОО о 4© |
«ri v^ ем — — С 1 VI VI VI VI VI Vl « « . 7 । । |
©4 04 ОС tn |
о |
ОС о о |
tn о |
СМ |
ее, О О ° II н 7 г |
е О ч© 40 ОС О Чо ° II II - 00 00 - |
СМ © О 7 о 7 o’ |
|
IT. |
7 о Я и |
гч |
те га a |
st гч ^ |
04 |
tn ОС ОС ОС см |
ОО |
о o' 04. |
"С tn |
О o' 04. |
о чО см |
^ |
40 04 |
ОС о |
Ог 4СГ |
п о см гч о X «п тег о |
00 in 4©' |
ем чо ем VI VI VI VI VI VI ем Ф 22 77 । |
О см |
2 in |
04 |
СП 40 'Ч |
СМ |
г ОО 04 40 ОС г 3 5 £ |
ОС 04 40 Г-теГ О Ч о 7 11 Г-1 - 7 00 £ |
СМ >n 7 ш ч© о |
|
“Т |
и И 3 к и |
<О о СП 40 |
те га a a Н |
al |
об" о |
СЮ о ОГ |
© in |
■3 ОС |
in 40 *4 оС |
5 2 |
СМ 04 |
см |
2 |
7 |
о. гм 40 |
см o' X гп о X 04 о |
ОО ОО 40 |
теГ 7 О — — ci VI VI VI VI VI vi г+ О Z — м 7 । 1 |
ос in о о ОО |
о гч 00 |
о гч а о’ |
о о |
40 |
е- СМ СМ — Г- 4© СМ О Ч о ° II II ем - ^ |
m о Оф ° II и 7 - о; S |
■да ч о” |
|
m |
и О к и |
о tn in |
те га a о 2 |
гч a. |
CM ^r о |
in |
in с о |
о о о 04. |
04 00 04 4© o' о |
о § |
in in ОС гч |
’Г |
О |
04 |
о 40 |
СП о X ГП о X 40 м о |
ОО ОО о |
Г"- *П 04 ^ см гч VI VI VI -st ^ ^ VI VI Vl 40 $4 77" |
©4 СМ ОО |
о 04, СП |
40 О ОС о. о |
гч 40 О |
ОО теГ |
40 1П — 4© ° ГЧ "г o' 7 |
7 3 2 ° и л 7 - о; « S |
'да 7 <4 7 |
|
см |
и 7 О ^ о |
04 5 о |
a a a 2 |
к s |
tn ОС ОС о о |
04 *4 |
о ОС' in |
о Ог о 04 |
in 40 сп in о |
о О о" 04 |
Ct in 40 CM |
't |
04 О © |
гч |
о см см |
■да о X ГП о X in о |
о 00 in |
О ОС 40 ~ гч см VI VI VI Vl VI VI ф ж 7 7 7 । |
in ОО |
о ОС СМ |
in о о о |
2 о |
СП |
~ ° ° и и 7 - ч s |
Ч© 2 Г- СМ 00 — Ое О О II II гч - 00 £ |
о 7 o' |
|
w* |
О |
ОО in гч in |
те a s |
Q |
сч ■да сь 04 |
ОС ОС 04 ос |
ОО 04 |
о” 04 |
СМ см СП 04 ©* о |
о о o' 04. |
'I о" ОО гч ГЧ |
04 Я |
те? |
о ОС о |
04. о о X СП о X 7 о |
4© о 7 ос |
r i ri г— см —• VI VI VI -s: -^ -" VI VI VI ем ем 40 77 । |
гч |
04 о см |
теГ СМ О, о" |
© П1 |
О'. ГЧ СМ |
г см 40 о tn tn Ое О 5 7 «1 |
ОС о •п ш 3,5 * * |
ГЧ 04 о 7 о °^ о |
|
|
В s я а К |
К аз о а Р О- >. X V 5 |
5 |
те a о и |
те га да я H ^ О ex c |
°*С |
«^ |
“£ |
5 & в |
# е |
5 Р |
«с к |
N |
сп |
's i |
о о о с |
г 2 га a 0 * Он О га С- |
га 2 о ^ ^ ф Я 7 О О га х a a ч 5 |
да о да о a a a о га a я a Ч |
X a a со — О 2 2 сп да а -е-о 2 да ^ a т |
X 3 а щ = 8 да 2 2 ^ да с о - е « 8 “ о a 07 |
7 |
о о 43 |
да о 0 г га га a о да о a ^ |
s 0 (М А о a О. о га ^ ci |
2 о о « 2 S Й с о 3 о о. ч о л. g К 7 |
да о 5^7 2 2 о Е с о £ те .S я 2 Ё О я S |
Обсуждение результатов
Показано, что карбоксилатах тетрафенилсурьмы 1 - 8 атом сурьмы имеет тригонально-бипирамидальную координацию (см. рисунок). Анализ структурных данных карбоксилатов тет-рафенилсурьмы показывает (табл. 2), что искажение тригонально-бипирамидальной конфигурации молекул проявляется в разной степени. Длины связей С=О (1,197(3) - 1,284(7) А) короче длин связей С - О (1,196(18) - 1,231(8) А) (длины двойных связей в карбоновых кислотах (1,226-1,229 А [13]). Расстояния Sb-С в молекулах 1 - 8 находятся в интервале 2,095(6) - 2,167 А, причем расстояние Sb-С акс (2,154(3) А ( 2 ) - 2,174(4) А ( 5 )) выше экваториальных связей Sb - Cэкв. Кроме того, имеются внутримолекулярные контакты между атомом сурьмы и карбонильным кислородом (3,100(5) А ( 5 ) - 3,517(6) А ( 2 )), что меньше суммы ван-дер-ваальсовых радиусов этих атомов (3,700 Å). Максимальный экваториальный угол со стороны контакта Sb∙∙∙O=C
(120,7(2) °- 130,67(14) ° ) меньше двух других экваториальных углов. Величины аксиальных углов CаксSbO варьируют от 171,97 ° ( 1 ) до 179,12(6) ° ( 8 ). Эффект транс -влияния в ряду карбоксилатов тетрафенилсурьмы (при возрастании длины связи Sb - O расстояние Sb - С акс укорачивается) в основном выполняется.
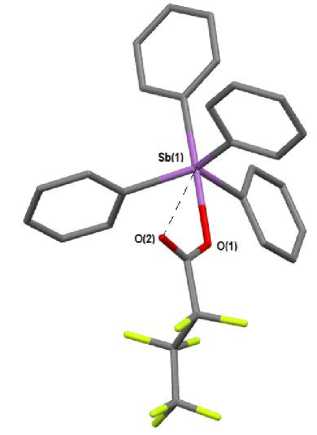
Строение гептафторбутаната тетрафенилсурьмы (3). (атомы водорода не показаны)
Таблица 2
Проявление бидентатных свойств карбоксилатного лиганда в карбоксилатах тетрафенилсурьмы
|
№ |
Соединение |
d Sb - O, А |
d Sb∙∙∙O=C, Å |
d Sb∙∙∙O=C d Sb - O |
d Sb - C aK„ Å |
^ max C экв SbC экв |
^ C акс SbO |
|
3 |
Ph 4 SbOC(O)C 6 H 4 Cl-2 |
2,278(4) |
3,352(5) |
1,47 |
2,167(5) |
127,5(2) |
177,19(18) |
|
6 |
Ph 4 SbOC(O)C 6 H 3 F 2 -2,3 |
2,2838(19) |
3,183(19) |
1,394 |
2,165(2) |
129,29(8) |
177,84(6) |
|
4 |
Ph 4 SbOC(O)C 6 H 4 Br-3 |
2,294(2) |
3,139(4) |
1,37 |
2,171(3) |
129,36(9) |
177,79(6) |
|
1 |
Ph 4 SbOC(O)CHF 2 |
2,303(8) |
3,454(9) |
1,5 |
2,161(6) |
120,7(2) |
171,97(2) |
|
7 |
Ph 4 SbOC(O)C 6 F 4 H-2 |
2,3070(18) |
3,233(19) |
1,401 |
2,1705(19) |
127,86(7) |
177,92(4) |
|
8 |
Ph 4 SbOC(O)C 6 F 5 |
2,3176(15) |
3,510(16) |
1,514 |
2,1666(19) |
130,31(7) |
179,12(6) |
|
5 |
Ph 4 SbOC(O)C 6 H 3 F 2 -2,5 |
2,318(3) |
3,100(4) |
1,337 |
2,174(4) |
130,67(14) |
177,73(10) |
|
2 |
Ph 4 SbOC(O)CF 2 CF 2 CF 3 |
2,340(2) |
3,517(3) |
1,5 |
2,154(3) |
124,46(10) |
178,87(8) |
Длины связей Sb–O в карбоксилатах тетрафенилсурьмы 1–8 изменяются в диапазоне (2,278– 2,340 Å), и значительно превышают сумму ковалентных радиусов атомов сурьмы и кислорода (2,07 Å [6]). Минимальное отклонение длины связи Sb–O от суммы ковалентных радиусов атомов сурьмы и кислорода имеет место в соединении 3, максимальное – в соединении 2. Геометри- ческие параметры синтезированных соединений 1–8 близки к аналогичным для известных карбоксилатов тетрафенилсурьмы [15-25].
Заключение
Таким образом, в карбоксилатах тетрафенилсурьмы, полученных с выходом до 90 % из пен-тафенилсурьмы и карбоновой кислоты, атомы сурьмы имеют искаженную тригонально-бипирамидальную координацию с атомом кислорода в аксиальных положениях и тремя фенильными лигандами - в экваториальных. Анализ структурных данных полученных в работе карбоксилатов тетрафенилсурьмы показывает, что искажение тригонально-бипирамидальной конфигурации молекул 1–8 проявляется в разной степени, а их геометрические параметры близки к аналогичным, наблюдаемым в известных карбоксилатах тетрафенилсурьмы.


