Структура 1,1′-(2,6-пиридиндиил)бис[6,7-дигидро-4-(4-метоксифенил)-5H- циклопента[с]пиридина
Автор: Рыбакова А.В., Ватолина C.E., Криночкин А.П., Гавико В.С., Шабунина О.В., Сайфутдинова Ю.М., Маркина А.С., Алексеева А.С., Копчук Д.С., Зырянов Г.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 1 т.18, 2026 года.
Бесплатный доступ
1,1′-(2,6-Пиридиндиил)бис[6,7-дигидро-4-(4-метоксифенил)-5H-циклопента[c]пиридин был с хорошим выходом (52 %) получен взаимодействием 3,3′-(2,6-пиридиндиил)бис[6-(4- метоксифенил)-1,2,4-триазина] с 1-морфолинциклопенетном при сплавлении в отсутствие раствори- теля при 200 °С, т. е. был реализован PASE-подход в отличие от ранее предложенного в литературе кипячения в 1,4-диоксане. Структура полученного соединения была подробно изучена с помощью рентгеноструктуного анализа его монокристалла, проведено сравнение с ранее описанными в лите- ратуре сведениями (в частности, длин связей между атомами и валентных углов, а также взаимного расположения ароматических фрагментов). Описаны особенности супрамолекулярной структуры данного соединения, не описанные ранее для данной структуры, в частности, выявлено расположение двух мономеров, сложенных по принципу «голова к голове», обеспечивающее минимальное расстояние между соседними структурами.
2, 2':6', 2''-терпиридины, реакция Боджера, рентгеновская кристаллография
Короткий адрес: https://sciup.org/147253376
IDR: 147253376 | УДК: 548.3 | DOI: 10.14529/chem260110
The structure of 1,1′-(2,6- pyridindiyl)bis[6,7-dihydro-4-(4-methoxyphenyl)-5H-cyclopenta[c]pyridine
1,1'-(2,6-Pyridinediyl)bis[6,7-dihydro-4-(4-methoxyphenyl)-5H-cyclopenta[c]pyridine was obtained in good yield (52%) by reacting 3,3'-(2,6-pyridinediyl)bis[6-(4-methoxyphenyl)-1,2,4-triazine] with 1-morpholincyclopene during its solvent-free fusion at 200 °C, i.e., the PASE approach was implemented in contrast to the previously proposed boiling in 1,4-dioxane in the literature. The structure of the obtained compound was studied in detail using X-ray structure analysis of its single crystal, and a comparison was made with information previously described in the literature (in particular, the bond lengths between atoms and the valence angles, as well as the mutual arrangement of aromatic fragments). The features of the supramolecular structure of the obtained compound that had not been described previously were characterized, including the arrangement of two monomers stacked head-to-head, which ensured the minimal distance between adjacent structures.
Текст научной статьи Структура 1,1′-(2,6-пиридиндиил)бис[6,7-дигидро-4-(4-метоксифенил)-5H- циклопента[с]пиридина
2,2':6',2''–Терпиридины представляют существенный практический интерес. В частности, они могут быть использованы для получения линейных макромолекул [1]. Также они являются лигандами для получения металлокомплексов с перспективными свойствам. Они могут найти применение при создании новых материалов благодаря наличию фотолюминесцентных свойств [2, 3], а также участвовать в различных каталитических, электрохимических и фотохимических процессах [4–6].
Одним из подходов к 2,2':6',2''-терпиридинам является синтез через их бис -1,2,4-триазиновые прекурсоры в результате реакции Боджера [7]. При этом возможно аннелирование циклоалкановых фрагментов к вновь образующимся пиридиновым кольцам при использовании в данной реакции енаминов [8, 9]. В частности, по такой методологии был получен 1,1′-(2,6-пиридиндиил) бис [6,7-дигидро-4-(4-метоксифенил)-5 H -циклопента[ c ]пиридин 1 [10] в результате гетероциклизации гидразона 4'-метоксиизонитрозоацетофенона 2 и пиридин-2,6-дикарбальдегида, а последующее превращение бис -1,2,4-триазинового прекурсора 3 в соответствующий терпири-дин было выполнено при кипячении в 1,4-диоксане в течение 6 ч (схема 1). В этой же работе была описана структура соединения 1 .
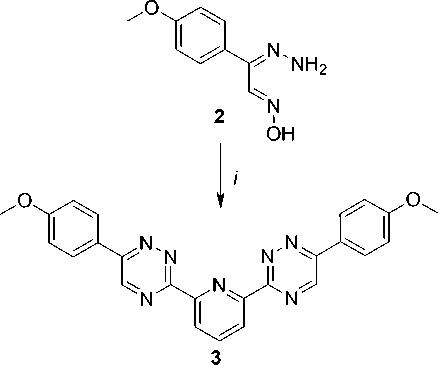
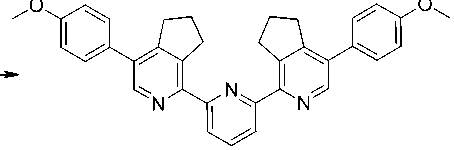
Схема 1. Ранее описанный синтез соединения 1. Реагенты и условия: i) пиридин-2,6-дикарбальдегид / AcOH, кипячение (1 мин);
ii) ii ) 1-морфолинциклопентен / диоксан, кипячение, 6 ч
В то же время известно, что в случае наличия в структуре 1,2,4-триазинового субстрата электронодонорных заместителей их активность в реакциях аза-Дильса–Альдера снижается, эффективным способом их трансформации в соответствующие пиридины в этом случае является взаи- модействие с 1-морфолинциклопентеном в отсутствие растворителя [11, 12], применимость данной методологии была показана в том числе на примере получения 2,2':6',2''–терпиридинов [13].
Целью настоящей работы является исследование возможности синтеза 1,1′-(2,6-пиридиндиил) бис [6,7-дигидро-4-(4-метоксифенил)-5 H -циклопента[ c ]пиридина без использования растворителя (PASE-подход), а также изучение его структуры методом РСА, в сравнении с имеющимися в литературе сведениями.
Экспериментальная часть
Исходный 3,3′-(2,6-пиридиндиил) бис [6-(4-метоксифенил)-1,2,4-триазин] ( 3 ) был получен по ранее предложенной методике [7]. Все остальные реагенты коммерчески доступны.
Синтез 1,1′-(2,6-пиридиндиил) бис [6,7-дигидро-4-(4-метоксифенил)-5 H -циклопента[ c ]пи-ридина (1).
Смесь 1,2,4-триазина 3 (224 мг, 0,50 ммоль) и 1-морфолинциклопентена (0,8 мл, 5,0 ммоль) перемешивают на магнитной мешалке при 200 ºС в атмосфере аргона в отсутствие растворителя в течение 2 ч. Затем к реакционной смеси добавляют дополнительную порцию 1-морфолинциклопентена (0,4 мл, 2,5 ммоль) и реакционную массу перемешивают при 200 °С в течение дополнительного часа. Продукт выделяют колоночной хроматографией (элюент – хло-роформ-этилацетат (9:1), R f 0,5). Аналитический образец получен перекристаллизацией из этанола. Выход 137 мг (52 %). Спектр ЯМР 1H (400 МГц, CDCl 3 , м. д., J /Гц): 2,03–2,11 (м, 4Н, C(6)H 2 ); 3,06 (т, 2H, C(7)H 2 , 3 J = 7,6 Гц); 3,43 (т, 2H, C(5)H 2 , 3 J = 7,6 Гц); 3,88 (c, 6H, OMe); 7,00–7,06 (м, 4Н, C 6 H 4 OMe); 7,44–7,49 (м, 4Н, C 6 H 4 OMe); 7,96 (дд, 1Н, 3 J = 8,0, 8,0 Гц, H-4(Py); 8,17 (д, 2Н, 3 J = 8,0 Гц, H-3(Py) и H-5(Py)); 8.55 (с, 2Н, Н-5′(Py) и Н-5′′(Py)). MS ESI: m/z ( I , %): 526,25 (100) [M+H]+. Найдено (%): C 79,89; H 5,83; N 8,12. C 35 H 31 N 3 O 2 . Вычислено (%): C 79,97; H 5,94; N 7,99.
Масс-спектр (тип ионизации – электрораспыление) записан на приборе Agilent Infinity II фирмы Agilent Technologies.
Спектр ЯМР 1H записан на спектрометре Bruker Avance-400 (400 МГц, внутренний стандарт – SiMe 4 ).
Элементный анализ выполнен на CHN анализаторе РЕ 2400 II фирмы Perkin Elmer.
Рентгеноструктурный анализ (РСА) кристалла соединения 1 был проведён на автоматическом четырехкружном дифрактометре Rigaku XtaLAB Synergy с CCD-детектором HyPix-6000HE и источником рентгеновского излучения PhotonJet по стандартной процедуре (MoKα-излучение, графитовый монохроматор, ω-сканирование с шагом 1°) при T = 295(2) K. Была применена эмпирическая поправка на поглощение. Данные измеренных отражений проиндексированы, интегрированы и масштабированы с использованием пакета программ CrysAlisPro [14]. Структуры расшифрованы методом внутренней фазировки по программе SHELXT [15] и уточнены методом наименьших квадратов по F2 с использованием программы SHELXL [16]. Расшифровка и уточнение структуры проведены в программной оболочке Olex2 [17]. Неводородные атомы уточнены в анизотропном приближении. Атомы водорода при атомах кислорода выявлены из разностных рядов Фурье. Все остальные атомы водорода помещены в вычисленные положения в соответствии со стереохимическими критериями и уточнены по «схеме наездника». Результаты РСА зарегистрированы в Кембриджской базе структурных данных под номером CCDC 2513600. Эти данные находятся в свободном доступе и могут быть запрошены по адресу
Основные кристаллографические данные и результаты уточнения структуры 1,1′-(2,6-пиридиндиил)бис[6,7-дигидро-4-(4-метоксифенил)-5H-циклопента[c]пиридина приведены в табл. 1.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 1,1′-(2,6-пиридиндиил) бис [6,7-дигидро-4-(4-метоксифенил)-5 H -циклопента[ c ]пиридина
|
Параметр |
Значение |
Параметр |
Значение |
|
Формула |
C 35 H 31 N 3 O 2 |
ρ (выч.), г/см3 |
1,247 |
|
М |
525,63 |
µ , мм–1 |
0,078 |
|
Сингония |
моноклинная |
F (000) |
1112,0 |
Окончание табл. 1
|
Параметр |
Значение |
Параметр |
Значение |
|
Пр. группа |
С 2/c |
Размер кристалла, мм |
0,422 × 0,207 × 0,087 |
|
a , Å |
16,4000(4)) |
Область сбора данных по 2 θ , град. |
5,22–48,434 |
|
b, Å |
15,6021(4) |
Интервалы индексов отражений |
–21 ≤ h ≤ 22, –21 ≤ k ≤ 20, –14 ≤ l ≤ 15 |
|
c, Å |
11,0445(2) |
Измерено отражений |
46590 |
|
α, град. |
90 |
Независимых отражений |
3617 [R int = 0,0518, R sigma = 0,0275] |
|
β, град. |
97,850(2) |
Переменных уточнения |
199 |
|
γ, град. |
90 |
GOOF |
1,019 |
|
V , Å3 |
2799,52(11) |
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0583, wR 2 = 0,1546 |
|
Z |
4 |
R -факторы по всем отражениям |
R 1 = 0,1026, wR 2 = 0,1829 |
|
Остаточная электронная плотность (min/max), e /Å3 |
0,23/–0,21 |
Обсуждение результатов
В настоящей работе синтез соединения 1 был выполнен взаимодействием его прекурсора 3 с 1-морфолинциклопентеном при нагревании до 200 °С в инертной атмосфере в отсутствие растворителя в течение 3 ч (схема 2). Последующая чистка колоночной хроматографией (элюент – хло-роформ-этилацетат (9:1), R f 0,5) позволила получить целевой продукт с выходом 52 %. Его кристаллы, пригодные для РСА, были получены нами в результате медленного упаривания раствора в хлороформе.
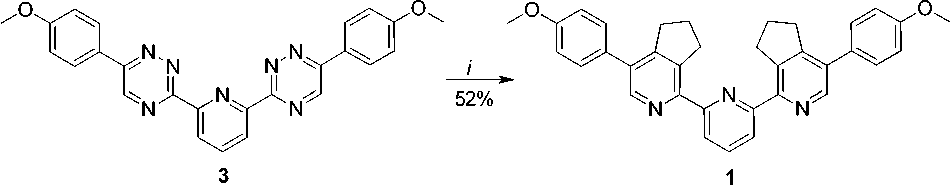
Схема 2. Разработанный синтез соединения 1. Реагенты и условия: i ) 1-морфолинциклопентен, 200 °С, 3 ч
В нашем случае соединение 1 аналогично известным данным [10] кристаллизуется в моноклинной сингонии с пространственной группой C2/c. Три пиридиновых звена в терпиридиновом мотиве принимают трансоидную конфигурацию по отношению к межкольцевым связям C–C (рис. 1), что минимизирует электростатические взаимодействия между неподеленными парами атомов азота.
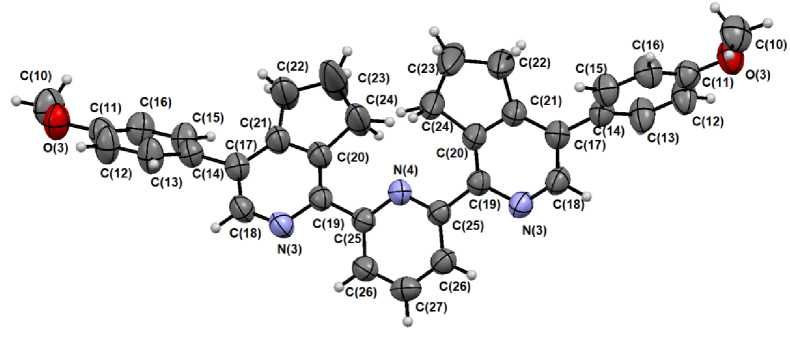
Рис. 1. Данные РСА соединения 1 и принятая в структурном эксперименте нумерация атомов
Полученные длины связей и валентные углы аналогичны таковым для известных производных терпиридина [10, 18–20]. Например, определенные валентные углы между тремя атомами азота составляют 118,6(2) для C18-N3-C19 и 118,6(0) для C25-N4-C25. Ароматические кольца скручены относительно друг друга, при этом угол между центральным пиридиновым звеном и пиридиновым фрагментом 6,7-дигидро-5 H -циклопента[ с ]пиридина составляет 23,64° (лит. 23,61(6)° [10]). По-видимому, такое пространственное расположение обеспечивает наиболее выгодную ориентацию циклопентильных колец с меньшим стерическим напряжением и меньшим межкольцевым отталкиванием H⋯H.
Наиболее интересной особенностью кристаллической структуры является характер межмолекулярных взаимодействий, не описанный ранее для данной структуры. Расположение двух мономеров, сложенных по принципу «голова к голове», описывается минимальным расстоянием между атомом водорода циклопентильного цикла в 5-том положении бициклической системы и атомом углерода метильной группы (С(22)-Н(22А)…С(10) 2,97 Å). Для каждого из мономеров наблюдаются минимальные расстояния С(26)-Н(26)…С(10) 2,87 Å с соседними молекулами. Кроме того, межмолекулярные расстояния С(13)-Н(13)…С(18) 2,87 Å между атомом водорода электроноизбыточного метоксифенильного заместителя и атомом углерода электронодефицитного центрального пиридинового цикла позволяют предположить присутствие слабых π-π стэкин-говых взаимодействий. При этом угол между плоскостями ароматических колец составляет 84,54 º, а расстояние между центроидами 4,92 Å. Это позволяет предположить участие слабых контактов С-Н…С и π-π стэкинга в стабилизации кристаллической структуры (рис. 2).
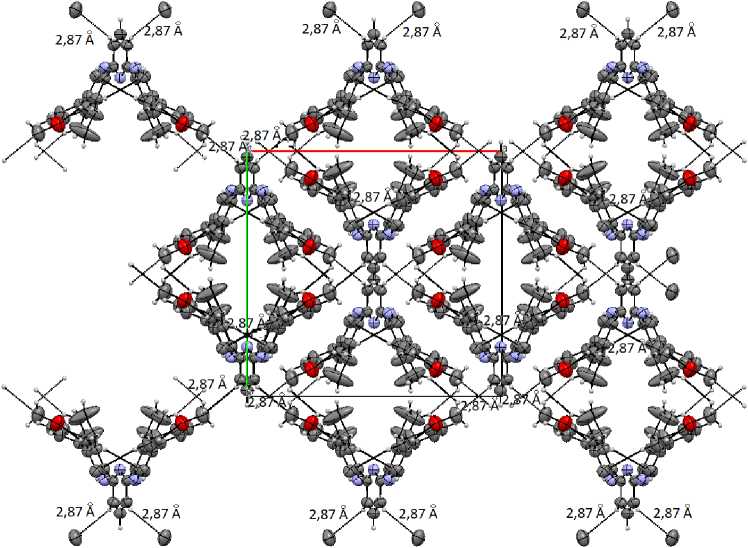
Рис. 2. Упаковка молекул в кристалле соединения 1 (показана проекция вдоль кристаллографической оси с )
Авторами работы [10] отмечена разупорядоченность атома углерода в 6-том положении бицикла циклопента[с]пиридина, однако в нашем случае этого не наблюдается. Но следует отметить, что эллипсоиды тепловых колебаний аналогичного атома углерода (С(23)), а также соседних атомов С(22) и С(24) каждого циклопентильного кольца сильно растянуты в направлении, перпендикулярном плоскости кольца (рис. 3). Подобные явления встречаются и для других цик-лопента[с]пиридиновых бициклических структур, депонированных в Кембриджской Структурной Базе Данных (Cambridge Structural Database (например, в работе [21]).
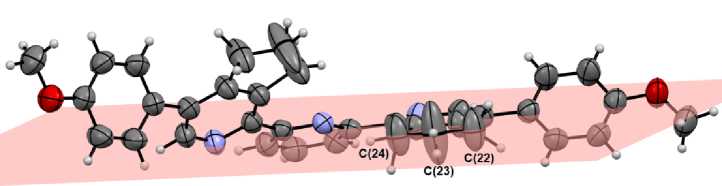
Рис. 3. Представление эллипсоидов вероятностей тепловых колебаний атомов углерода С(23), С(22) и С(24) циклопентильного кольца относительно его плоскости (закрашена цветом)
Заключение
Таким образом, нами исследована возможность применения PASE-подхода к синтезу 1,1′-(2,6-пиридиндиил) бис [6,7-дигидро-4-(4-метоксифенил)-5 H -циклопента[ c ]пиридина (проведение синтеза в условиях отсутствия растворителя), показана успешность применения данной методологии для получения целевого продукта с хорошим выходом (52 %), а также проведено детальное изучение структуры его монокристалла в сравнении с имеющимися в литературе сведениями. Описаны особенности супрамолекулярной структуры данного соединения, не описанные ранее для данной структуры, в частности, выявлено расположение двух мономеров, сложенных по принципу «голова к голове», обеспечивающее минимальное расстояние между соседними структурами.

![Структура 1,1′-(2,6-пиридиндиил)бис[6,7-дигидро-4-(4-метоксифенил)-5H- циклопента[с]пиридина Структура 1,1′-(2,6-пиридиндиил)бис[6,7-дигидро-4-(4-метоксифенил)-5H- циклопента[с]пиридина](/file/cover/147253376/struktura-1126-piridindiil-bis-67-digidro-44-metoksifenil5h.png)
