Структура атеросклеротической бляшки как определяющий фактор цереброваскулярной реактивности при стенозирующем атеросклерозе сонных артерий
Автор: Максимова Александра Сергеевна, Бобрикова Евгения Эдуардовна, Буховец Ирина Львовна, Плотников Михаил Павлович, Усов Владимир Юрьевич
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 2 т.31, 2016 года.
Бесплатный доступ
Цель исследования: сопоставление структуры каротидной бляшки, визуализированной с помощью магнитно-резонансной томографии (МРТ), и реактивности сосудов головного мозга, оцененной с помощью ультразвукового исследования, у пациентов с распространенным атеросклерозом и стенозирующим поражением сонных артерий. Всем пациентам выполнялась МРТ головного мозга и области сонных артерий. Цереброваскулярный резерв оценивали с помощью транскраниального ультразвукового исследования средних мозговых артерий с определением показателей кровотока в условиях функциональных тестов: проб с задержкой дыхания и гипервентиляцией. При проведении пробы с задержкой дыхания у большинства (56%) пациентов с гипоинтенсивной в Т1-ВИ (взвешенных изображениях) и гиперинтенсивной в Т2-ВИ МРТ-картиной бляшки наблюдалась однонаправленная с обеих сторон положительная реакция при функциональной гиперкапнической нагрузке с задержкой дыхания. Напротив, однонаправленная отрицательная либо отрицательная реакция на стороне стеноза выявлялись у пациентов, имеющих гиперинтенсивную бляшку в Т1-ВИ и гипоинтенсивную в Т2-ВИ, по данным МРТ. Проведение МРТ стенок артерий с оценкой структуры атеросклеротической бляшки может быть рекомендовано в качестве скринингового метода у всех пациентов групп риска атеросклероза.
Атеросклероз, сонные артерии, магнитно-резонансная томография, цереброваскулярный риск
Короткий адрес: https://sciup.org/14920106
IDR: 14920106 | УДК: 616.133.333-073.43-073.8
The structure of atherosclerotic plaque as a defining factor of cerebrovascular reactivity in patients with carotid atherosclerosis
The aim of our study was to compare the magnetic resonance imaging (MRI)-based structure of atherosclerotic plaques and cerebral vascular reactivity quantified by echocardiography. All patients underwent MRI of the carotid arteries. To assess the cerebrovascular reactivity, transcranial ultrasound of middle cerebral artery was carried out with quantification of blood flow parameters at rest and during stress tests: first with breath holding and then with hyperventilation, with calculation of reactivity index. Data showed a statistically significant association between MRI plaque structure and type of the reaction during breath holding in hypercapnic test, whereas no significant differences were found in hyperventilation test. In breath-holding test, 56% of patients with hypointense plaques on T1- and hyperintense plaques on T2-weighted MRI scans had unidirectional positive response to functional hypercapnic stress. On the contrary, pathologic unidirectional negative or negative response on a side of the stenosis was observed in patients with MRI evidence of hyperintense plaques on T1- and hypointense plaques on T2-weighted scans. Atherosclerotic lesions of the internal carotid artery with intra-plaque hemorrhage were accompanied with critical deterioration of cerebrovascular reactivity. Any hemorrhage to carotid plaque could probably be assumed as critical risk factor requiring removal of the plaque by carotid endarterectomy. High-resolution MRI of carotid arteries may be suggested as screening test for all patients in atherosclerosis risk groups.
Текст научной статьи Структура атеросклеротической бляшки как определяющий фактор цереброваскулярной реактивности при стенозирующем атеросклерозе сонных артерий
В настоящее время в большинстве стран атеросклероз и его осложнения остаются одной из основных причин смертности взрослого населения, в первую очередь, за счет инфаркта миокарда (ИМ) и ишемического инсульта [1, 2]. При этом нетрудоспособность не только ухудшает функциональное состояние и социальную роль выживших после инсульта, но также приводит и к весьма существенным бюджетным затратам. В последние годы представлены убедительные свидетельства давно сформулированной концепции [1, 3], что едва ли не основную роль в прогрессировании атеросклеротических бляшек и нарушении их стабильности играют vasa vasorum бляшки, развивающиеся при ее патологической васкуляриза- ции. По мере развития атеросклеротической бляшки vasa vasorum обильно врастают в нее и создают обширную поверхность для миграции лейкоцитов, проникновения атрогенных липидов и формирования микрогеморрагий внутрь бляшки [4, 5]. Для оценки морфологии собственно атеросклеротических бляшек, изменений стенок артерий, наряду с ультразвуковыми технологиями, в последнее время широко применяется МРТ и магнитно-резонансная ангиография (МРА) [6, 7]. В свою очередь для оценки состояния цереброваскулярного сосудистого резерва при атеросклеротическом поражении сосудов шеи и головного мозга неизменно широко используются методы ультразвуковой диагностики. При этом проведение нагрузочного тестирования, направленного на активацию механизмов ауторегуляции, позволяет зарегистрировать локальные и/или генерализованные нарушения цереброваскулярной реактивности. Однако парадоксальным образом взаимоотношения цереброваскулярной реактивности у пациентов с гемодинамически значимым стенозом брахиоцефальных артерий с конкретными характеристиками выявленных атеросклеротических бляшек остаются малоизученными.
Цель исследования: оценка взаимосвязи структуры бляшки пораженной артерии, визуализированной с помощью МРТ, и реактивности сосудов головного мозга, определяемой с помощью ультразвуковых методик, у пациентов с каротидным атеросклерозом.
Задачи:
-
1. Изучить МРТ-структуру атеросклеротической бляшки, сгруппировать возможные типы бляшек по данным МРТ.
-
2. Оценить реактивность сосудов головного мозга с помощью транскраниальной допплерографии, сгруппировать наблюдаемые типы реакций мозгового кровотока.
-
3. Сопоставить структуру бляшки по данным МРТ и тип реактивности церебрального кровотока по данным ультразвуковых методик.
Материал и методы
В исследование включен 21 пациент в возрасте от 50 до 78 лет с гемодинамически значимым стенозом брахиоцефальных артерий более 70%. Крупноочаговые инсульты головного мозга не были отмечены ни у кого из включенных в исследование и служили критерием исключения. Всем пациентам впоследствии была проведена каротидная эндартерэктомия (КЭЭ) с проведением затем морфологического исследования удаленной атеросклеротической бляшки.
Исследование проводилось на томографе Toshiba Titan Vantage с индукцией магнитного поля 1,5 Т. Всем пациентам выполнялась МРТ области сонных артерий перпендикулярно ходу общей сонной артерии с получением аксиальных томосрезов сонных артерий толщиной 1– 2,5 мм. Были получены Т1- и Т2-взвешенные МРТ-изоб-ражения (Т1-ВИ и Т2-ВИ), а также изображения в 3D вре-мя-пролетном режиме области бифуркации сонных артерий. Параметры исследований составляли соответственно: Т1-ВИ: TR=900–1000 мс, TE=10 мс, запись проводилась в матрицу 256х256 вокселей, при этом размер вокселя составлял соответственно 0,2х0,2х2 мм. Для Т2-ВИ: TR=3000–4000 мс, TE=100–105 мс. По данным визуальной оценки T1-ВИ и T2-ВИ области каротидного стеноза были выделены четыре возможных типа наблюдаемых бляшек:
-
1. Смешанная бляшка с выраженным фиброзированием и липидным ядром – изображение бляшки усилено в T1-ВИ и в T2-ВИ.
-
2. Бляшка с преобладанием липидного компонента – изображение не усилено в T1-ВИ и усилено в T2-ВИ.
-
3. Бляшка с микрогеморрагиями – изображение усиле-
- но в T1-ВИ и не усилено в T2-ВИ.
-
4. Кальцинированная бляшка – изображение не усилено ни в T1-ВИ, ни в T2-ВИ.
Впоследствии тип бляшки, определенный при МРТ-исследовании сонных артерий, был подтвержден данными морфологического послеоперационного исследования во всех случаях.
Исследование проводилось на ультразвуковом диагностическом аппарате General Electric – Vivid 7 Dimension и Vivid 9 в В-режиме, режимах цветного и импульсноволнового допплеровского картирования. Транскраниальное исследование средних мозговых артерий (СМА) проводилось по общепринятой методике с помощью секторного датчика M5S (1,5–4,5 МГц). Ультразвуковое исследование синхронизировалось с работой сердца под контролем артериального давления и частоты сердечных сокращений. Для оценки цереброваскулярного резерва фоновые параметры кровотока по СМА определяли в исходном состоянии и в условиях функциональных тестов: в условиях модифицированной гиперкапнической пробы с произвольной задержкой дыхания на максимально возможное для пациента время и модифицированной гипокапнической – гипероксической пробы с форсированной гипервентиляцией в течение 60 с [8]. Рассчитывалась усредненная по времени максимальная скорость кровотока (TAMX) в СМА с обеих сторон. На основании полученных данных определяли индекс реактивности, отражающий изменения параметра TAMX. При проведении теста с задержкой дыхания вазодилататорной направленности индекс реактивности рассчитывался как отношение показателя TAMX после пробы к аналогичному значению до пробы (ИР=TAMXпосле/TAMXдо). При оценке индекса реактивности после вазоконстрикторной нагрузки (проба с форсированным дыханием) рассчитывалось соотношение показателя TAMX до пробы и после пробы (ИР=TAMXдо/TAMXпосле) [9]. В контрольную группу исследования вошли 7 здоровых добровольцев, не имеющих данной патологии.
Для оценки типа реакции кровотока на проводимую стимуляцию и последующего анализа активности ауторегуляторных механизмов использовалась следующая общепринятая классификация [9]:
– положительная реакция (соответствует норме – сохранности цереброваскулярного резерва), индекс реактивности 1,1–1,4;
– отрицательная реакция (соответствует исчерпанности цереброваскулярного резерва при функциональной пробе), индекс реактивности 0,9–1,1;
– парадоксальная реакция (соответствует фактической декомпенсации цереброваскулярного резерва в покое), индекс реактивности менее 0,9.
Статистическая обработка результатов была проведена в программе SPSS 11.05.0, с применением t-критерия Стьюдента для анализа количественных данных, подчиняющихся нормальному закону распределения, а также точного критерия Фишера для анализа малых выборок качественных данных.
Таблица 1
Соотношение положительных, отрицательных и парадоксальных реакций в СМА при проведении нагрузочных тестов с задержкой дыхания и гипервентиляцией
|
Показатели |
Положительная реакция |
Отрицательная реакция |
Парадоксальная реакция |
|
|
Проба с гиперкапнией (n=21) |
Сторона стеноза |
7 |
6 |
8 |
|
Контралатеральная сторона |
11 |
6 |
4 |
|
|
Проба с гипокапнией (n=15) |
Сторона стеноза |
11 |
3 |
1 |
|
Контралатеральная сторона |
9 |
1 |
5 |
|
Таблица 2
Соотношение типов реакций в одноименных СМА при проведении нагрузочных тестов с задержкой дыхания и гипервентиляцией
|
Показатели |
Однонаправленная положительная реакция |
Однонаправленная отрицательная реакция |
Разнонаправленная реакция |
|
Проба с гиперкапнией (n=21) |
5 |
8 |
8 |
|
Проба с гипокапнией (n=15) |
7 |
2 |
2 |
Таблица 3
Показатели индекса реактивности СМА (среднее±стандартное отклонение) при проведении функциональных проб в группе исследования и контрольной группе
|
Показатели |
Группа исследования |
Контрольная группа |
||
|
Сторона стеноза |
Контралатеральная сторона |
Правая сторона |
Левая сторона |
|
|
Проба с гиперкапнией (n=21) |
0,98±0,20 p<0,001 |
1,16±0,35 p>0,05 |
1,28±0,14 |
1,14±0,20 |
|
Проба с гипокапнией (n=15) |
1,28±0,29 p>0,05 |
1,18±0,36 p>0,05 |
1,10±0,22 |
1,33±0,15 |
Примечание: * – уровень статистической значимости различий p – по сравнению с контрольной группой.
Результаты
По направленности реакции мозгового кровотока при функциональном тестировании с оценкой методом транскраниального ультразвукового исследования (УЗИ) все пациенты были разделены на три группы:
-
1. С однонаправленной положительной реакцией (при положительной реакции в парных СМА).
-
2. С однонаправленной отрицательной реакцией (при двусторонних отрицательных либо парадоксальных реакциях или их сочетании в СМА).
-
3. С разнонаправленной реакцией (при односторонней положительной реакции в сочетании с отрицательным либо парадоксальным ответом контралатераль-но) [9].
Данные о распределении пациентов на группы представлены в таблице 1.
При оценке изменений параметров кровотока по СМА в ответ на определенное воздействие оценивали реакцию не только в бассейне пораженной артерии, но и на про- тивоположной стороне (табл. 2). При проведении пробы с задержкой дыхания у большинства пациентов наблюдалась однонаправленная отрицательная либо парадоксальная реакция, при проведении гипероксической пробы – однонаправленная положительная реакция.
У пациентов с гемодинамически значимым стенозом наблюдались статистически значимые различия индекса реактивности на стороне стеноза при проведении пробы с задержкой дыхания в сравнении с контрольной группой, тогда как при проведении гипервентиляционного теста значимых различий обнаружено не было (табл. 3).
При анализе МРТ области сонных артерий у наших пациентов мы в данной работе сознательно ограничились результатами исследований без дополнительного парамагнитного контрастирования. Это вызвано тем, что в рутинной практике время-пролетная МРА сосудов головного мозга выполняется намного чаще и в выполнении легче, чем методики контрастированной МРА. В связи с этим выглядит весьма важным и заманчивым получение возможности выявлять наиболее прогностически опасные бляшки каротидных артерий уже по данным исходного неконтрастированного МРТ-исследова-ния в соответствии с представленными выше типами бляшек [10].
По выделенным нами группам гиперинтенсивное изображение бляшки в T1-ВИ и T2-ВИ (смешанная бляшка с выраженным фиброзированием и липидным ядром) было обнаружено у одного пациента; гипоинтенсивное в Т1-ВИ и гиперинтенсивное в T2-ВИ (бляшка с преобладанием липидного компонента) – у 9 пациентов; гиперинтенсивное изображение в T1-ВИ, гипоинтенсивное в Т2-ВИ (бляшка с микрогеморрагиями) – у 5 пациентов; полностью кальцинированных бляшек, дающих одновременно гипоинтенсивный сигнал и в Т1-ВИ, и в Т2-ВИ, обнаружено не было.
Поскольку целью данного исследования было сопоставление структуры атеросклеротической бляшки и реактивности СМА, мы оценили взаимосвязь непосредственно МРТ-картины атеросклеротической бляшки (типы бляшек) и сочетанную реакцию реактивности (однонаправленная положительная, однонаправленная отрицательная и разнонаправленная реакция) при проведении функциональных проб на обеих сторонах исследования. Полученные результаты при проведении пробы с задер-
Таблица 4
Взаимосвязь структуры бляшки, определенной по данным МРТ, и направленности реакции мозгового кровотока при функциональной пробе с задержкой дыхания – гиперкапнией, по данным ультразвукового исследования (n=15)
|
Показатели |
Структура бляшки (тип по данным МРТ) |
|
Т1-ВИ усилен, Т1-ВИ не усилен, Т1-ВИ усилен, Т1-ВИ не усилен, Т2-ВИ усилен Т2-ВИ усилен Т2-ВИ снижен Т2-ВИ не усилен |
|
|
Однонаправленная положительная реакция Однонаправленная отрицательная реакция Разнонаправленная реакция (отрицательная на стороне стеноза) |
–5–– 132– –13– |
Таблица 5
Взаимосвязь структуры бляшки, по данным МРТ-исследования, и направленности реакции мозгового кровотока при функциональной пробе с гипервентиляцией, по данным ультразвукового исследования (n=11)
|
Показатели |
Структура бляшки (тип по данным МРТ) |
|
Т1-ВИ усилен, Т1-ВИ не усилен, Т1-ВИ усилен, Т1-ВИ не усилен, Т2-ВИ усилен Т2-ВИ усилен Т2-ВИ не усилен Т2-ВИ не усилен |
|
|
Однонаправленная положительная реакция Однонаправленная отрицательная реакция Разнонаправленная реакция (отрицательная на стороне стеноза) |
13–– –11– –23– |
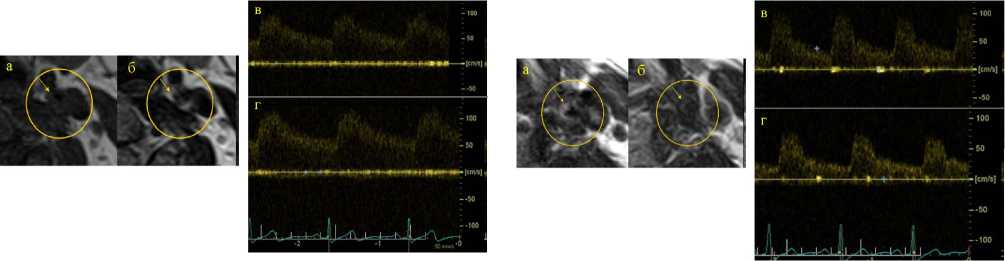
Рис. 2. МРТ-исследование в аксиальных срезах и ультразвуковое исследование – допплеровский спектр кровотока СМА у пациента с разнонаправленной реакцией на нагрузку при проведении гиперкапнической пробы. а – Т1-взв. SE МРТ; б – Т2-взв. SE МРТ; в – допплеровский спектр СМА на стороне гемодинамически значимого стеноза у пациента в покое; г – допплеровский спектр СМА на стороне гемодинамически значимого стеноза (75%) у пациента при проведении пробы с задержкой дыхания. На МРТ видна гиперинтенсивная в Т1-ВИ и гипоин-тенсивная в Т2-ВИ атеросклеротическая бляшка (стрелки) – вследствие микрогеморрагии в бляшку. Индекс реактивности СМА на этой стороне при проведении гиперкапнической пробы = 0,78 – парадоксальная реакция
Рис. 1. МРТ-исследование в аксиальных срезах и ультразвуковое исследование – допплеровский спектр кровотока СМА у пациента с однонаправленной положительной реакцией на нагрузку. а – Т1-взв. SE МРТ; б – Т2-взв. SE МРТ; в – допплеровский спектр СМА на стороне гемодинамически значимого стеноза у пациента в покое; г – допплеровский спектр СМА на стороне гемодинамически значимого стеноза у пациента при проведении пробы с задержкой дыхания. На МРТ визуализируется гипоинтенсивная в Т1-ВИ и гиперинтенсивная в Т2-ВИ атеросклеротическая бляшка (стрелки) – с преобладанием липидного ядра. Индекс реактивности СМА при проведении гиперкапнической пробы = 1,12 – положительная реакция жкой дыхания представлены в таблице 4, при проведении пробы с гипервентиляцией – в таблице 5.
Проведенный статистический анализ показал, что при использовании нагрузочного теста с задержкой дыхания найдена взаимосвязь между определенной при МРТ структурой бляшки и направленностью реакции кровотока (p=0,081), при этом можно предположить, что при увеличении выборки вероятность ошибки станет меньше, так как полученное значение p достаточно близко к пороговому. При проведении пробы с гипервентиляцией значимых различий обнаружено не было. При проведении пробы с задержкой дыхания у большинства (56%) пациентов с гипоинтенсивной в Т1-ВИ и гиперинтенсивной в Т2-ВИ МРТ-картиной бляшки наблюдалась однонаправленная положительная реакция на нагрузку (типичный пример представлен на рисунке 1). Однонаправленная отрицательная либо отрицательная реакция на стороне стеноза (разнонаправленная в целом) выявлялись у пациентов, имеющих гиперинтенсивную бляшку в Т1-ВИ и гипоинтенсивную в Т2-ВИ по данным МРТ (типичный пример на рисунке 2).
Обсуждение
В доступной литературе нам не удалось найти прямых сопоставлений показателей типологии атеросклеротических бляшек сонных артерий, по данным МРТ (или иного лучевого исследования) и показателей реактивности кровотока в артериях головного мозга при дуплексном сканировании, хотя взаимосвязь между наличием критического стеноза и патологическими очаговыми изменениями головного мозга по данным МРТ хорошо подтверждена [6, 7]. Поэтому наше исследование имело своей целью, в первую очередь, выявить типы атеросклеротических бляшек, видимых при МРТ-исследовании уже и до проведения контрастирования парамагнетиком, которые сопровождаются патологическими типами реакций кровотока в СМА в условиях функциональных тестов с гипер- и гипокапнией, то есть представляют непосредственную опасность развития ишемического инсульта.
В контрольной группе в условиях нагрузочных тестов были получены положительные реакции, что свидетельствует о нормальной активности ауторегуляторных механизмов [1, 7]. Оказалось, что для практических целей у наших пациентов проба с гипероксией – гипокапнией (гипервентиляционная) не дает информации о взаимоотношениях реактивности сосудистого русла мозга и структуры атеросклеротической каротидной бляшки. Напротив, при использовании гиперкапнической пробы с задержкой дыхания (методически наиболее легко применимой у всех групп больных) такая связь выявляется. При этом патологические реакции мозгового кровотока у пациентов с бляшками с выраженным липидным ядром выявляются в 44% случаев. А при развитии внутрибляшеч-ных геморрагий, но без нарушений эндотелиальной целостности бляшки – ни в одном из наших случаев бляшка не сопровождалась разрывом интимы и тромбозом – такие нарушения цереброваскулярной реактивности в условиях гиперкапнической нагрузки отмечались у всех пациентов. Наличие внутрибляшечных геморрагий с повреждениями интимы уже однозначно расценивается как показание к хирургическому вмешательству [2, 8]. Нарушение цереброваскулярного сосудистого резерва, определяемое при функциональной пробе с гиперкапнией, представляет собой доказательство гемодинамической значимости бляшки и вследствие этого, вероятно, также необходимости проведения КЭЭ [3, 8]. Ранее было также показано, что интенсивно контрастируемые парамагнетиком каротидные бляшки ассоциированы с высоким риском развития ишемических цереброваскулярных нарушений [7]. Полученные нами данные показывают, что при атеросклеротическом стенозе ВСА внутрибляшечные геморрагии даже и без повреждения эндотелия сосуда сопровождаются критическим нарушением цереброваскулярной реактивности, оцениваемой по кровотоку в СМА. Следовательно, обоснованно считать визуально определяемые при МРТ внутрибляшечные геморрагии критическим фактором риска, требующим удаления такой бляшки открытой КЭЭ или интервенционным методом (внутрисосудистым баллонированием и стентированием). Практически крайне важно, что выявление таких осложненных бляшек возможно в ходе обычного МРТ-исследования головного мозга с охватом в поле зрения области каротидной бифуркации, с получением МР-то-мосрезов этой области в Т1- и Т2-взвешенных спин-эхо режимах тонкими срезами по 1–2,5 мм, что доступно сегодня абсолютно на всех современных рутинных МР-то-мографах.
Таким образом, проведение МРТ-исследования области общей и ВСА может быть рекомендовано в качестве скринингового у всех пациентов, входящих в группу риска по данной патологии. Однако для выявления реальной значимости такого скринингового применения представленных здесь методик оценки характера атеросклеротической бляшки будет необходимо статистически более обширное, вероятно, меж- или многоцентровое исследование.
Выводы
-
1. Гемодинамически значимые атеросклеротические бляшки с микрогеморрагиями и без нарушения поверхности эндотелия вызывают патологические изменения реактивности артерий головного мозга, которые наблюдаются у 100% таких пациентов. При наличии бляшек с преобладанием липидного ядра патологические варианты реактивности кровотока СМА отмечаются лишь в 44% случаев.
-
2. Функциональная проба с гиперкапнией наиболее информативна для выявления функциональных нарушений кровотока головного мозга при атеросклеротических поражениях сонных артерий.
Список литературы Структура атеросклеротической бляшки как определяющий фактор цереброваскулярной реактивности при стенозирующем атеросклерозе сонных артерий
- Никитин Ю.П., Николаев К.Ю., Рагино Ю.И. и др. Эндотелиальная дисфункция, гипертония, атеросклероз. -Новосибирск: Изд-во СО РАН, 2014. -132 с.
- Parmar J.P., Rogers W.J, Mugler J.P. et al. Magnetic resonance imaging of carotid atherosclerotic plaque in clinically suspected acute transient ischemic attack and acute ischemic stroke//Circulation. -2010. -Vol. 122(20). -P. 2031-2038.
- Грацианов Д.А. Влияние тренировки к холестерину на развитие экспериментального атеросклероза. -Томск: Изд-во ТГУ, 1982. -97 с.
- Carlier S., Kakadiaris I., Dib N. et al. Vasa vasorum imaging: A new window to the clinical detection of vulnerable atherosclerotic plaques//Curr. Atheroscler. Rep. -2005. -Vol. 7(2). -P. 164-169.
- Рагино Ю.И. Факторы и механизмы коронарного Атеросклероза и его осложнений//Атеросклероз. -2012. -Т. 8, № 1. -С. 61-64.
- Абрамова Н.Н. Магнитно-резонансная томография и магнитно-резонансная ангиография в визуализации сосудистых структур//Вестн. рентгенол. и радиол. -1997. -№ 2. -C. 50-54.
- Бобрикова Е.Э., Щербань Н.В., Ханеев В.Б. и др. Оценка состояния атеросклеротических бляшек брахиоцефальных артерий средствами высокоразрешающей контрастированной МРТ: взаимосвязь с ишемическим повреждением головного мозга//Мед. визуал. -2013. -№ 1. -С. 26-31.
- Национальные рекомендации по ведению пациентов с заболеваниями брахиоцефальных артерий. Российский согласительный документ. -М., 2013. -72 с.
- Лелюк В.Г., Лелюк С.Э. Ультразвуковая ангиология. -М.: Реальное время, 2003. -324 с.
- Cai J.M., Ferguson M.S., Polissar N. et al. Classification of human carotid atherosclerotic lesion using in Vivo multi-contrast MR imaging//Circulation. -2002. -Vol. 106. -P. 1368-1373.
- Страздень Е.Ю., Шария М.А., Тарарак Э.М. и др. Применение магнитно-резонансной томографии в определении стабильности атеросклеротической бляшки//Рос. электрон. журн. лучевой диагностики. -2013. -Т. 3, № 1(9). -С. 57-62.


