Сурьмаорганические производные дикарбоновых кислот. Синтез и строение (обзор)
Автор: Губанова Юлия Олеговна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 3 т.9, 2017 года.
Бесплатный доступ
Рассматриваются методы синтеза сурьмаорганических производных дикарбоновых кислот, в которых атомы сурьмы имеют в различной степени искаженную тригонально-бипирамидальную координацию.
Пентафенилсурьма, дикарбоновая кислота, рентгеноструктурный анализ, карбоксилат бис(тетрафенилсурьмы), кислый карбоксилат тетрафенилсурьмы
Короткий адрес: https://sciup.org/147160401
IDR: 147160401 | УДК: 546.865+547.53.024+548.312.5 | DOI: 10.14529/chem170310
Organoantimony derivatives of dicarboxylic acids. Synthesis and structure (overview)
The overview discusses the methods of synthesis of tetraarylantimony carboxylates, which have received from pentaphenylantimony and dicarboxylic acid in different conditions (moleratio, solvent, temperature, nature of the acid). The antimony atoms have a distorted in different degrees trigonal-bipyramidal coordination.
Текст научной статьи Сурьмаорганические производные дикарбоновых кислот. Синтез и строение (обзор)
Методы синтеза сурьмаорганических производных дикарбоновых кислот и изучение особенностей их строения практически не изучены, поэтому актуальность настоящей работы очевидна.
Первым структурно охарактеризованным дикарбоксилатом бис (тетрафенилсурьмы) является оксалат бис (тетрафенилсурьмы), полученный в 1992 году из бромида тетрафенилсурьмы и оксалата серебра в толуоле с выходом 79 % [1].
2Ph 4 SbBr + AgO(O)C–C(O)OAg → Ph 4 SbO(O)C–C(O)OSbPh 4 + 2AgBr
Более эффективный метод синтеза подобных соединений сурьмы, позволяющий выделять целевой продукт с более высоким выходом, основан на реакции пентафенилсурьмы с дикарбоновыми кислотами в растворе ароматического углеводорода. Как правило, взаимодействие исходных реагентов протекает при комнатной температуре, для завершения реакции требуется непродолжительное нагревание реакционной смеси до 80-100 ° С. В зависимости от мольного соотношения исходных реагентов могут быть получены как кислые карбоксилаты тетрафенилсурьмы, так и дикарбоксилаты бис (тетрафенилсурьмы).
Так, взаимодействие пентафенилсурьмы с дикарбоновыми кислотами в толуоле при мольном соотношении 2:1 приводит к образованию карбоксилатов бис (тетрафенилсурьмы) [2–8]. Для завершения реакции необходимо нагревание на водяной бане в течение часа. Температуры плавления и выходы карбоксилатов бис (тетрафенилсурьмы) приведены в табл. 1.
2 Ph 5 Sb + HOC(O)R(O)OH→ Ph 4 SbOС(О)R(O)COSbPh 4 + 2 PhH
R =–СH(OH)–CH 2 –,–СH(OH)–CH(OH)–; 1,2-C 6 H 4 –C≡C–; –СH 2 –CH 2 –; 1,2-С 6 F 4 ; 1,2-C 6 Cl 4 ; С 2 B 10 H 10
Таблица 1
Выходы и температуры плавления соединений (Ar 4 Sb) 2 R, полученные из пентафенилсурьмы и дикарбоновой кислоты при мольном соотношении 2:1
|
№ |
R |
Т. пл., °С |
Выход, % |
Литература |
|
1 |
–СH(OH)–CH 2 – |
165–167 |
92 |
[2] |
|
2 |
–СH(OH)–CH(OH)– |
167–168 |
94 |
[2] |
|
3 |
1,2-C 6 H 4 |
238 |
93 |
[3] |
|
4 |
–СH=CH– |
232 |
99 |
[4] |
|
5 |
–C≡C– |
178 |
90 |
[5] |
|
6 |
–СH 2 –CH 2 – |
193–194 |
98 |
[2] |
|
7 |
1,2-С 6 F 4 |
214 |
85 |
[6] |
|
8 |
1,2-C 6 Cl 4 |
227–228 |
91 |
[7] |
|
9 |
С 2 B 10 H 10 |
157 |
94 |
[8] |
При мольном соотношении 1:1 удалось получить кислые карбоксилаты тетраарилсурьмы [4, 9–11]. Температуры и выходы синтезированных соединений приведены в табл. 2.
Ar 5 Sb + HOC(O)–R–(O)COH → Ar 4 SbOC(O)–R–C(O)ОH + ArH
Ar = Ph, R= –СH=CH–,–СH 2 –CH 2 –, 1,2-C 6 H 4
Ar = p -Tol, R= 1,2-C 6 H 4
Таблица 2
Выходы и температуры плавления соединений Ar 4 SbRH, полученные из пентафенилсурьмы и дикарбоновой кислоты при мольном соотношении 1:1
|
№ |
Ar |
R |
T. пл, °С |
Выход, % |
Литература |
|
10 |
Ph |
–СH=CH– |
165 |
87 |
[4] |
|
11 |
Ph |
–СH 2 –CH 2 –, |
147 |
97 |
[9] |
|
12 |
Ph |
1,2-C 6 H 4 |
190-191 |
98 |
[10] |
|
13 |
p -Tol |
1,2-C 6 H 4 |
175 |
98 |
[11] |
В некоторых случаях при мольном соотношении 1:1 вместо ожидаемого продукта – кислого карбоксилата тетрафенилсурьмы были синтезированы карбоксилаты тетрафенилсурьмы: происходило декарбоксилирование одной из карбоксильных групп. Так были получены пропиолат тет-рафенилсурьмы (т. пл. 174 °С, выход 76 %) [5] и карборанилкарбоксилат тетрафенилсурьмы (т. пл. 148 °С, выход 88 %) [8]:
Ph 5 Sb + HOC(O)R(O)COH → Ph 4 SbOС(О)RH + PhH + CO 2
R = C≡C, C 2 B 10 H 10
Cледует отметить, что декарбоксилирование сурьмаорганического производного ацетилендикарбоновой кислоты протекало при нагревании, а производного карборанилдикарбоновой кислоты – при комнатной температуре. Минорным продуктом реакции пентафенилсурьмы с ацетилендикарбоновой кислотой являлся также карбонат бис (тетрафенилсурьмы) с выходом 10 %, идентифицированный по температуре плавления и ИК-спектру [12].
Таблица 3
Основные геометрические параметры молекул 1–9
|
№ |
R |
d Sb-O, Å |
d Sb-C экв , Å |
d Sb-C акс , Å |
ωOSbC aкс , град |
∑ω C экв SbС экв , град |
|
1 |
–СH(OH)– CH 2 – |
2,243(4) 2,267(7) |
2,111(6)–2,116(6) |
2,164(5) |
174,8(2) |
356,7 |
|
2* |
–СH(OH)– CH(OH)– |
2,252(7) 2,284(7) |
2,074(12)–2,121(9) 2,072(13)–2,102(11) |
2,164(11) 2,169(11) |
176,4(4) 177,4(3) |
356,0 358,0 |
|
3 |
1,2-C 6 H 4 |
2,242(3) |
2,115(5)–2,137(4) |
2,176(5) |
177,83(3) |
357,29 |
|
4 |
–СH=CH– |
2,207(3) 2,217(3) |
2,111(4)–2,127(4) 2,109(4)–2,114(5) |
2,172(4) 2,168(5) |
178,1(2) 177,2(2) |
357,9 357,98 |
|
5 |
–C≡C– |
2,287(4) 2,389(4) |
2,110(7)–2,133(6) 2,108(6)–2,119(6) |
2,179(6) 2,165(6) |
175,5(2) 174,7(2) |
357,0 356,2 |
|
6 |
–СH 2 –CH 2 – |
2,319(2) 2,528(2) |
2,138(3)–2,147(3) |
2,176(3) |
166,80(8) |
355,12 |
|
7 |
1,2-С 6 F 4 |
2,283(3) 2,357(3) |
2,100(5)–2,113(4) 2,108(4)–2,124(4) |
2,158(4) 2,141(4) |
176,18(14) 177,42(14) |
356,19 355,58 |
|
8 |
1,2-C 6 Cl 4 |
2,474(1) 2,310(1) |
2,098(2)–2,116(2) 2,100(2)–2,116(2) |
2,147(2) 2,164(2) |
170,14(6) 175,31(6) |
356,76 355,19 |
|
9 |
С 2 B 10 H 10 |
2,275(3) 2,364(3) |
2,115(4)–2,122(4) 2,112(4)–2,118(4) |
2,173(4) 2,165(4) |
176,77(13) 175,74(13) |
357,16 355,25 |
*Два типа кристаллографически независимых молекул.
Химия элементоорганических соединений
Согласно данным рентгеноструктурного анализа атомы сурьмы в молекулах 1–8 имеют искаженную тригонально-бипирамидальную координацию. Карбоксилатный лиганд выполняет мостиковую функцию, соединяя два фрагмента Ph 4 Sb. Аксиальные углы OSbC варьируют от 166,80(8)° до 166,80(8), суммы углов в экваториальных плоскостях от 355,12° до 358,0° (табл. 3). Аксиальные связи во всех случаях длиннее экваториальных и лежат в диапазоне 2,141(4)– 2,179(6) Å. Длины связей Sb–O варьируют в диапазоне 2,242(3)–2,528(2) Å, что больше суммы ковалентных радиусов атомов сурьмы и кислорода (2,07Å [12]).
В молекуле карборанилкарбоксилата тетрафенилсурьмы тригонально-бипирамидальная координация центрального атома сурьмы наиболее искажена. В аксиальных положениях находятся карбоксилатный и фенильные лиганды. Сумма углов в экваториальной плоскости равна 352,38(14)°. Аксиальный угол OSbC акс равен 174,06(12)°. Валентные углы OSbC экв меньше 90° и лежат в диапазоне 76,71(12)–86,89(13)°, при этом углы C акс SbC экв (97,58(15)–101,19(14)°) больше 90°. Расстояния Sb–C экв варьируют в диапазоне 2,095(4)–2,116(3) Å. Аксиальная связь длиннее экваториальных и равна 2,136(4) Å. Расстояние Sb–O составляет 2,469(3) Å, что меньше суммы ковалентных радиусов сурьмы и кислорода (2,07 Å [12]).
Таблица 4
Основные геометрические параметры молекул 10–13
|
№ |
Ar |
R |
d Sb-O, Å |
d Sb-C экв , Å |
d Sb-C акс , Å |
ωOSbC aкс , град |
∑ω C экв SbС экв , град |
|
10 |
Ph |
–СH=CH– |
2,509(1) |
2,092(2)–2,108(4) |
2,130(2) |
173,46(7) |
351,7 |
|
11 |
Ph |
–СH 2 –CH 2 – |
2,302(1) |
2,111(2)–2,121(2) |
2,169(2) |
175,78(7) |
355,99 |
|
12 |
Ph |
1,2-C 6 H 4 |
2,530(3) |
2,099(4)–2,117(4) |
2,129(4) |
177,5(1) |
352,7 |
|
13 |
p-Tol |
1,2-C 6 H 4 |
2,463(9) |
2,066(11)–2,105(10) |
2,117(11) |
176,5(4) |
352,5 |
В молекулах 10–13 тригонально-бипирамидальная координация атома сурьмы искажена в большей степени по сравнению с карбоксилатами бис (тетрафенилсурьмы). Суммы углов в экваториальной плоскости лежат в диапазоне 351,7–355,99°, углы OSbC акс 173,46(7)–177,5(1)°. Связи Sb– C акс составляют 2,117(11)–2,169(2) Å, Sb–C экв 2,066(11)–2,121(2) Å, Sb–O 2,302(1)–2,530(3) Å. Искажение валентных углов, удлинение связи Sb–O наряду с укорочением аксиальной связи демонстрируют тенденцию перехода фрагмента Ph 4 Sb в тетраэдрическую конфигурацию.
При замене ароматического углеводорода на диоксан взаимодействие пентафенилсурьмы с щавелевой кислотой (мольное соотношение 2:1) приводит к образованию сольвата оксалата бис (тетрафенилсурьмы) с диоксаном ( 14 ) [13]:
C 4 H 8 O 2
2Ph 5 Sb + HOC(O)C(O)OH → Ph 4 SbOC(O)C(O)OSbPh 4 ⋅ С 4 H 8 O 2 + 2 PhH
По данным РСА, в молекуле 14 атомы сурьмы имеют искаженное октаэдрическое окружение. В экваториальной плоскости октаэдра находятся атомы кислорода тетрадентатного лиганда, наряду с двумя атомами углерода фенильных групп, в аксиальных позициях находятся атомы углерода двух других фенильных групп. Следует отметить, что сольватная молекула диоксана не участвует в образовании внутри- и межмолекулярных водородных связей.
Взаимодействием сукцината бис (тетрафенилсурьмы) с йодом получен сольват трииодида [(μ4-сукцинато)гексадекафенилтетрасурьмы] с бензолом ( 15 ) [14]:
PhH
2Ph 4 SbOC(O)CH 2 CH 2 C(O)OSbPh 4 + 3I 2 → (Ph 4 Sb) 2 O(О)CCH 2 CH 2 C(O)О(Ph 4 Sb) 2 ][I 3 ] 2 ∙4PhH
Реакция сукцината бис (тетрафенилсурьмы) с йодом протекала с разрывом связи сурьма– кислород и образованием центросимметричных сукцинат-анионов, каждый из которых координирует на себя четыре катиона Ph 4 Sb; в качестве противоионов выступают трииодид-анионы.
Другой метод получения сурьмаорганических производных дикарбоновых кислот, основанный на реакции дигалогенида трифенилсурьмы с натриевыми солями дикарбоновых кислот в метаноле и последующим нагреванием с обратным холодильником в течение 8–12 часов, эффективен в синтезе ( μ -2,3-дибромсукцинато- κ 2 О 1: О 4) бис [метокси- κO ]трифенилсурьмы( 16 ) [15]:
CH 3 ONa
Ph 3 SbCl 2 + HO(O)C–CH(Br)–CH(Br)–C(O)OH→
→ Ph 3 (OCH 3 )SbO(O)C–CH(Br)–CH(Br)–C(O)OSb(OCH 3 )Ph 3 16
В молекуле 16 атомы сурьмы имеют незначительно искаженную тригонально-бипирамидальную координацию. В экваториальных положениях находятся атомы углерода фенильных групп, в аксиальных атомы кислорода карбоксилатного лиганда и метоксигруппы.
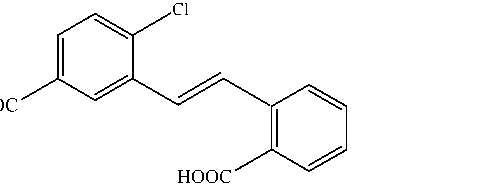
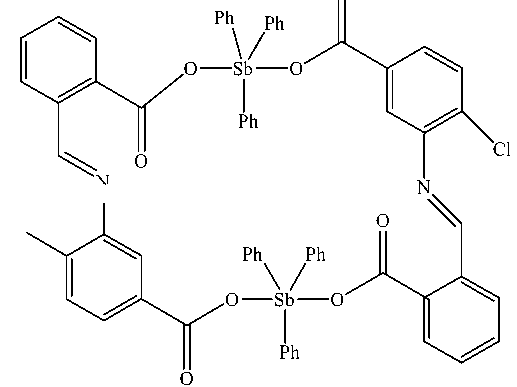
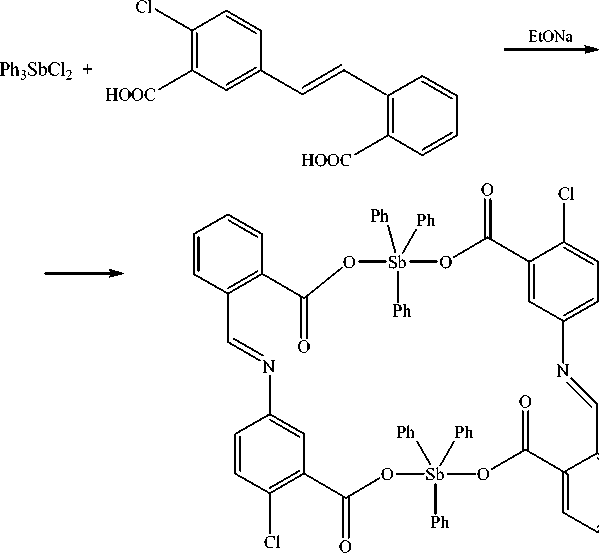
Взаимодействием хлорида трифенилсурьмы с основаниями Шиффа в присутствии метилата натрия при нагревании с обратным холодильником в течение 12 часов при мольном соотношении 1:1 были получены два 24-членных макроцикла симметричного строения общей формулы [Ph 3 SbL] 2 , где H 2 L–5-{[(2-карбоксифенил)метилен]амино}-4-хлорбензойная кислота и 5-{[(2-карбоксифенил)метилен]амино}-2-хлорбензойная кислота. В состав молекул 17 , 18 входит два атома сурьмы, содержащие два атома сурьмы, связанные между собой основаниями Шиффа, выполняющими мостиковую функцию [16].
|
Ph3SbCl2 + HOOC Cl |
Cl EtONa HOOC O Ph Ph O Sb O । I Ph O Cl NN O N Ph Ph O Sb O Ph O 17 |
Химия элементоорганических соединений
Заключение
Взамодействием пентаарилсурьмы с дикарбоновыми кислотами образуются 2 типа продуктов: 1) карбоксилаты бис (тетрафенилсурьмы), полученные из пентафенилсурьмы и дикарбоновой кислоты в толуоле при нагревании и мольном соотношении 2:1; 2) кислые карбоксилаты тетра-фенилсурьмы, синтезируемые из пентаарилсурьмы и дикарбоновой кислоты при мольном соотношении 1:1. В случае взаимодействия пентафенилсурьмы с ацетилендикарбоновой и карбора-нилдикарбоновой кислотами происходит декарбоксилирование одной из карбоксильных групп и образование пропиолата и карборанилкарбоксилата тетрафенилсурьмы соответственно. Второй метод синтеза сурьмаорганических производных дикарбоновых кислот, основанный на реакции дихлорида трифенилсурьмы с натриевыми солями дикарбоновых кислот, позволяет синтезировать биядерные макроциклические сурьмаорганические соединения, в которых карбоксилатные лиганды выполняют мостиковую функцию. Реакция сукцината бис (тетрафенилсурьмы) с йодом протекает с образованием центросимметричных сукцинат-анионов, каждый из которых координирует на себя четыре катиона Ph4Sb; в качестве противоионов выступают трииодид-анионы.
Список литературы Сурьмаорганические производные дикарбоновых кислот. Синтез и строение (обзор)
- Millington, P.L. Phenylantimony (V) Oxalates: Isolation and Crystal Structures of , 2ox and (SbPh4)2ox/P.L. Millington, D.B. Sowerby//J. Chem. Soc., Dalton Trans. -1992. -No. 7. -P. 1199-1204.
- Шарутин, В.В. Синтез и строение сукцината, малата и тартрата бис(тетрафенилсурьмы)/В.В. Шарутин, О.К. Шарутина//Коорд. химия. -2014. -Т. 40, № 9. -С. 559-563 DOI: 10.1134/S1070328414090073
- Синтез, строение и реакции μ-оксо-бис/В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин и др.//Коорд. химия. -2001. -Т. 27, № 9. -С. 710-716. DOI: 10.1023/a:1017909824029
- Reactions of pentaphenylantimony with dycarboxylicasids/V.V. Sharutin, O.K Sharutina, A.P. Pakusina et al.//J.Organometal. Chem. -1997. -V. 536-537, № 1-2. -P. 87-92 DOI: 10.1016/s0022-328x(96)06463-7
- Sharutin, V.V. Interaction of pentaphenylantimony with acetylenedicarboxylic acid. Molecular structure of bis(tetraphenylantimony)acetylenedicarboxilate/V.V. Sharutin, O.K. Sharutina, Yu.O. Gubanova//Вестник ЮУрГУ. Серия «Химия». -2015. -Т. 7, № 4. -С. 17-22 DOI: 10.14529/chem150403
- Синтез и строение тетрафторфталата бис(тетрафенилсурьмы)/В.В. Шарутин, О.К. Шарутина, Е.А. Бондарь и др.//Журн. общ. химии. -2002. -Т. 72, Вып. 2. -С. 2029-2032 DOI: 10.1023/A:1023411228493
- Шарутин, В.В. Синтез и строение тетрахлорфталата бис(тетрафенилсурьмы)/В В. Шарутин, O.K. Шарутина//Журн. неорг. химии. -2015. -Т. 60, №. 3. -С. 292-294 DOI: 10.1134/S0036023615030171
- Interaction of pentaphenylantimony with carboranedicarboxylic acid/V.V. Sharutin, O.K. Sharutina, Yu.O. Gubanovaet al.//Journal of organometallic chemistry. -2015. -V. 798. -P. 41-45 DOI: 10.1016/j.jorganchem.2015.09.002
- Шарутин, В.В. Синтез и строение кислого сукцината тетрафенилсурьмы/В.В. Шарутин, О.К. Шарутина, Ю.О. Губанова//Бутлеровские сообщения. -2014. -Т. 39, № 7. -С. 139-141.
- Синтезистроениекислогофталататетрафенилсурьмы/В.В. Шарутин, О.К. Шарутина, И.Г. Мельникова и др.//Изв. РАН. Сер. хим. -1996. -№ 8. -С. 2082-2085 DOI: 10.1007/bf01457791
- Шарутин, В.В. Реакции пентаарил сурьмы с диацилатами триарилсурьмы/В.В. Шарутин, О.К. Шарутина, А.П. Пакусина, В.К. Бельский//Журн. общ. химии. -1997. -Т. 67, Вып. 9. -С. 1536-1541.
- Бацанов, С.С. Атомные радиусы элементов/С.С. Бацанов//Журн. неорг. химии. -2001. -Т. 36, № 12. -С. 3015-3037.
- Синтез и строение сольвата оксалата бис(тетрафенилсурьмы) с диоксаном/В.В. Шарутин, О.К. Шарутина, Е.В. Артемьева и др.//Бутлеровские сообщения. -2016. -Т. 47, № 19. -С. 17-20.
- Синтез и строение сольвата трииодида с бензолом 2⋅ 4PhH/В. В. Шарутин, О.К. Шарутина, Ю.О. Губанова и др.//Коорд. химия. -2017. -Т. 43, № 7. -С. 444-448 DOI: 10.7868/S0132344X17060093
- Quan, L. (μ-2,3-Dibromo-succinato-κO:O)bis-/L.Quan, H. Yin, W. Fu//ActaCryst. Sec. E. -2011. -V. E67. -M. 713 DOI: 10.1107/S1600536811016114
- Highly symmetrical 24-membered macrocyclic organoantimony(V) complexes constructed from Schiff base ligands possessing two terminal carboxyl groups/M. Hong, H.-D. Yin, W.-K. Li et al.//Inorg. Chem. Communications. -2011. -V. 14, no 10. -P. 1616-1621 DOI: 10.1016/j.inoche.2011.06.023


