Технические аспекты и результаты применения клапанных гомографтов в хирургии атриовентрикулярных клапанов сердца: систематический обзор
Автор: Нуждин Михаил Дмитриевич, Комаров Р.Н., Мацуганов Д.А., Мельников И.Ю., Царегородцев А.В.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Обзоры
Статья в выпуске: 2 т.27, 2023 года.
Бесплатный доступ
Цель. Систематизировать мировой опыт использования гомографтов в хирургии митрального и трикуспидального клапанов и дать ему критическую оценку. Методы. Систематический обзор провели в соответствии с критериями PRISMA. В качестве поисковых запросов в базах данных использовали термины: ((mitral homograft) OR (tricuspid homograft) OR (homograft) AND (valve replacement) OR (valve repair)). Поиск вели в доступных базах данных PubMed (National Center for Biotechnology Information), Cochrane Library, Web of Science (Clarivate), Google Scholar. Результаты. После проведения поиска в соответствии с критериями включения и исключения с привлечением трех специалистов в анализ отобрали 23 публикации за период с 1988 по 2021 г. Средний срок наблюдения 15 [6-60] мес. Выживаемость на конец периода наблюдения составила 100 [90,7-100,0] %, свобода от дисфункции графта - 100 %, свобода от реоперации - 100 [79-100] %. Заключение. Использование гомографтов в хирургии атриовентрикулярных клапанов ограничено небольшими сериями случаев с вариабельными хирургическими аспектами, гетерогенным периодом наблюдения. Представленные непосредственные результаты применения гомографтов позволяют рассматривать их как альтернативный клапанный заменитель при широком спектре патологии как у первичных, так и повторных пациентов.
Гомографт, митральный клапан, протезирование клапана, трикуспидальный клапан
Короткий адрес: https://sciup.org/142238248
IDR: 142238248 | DOI: 10.21688/1681-3472-2023-2-42-53
Technical aspects and outcomes of using homografts in atrioventricular valve surgery: a systematic review
Objective: To summarize and critically appraise the world experience with homografts in mitral and tricuspid valve surgery. Methods: We conducted a systematic review according to the PRISMA criteria. We searched the following terms in available databases, such as PubMed (National Center for Biotechnology Information), Cochrane Library, Web of Science (Clarivate), and Google Scholar: ((mitral homograft) OR (tricuspid homograft) OR (homograft) AND (valve replacement) OR (valve repair)). Results: We recruited 3 specialists to search the information matching our inclusion and exclusion criteria and selected 23 publications covering the period 1988-2021 for analysis. The mean follow-up period was 15 [6-60] months. Survival at the end of the follow-up period was 100% [90.7%-100.0%]; freedom from graft dysfunction was 100%, and freedom from reoperation was 100% [79%-100%]. Conclusion: The world experience with homografts in atrioventricular valve surgery is limited to small case series with inconclusive surgical aspects and a heterogeneous follow-up period. The immediate results suggest that homografts could be used as an alternative valve substitute for a wide spectrum of diseases both in primary and revision surgery.
Текст научной статьи Технические аспекты и результаты применения клапанных гомографтов в хирургии атриовентрикулярных клапанов сердца: систематический обзор
М.Д. Нуждин, Р.Н. Комаров, Д.А. Мацуганов, И.Ю. Мельников, А.В. Царегородцев,
Применение гомографтов (ГГ) клапанов сердца традиционно рассматривалось как метод реконструкции или протезирования клапанов сердца при клапанном нативном и протезном эндокардите [1–4]. По данным J.B. Kim и соавт., использование ГГ не повлияло на снижение смертности или частоту реинфекции в случаях клапанного инфекционного эндокардита (ИЭ) [2]. Природная биосовместимость аллографтов считается основным фактором высокой резистентности к повторной инфекции и является хорошим аргументом для использования их при распространенных формах клапанного (абсцессы корня аорты) и протезного ИЭ, но исследования ограничены изучением эффективности ГГ в аортальной позиции [5–7]. С другой стороны, несмотря на обнадеживающие результаты имплантации ГГ и расширение возможностей хирургического лечения различных форм ИЭ, по данным T.E. David, J.-F. Avierinos и соавт., механические протезы и ксе-нографты могут обеспечивать сопоставимые результаты, в том числе свободу от реинфекции в случае полного удаления пораженных тканей во время операции [8; 9].
Несмотря на противоречивый опыт и результаты применения, криосохраненные ГГ показали схожие гемодинамические характеристики с биологическими ксенографтами, а также некоторые преимущества над традиционными биологическими протезами, механическими протезами и ксенографтами: меньшую тромбогенность, отсутствие необходимости в антикоагулянтной терапии, низкую частоту неврологических осложнений, а также возможность задействовать транскатетерные технологии в случаях структурной дегенерации [10]. Преждевременная дегенерация биопротезов и протезный ИЭ, особенно у молодых пациентов, подталкивали к поиску новых путей решения данной проблемы, в том числе путем имплантации ГГ в митральную и трикуспидальную позиции, и актуальность использования последних сохраняется [11–14].
В недавнем мультицентровом проспективном исследовании ARISE показаны превосходные гемодинамические и клинические результаты применения децеллюляризированных ГГ в аортальной позиции даже в сравнении с легочными аутографтами, что демонстрирует перспективы использования аллографтов в хирургическом лечении пороков сердца [15].
Значительно сложнее вопрос их использования в хирургии атриовентрикулярных клапанов. С одной стороны, применение ГГ в митральной пози- ции демонстрирует хорошие гемодинамические и клинические показатели, сравнимые с реконструктивными операциями на митральном клапане, риск структурной дегенерации графта сопоставим с наблюдаемым на биологических протезах. С другой стороны, техническая сложность имплантации, меньшая доступность ограничивают применение [16]. Использование ГГ в трикуспидальной позиции в мировой литературе представлено небольшими сериями случаев с положительными непосредственными результатами, однако судить об их роли в лечении трикуспидальных пороков не представляется возможным. Актуальность применения альтернативных клапанных заменителей в хирургии трикуспидального клапана продиктована высокой долей имплантации биологических и механических протезов с весьма противоречивыми результатами, низкой доступностью транскатетерных технологий, которые не могут считаться идеальным методом выбора из-за сложной анатомии трикуспидального клапана и полости правого желудочка, невозможности использовать в случаях активного инфекционного и протезного инфекционного эндокардита [17–19].
Цель исследования — систематизация и критическая оценка мирового опыта применения ГГ в хирургии атриовентрикулярных клапанов сердца.
Методы
Поиск и отбор публикаций
Систематический обзор выполнили в соответствии с рекомендациями и положениями отчетности для систематических обзоров и метаанализов (PRISMA) [20]. Поиск вели в электронных базах данных PubMed (National Center for Biotechnology Information), Cochrane Library, Web of Science (Clarivate), Google Scholar. Поиск в базе данных Embase не проводили из-за наложенных ограничений на выбранный регион с получением официального уведомления. Ограничения по дате публикаций выставили с 1988 г. по март 2023 г. Три независимых исследователя отдельно друг от друга проводили поиск и отбор статей с помощью поисковых запросов, ключевых слов (в том числе по рубрикатору Medical Subject Headings (MeSH)). В качестве поисковых запросов в базах данных использовали термины: ((mitral homograft) OR (tricuspid homograft) OR (homograft) AND (valve replacement) OR (valve repair)). Любые разногласия решали путем привлечения третьего исследователя. Критерии включения: применение клапанных ГГ для
Идентификация исследований через базы данных



Идентификация данных через базы данных и регистры
Идентификация данных другими методами
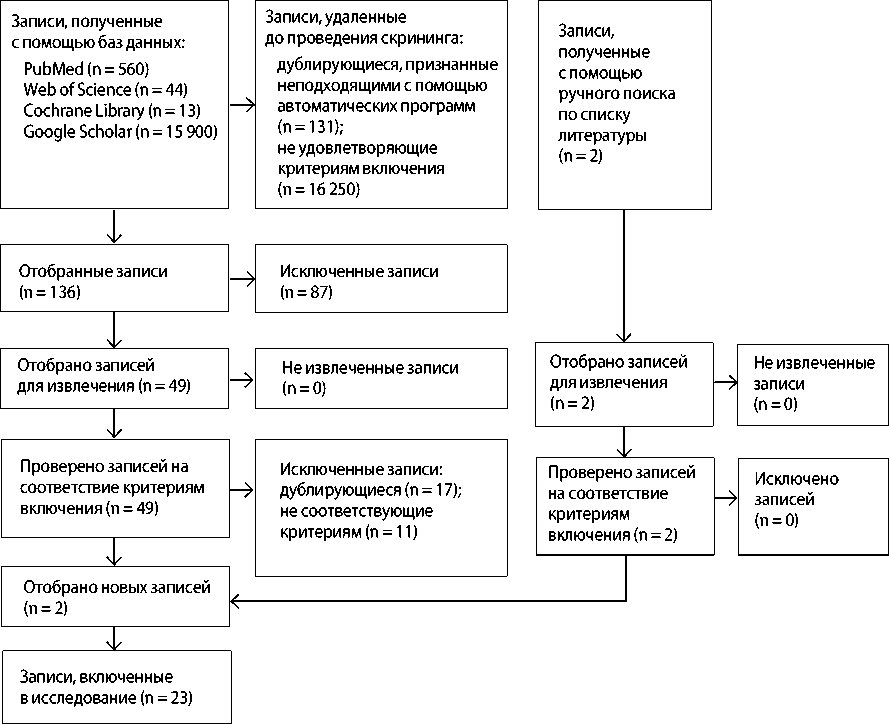
протезирования митрального и/или трикуспидального клапана; полнотекстовые статьи и/или структурированные резюме на английском языке, отражающие оперативную технику имплантации ГГ и/или непосредственные и/или среднеотдаленные результаты. С учетом эксклюзивности выбранной тематики и низкой частоты публикаций в исследование включили в том числе случаи из практики, которые отражают технические аспекты имплантации аллографтов.
Из скрининга и анализа исключили статьи на других языках, обзоры и мнения авторов. Приемлемость каждой работы для включения проверяли в два этапа: просмотр названия и аннотации; просмотр полного текста. Дублирующиеся публикации исключали автоматически с помощью программы Zotero (Corporation for Digital Scholarship, Виенна, США) и вручную.
Извлечение и синтез данных
Для каждого исследования регистрировали следующие данные: первый автор, год публикации, количество случаев, этиология поражения клапана, вид используемого ГГ, период наблюдения, технические аспекты имплантации, непосредственная и 30-дневная летальность, ранняя дисфункция ГГ, послеоперационные осложнения, свобода от дисфункции графта, свобода от повторной операции, выживаемость на конец периода наблюдения.
Статистический анализ
Метаанализ данных не проводили с учетом высокой гетерогенности исследований, существенных различий в технике, видах используемых ГГ, подходах к регистрации конечных точек.
Результаты и обсуждение
По итогам первоначального электронного поиска по запросу получили следующее количество публикаций: PubMed — 560, Web of Science — 44, Cochrane Library — 13, Google Scholar — 15 900. Из анализа исключили работы, посвященные сочетанной имплантации аортальных и митральных ГГ при осложненных формах ИЭ, коррекции сопутствующей врожденной патологии у детей, применению транскатетерных технологий для лечения дисфункции аллографта. Всего после удаления повторяющихся статей, исследований, не соответствующих критериям включения и исключения, осталось 49 работ. Два независимых исследователя просмотрели полнотекстовые и/или структурированные аннотации оставшихся публикаций и выявили 5 и 44 статей соответственно. После коллегиального обсуждения и привлечения третьего специалиста в анализ отобрали 23 публикации. Алгоритм поиска представлен на рисунке .
Актуальный мировой опыт использования ГГ для пластики или протезирования атриовентрикулярных клапанов отражен в 23 исследованиях с 1988 по 2021 г. Более ранние работы не включали в анализ по следующим причинам: 1) существенная разница в технологиях заготовки и хранения ГГ; 2) отсутствие научно обоснованной технологии имплантации с учетом последних данных об анатомии и физиологии атриовентрикулярных клапанов, корня аорты, корня легочной артерии; 3) существенное изменение показаний к операциям с учетом последних данных доказательной медицины; 4) изменение и совершенствование технологий визуализации клапанов сердца, оценки их функции в раннем и отдаленном послеоперационных периодах.
Систематизацию данных и анализ использования легочного аутографта для протезирования атриовентрикулярных клапанов не проводили ввиду малой актуальности данной процедуры в кардиохирургической практике. Технические аспекты имплантации ГГ, этиология поражения клапанного аппарата отражены в табл. 1. Из 23 проанализированных работ 14 содержат описание клинических случаев и ограничены 1–3 пациентами, тем не менее они включены в исследование, так как отражают оригинальные подходы к использованию ГГ в хирургии митрального и трикуспидального клапанов. Четыре статьи представляют собой описания серий случаев от 4 до 9 больных, четыре — оригинальные исследования с включением 9 и более пациентов.
Этиология поражения клапанного аппарата и показания к использованию гомографтов
Этиологией поражения клапанного аппарата являлись ИЭ, ревматизм, системная красная волчанка, дегенеративные и врожденные пороки клапанов сердца, в том числе аномалия Эбштейна. Основным показанием к использованию ГГ был клапанный ИЭ. Исключение составляют работы R. McKay и соавт., N. Kumar и соавт., J.V. Nozar и со-авт., в которых клапанные ГГ применяли при врожденной патологии митрального или трикуспидального клапана. Имплантацию производили как при первичном поражении, так и при повторных операциях [21; 24; 29]. Максимальный опыт использования ГГ в хирургии митрального клапана представили S. Olivito и соавт. (n = 106), A.S. Kumar и со-авт. (n = 37), D.B. Doty и соавт. (n = 20), H. Gulbins и соавт. (n = 14) [16; 30; 31; 34].
Виды клапанных аллографтов, используемых в хирургии атриовентрикулярных клапанов
В отобранных исследованиях для протезирования атриовентрикулярных клапанов сердца использовали легочный, аортальный, трикуспидальный и митральный ГГ. Наибольший опыт применения митральных ГГ для протезирования трикуспидального клапана представили U. Hvass и соавт. (n = 9), J.-P.A. Couetil и соавт. (n = 7), A. Kalangos и соавт. (n = 8), хотя все три работы ограничены описанием серий случаев [32; 33; 36]. Максимальное число имплантаций трикуспидального ГГ в трикуспидальную позицию отражено в оригинальном исследовании B.M.S. Shrestha и соавт. (n = 14) [14]. Легочный ГГ для протезирования трикуспидального клапана применили G.B. Luciani и соавт., R. McKay и со-авт., K.-M. Chiu и соавт. [12; 21; 37]. Аортальный ГГ использовали только две группы авторов: N. Kumar и соавт. и M.-S. Kim и соавт. [24; 39]. Хотя легочные и аортальные ГГ эпизодически выбирают для коррекции пороков атриовентрикулярных клапанов даже в настоящее время, их применение вряд ли может гарантировать предсказуемые результаты в свете фиксации комиссуральных стержней в полости правого желудочка, а также фиксации малого фиброзного кольца в большее фиброзное кольцо трикуспидального клапана. Использование же вспомогательных сосудистых протезов для стабилизации легочного или аортального ГГ с последующей имплантацией тубулярного синтетического протеза в полость правого желудочка не может обеспечить нормальную анатомию, гемодинамику
Табл. 1. Хирургические аспекты протезирования атриовентрикулярных клапанов гомографтами
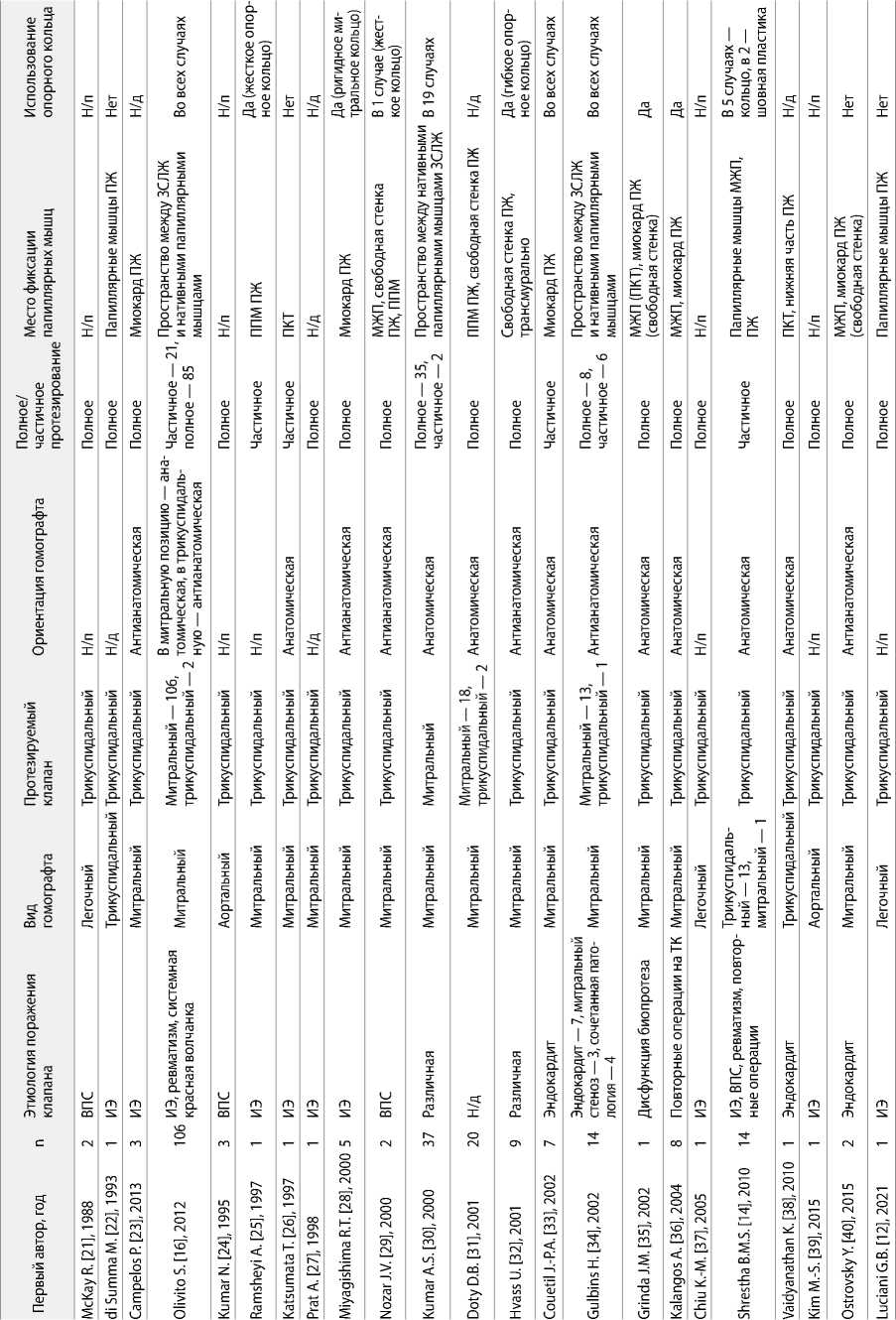
Примечание. n — количество пациентов; ВПС — врожденный порок сердца; Н/п — не применимо; ИЭ — инфекционный эндокардит; Н/д — нет данных; ПЖ — правый желудочек; ЗСЛЖ — задняя стенка левого желудочка; ЛЖ — левый желудочек; ПКТ — перегородочно-краевая трабекула; МЖП — межжелудочковая перегородка; ППМ — передняя папиллярная мышца; ТК — трикуспидальный клапан.
и профилактику тромбообразования и инфицирования графта. Из этого следует очень малое количество публикаций единичных случаев из практики.
Протезирование трикуспидального клапана трикуспидальным ГГ, на первый взгляд, является наиболее физиологичным с точки зрения анатомии и гемодинамики, однако трикуспидальный клапан — крайне сложная структура с несколькими точками фиксации сухожильных хорд, вариантной анатомией папиллярных мышц и створок клапана, отсутствием развитого фиброзного кольца, что ограничивает его применение в повседневной практике для полного протезирования трикуспидального клапана. Альтернативным вариантом использования ГГ в трикуспидальной позиции является митральный ГГ. Концепция бикуспидализации правого атриовентрикулярного отверстия не новая, а имплантация атриовентрикулярного алло-графта в атриовентрикулярную позицию теоретически должна обеспечивать физиологический поток крови, низкий градиент давления и свободу от необходимости в антикоагулянтной терапии. Кроме того, наличие в хирургическом арсенале митрального ГГ расширяет возможности реконструктивной хирургии трикуспидального клапана. С анатомической точки зрения митральный клапанный аппарат имеет более развитое фиброзное кольцо, меньшее количество головок папиллярных мышц для фиксации, что в совокупности с физиологической работой в условиях системного давления может обеспечивать преимущество над трикуспидальным гомографтом.
Технические аспекты использования атриовентрикулярных гомографтов при протезировании митрального и трикуспидального клапанов
Атриовентрикулярные ГГ возможно применять как для полного, так и для частичного протезирования митрального и трикуспидального клапанов. В 8 из 23 исследований митральный ГГ использовали исключительно для полного протезирования трикуспидального клапана [23; 27–29; 32; 35; 36; 40]. S. Olivito и соавт. сделали акцент на полном протезировании митрального клапана митральным ГГ как оптимальном варианте коррекции при выборе ГГ в митральную позицию; частичное протезирование выполняли только на начальных этапах приобретения опыта данной операции [16]. Частичное протезирование митрального клапана митральным ГГ отражено в ранних работах C. Acar и соавт. и H. Gulbins и соавт. [13; 34]. В отношении объема коррекции трикуспидальных пороков частичное протезирование митральным и трикуспидальным ГГ описали A. Ramsheyi и соавт., T. Katsumata и соавт., J.-P.A. Couetil и соавт., B.M.S. Shrestha и соавт. [14; 25; 26; 33]. По данным авторов, которые использовали митральный или трикуспидальный ГГ для частичного протезирования атриовентрикулярного клапана, данный способ можно применять при локализованных формах поражения клапанного аппарата.
Реимплантация папиллярных мышц гомографта
Способ фиксации головок папиллярных мышц при полном протезировании митрального клапана впервые предложили C. Acar и соавт., и другие авторы придерживались данной методики [13]. Наибольший интерес представляет фиксация папиллярных мышц митрального ГГ в трикуспидальной позиции. В исследованиях нет единого мнения ни о месте фиксации папиллярных мышц и их ориентации в полости правого желудочка, ни о том, каким образом ориентировать митральный ГГ в правом атриовентрикулярном отверстии. Описанными зонами фиксации головок папиллярных мышц являются миокард межжелудочковой перегородки, нативные головки папиллярных мышц, свободная стенка правого желудочка. Последнюю использовали для фиксации, в том числе выведения наружу головок папиллярных мышц, в большинстве работ [14; 23; 28; 29; 32; 33; 35; 36; 40]. Недостатки данного способа — необходимость выведения головок на переднюю поверхность правого желудочка, трудно предсказуемое смещение их в случае дальнейшей дилатации полости правого желудочка, травматизация свободной стенки правого желудочка.
Ориентация гомографта в полости правого желудочка
Вопрос ориентации аллографта в полости правого желудочка актуален при использовании митрального ГГ. Анатомическую ориентацию митрального ГГ в трикуспидальной позиции описали только T. Katsumata и соавт., J.-P.A. Couetil и соавт., J.M. Grinda и соавт., A. Kalangos и соавт. [26; 33; 35; 36], в остальных случаях передняя створка митрального ГГ была ориентирована к септальной створке трикуспидального клапана. Судить о преимуществах и недостатках того или иного способа ориентации митрального ГГ в трикуспидальной позиции не представляется возможным, поскольку сравнение групп не проводилось.
Аннулопластика атриовентрикулярных клапанов при имплантации гомографта
Использование опорного кольца после имплантации атриовентрикулярных ГГ в митральную или трикуспидальную позицию также представляет научный и практический интерес с позиции непосредственных и отдаленных результатов. Опорное кольцо применяли во всех случаях протезирования митрального и трикуспидального клапанов S. Olivito и соавт., которые представили наибольший опыт имплантации митральных ГГ [16]. В других исследованиях гибкое или жесткое опорное кольцо задействовали во всех или отдельных случаях A. Ramsheyi и соавт., R.T. Miyagishima и соавт., J.V. Nozar и соавт., A.S. Kumar и соавт., U. Hvass и соавт., J.-P.A. Couetil и соавт., H. Gulbins и соавт., J.M. Grinda и соавт., A. Kalangos и соавт., B.M.S. Shrestha и соавт. [14; 25; 28–30; 32–36]. Судить о преимуществах аннулопла-стики с использованием гибких, жестких колец или шовных методик также невозможно из-за отсутствия систематических данных, сравнительных анализов по данному вопросу.
Непосредственные и отдаленные результаты использования аллографтов в хирургии атриовентрикулярных клапанов
Непосредственные результаты представлены в табл. 2. Средний срок наблюдения составил 15 [6–60] мес., операционная летальность наблюдалась только в исследованиях S. Olivito и соавт. — 4,7 % и A.S. Kumar и соавт. — 13,5 % [16; 30]. Остальные авторы заявляли об отсутствии операционной и 30-дневной смертности. Осложнения зарегистрировали две группы ученых: Y. Ostrovsky и соавт. — развитие полной атриовентрикулярной блокады и G.B. Luciani и соавт. — кровотечение из послеоперационной раны, которое потребовало ее ревизии [12; 40]. О ранней дисфункции графта (митрального в митральной позиции) сообщили S. Olivito и соавт. (4,7 %) [16]. Выживаемость на конец периода наблюдения составила 100 [90,7–100,0] %, свобода от дисфункции ГГ — 100 %, свобода от реоперации — 100 [79–100] %.
Свобода от повторных операций составила: у S. Olivito и соавт. — 64,0 %, A.S. Kumar и соавт. — 72,4 %, D.B. Doty и соавт. — 72,0 %, H. Gulbins и со-авт. — 79,0 %, B.M.S. Shrestha и соавт. — 78,6 % [14; 16; 30; 31; 34]. Только последний коллектив авторов описал свободу от реопераций при использовании графта в трикуспидальной позиции, остальные исследования касались повторных вмешательств после имплантации митрального ГГ в митральную позицию. В рабо- те H. Gulbins и соавт. у двух пациентов в течение двух лет после операции развился ИЭ, что потребовало повторного вмешательства с использованием механического протеза, одного больного направили на реоперацию через 3 года после вмешательства в связи с отрывом хорд митрального ГГ, у остальных митральный аллографт не претерпел морфологических изменений [34].
В наиболее крупном исследовании S. Olivito и со-авт. было 5 ранних реопераций в течение 3 мес. в связи с недостаточностью ГГ. У всех пациентов были технические причины дисфункции ГГ: рестрикция створок из-за неправильного позиционирования папиллярных мышц (n = 3), отрыв створки (n = 1), отрыв хорды шовным материалом (n = 1). В течение среднего периода наблюдения, позднее 30-дневного срока, повторно прооперировали 30 человек. Поздние повторные вмешательства были преимущественно обусловлены дегенеративными изменениями графта (n = 23), ИЭ (n = 5), патологией аортального клапана (n = 2). При анализе причин реопераций авторы не нашли значимой связи с видом техники, возрастом пациентов, размером имплантируемого опорного кольца, однако более высокий риск повторного вмешательства был у больных, которым имплантировали ГГ в возрасте до 18 лет, и при использовании опорного кольца 28-го размера. Авторы подчеркнули сопоставимые гемодинамические характеристики митрального ГГ с пластическими коррекциями клапана, а рискдегенеративных изменений — с таковым при биологическом протезе [16].
По данным A.S. Kumar и соавт., 8 пациентам понадобилась повторная операция в срок от 6 нед. до 58 мес. после первичной [30]. Ранняя дисфункция ГГ была связана с отрывом папиллярной мышцы (n = 2), поздняя — с патологией створок (n = 6). Всем больным имплантировали механический протез, и все они выжили после реоперации. В отличие от S. Olivito и соавт., авторы указанной работы не рекомендовали имплантировать митральный ГГ в митральную позицию, что, вероятнее всего, связано с негативным опытом на начальных этапах освоения методики. Это, в свою очередь, оттолкнуло исследователей от дальнейшего ее использования, в отличие от S. Olivito и соавт.
По данным D.B. Doty и соавт., все 5 пациентов, которым потребовалось повторное вмешательство, были оперированы в течение первого года, анализа причин авторы не приводят. Профиль реопераций при использовании трикуспидального ГГ для частичного протезирования трикуспидального клапана представлен только в работе B.M.S. Shrestha и соавт.
Трех пациентов (21,4 %) подвергли повторной операции по поводу резидуальной трикуспидальной недостаточности через 23, 56, и 89 мес. соответственно. Причины трикуспидальной недостаточности после вмешательства: частичный отрыв одной из папиллярных мышц в одном случае, прогрессирование трикуспидальной недостаточности на фоне исходной высокой легочной гипертензии и недостаточности клапана легочной артерии. Двум пациентам выполнили протезирование клапана биологическим протезом, одному — пластику ГГ. Авторы подчеркнули значимость исходной степени легочной гипертензии и патологии клапана легочной артерии при выборе метода реконструкции с использованием трикуспидального аллографта [31].
Таким образом, исходя из отдаленных результатов, повторные операции требовались больным, которым протезировали митральный клапан митральным ГГ, при этом все авторы столкнулись с реоперациями на начальных этапах освоения методики. Основными причинами дисфункции графта в отдаленном периоде были технические ошибки, которые проявлялись на более раннем сроке, а также дегенеративные изменения митрального ГГ в митральной позиции со временем, что обусловливало позднюю дисфункцию. К дисфункции трикуспидального ГГ чаще всего приводили технические причины и дальнейшая дилатация полости правого желудочка. Стоит отметить, что S. Olivito и соавт. указывали на большую частоту ранней дисфункции ГГ при
Табл. 2. Непосредственные и отдаленные результаты использования гомографтов в хирургии атриовентрикулярных клапанов сердца
|
Первый автор, год |
n |
Период наблюдения, мес. |
Операционная, 30-дневная летальность, % |
Выживаемость, % |
Свобода от дисфункции графта, % |
Свобода от реоперации, % |
|
McKay R. [21], 1988 |
2 |
2 |
0 |
100 |
Н/д |
100 |
|
di Summa M. [22], 1993 |
1 |
6 |
0 |
100 |
Н/д |
100 |
|
Campelos P. [23], 2013 |
3 |
252 |
0 |
33 |
Н/д |
33 |
|
Olivito S. [16], 2012 |
106 |
213,6 |
4,7 |
80 |
Н/д |
64 |
|
Kumar N. [24], 1995 |
3 |
12 |
0 |
100 |
100 |
100 |
|
Ramsheyi A. [25], 1997 |
1 |
18 |
0 |
100 |
Н/д |
100 |
|
Katsumata T. [26], 1997 |
1 |
6 |
0 |
100 |
100 |
100 |
|
Prat A. [27], 1998 |
1 |
0,75 |
0 |
100 |
100 |
100 |
|
Miyagishima R.T. [28], 2000 |
5 |
12 |
0 |
80 |
Н/д |
Н/д |
|
Nozar J.V. [29], 2000 |
2 |
48 |
0 |
100 |
100 |
100 |
|
Kumar A.S. [30], 2000 |
37 |
60 |
13,5 |
90,7 |
Н/д |
72,4 |
|
Doty D.B. [31], 2001 |
20 |
38,8 |
0 |
100 |
Н/д |
72 |
|
Hvass U. [32], 2001 |
9 |
3 |
0 |
100 |
100 |
100 |
|
Couetil J.-P.A. [33], 2002 |
7 |
46 |
0 |
85,8 |
Н/д |
100 |
|
Gulbins H. [34], 2002 |
14 |
60 |
0 |
79 |
79 |
79 |
|
Grinda J.M. [35], 2002 |
1 |
12 |
0 |
100 |
100 |
100 |
|
Kalangos A. [36], 2004 |
8 |
68 |
0 |
100 |
100 |
100 |
|
Chiu K.-M. [37], 2005 |
1 |
Н/д |
0 |
Н/д |
Н/д |
Н/д |
|
Shrestha B.M.S. [14], 2010 |
14 |
126 |
0 |
100 |
100 |
78,6 |
|
Vaidyanathan K. [38], 2010 |
1 |
9 |
0 |
100 |
100 |
100 |
|
Kim M.-S. [39], 2015 |
1 |
12 |
0 |
100 |
100 |
100 |
|
Ostrovsky Y. [40], 2015 |
2 |
3 |
0 |
100 |
100 |
100 |
|
Luciani G.B. [12], 2021 |
1 |
18 |
0 |
100 |
100 |
100 |
Примечание. Н/д — нет данных.
частичном протезировании митрального клапана, тогда как при полном протезировании риск был ниже. Эти данные, возможно, коррелируют с полученными B.M.S. Shrestha и соавт., которые выполняли частичное протезирование трикуспидального клапана трикуспидальным ГГ. Детальный анализ отдаленных результатов применения атриовентрикулярных ГГ не проводился, связь с размером использованного графта в литературе не представлена. Отсутствуют исследования, посвященные непосредственным и отдаленным результатам полного протезирования трикуспидального клапана митральным гомографтом.
Все авторы, которые использовали ГГ для лечения клапанного и протезного ИЭ, заявляли о полном купировании инфекционно-воспалительного процесса.
Ограничения
Существенная гетерогенность представленных исследований в значительном временном промежутке, большое количество случаев из практики.
Заключение
Использование ГГ в хирургии корня аорты, по сравнению с хирургией атриовентрикулярных клапанов, освещено в мировой литературе в большем объеме с представлением непосредственных, отдаленных результатов, сопоставлением с механическими, биологическими протезами, ксенограф-тами. Интерес к применению ГГ как альтернативных клапанных протезов сохраняется и в ряде случаев расширяет хирургический арсенал. Существенно меньший опыт имплантации атриовентрикулярных ГГ для коррекции пороков митрального и трикуспидального клапанов обусловлен отсутствием единых подходов к определению показаний к операции, сложностью хирургической техники, низкой доступностью ГГ. Имеющийся мировой опыт применения атриовентрикулярных ГГ в митральной и трикуспидальной позициях демонстрирует хорошие непосредственные клинические, а в ряде случаев и отдаленные результаты, что, в свою очередь, говорит о возможности их достижения, анализа и сравнения с традиционными методами коррекции пороков митрального и трикуспидального клапанов. Тем не менее имеющийся опыт и отдаленные результаты в литературе сильно ограничены, анализ связи с исходной патологией, размером графта не проводился. Использование аортального и легочного ГГ в митральной или трикуспидальной позициях вряд ли когда-либо будет являться достойной альтернативой традиционным методам хирургического лечения или имеющимся атриовентрикулярным ГГ. Перспективы имплантации ГГ как в аортальную, так и атриовентрикулярную позицию преимущественно зависят от улучшения технологии консервации тканей, доступности ГГ, логистики, определения целевой группы пациентов и стандартизации хирургической техники. Для определения показаний к использованию ГГ в атриовентрикулярной позиции, разработки тактики оперативного лечения необходимо сравнение с традиционными биологическими или механическими протезами на больших группах пациентов в непосредственном и отдаленном периодах наблюдения.
Список литературы Технические аспекты и результаты применения клапанных гомографтов в хирургии атриовентрикулярных клапанов сердца: систематический обзор
- Jassar A.S., Bavaria J.E., Szeto W.Y., Moeller P.J., Maniaci J., Milewski R.K., Gorman J.H. 3rd, Desai N.D., Gorman R.C., Pochettino A. Graft selection for aortic root replacement in complex active endocarditis: does it matter? Ann Thorac Surg. 2012;93(2):480-487. PMID: 22195976. https://doi. org/10.1016/i.athoracsur.2011.09.074
- Kim J.B., Ejiofor J.I., Yammine M., Camuso J.M., Walsh C.W., Ando M., Melnitchouk S.I., Rawn J.D., Leacche M., MacGillivray T.E., Cohn L.H., Byrne J.G., Sundt T.M. Are homografts superior to conventional prosthetic valves in the setting of infective endocarditis involving the aortic valve? J Thorac Cardiovasc Surg. 2016;151 (5):1239-1248.e2. PMID: 26936004. https://doi. org/10.1016/j.jtcvs.2015.12.061
- Savage E.B., Saha-Chaudhuri P., Asher C.R., Brennan J.M., Gammie J.S. Outcomes and prosthesis choice for active aortic valve infective endocarditis: analysis of the Society of Thoracic Surgeons Adult Cardiac Surgery Database. Ann Thorac Surg. 2014;98(3):806-814. PMID: 25085561. https://doi. org/10.1016/j.athoracsur.2014.05.010
- Kirklin J.K. Challenging homografts as the holy grail for aortic valve endocarditis. J Thorac Cardiovasc Surg. 2016;151 (5):1230-1231. PMID: 26778216. https://doi. org/10.1016/j.jtcvs.2015.12.009
- Lopes S., Calvinho P., de Oliveira F., Antunes M. Allograft aortic root replacement in complex prosthetic endocarditis. Eur J Cardiothorac Surg. 2007;32(1):126-130; discussion 131-132. PMID: 17408962. https://doi.org/10.1016/i. ejcts.2007.01.076
- Musci M., Weng Y., Hubler M., Amiri A., Pasic M., Kosky S., Stein J., Siniawski H., Hetzer R. Homograft aortic root replacement in native or prosthetic active infective endocarditis: twenty-year single-center experience. J Thorac Cardiovasc Surg. 2010;139(3):665-673. PMID: 19767017. https://doi.org/10.1016Xi.jtcvs.2009.07.026
- Klieverik L.M., Yacoub M.H., Edwards S., Bekkers J.A., Roos-Hesselink J.W., Kappetein A.P., Takkenberg J.J., Bogers A.J. Surgical treatment of active native aortic valve endocarditis with allografts and mechanical prostheses. Ann Thorac Surg. 2009;88(6): 1814-1821. PMID: 19932241. https://doi. org/10.1016/i.athoracsur.2009.08.019
- David T.E. Aortic valve repair for active infective endocarditis. Eur J Cardiothorac Surg. 2012;42(1):127-128. PMID: 22345288. https://doi.org/10.1093/eicts/ezr283
- Avierinos J.-F., Thuny F., Chalvignac V., Giorgi R., Tafanelli L., Casalta J.-P., Raoult D., Mesana T., Collart F., Metras D., Habib G., Riberi A. Surgical treatment of active aortic endocarditis: homografts are not the cornerstone of outcome. Ann Thorac Surg. 2007;84(6):1935-1942. PMID: 18036910. https://doi. org/10.1016/i.athoracsur.2007.06.050
- Nappi F., Spadaccio C., Acar C. Use of allogeneic tissue to treat infective valvular disease: Has everything been said? J Thorac Cardiovasc Surg. 2017;153(4):824-828. PMID: 27866779. https://doi.org/10.1016/Utcvs.2016.09.071
- Pomar J.L., Mestres C.A. Tricuspid valve replacement using a mitral homograft. Surgical technique and initial results. J Heart Valve Dis. 1993;2(2):125-128. PMID: 8261148.
- Luciani G.B., de Manna N.D., Segreto A., Lanzoni L., Faggian G. Scalloped freehand pulmonary homograft for prosthetic tricuspid valve replacement. Ann Thorac Surg. 2021 ;112(1):e61-e64. PMID: 33662315. https://doi. org/10.1016/i.athoracsur.2020.12.089
- Acar C., Tolan M., Berrebi A., Gaer J., Gouezo R., Marchix T., Gerota J., Chauvaud S., Fabiani J.N., Deloche A., Carpentier A. Homograft replacement of the mitral valve. Graft selection, technique of implantation, and results in forty-three patients. J Thorac Cardiovasc Surg. 1996;111 (2):367-378; discussion 378-380. PMID: 8583810. https://doi.org/10.1016/s0022-5223(96)70446-4
- Shrestha B.M.S., Fukushima S., Vrtik M., Chong I.H., Sparks L., Jalali H., Pohlner P.G. Partial replacement of tricuspid valve using cryopreserved homograft. Ann Thorac Surg. 2010;89(4):1187-1194. PMID: 20338330. https://doi. org/10.1016/i.athoracsur.2009.12.047
- Horke A., Tudorache I., Laufer G., Andreas M., Pomar J.L., Pereda D., Quintana E., Sitges M., Meyns B., Rega F., Hazekamp M., Hübler M., Schmiady M., Pepper J., Rosendahl U., Lichtenberg A., Akhyari P., Jashari R., Boethig D., Bobylev D., Avsar M., Cebotari S., Haverich A., Sarikouch S. Early results from a prospective, single-arm European trial on decellularized allografts for aortic valve replacement: the ARISE study and ARISE Registry data. Eur J Cardiothorac Surg. 2020;58(5):1045-1053. PMID: 32386409; PMCID: PMC7577293. https://doi.org/10.1093/eicts/ezaa100
- Olivito S., Lalande S., Nappi F., Hammoudi N., D'Alessandro C., Fouret P., Acar C. Structural deterioration of the cryopreserved mitral homograft valve. J Thorac Cardiovasc Surg. 2012;144(2):313-320.e1. PMID: 21855094. https://doi. org/10.1016/i.itcvs.2011.06.041
- McElhinney D.B., Aboulhosn J.A., Dvir D., Whisenant B., Zhang Y., Eicken A., Ribichini F., Tzifa A., Hainstock M.R., Martin M.H., Kornowski R., Schubert S., Latib A., Thomson J.D.R., Torres A.J., Meadows J., Delaney J.W., Guerrero M.E., Salizzoni S., El-Said H., Finkelstein A., George I., Gewillig M., Alvarez-Fuente M., Lamers L., Cheema A.N., Kreutzer J.N., Rudolph T., Hildick-Smith D., Cabalka A.K.; VIVID Registry. Mid-term valve-related outcomes after transcatheter tricuspid valve-in-valve or valve-in-ring replacement. J Am Coll Cardiol. 2019;73(2):148-157. PMID: 30654886. https://doi.org/10.1016/Uacc.2018.10.051
- Fam N.P., Braun D., von Bardeleben R.S., Nabauer M., Ruf T., Connelly K.A., Ho E., Thiele H., Lurz P., Weber M., Nickenig G., Narang A., Davidson C.J., Hausleiter J. Compassionate use of the PASCAL transcatheter valve repair system for severe tricuspid regurgitation: a multicenter, observational, first-in-human experience. JACC Cardiovasc Interv. 2019;12(24):2488-2495. PMID: 31857018. https://doi.Org/10.1016/i.icin.2019.09.046
- Lurz P., Stephan von Bardeleben R., Weber M., Sitges M., Sorajja P., Hausleiter J., Denti P., Trochu J.-N., Nabauer M., Tang G.H.L., Biaggi P., Ying S.-W., Trusty P.M., Dahou A., Hahn R.T., Nickenig G.; TRILUMINATE Investigators. Transcatheter edge-to-edge repair for treatment of tricuspid regurgitation. J Am Coll Cardiol. 2021;77(3):229-239. PMID: 33478646. https://doi.org/10.1016/uacc.2020.11.038
- Page M.J., McKenzie J.E., Bossuyt P.M., Boutron I., Hoffmann T.C., Mulrow C.D., Shamseer L., Tetzlaff J.M., Akl E.A., Brennan S.E., Chou R., Glanville J., Grimshaw J.M., Hröbjartsson A., Lalu M.M., Li T., Loder E.W., Mayo-Wilson E., McDonald S., McGuinness L.A., Stewart L.A., Thomas J., Tricco A.C., Welch V.A., Whiting P., Moher D. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ. 2021;372:n71. PMID: 33782057; PMCID: PMC8005924. https:// doi.org/10.1136/bmi.n71
- McKay R., Sono J., Arnold R.M. Tricuspid valve replacement using an unstented pulmonary homograft. Ann Thorac Surg. 1988;46(1):58-62. PMID: 3382288. https://doi.org/10.1016/ s0003-4975(10)65853-5
- di Summa M., Donegani E., Zattera G.F., Pansini S., Morea M. Successful orthotopic transplantation of a fresh tricuspid valve homograft in a human. Ann Thorac Surg. 1993;56(6):1407-1408. PMID: 8267452. https://doi.org/10.1016/0003-4975(93)90698-h
- Campelos P., Encalada J.F., Ramirez J., Pomar J.L., Mestres C.-A. An old mitral homograft in the tricuspid position. J Heart Valve Dis. 2013;22(5):732-734. PMID: 24383389.
- Kumar N., Gallo R., al-Halees Z., al-Fadley F., Duran C.M. Unstented semilunar homograft replacement of tricuspid valve in Ebstein's malformation. Ann Thorac Surg. 1995;59(2):320-322. PMID: 7847943. https://doi. org/10.1016/0003-4975(94)00803-f
- Ramsheyi A., D'Attellis N., Le Lostec Z., Fegueux S., Acar C. Partial mitral homograft for tricuspid valve repair. Ann Thorac Surg. 1997;64(5): 1486-1488. PMID: 9386736. https://doi. org/10.1016/S0003-4975(97)00944-2
- Katsumata T., Westaby S. Mitral homograft replacement of the tricuspid valve for endocarditis. Ann Thorac Surg. 1997;63(5):1480-1482. PMID: 9146356. https://doi. org/10.1016/s0003-4975(97)00255-5
- Prat A., Fabre O.H., Vincentelli A., Doisy V., Shaaban G. Ross operation and mitral homograft for aortic and tricuspid valve endocarditis. Ann Thorac Surg. 1998;65(5):1450-1452. PMID: 9594888. https://doi.org/10.1016/s0003-4975(98)00100-3
- Miyagishima R.T., Brumwell M.L., Eric Jamieson W.R., Munt B.I. Tricuspid valve replacement using a cryopreserved mitral homograft. Surgical technique and initial results. J Heart Valve Dis. 2000;9(6):805-808; discussion 808-809. PMID: 11128789.
- Nozar J.V., Anzibar R., Picarelli D., Tambasco J., Leone R.W. Mitral homograft replacement of tricuspid valve in children. J Thorac Cardiovasc Surg. 2000;120(4):822-823. PMID: 11003774. https://doi.org/10.1067/mtc.2000.108694
- Kumar A.S., Choudhary S.K., Mathur A., Saxena A., Roy R., Chopra P. Homograft mitral valve replacement: five years' results. J Thorac Cardiovasc Surg. 2000;120(3):450-458. PMID: 10962404. https://doi.org/10.1067/mtc.2000.107829
- Doty D.B., Doty J.R., Flores J.H., Millar R.C. Cardiac valve replacement with mitral homograft. Semin Thorac Cardiovasc Surg. 2001;13(4 Suppl 1):35-42. PMID: 11805947.
- Hvass U., Baron F., Fourchy D., Pansard Y. Mitral homografts for total tricuspid valve replacement: comparison of two techniques. J Thorac Cardiovasc Surg. 2001;121(3):592-594. PMID: 11241100. https://doi.org/10.1067/mtc.2001.110678
- Couetil J.-P.A., Argyriadis P.G., Shafy A., Cohen A., Berrebi A.J., Loulmet D.F., Chachques J.-C., Carpentier A.F. Partial replacement of the tricuspid valve by mitral homografts in acute endocarditis. Ann Thorac Surg. 2002;73(6):1808-1812. PMID: 12078773. https://doi.org/10.1016/s0003-4975(02)03574-9
- Gulbins H., Anderson I., Kilian E., Schrepfer S., Uhlig A., Kreuzer E., Reichart B. Five years of experience with mitral valve homografts. Thorac Cardiovasc Surg. 2002;50(4):223-229. PMID: 12165872. https://doi.org/10.1055/s-2002-33094
- Grinda J.M., Zegdi R., Leroux R., Deloche A. Tricuspid bioprosthesis replacement with cryopreserved mitral homograft. Eur J Cardiothorac Surg. 2002;21 (4):763-764. PMID: 11932182. https://doi.org/10.1016/s1010-7940(02)00027-1
- Kalangos A., Sierra J., Beghetti M., Trigo-Trindade P., Vala D., Christenson J. Tricuspid valve replacement with a mitral homograft in children with rheumatic tricuspid valvulopathy. J Thorac Cardiovasc Surg. 2004;127(6):1682-1687. PMID: 15173724. https://doi.org/10.1016/Utcvs.2003.12.030
- Chiu K.-M., Lin T.-Y., Chen J.-S., Li S.-J., Chu S.-H. Tricuspid valve replacement with a cryopreserved pulmonary homograft. J Thorac Cardiovasc Surg. 2005;130(5):e1-e2. PMID: 16256770. https://doi.org/10.1016Ajtcvs.2005.07.022
- Vaidyanathan K., Agarwal R., Johari R., Cherian K.M. Tricuspid valve replacement with a fresh antibiotic preserved tricuspid homograft. Interact Cardiovasc Thorac Surg. 2010;10(6):1061-1062. PMID: 20351018. https://doi.org/10.1510/ icvts.2010.234757
- Kim M.-S., Chang H.W., Lee S.-P., Kang D.K., Kim E.-C., Kim K.-B. Relapsing tricuspid valve endocarditis by multidrug-resistant Pseudomonas aeruginosa in 11 years: tricuspid valve replacement with an aortic valve homograft. J Cardiothorac Surg. 2015;10:82. PMID: 26051245; PMCID: PMC4459454. https://doi.org/10.1186/s13019-015-0287-9
- Ostrovsky Y., Spirydonau S., Shchatsinka M., Shket A. Surgical treatment of infective endocarditis with aortic and tricuspid valve involvement using cryopreserved aortic and mitral valve allografts. Interact Cardiovasc Thorac Surg. 2015;20(5):682-684. PMID: 25697982. https://doi.org/10.1093/icvts/ivv028


