Техногенное загрязнение почв подотвальными водами в районе угледобычи
Автор: Артамонова Валентина Сергеевна, Бортникова Светлана Борисовна, Оплеухин Алексей Александрович
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Биологические науки
Статья в выпуске: 4 (28), 2016 года.
Бесплатный доступ
В представленной работе впервые показано изменение химического состава прибрежных почв по ходу водотока. Доказана роль гидроминералообразования, пресноводных водорослей, мхов, рогоза, ивы в депонировании металлов и неметаллов, что способствует локальному выведению их из воды. Акцентируется внимание на избирательность поглощения химических элементов растениями. Установлено, что несмотря на полиметаллическое загрязнение почв, азотобактер сохраняет повсеместную встречаемость. Такая экологическая стратегия роста популяции азотобактерии в районе добычи антрацита обеспечивает сохранение её участия в пополнении почв биогенным азотом.
Угольные отвалы, подотвальные воды, техногенное загрязнение, почва, растения, азотфиксирующие бактерии
Короткий адрес: https://sciup.org/14992862
IDR: 14992862 | УДК: 631.4
The technogenic pollution of soils by underspoil waters in the area of coal mining
Pollution of dark grey forest soils with underspoil waters in the area of hard coal extraction in territory of Western Siberia is studied. Manmade streams are formed under multiyear bulk and host rocks, are spread in streambeds, affect the environment. For the first time the change in the chemical composition of coastal soils along the watercourse is shown. The role of hydromineral formation, freshwater algae, mosses, cattails, willows in sorption of metals and nonmetals is proved that promotes their local removal from water. At the source, algae act as powerful "aquafilters", in the watercourse and the mouth geo- and phyto-barriers carry out active water treatment. Subalkali conditions promote the formation of mineral barriers. The attention is accented on the selectivity of absorption of chemical elements by plants. The algal biomass showed maximum content of Ni and Zn, in mosses - Sr. In willow leaves high content of Zn, Sr is revealed, but it is less than in the lower plants. Cattail roots accumulate significant amount of Fe, Cu, Mg, Ca, Zn, but especially Ni and Zn, leavesmainly K, Mn, Ge, Br. High accumulation of heavy metals by plants limits their entry in soil, however level of soil pollution with Ni and Zn near the source remains the highest. It is established that, despite the polymetallic pollution of soils, azotobacter retains widespread occurrence. At the stream source the growth rate of a bacterium in soil is minimal. Slowdown of azotobacter growth is observed in the experiment with addition of technogenic water in control soil. In either case intensive production of brown exometalbolites by azotobacter is registered. With distance from the source the growth rate of a bacterium not only reaches control value, but even slightly exceeds it. This environmental strategy of azotobacter population growth in the area of anthracite extraction provides its participation in replenishment of soils by biogenic nitrogen. Adaptive-physiological variability of the azotobacter population at technogenic pollution of soils is caused by the realization of hereditary potentialities. The authors consider that natural population of a bacterium of dark grey forest soil is evolutionally adapted for the presence of high concentrations of metals and notmetals contained in litozeme of anthracite deposits. The information on the growth of azotobacter in coastal soil, as well as on the chemical composition of hydrobiota is extremely important for the assessment of the quality of fertile soils and meadow lands near the coal piles. The obtained material is of great value for solving strategic and tactical problems in complex environmental monitoring of watercourses and soils of natural-anthropogenic landscapes.
Текст научной статьи Техногенное загрязнение почв подотвальными водами в районе угледобычи
Добыча полезных ископаемых неизбежно влечёт за собой нарушение почвенно-растительного покрова и рельефа местности. Присалаирье, расположенное на границе с Салаиро-Кузнецкой горной областью и богатое природными ресурсами, в этом отношении не исключение. Многолетнее освоение месторождения антрацита на его территории (Горловское месторождение, Новосибирская область) обусловило формирование техногенных ландшафтов, в том числе из отвалов вскрышных и вмещающих пород каменноугольных разрезов. Отходы угледобычи складированы на поверхности плодородных почв, что привело к сокращению площади пахотных земель, появлению риска техногенного загрязнения природной среды смежных территорий в ходе водной и ветровой эрозии отвалов, миграции экотоксикантов с подотвальными водами.
Тяжёлые металлы (ТМ) регистрируются в углях разных месторождений [1, 2]. Металлы 1-го и 2-го классов опасности встречаются в антраците разной степени выветренности и в молодых почвах [3]. Однако информация о загрязнении тёмно-серых лесных почв металлами подотвальных ручьёв в районе угледобычи и его влиянии на развитие азотфиксирующей бактерии Azotobacter chroococ-cum Beyerinck нет. Интерес к азотобактеру вызван тем, что он обеспечивает приток биогенного азота растениям и педобиоте, проявляет адаптацию к загрязнению ТМ, входит в состав показателей эколого-гигиенической оценки опасности отходов производства и потребления [4]. Сведения о роли природных гео- и фитобарьеров в выведении металлов из транзита с подотвальными водами, а значит, и снижение загрязнения почв, отсутствуют. Накопление ТМ водными растениями приводится для озёр рудных полей [5]. В зонах открытой разработки полиметаллических месторождений отмечаются факты негативного влияния техногенной воды на фито-и зоопланктонные ценозы [6]. Сведения о поведении азотобактера в техногенно загрязнённой среде обитания малочисленны.
Цель работы – установить влияние подотвальных вод на состояние азотобактера в тёмносерой лесной почве по ходу техногенного ручья и определить роль гидробионтов и вторичного минералообразования в выведении металлов из транзита.
Материал и методы
Объект исследований – тёмно-серая лесная почва, расположенная на территории Горловского месторождения антрацита (Искитимский р-н Новосибирской области) и подверженная техногенному загрязнению водами подотвального ручья, который впадает в р. Бердь. Возраст отвала к моменту отбора проб (лето 2015 г.) составил 30 лет. На расстоянии 50 м от истока техногенного ручья наблюдается гидроминералообразование, которое к моменту биогеохимических наблюдений достигло размеров визуально выделяемой минеральной плат- формы толщиной до 20 см, длиной до 10 м, общей площадью – около 30 м2.
В качестве контроля выбрана незатронутая техногенезом зональная почва этого же типа. Она типична для повышенных элементов рельефа правобережной части Новосибирской области, сформирована на почвообразующих породах, представленных мелкозёмистыми отложениями, причем как карбонатными, так и бескарбонатными. Тёмно-серые лесные почвы встречаются под мелколиственными лесами колочного типа, занимают в Присала-ирье до 30% площади [7].
Сбор фактического материала (почвы, водорослевые разрастания, мхи, корни и листья рогоза, опавшая листва ивы) осуществлялся по ходу техногенного водотока в трех точках: у истока техногенного ручья, около гидроминералообразования, около устья ручья – на участке перехода в болото. Реакция подотвальной воды по ходу водотока равна 6,0 – 6,4 рН.
Определение химического состава почв и растений проводили методом РФА-СИ для твердых проб на станции ВЭПП-3 Института ядерной физики СО РАН. Предварительно почвенные и растительные пробы высушивали при комнатной температуре, затем измельчали до размера менее 0,1 мм. Порция порошка 30 мг спрессовывалась в таблетки диаметром 10 мм при давлении 100 кг/см2 . Измерения проведены при энергии активации 30 keV, обработка эмиссионных спектров – с помощью программы AXIL. Стандартные образцы СГХМ-4, СДО-4и РУС-1 выбраны в качестве образцов сравнения [8]. Чувствительность определения элементов на базе СИ – 0,1 г/т. Содержание валовых и подвижных форм ТМ выявляли традиционными в почвоведении методами.
Встречаемость (обилие) азотобактера в почве выявляли методом обрастания почвенных комочков, который предполагает рост бактерии в условиях, наиболее приближенных естественным. Метод обеспечивает определение азотобактера при низком содержании живых клеток и цист. Предварительно почву просеивали через сито № 2, мелкозём увлажняли дистиллированной водой до «кашицы» и раскладывали мелкими порциями (по 50 штук в 3 чашки Петри, на заранее разлитую в них и затвердевшую безазотистую питательную среду Эшби), затем чашки с содержимым помещали в термостат при t=28°С [9]. Частоту обрастания почвенного мелкозёма бактерией регистрировали визуально через одни сутки [10]. Содержимое чашек фотографировали, изображение переносили в программу «Corel» и на экране монитора оконтуривали границы роста бактерии вокруг каждого комочка мелкозёма, а также границы самого комочка. С помощью заданных функций компьютерной программы определяли площади ореола роста и мелкозёмистого комочка. Полученные результаты обрабатывались с применением компьютерных программ математической статистики и корреляционного анализа (Statistica 6.0).
Результаты и обсуждение
Исследования показали, что тёмно-серая лесная почва, прилегающая к техногенному ручью, на всем его протяжении заселена азотобактером. Встречаемость бактерии 100 %-ная. Рост бактерии ускоренный, о чём свидетельствует присутствие ореола роста азотобактерии вокруг комочков мелкозёмистых частиц (n=150) уже через 24 ч. во всех точках отбора. Это присуще быстрорастущим штаммам. Достоверные значения суммарной площади бактериальной колонии (ореол + мелкозём) в контрольной почве составили 139,9 мм2, в то время как в почве по ходу стока они оказались выше: 145,4 – 174,7 мм2, достигая максимума в почве около устья (табл.1). Площадь самого ореола роста вокруг мел-
В почве, прилегающей к истоку, скорость размножения бактерии была ниже, чем в контроле, но выше, чем в эксперименте. В почвах, наиболее удаленных от истока (около вторичного минералообразования и особенно напротив устья), скорость размножения бактерии превысила исходный контрольный вариант.
Культурально-морфологическое разнообразие колоний азотобактера в исходной почве и почве, испытывающей влияние подотвальных вод, различалось. В контрольной почве колонии бактерии обнаружили типичный вид, во всех других случаях бактерии выделяли в окружающую среду экзопигмент бурого цвета, особенно около истока, регистрируемый уже через сутки. В почве около устья продуцирование пигмента снизилось. В этой связи
Таблица 1
Статистические показатели роста азотобактера в тёмно-серой лесной почве, сут., n=150
Существенное замедление роста бактерии проявилось в почве, искусственно загрязнённой техногенной водой, взятой из истока (10 мл воды на 20 мг почвенного мелкозёма). Площадь ореола роста вокруг мелкозёма в данном случае снизилась до 58%, в то время как по мере перемещения от истока к устью увеличивалась с 63 до 67 % по сравнению с контролем. Диапазон значений площади ореола роста азотобактера вокруг мелкозёма исходно контрольного и опытного вариантов составил 70,1 – 89,6 мм2 соответственно.
Исходя из полученных средних данных площади бактериального ореола и площади почвенного комочка, была рассчитана скорость роста бактерии вокруг 1 мм2 мелкозёма в сутки. Оказалось, что минимальная скорость бактерии наблюдалась в почве, в которую была добавлена вода из истока (рис.1).
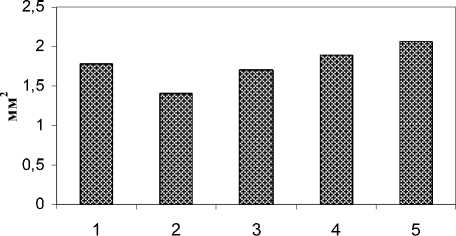
Рис. 1. Скорость роста азотобактера вокруг комочка мелкозёма (1 мм2 /сут. ) тёмно-серой лесной почвы по ходу ручья: 1 – контроль, 2 – контроль с добавлением техногенной воды, 3 – у истока ручья, 4 – у геобарьера, 5 – у устья ручья.
возникло предположение, что по мере снижения загрязнённости воды уменьшается и техногенная нагрузка на почвенную среду обитания азотобакте- ра. Для подтверждения был проведен химический анализ почвы и гидробионтов.
Химический состав почв показал, что в почве у истока ручья диагностируется наибольшее валовое содержание металлов, в том числе тяжёлых. Максимальных значений достигают Ni, Zn, Cd, Co, Cu, Rb, Y. Такие элементы, как Ni, Zn, Sr Zr, As, Mo, Ca (табл. 2) превышают кларковое содержание в земной коре [11], а в почве у истока содержание Ni и Zn (табл. 3) оказались также выше ОДК ТМ [12] и ПДК фитотоксичности грунтов [13]. В прибрежных почвах, расположенных по ходу водотока, их содержание почти в два раза снижается около участка гидроминералообразования. Одновременно наблюдается уменьшение пула Fe, Cr, Mo, Mn, Rb, K.
Таблица 2
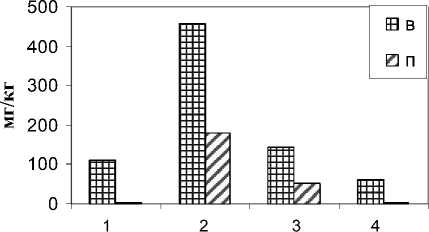
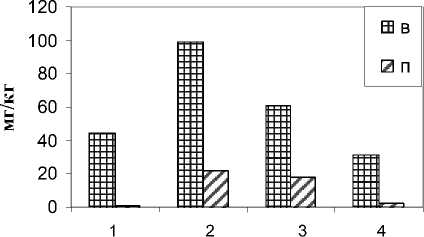
Сравнение валового содержания и подвижных форм Ni, Zn, Cd (рис. 2) в почве по ходу водотока позволило выявить схожую тенденцию снижения количества данных металлов около геохимического барьера. Этому способствуют, по-видимому, карбонаты, которые позитивно влияют на хемосорбцию ТМ [14]. Количество как валовых, так и подвижных форм Са в почве около геобарьера превысило их количество в контрольной почве в 7,8 раза (рис. 3), а около устья – в 2,4 и 2,0 раза соответственно. Учитывая, что эти двухвалентные ТМ обладают большой подвижностью вследствие особенности связываться с низкомолекулярными органическими соединениями [15], снижение их пула имеет большое значение для улучшения экологии почв, снижения их «стресс-индексов», в том числе для азотобактера.
Геохимический состав тёмно-серой лесной почвы по ходу техногенного ручья, мг/кг
|
Элементы |
Исток |
Геобарьер |
Устье |
Кларк земной коры [11] |
|
K,% |
1,45 |
1,18 |
1,32 |
2,50 |
|
Ca,% |
7,89 |
9,43 |
6,76 |
2,96 |
|
Mn,% |
0,099 |
0,030 |
0,204 |
0,1 |
|
Fe,% |
2,32 |
1,79 |
2,64 |
4,65 |
|
V |
45 |
47 |
44 |
90 |
|
Cr |
54 |
53 |
64 |
83 |
|
Ni |
140 |
75 |
57 |
58 |
|
Cu |
25 |
19 |
22 |
47 |
|
Zn |
450 |
140 |
65 |
83 |
|
Pb |
11 |
7,3 |
12 |
16 |
|
Ga |
11 |
9,4 |
11 |
19 |
|
Ge |
1,6 |
0,78 |
1,4 |
1,4 |
|
Rb |
69 |
54 |
61 |
150 |
|
Sr |
720 |
1100 |
260 |
340 |
|
Y |
26 |
20 |
22 |
29 |
|
Zr |
230 |
240 |
180 |
170 |
|
As |
5,8 |
7,1 |
11 |
1,7 |
|
Mo |
1,4 |
1,1 |
1,5 |
1,1 |
Таблица 3
Zn
Ni
Допустимое и фитотоксичное содержание тяжелых металлов и мышьяка в почвах и грунтах, мг/кг
|
Элемент |
ОДК ТМ с учетом фона в почве [12 ] |
Фитотоксичность грунтов, ПДК [13 ] |
|
Cr |
Нет данных |
100 |
|
Ni |
80 |
100 |
|
Zn |
220 |
300 |
|
Pb |
130 |
100 |
|
Cu |
132 |
100 |
|
Cd |
2,0 |
Нет данных |
|
As |
10 |
20 |
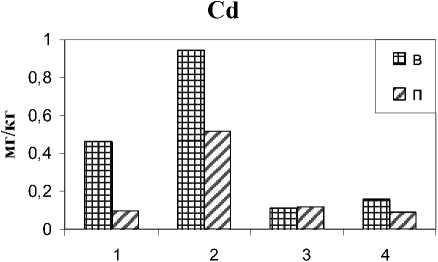
Рис. 2. Содержание металлов в почвах по ходу стока, мг/кг: 1 – контроль; 2 – у истока ручья; 3 – у геобарьера; 4 – у устья ручья; в – валовые формы; п – подвижные формы.
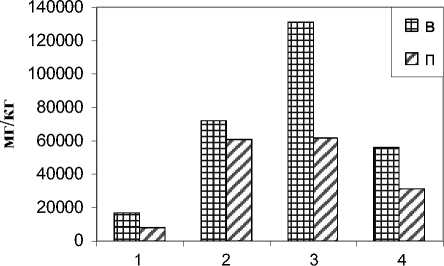
Рис. 3. Содержание кальция в почвах по ходу стока, мг/кг: 1 – контроль; 2 – у истока ручья; 3 – у геобарьера; 4 – у устья ручья; в – валовые формы; п – подвижные формы.
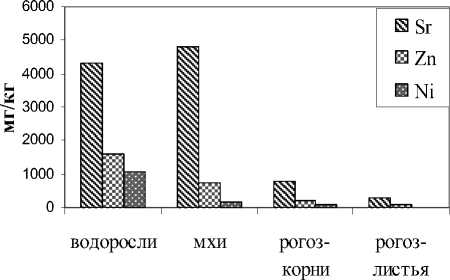
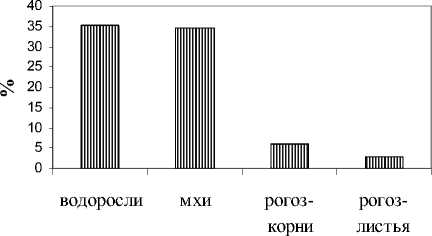
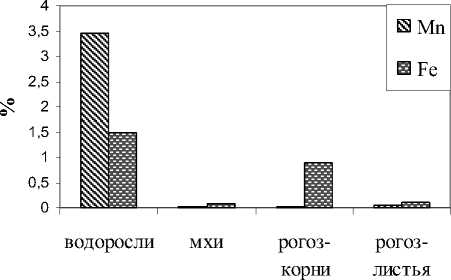
Наряду с позитивной ролью геобарьера в выведении металлов из водотока нами установлено участие растений в аккумуляции тех или иных химических элементов. В биомассе водорослей выявлено максимальное присутствие Ni и Zn, мхов – Sr (рис. 4). Опавшие листья ивы обнаружили высокое содержание Zn, Sr, но оно не превысило таковое в водорослях и мхах. В корнях рогоза выявлены наибольшие количества Fe, Cu, Mo, Ca на фоне высокого содержания Zn, Ni, но уступающего таковому в низших растениях. В листьях наблюдалось присутствие высоких количеств K, Mn, Ge, Br.
Избирательность поглощения химических элементов растениями, как и групповое концентрирование ими микроэлементов, чрезвычайно интересны, но изучены недостаточно. Так, в сухой биомассе водорослей у истока зарегистрировано максимальное содержание Ni – 1000 мг/кг и Zn – 1600
Mo
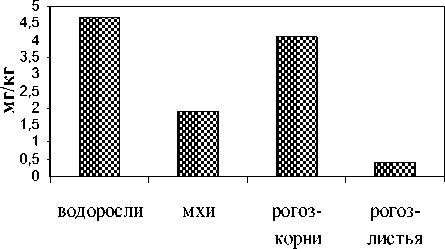
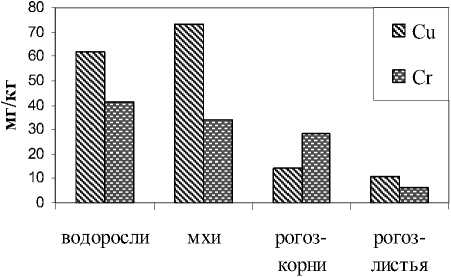
Рис. 4. Максимальная
As
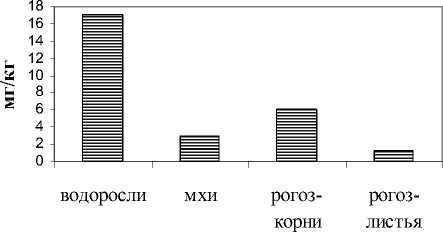
аккумуляция химических элементов растениями.
мг/кг (или 1,0 мг/г и 1,6 мг/г соответственно). В биомассе водорослей из водотока ниже по течению ручья, как и в прибрежных почвах, валовое содержание этих элементов ниже на порядок и более. Преимущественное накопление химических элементов водорослями у истока позволяет рассматривать их как аквафильтры, которые препятствуют миграции ТМ. Механизмы их аккумуляции биотой активно обсуждаются в литературе, но по-прежнему далеки от понимания [16]. Что касается рогоза, то накопленный им состав химических элементов из-за жесткой структуры тканей, их медленного разложения после вегетации, слабого развития гидродинамических процессов на малых глубинах локализован, в основном, в донных отложениях в пределах зарослей. Принимая во внимание то, что этот гидрофит формирует разветвлённую корневую систему, а мощные ветвистые корневища, располагающиеся в поверхностных слоях ила, содержат сахар и крахмал, активизация брожения растительных остатков будет способствовать заилению и частичному снижению рН воды. Это может спровоцировать увеличение растворимости минеральных соединений и подвижности металлов. Ускорение процесса заболачивания, которое наблюдается на участке после вторичного минералообразования, сопровождается вовлечением поливалентных катионов, в частности Cr, Mn, Fe, в восстановительные процессы. Это может привести к ухудшению качества воды (ПДК питьевой воды по железу равна 0,3 мг/л), а также повышению в почве токсичной для растений закиси железа. Фитотоксичность может быть вызвана также присутствием ионов Cr6+ (ПДК р/х=0,02 мг/л), проявляющих канцерогенные и терагенные свойства [17], либо Cr3+ (ПДК р/х=0,07). В нашем случае в самоочищении воды от хрома в истоке участвуют водоросли – хром в них аккумулируется около истока (41,4 мг/кг сухой биомассы). Хотя в почве хром постоянно регистрируется вдоль всего водотока (до 64 мг/г). Медь аккумулируется в наибольших количествах опять же водорослями в истоке (до 62 мг/г биомассы) и мхах на геобарьере (73 мг/г биомассы). Интересно, что присутствующие на геобарьере мхи, аккумулируют также Sr в количестве 2300 – 9500 мг/ кг (2,3 – 9,5 мг/г, соответственно), тем самым выступая биофильным барьером в миграции этого элемента. Листовой опад ивы аккумулирует Zn, Са, Sr в количествах, превышающих таковые в почве, что также позволяет их рассматривать как фитобарьер.
Высокое содержание Sr в водных растениях и почве, расположенной вдоль техногенного водотока, поддерживается высоким содержанием кальция. В биосфере и почвах Sr тесно связан с минералами Са вследствие близости их ионных радиусов, отчего легко захватывается арагонитом, ангидритом, кальцитом и другими минералами. Помимо того, стронций образует и собственные минералы, например целестин, которые встречаются в рассеянном состоянии в осадочных породах, подпочвах и почвах [18]. При выветривании пород он выносится в виде бикарбонатов и других соединений. Карбонаты Sr менее растворимы, чем соответ- ствующие соли Ca. Но растворимость бикарбонатов Sr выше, чем растворимость бикарбоната Ca, отчего стронций должен выноситься водотоком интенсивнее, чем кальций. В то же время Sr может осаждаться в виде карбонатов при потере СО2 из растворов, содержащих бикарбонат. В ходе миграции из водотока в почву стронций может захватываться глинистыми и органическими коллоидами и входить в состав кальциевых минералов. Азотобактер, чрезвычайно нуждающийся в Са, а также продуцирующий слизистые экзометаболиты, способствует частичному биогенному закреплению этого элемента в почве. Благоприятные условия для развития биоты складываются, как известно, при уменьшении в почвах отношения Sr:Са. Следовательно, в пойменных почвах, для которых вообще характерно накопление Sr, в условиях техногенеза необходимо особенно внимательно относиться к соотношению этих элементов.
Заключение
Таким образом, итоги проведенных исследований свидетельствуют о сохранности азотобактера в почвах, испытывающих влияние подотвальных вод. Ростовые показатели азотобактерии отражают ответные реакции на комплексное загрязнение экотоксикантами, выносимыми ручьём из-под насыпного угольного отвала. Важное значение в детоксикации тяжёлых металлов и неметаллов в самом ручье играют водоросли, мхи и высшие растения. В истоке мощными «аквафильтрами» выступают водоросли, в русле и устье очистку воды активно осуществляют гео- и фитобарьеры. Формированию минеральных барьеров способствует слабощелочная обстановка.
Гидробиота обнаруживает особую стратегию устойчивости к ТМ, которая проявляется в избирательности поглощения химических элементов. В биомассе водорослей выявлено максимальное присутствие Ni и Zn, мхах – Sr. В листьях ивы обнаружено высокое содержание Zn, Sr, но оно меньше, чем в низших растениях. Корни рогоза аккумулируют значительное количество Fe, Cu, Mo, Ca, но особенно Zn и Ni, листья – преимущественно K, Mn, Ge, Br. Гипераккумуляция ТМ растениями наряду с вторичным минералообразованием ограничивают приток химических элементов в прибрежную почву. Однако около истока уровень загрязнения почвы Ni и Zn выявляется наибольшим, хотя водоросли уже мобилизуют существенные количества ТМ. Несмотря на полиметаллическое загрязнение почв, азотобактер сохраняет повсеместную встречаемость. Скорость роста бактерии минимальна в почве у истока ручья. Замедление роста азотобактера наблюдается в эксперименте с добавлением техногенной воды в контрольную почву. В том и другом случае регистрируется интенсивное продуцирование азотобактером слизистых экзометаболитов бурого цвета, что следует рассматривать как проявление диссоциирования. По мере удалённости от истока пигментообразование исчезает, скорость роста бактерии не только достигает контрольного значения, но даже несколько превышает его. Такая экологическая стратегия роста популяции азотобактерии в районе добычи антрацита обеспечивает сохранение её участия в пополнении почв биогенным азотом. Адаптивно-физиологическая изменчивость популяции азотобактера при техногенном загрязнении почв обусловлена реализацией наследственных потенций. Авторы статьи считают, что природная популяция бактерии тёмно-серой лесной почвы эволюционно приспособлена к присутствию высоких концентраций металлов и неметаллов, содержащихся в литозёме месторождения антрацита. Информация о росте азотобактера в прибрежной почве, как и о химическом составе гидробиоты чрезвычайно важна для оценки качества плодородных почв и кормовых угодий вблизи угле-отвалов. Полученный материал представляет несомненную ценность для решения стратегических и тактических задач в комплексном экологическом мониторинге водотоков и почв природно-техногенных ландшафтов. Исследования устойчивости живых организмов к комбинированному загрязнению и особенно избирательного аккумулирования ими химических элементов сохраняют свою актуальность и перспективность.
Работа была выполнена в рамках проектов НИР ИПА СО РАН VI.54.1.3 и ИНГГ СО РАН VIII.80.1.4 и при частичной финансовой поддержке РФФИ (грант № 14-05-00293).
Список литературы Техногенное загрязнение почв подотвальными водами в районе угледобычи
- Алексеенко В.А., Алексеенко Л.П. Геохимические барьеры. М.: Логос, 2003. 144 с
- Мазикин В.П. Кузбасс рассчитывает на научную поддержку//Газета «Наука в Сибири». 2012. № 18. С. 3
- Артамонова В.С. Развитие Azotobacter chroococcum на угольных отвалах в Западной Сибири//Природно-техногенные комплексы: современное состояние и перспективы восстановления: Материалы межд. науч. конф. (13 -18 июня 2016 г., Новосибирск)/Институт почвоведения и агрохимии СО РАН. Новосибирск, 2016. С.21-25
- СП 2.1.7.1386-03. Почва, очистка населенных мест. Отходы производства и потребления. Определение класса опасности токсичных отходов производства и потребления. М., 2003. 15 с
- Бортникова С.Б., Гаськова О.Л., Айриянц А.А. Техногенные озёра: формирование, развитие и влияние на окружающую среду. Новосибирск: Изд-во СО РАН, филиал «Гео», 2003. 120 с
- Корнеева Т.В. Геохимия взаимодействия рудничного дренажа с природными водоёмами как естественными гидрохимическими барьерами: автореф. дис. …канд. геолого-минер. наук. Новосибирск, 2010. 16 с
- Хмелёв В.А., Танасиенко А.А. Земельные ресурсы Новосибирской области и пути их рационального использования. Новосибирск: Изд-во СО РАН, 2009. 349 с
- Арнаутов Н.В. Стандартные образцы химического состава природных минеральных веществ. Методические рекомендации. Новосибирск: Изд-во ИГГ СО РАН, 1990. 220 с
- Бабьева И.П., Агре Н.С. Практическое руководство по биологии почв. М.: Изд-во Моск. ун-та, 1971. С. 106
- Сэги Й. Методы почвенной микробиологии. М.: Колос, 1983. 296 с
- Виноградов А. П. Средние содержания химических элементов в главных типах изверженных горных пород земной коры//Геохимия, 1962. № 7. С. 555-571
- ГН 2.1.7.020-94. Ориентировочно допустимые концентрации (ОДК) тяжёлых металлов и мышьяка в почвах с различными физико-техническими свойствами (валовое содержание, мг/кг). (Дополнение №1 к перечню ПДК и ОДК № 6229-91)
- Методические указания по оценке городских почв при разработке градостроительной и архитектурно-строительной документации. М., 1996. С.17
- Минкина Т.М., Мотухзова Г.В., Назаренко О.Г. Состав тяжёлых металлов в почвах. Ростов-на-Дону: Изд-во «Эверест», 2009. 208 с
- Бреховских В.Ф., Казмирук В.Д., Вишневская Г.Н. Биота в процессах массопереноса в водных объектах. М.: Наука, 2008. 315 с
- Титов А.Ф., Таланова В.В., Казнина Н.М., Лайдинен Г.Ф. Устойчивость растений к тяжёлым металлам. Петрозаводск: Карельский научный центр РАН, 2007. 172 с
- Федорова Е.А., Гудков А.А., Гейер Р.В., Плакина Н.Л. Обоснование выбора способа редуцирования ионов поливалентных металлов из водных сред//Фундаментальные исследования. 2011. № 8 (часть 2). С. 410-412
- Ковальский В.В., Андрианова Г.А. Микроэлементы в почвах СССР. М.: Изд-во «Наука», 1970. 180 с


