Технология получения купрата бария-лантана
Автор: Нифталиев С.И., Лыгина Л.В., Кузнецова И.В., Лопатина Е.А.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 3 (81), 2019 года.
Бесплатный доступ
С помощью глицин-нитратной технологии получены наночастицы сложного оксида купрата бария-лантана, изучены его свойства. Согласно данным рентгенофазового анализа синтезированный образец является однофазным. Сложный оксид имеет структуру перовскита с пространственной группой Pmmm (47). Определены параметры кристаллической решетки, рассчитанные из дифрактограммы. Микроструктура полученных композиций определена с помощью сканирующей электронной микроскопии. Образец имеет пористую пенообразную микроструктуру, состоит из агрегатов, имеющих размер 15-98 нм. С помощью термического анализа было обнаружено, что на протяжении нагрева терялась масса образца (4,19%). Наибольшая потеря массы наблюдалась в интервале 318-372 °С, процесс сопровождался эндотермическим эффектом, что соответствовало потере связанной воды, которая сорбировалась в поры и вошла в структуру сложного оксида. Подтверждена возможность перовскитной слоистой структуры интеркалировать воду и ионы в межслоевое пространство, структура которой представляет собой «нанореактор» для дальнейших химических превращений...
Сложные оксиды, купрат бария-лантана, глицин-нитратный метод, дифференциально-сканирующая калориметрия, элементный анализ
Короткий адрес: https://sciup.org/140246428
IDR: 140246428 | УДК: 546.562 | DOI: 10.20914/2310-1202-2019-3-231-235
Technology of production of barium-lanthanum cuprate
With the help of glycine-nitrate technology, nanoparticles of barium-lanthanum cuprate complex oxide were obtained and its properties were studied. According to x-ray phase analysis, the synthesized sample is single-phase.The complex oxide has a perovskite structure with the spatial group Pmmm (47). The parameters of the crystal lattice calculated from the diffractogram are determined. The microstructure of the obtained compositions was determined by scanning electron microscopy. The sample has a porous foam-like microstructure, consists of aggregates having a size of 15-98 nm. Using thermal analysis, it was found that during heating the mass of the sample was lost (4.19%). The greatest loss of mass is observed in the range 318-372 °C, the process is accompanied by an endothermic effect, which corresponds to the loss of bound water, which was sorbed into the pores and entered the structure of the complex oxide. The possibility of the perovskite layered structure to intercalate water and ions into the interlayer space, the structure of which is a "nanoreactor" for further chemical transformations, is confirmed...
Текст краткого сообщения Технология получения купрата бария-лантана
Решение практических задач синтеза нанопорошков сложных оксидов металлов в виде импортозамещающих компонентов автомобильных катализаторов и перспективных керамических материалов с заданными функциональными свойствами остается достаточно перспективным направлением в химической технологии. Купраты редкоземельных элементов могут использоваться в качестве катодных Для цитирования
материалов твердооксидных топливных элементов и обладать сверхпроводимостью [1]. Для сложных оксидов в системе Lа 2 О 3 –ВаО–СuО возможно образование различных анион-дефи-цитных перовскитных структур Lа 1-х Ва х СuО 3-δ (0.2 ≤ x ≤ 0.4) и Lа1-хВахСuО 3-δ (0.43 ≤ x ≤ 0.66). В литературе эти структуры получили цифровые обозначения 415 и 336, что показывает соотношение катионов металлов в этих оксидах [2].
This is an open access article distributed under the terms of the Creative Commons Attribution 4.0 International License
В работе [3] синтезирован и исследован перспективный сверхпроводящий наноматериал LаВа 2 Сu 3 О 7–δ . Авторы отметили необходимость развития различных методов синтеза данной керамики для получения материалов с заданными свойствами и способностью генерировать сильные токи в магнитных полях.
В последнее время активно развивается метод растворного горения, и, в частности, глицин-нитратный синтез [4], который позволяет получать оксидные вещества в форме пористых пенообразных малоагломерирован-ных композиций.
Цель работы – синтез наноструктурного сложного оксида в виде купрата бария-лантана глицин-нитратным методом и исследование его свойств.
Материалы и методы
В качестве исходных реагентов были использованы нитраты лантана, бария – La(NО 3 ) 3 ·9Н 2 O (x. ч.), Ba(NО 3 ) 2 ·6Н 2 O (x. ч.), оксалат меди СuС 2 О 4 (x. ч.) и глицин – С 2 Н 5 NО 2 (x. ч.), которые были взяты в стехиометрическом соотношении согласно реакции: 36Ва(NО ) +18Lа(NО ) +54СuС О +56С Н NО = =18LаВа Сu О +220СО +140Н O+91N
Синтез LаВа2Сu3О7 осуществляли по схеме (рисунок 1).
Приготовление 1М раствора
Preparation of 1M solution
Ba(N↓ o 3 ) 2 La(N↓ o 3 ) 3 CaC↓ 2 O 4
↓
Добавление кристаллического C2H5NO2 Addition of crystalline
C2H5NO2 ↓
Упаривание смеси
Evaporation of the mixture
↓
Самораспространяющийся высоко-температурный синтез
Self-propagating high-temperature synthesis ↓
Прокаливание при 300 °С
Calcination at 300 °С
Рисунок 1. Технологическая схема получения купрата бария-лантана
Figure 1. Technological scheme of obtaining bariumlanthanum cuprate
Взятые в выбранном соотношении исходные реагенты растворялись в дистиллированной воде при интенсивном перемешивании. Растворы солей металлов смешивали между собой
Фазовый состав оксида исследовали методом рентгеновской дифрактометрии в геометрии Брегга–Брентано с использованием CuKα-излу-чения на рентгеновском дифрактометре ARL X’TRA (ThermoScientific, Швейцария). Дифрак-тограммы получали с приповерхностного слоя (~15 мкм). Дискриминация неупруго рассеянного излучения осуществлялась полупроводниковым энергодисперсионным детектором с разрешением 250 эВ и охладителем на элементах Пельтье.
Микроструктуру полученных композиций определяли с помощью сканирующей электронной микроскопии (JSM-6380LV, в режиме вторичных электронов).
Термический анализ проводили на приборе синхронного термического анализа STA 449 F3, Jupter NETZSCH в алюминиевых тиглях. Образец нагревали до 450 °С в атмосфере аргона (скорость нагревания 10 К/мин).
Результаты и обсуждение
Сложный оксид купрата бария-лантана, полученный глицин-нитратным методом, исследовали методом рентгенофазового анализа, который позволяет идентифицировать фазовый состав образца и установить его чистоту (базы данных Power Diffraction File). Согласно данным рентгенофазового анализа синтезированный LаВа 2 Сu 3 О 7 является однофазным и не содержит примесных фаз (рисунок 2).
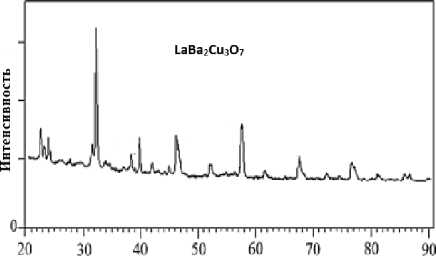
26, град.
Рисунок 2. Результаты рентгенофазового анализа
Figure 2. X-ray phase analysis results
Сложный оксид имеет структуру перовскита с пространственной группой Pmmm (47). Параметры кристаллической решетки, рассчитанные из дифрактограммы, представлены в таблице 1.
Таблица 1.
Структурные параметры соединения LаВа 2 Сu 3 О 7
Table 1.
The structural parameters
|
Соединение |
Структурные параметры, Å (база данных) structural parameters |
Структурные параметры, Å (синтезированное соединение) structural parameters |
|
LаВа 2 Сu 3 О 7 |
a = 3,925; b = 3,934; c = 11,707 |
a = 3,925; b = 3,934; c = 14,503 |
Расчеты параметров синтезированного образца показали увеличение параметра с с 11,707 до 14,503 Å, параметры a и b при этом не изменились. Как правило, это является признаком увеличения межслоевого расстояния, что обычно происходит при интеркалировании воды или других молекул.
На рисунке 3 показаны продукты глициннитратного синтеза. Образец имеет пористую пенообразную микроструктуру, состоит из агрегатов, имеющих размер 15–98 нм. В составе сложного оксида по данным элементного анализа (рисунок 4) присутствуют La, Ba, Cu, O. Углерод, часто присутствующий на поверхности вещества, полученного глицин-нитратным методом, не обнаружен.

ЮОмкт 1 Электронное изображение 1
Рисунок 3. Анализируемый участок в контрасте рентгеновского излучения
Figure 3. Analyzed area in x-ray contrast
Помимо основного процесса – формирования сложного оксида, по данным [4, 6] в ходе глицин-нитратного синтеза протекают физикохимические процессы, связанные с взаимодействием газообразных и твердофазных продуктов горения. Например, авторами [6] методом ИК-спектрометрии в составе конечного продукта глицин-нитратного синтеза феррата гадолиния были обнаружены: сорбированная вода, углекислый газ, угарный газ, непрореагировавшие нитрат-группы.
При исследовании нашего синтезированного образца методом сканирующей калориметрии и термогравиметрии (рисунок 5) было обнаружено, что на протяжении нагрева в интервале 25–450 °С терялась масса образца (общая потеря массы 4,19%). Наибольшая потеря массы наблюдалась в интервале 318–372 °С, это сопровождалась эндотермическим эффектом, возможно, этот эффект соответствует потере связанной воды, которая образовалась в результате реакции (1), сорбировалась в поры и вошла в структуру сложного оксида LаВа 2 Сu 3 О 7 nН 2 O.
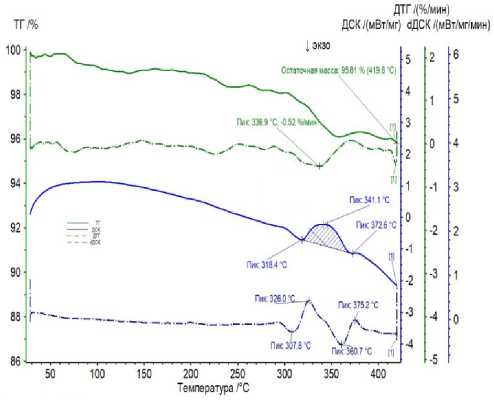
Рисунок 5. Термограмма синтезированного образца LаВа 2 Сu 3 О 7
Figure 5. Thermogram of the synthesized sample LаВа 2 Сu 3 О 7
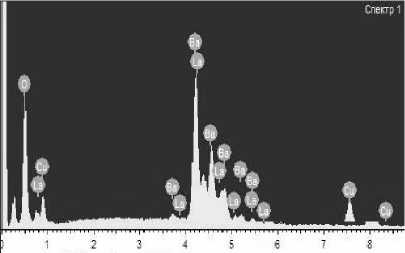
Рисунок 4. Спектр характеристического рентгеновского излучения синтезируемого образца
Figure 4. Spectrum of characteristic x-ray radiation of the synthesized sample
Свободная влага из пор соединения обычно выделяется до 100 °С. Температурный интервал потери массы 318–372 °С говорит о выделении связанной влаги. Возможности перовскитной слоистой структуры интеркалиро-вать воду и ионы в межслоевое пространство обсуждаются в литературе в последнее время [7]. Процесс интеркаляции не приводит к значимым структурным изменениям и характеризуется только увеличением линейных размеров в направлении, перпендикулярном к плоскости слоев, расширение слоев дает возможность протеканию процессов ионного обмена и внедрению других атомов в межслоевое пространство, что, несомненно, меняет функциональные свойства материалов. Структура межслоевого пространства в данном случае представляет собой «нанореактор» для дальнейших химических превращений. Рассчитанная из данных ТГ степень замещения равняется 100%, количество интерка-лированной воды – 1,04 моль. Формулу фазы, полученной при интеркаляции воды, можно записать LаВа2Сu3О7·1,04 Н2O. Процесс интеркаляции воды в межслоевое пространство сложного оксида выражается следующим уравнением:
LаВа Сu О +1,04Н O → LаВа Сu О ⋅ 1,04Н O.
При нагревании реакция протекает в обратном направлении. Энтальпия деинтеркаляции соответствует 2,052 кДж/моль, это значение коррелирует со значениями энтальпий деинтерколяции для перовскитных структур (1,5–17,0 кДж/моль) [7].
Заключение
С использованием глицин-нитратной технологии синтезирован сложный оксид, купрат бария-лантана. Составлены технологическая схема и уравнения реакции получения сложного оксида купрата лантана бария.
Согласно данным рентгенофазового анализа синтезированный образец купрата лантана бария является однофазным и не содержит примесных фаз. Сложный оксид имеет структуру перовскита с пространственной группой Pmmm (47). Рассчитаны параметры кристаллической решетки. Повышенное значение параметра с подтвердило интеркаляцию воды в пространство между слоями. Микроструктура полученных композиций определена с помощью сканирующей электронной микроскопии. Образец имеет пористую пенообразную микроструктуру, состоит из агрегатов, имеющих размер 15–98 нм. Потеря массы при нагревании синтезированного образца 4,19%. Наибольшая потеря массы сопровождается эндотермическим эффектом, что соответствует потере связанной воды, которая вошла в пространство между слоями сложного оксида. Определена формула фазы, полученной при интеркаляции воды: LаВа 2 Сu 3 О 7 ·1,04Н 2 O, рассчитана энтальпия процесса 2,052 кДж/моль. Подтверждена возможность перовскитной слоистой структуры интеркалировать воду в межслоевое пространство.
Список литературы Технология получения купрата бария-лантана
- Gao Z., Mogni L.V., Miller E.C., Railsback J.G. et al. Perspective on low-temperature solid oxide fuel cells // Energy Environ. Sci. 2016. V. 9. P. 1602-1644. DOI: 10.1039/C5EE03858H
- Lindemer T.B., Specht E.D., MacDougall C.S., Taylor G.M. et al. Nonstoichiometry and decompo-sition of La1+zBa2zCu3Oy and La4BaCu5O13w // Phys. C.: Superconductivity. 1993. V. 216. P. 99-110. DOI: 10.1016/0921-4534(93)90639-8
- Yip T.W.S., Cussen E.J. Ion Exchange and Structural Aging in the Layered Perovskite Phases // Inorg. Chem. 2013. V. 52. P. 6985-6993.
- Rivera A.M.M., Cuaspud J.A.G., V?argas C.A.P., Ramirez M.H.B. Synthesis and Characterization of LaBa2Cu3O7-? System by Combustion Technique // Journal of Superconductivity and Novel Magnetism. 2016. V. 29. P. 1163-1171. DOI: 10.1007/s10948-015-3311-3
- Ларин В.К., Кондаков В.М. Глицин-нитратный способ получения ультрадисперсных (нано-) порошков оксидов металлов и перспективные направления их применения // Известия вузов. Цветная металлургия. 2003. № 8. С. 59-64.
- Гимазтдинова М., Тугова Е.А., Томкович М.В., Попков В.И. Получение нанокристаллов GdFeO3 методом глицин-нитратного горения // Конденсированные среды и межфазные границы. 2016. Т. 18. № 3. С. 422-431.
- Silyukov O., Chislov M., Burovikhina A., Utkina T. et al. Thermogravimetry study of ion exchange and hydration in layered oxide materials // J. Therm. Anal. Calorim. 2012. V. 110. № 1. P. 187-192.
- Raghvendra P.S. Electrical conductivity of YSZ-SDC composite solid electrolyte synthesized via glycine-nitrate method // Ceramics International. 2017. V. 43. № 15. P. 11692-11698.
- Komova O.V., Simagina V.I., Mukha S.A., Netskina O.V. et al. A modified glycine-nitrate combustion method for one-step synthesis of LaFeO3 // Advanced Powder Technology. 2016. V. 27. № 2. P. 496-503.
- Martinson K.D., Kondrashkova I.S., Popkov V.I. Synthesis of EuFeO3 nanocrystals by glycine-nitrate combustion method // Russian Journal of Applied Chemistry. 2017. V. 90. № 8. P. 1214-1218.


