Термодинамика процессов взаимодействия иттрия, кальция, магния и алюминия с кислородом в жидкой стали
Автор: Михайлов Геннадий Георгиевич, Макровец Лариса Александровна, Смирнов Леонид Андреевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 2 т.16, 2016 года.
Бесплатный доступ
Иттрий находится в одной группе с лантаном и по своим химическим свойствам близок к лантану, поэтому иттрий относят к редким землям. Иттрий при введении в глубокораскисленный металл измельчает первичное литое зерно, уменьшает зону дентдритообразования, очищает границы зерна от интерметаллидов цветных металлов, измельчает размеры неметаллических включений, повышает жаростойкость и жаропрочность сталей специального назначения. Оптимальная присадка иттрия в металле не превышает 0,3-0,5 %. Комплексное взаимодействие иттрия с кислородом в присутствии в металле остаточных концентраций алюминия, кальция и магния совершенно не изучено. Выполнено термодинамическое моделирование процессов раскисления стали иттрием в присутствии малых концентраций алюминия, кальция или магния. Построены поверхности растворимости компонентов в жидкой стали (ПРКМ) для систем Fe-Y-Al-O-C, Fe-Y-Ca-O-C, Fe-Y-Mg-O-C. Для проведения расчетов определены возможные фазовые равновесия, проведено взаимосогласование зависимостей констант равновесия от температуры, определены энергетические параметры теории субрегулярных ионных растворов применительно к оксидным системам. Из вида ПРКМ следует, что в присутствии кальция и алюминия в стали раскисление иттрием будет проходить как комплексное. В продуктах раскисления будут появляться сложные по фазовому составу оксидные соединения на базе CaO, Al2O3 и Y2O3. В случае раскисления стали иттрием и магнием процесс будет носить альтернативный характер: либо раскислитель иттрий, либо магний.
Термодинамика, фазовые равновесия, диаграммы состояния, иттрий, алюминий, кальций, магний
Короткий адрес: https://sciup.org/147157020
IDR: 147157020 | УДК: 69.017 | DOI: 10.14529/met160201
Thermodynamics of yttrium, calcium, magnesium and aluminium interaction with oxygen in liquid steel
Yttrium belongs to the same group as lanthanum, and its chemical properties are close to those of the latter. Therefore, yttrium is referred to as a rare earth metal. When added to a heavily deoxidized metal, yttrium refines a primary cast grain, reduces the area of treeing, purifies grain boundaries of non-ferrous inter-metallic compounds, reduces the size of non-metallic inclusions, and enhances heat resistance and high temperature strength of special steels. Optimal yttrium additive in the metal does not exceed 0.3 to 0.5 wt. %. Complex interaction of yttrium with oxygen in the presence of residual concentrations of aluminum, calcium and magnesium in the metal was not studied at all. Thermodynamic modelling of steel deoxidation using yttrium in the presence of low concentrations of aluminum, calcium or magnesium is developed. The surfaces of component solubility in liquid steel are created for Fe-Y-Al-O-C, Fe-Y-Ca-O-C, and Fe-Y-Mg-O-C systems. To make calculations related to oxide systems, all possible phase equilibria are established, coordination of equilibrium constants dependency on temperature is carried out, and energy parameters of the subregular ionic solution theory are specified. The surfaces of component solubility show that deoxidation by yttrium is a complex process due to the presence of calcium and aluminum in steel. Deoxidation products will contain complex phase compositions of oxides based on CaO, Al2O3, and Y2O3. In case of steel deoxidation by yttrium and magnesium, the process is performed alternately. Either yttrium or magnesium acts as a deoxidizer.
Текст научной статьи Термодинамика процессов взаимодействия иттрия, кальция, магния и алюминия с кислородом в жидкой стали
Качество металла до сих пор в значительной мере определяется неметаллическими включениями, их фазовым и химическим составом, распределением по объему металла, размерами. Избежать образования неметаллических включений практически невозможно при открытой плавке стали, из-за взаимодействия металла с печной и цеховой атмосферой, технологическим шлаком, футеровкой металловмещающих агрегатов, а так же кристаллизационных явлений. Как правило, при разработке технологии новой марки стали, особое внимание обращается на организацию финишного этапа раскисления и модифицирования стали. Все большее применение в финишном этапе рафинирования стали находят редкоземельные элементы, к которым относится и иттрий, находящийся в одной группе с лантаном, и по химическим свойствам близок к свойствам лантаноидов, но имеет меньшую атомную массу (88,9) и очень высокую температуру кипения (3630 °С) [1]. Получают ит- трий в основном электролизом хлоридных расплавов. В черной металлургии иттрий используется либо в виде сплава с кремнием, либо в виде цериевого мишметалла. В соединениях с металлоидами проявляется валентность III [2, 3]. Сплав силико-иттрий используют в незначительных количествах. Чаще иттрий используется в мишметалле одновременно с церием, лантаном и другими РЗМ [4]. Иттрий, наряду с рафинирующим действием на металл, измельчает и глобулизирует неметаллические включения, повышает жаропрочность и жаростойкость сталей и поэтому применяется при выплавке сталей специального назначения [3]. Украинские исследователи Л.И. Тарасюк и Е.А. Казачков установили, что при введении иттрия в сталь 09Г2С снижаются показатели анизотропии и повышаются пластические характеристики металла при низких температурах [5].
Помимо вводимого иттрия в стали всегда есть некоторое остаточное количество высокоактивных элементов, таких как алюминий, кальций, магний, которые попадают в металл в незначительных количествах, и благодаря восстановительному действию глубокораскисленного металла на технологический шлак, а так же на ковшевую и трактовую футеровку [6, 7]. Для получения достоверных данных об участии введенного иттрия в рафинировании металла необходимо установить влияние участие каждого из этих компонентов на процесс рафинирования стали [8].
Наибольшую информацию о возможных реакциях рафинирования стали иттрием совместно с другими активными элементами можно получить в результате построения диаграмм растворимости взаимодействующих компонентов в жидком металле. Такую диаграмму состояний, на которой указаны составы жидкого металла, равновесного с неметаллической фазой, состав которой задан на сопряженной с областью существования жидкого металла оксидной диаграмме состояния, удобно называть поверхностью растворимости компонентов в металле (ПРКМ). В настоящей работе рассмотрены ПРКМ систем Fe–Y–Al–O–C, Fe–Y–Ca–O–C, Fe–Y–Mg–O–C.
При проведении расчетов активности компонентов жидкой оксидной фазы вычислялись с применением теории субрегулярных ионных растворов, построенной в варианте квадратичной зависимости координационного числа катионов от состава оксидного расплава. Подробно этот вариант теории изложен в монографии [9]. Энергетические параметры теории для оксидных расплавов систем
FeO–Al 2 O 3 –Y 2 O 3 , FeO–CaO–Y 2 O 3 , FeO–MgO–Y 2 O 3 [9, 10] приведены в табл. 1. Активности компонентов жидкой металлической фазы устанавливались с помощью удельных параметров взаимодействия. Значения параметров иттрия с компонентами металлических расплавов в литературе практически OCYY отсутствуют, кроме параметров e Y , e Y , e O , e C . Оценка параметра e Y Al по теории регулярных растворов для расплавов системы позволила получить значение e Y Al =0,039, тогда e Y Al = 0,039·27/89 ≈ 0,001, т. е. исчезающее малая величина, тем более что концентрации и иттрия, и алюминия в глубоко раскисленном металле не будут превышать сотые доли процентов. Данные по параметрам взаимодействия [11–14] представлены в табл. 2.
Данные по температурным зависимостям констант равновесия представлены в табл. 3. Значительная часть этих данных заимствована из справочников [15, 16] либо получена путем косвенных расчетов [10].
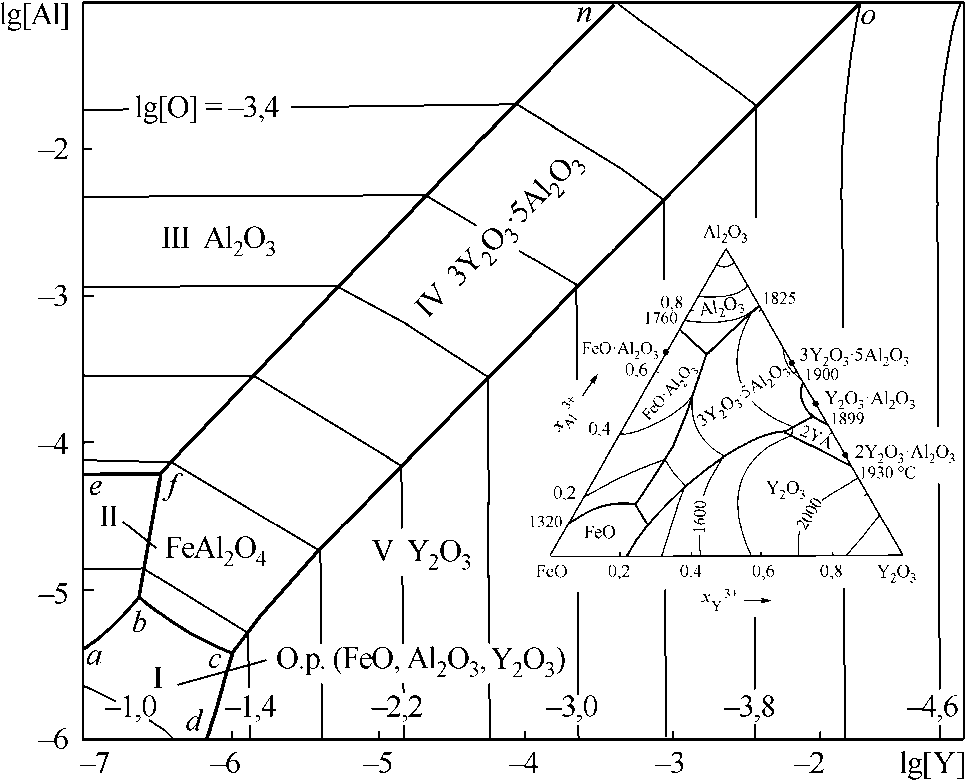
Строение ПРКМ для изучаемых систем приведены на рис. 1–3. На полях ПРКМ указаны составы металла, равновесного с обозначенной оксидной фазой. Так на рис. 1 в области I заданы составы металла, равновесного с оксидным расплавом (FeO, Al 2 O 3 , Y 2 O 3 ) переменного состава, в области II заданы составы металла, равновесного с герцинитом, в области III – с корундом, в области IV – с алюминатом 3Y 2 O 3 ·5Al 2 O 3 , в области V – с Y 2 O 3 . Здесь же указана сопряженная с этим металлом оксидная диаграмма состояний FeO–Al 2 O 3 –Y 2 O 3 .
Таблица 1
Значения параметров теории субрегулярных ионных растворов Q ijkl [9, 10]
|
Система |
Параметры теории Qijkl , кал/моль |
||
|
FeO–Y 2 O 3 |
0 |
0 |
0 |
|
Y 2 O 3 –Al 2 O 3 |
–4186 |
–1835 |
–7105 |
|
Y 2 O 3 –CaO |
–26 845 |
–42 106 |
–21 622 |
|
Y 2 O 3 –MgO |
5515 |
4099 |
2192 |
|
FeO–Y 2 O 3 –Al 2 O 3 |
–50 000 |
20 000 |
–50 000 |
|
FeO–Y 2 O 3 –CaO |
–36 438 |
–54 795 |
–56 469 |
|
FeO–Y 2 O 3 –MgO |
0 |
0 |
0 |
Таблица 2
Удельные параметры взаимодействия, T = 1600 °С для компонентов металлического расплава
|
Элемент i |
Элемент j |
|||||
|
Al |
Y |
Ca |
Mg |
O |
С |
|
|
Al |
0,045 |
– |
–0,0515 |
–0,00998 |
–1,62 |
0,0966 |
|
Y |
– |
0,030 |
– |
– |
–4,41 |
–1,21 |
|
Ca |
–0,0718 |
– |
–0,07 |
–0,1084 |
–3,507 |
–0,324 |
|
Mg |
–0,0089 |
– |
–0,064 |
–0,085 |
–3,008 |
0,14 |
|
O |
–0,96 |
–0,79 |
–1,41 |
–1,98 |
–0,2 |
–0,45 |
|
С |
0,043 |
–0,16 |
–0,34 |
0,07 |
–0,34 |
0,14 |
Таблица 3
Температурные зависимость констант равновесия реакций раскисления стали
|
Реакция |
lg K = – A / T + B |
|
|
A |
B |
|
|
(FeO) = [Fe] + [O] |
6320 |
4,734 |
|
(Y 2 O 3 ) = 2[Y] + 3[O] |
67 028 |
20,19 |
|
(Al 2 O 3 ) = 2[Al] + 3[O] |
58 320 |
18,02 |
|
(MgO) = [Mg] + [O] |
22 457 |
6,54 |
|
(CaO) = [Ca] + [O] |
31 480 |
12,55 |
|
|FeO| = [Fe] + [O] |
8069 |
5,80 |
|
|MgO| = [Mg] + [O] |
26 500 |
7,85 |
|
|CaO| = [Ca] + [O] |
34 103 |
13,46 |
|
|Al 2 O 3 | = 2[Al] + 3[O] |
64 000 |
20,48 |
|
|Y 2 O 3 | = 2[Y] + 3[O] |
71 400 |
21,81 |
|
|FeO·Al 2 O 3 |= [Fe] + 2[Al] + 4[O] |
74 580 |
26,37 |
|
|2Y 2 O 3 ·Al 2 O 3 |= 4[Y] + 2[Al] + 9[O] |
200 210 |
59,882 |
|
|Y 2 O 3 ·Al 2 O 3 |= 2[Y] + 2[Al] + 6[O] |
130 560 |
39,057 |
|
|3Y 2 O 3 ·5Al 2 O 3 |= 6[Y] + 10[Al] + 24[O] |
560 500 |
175,785 |
|
|CaO·2Y 2 O 3 |= [Ca] + 4[Y] + 7[O] |
178 305 |
55,181 |
|
|CaO·Y 2 O 3 |= [Ca] + 2[Y] + 4[O] |
106 769 |
34,066 |
|
|3CaO·Y 2 O 3 |= 3[Ca] + 2[Y] + 6[O] |
173 384 |
58,815 |
|
{CO} = [C] +[O] |
1168 |
–2,07 |
|
{CO 2 } = [C] +2[O] |
9616 |
2,51 |
|
{Ca} = [Ca] |
–1912 |
–2,69 |
|
{Mg} = [Mg] |
–6670 |
–6,48 |
На рис. 1, б в области VI заданы составы кипящего металла. Образование Y2O3·Al2O3, и 2Y2O3·Al2O3 в качестве неметаллических включений возможно при температурах выше 1800 °С.
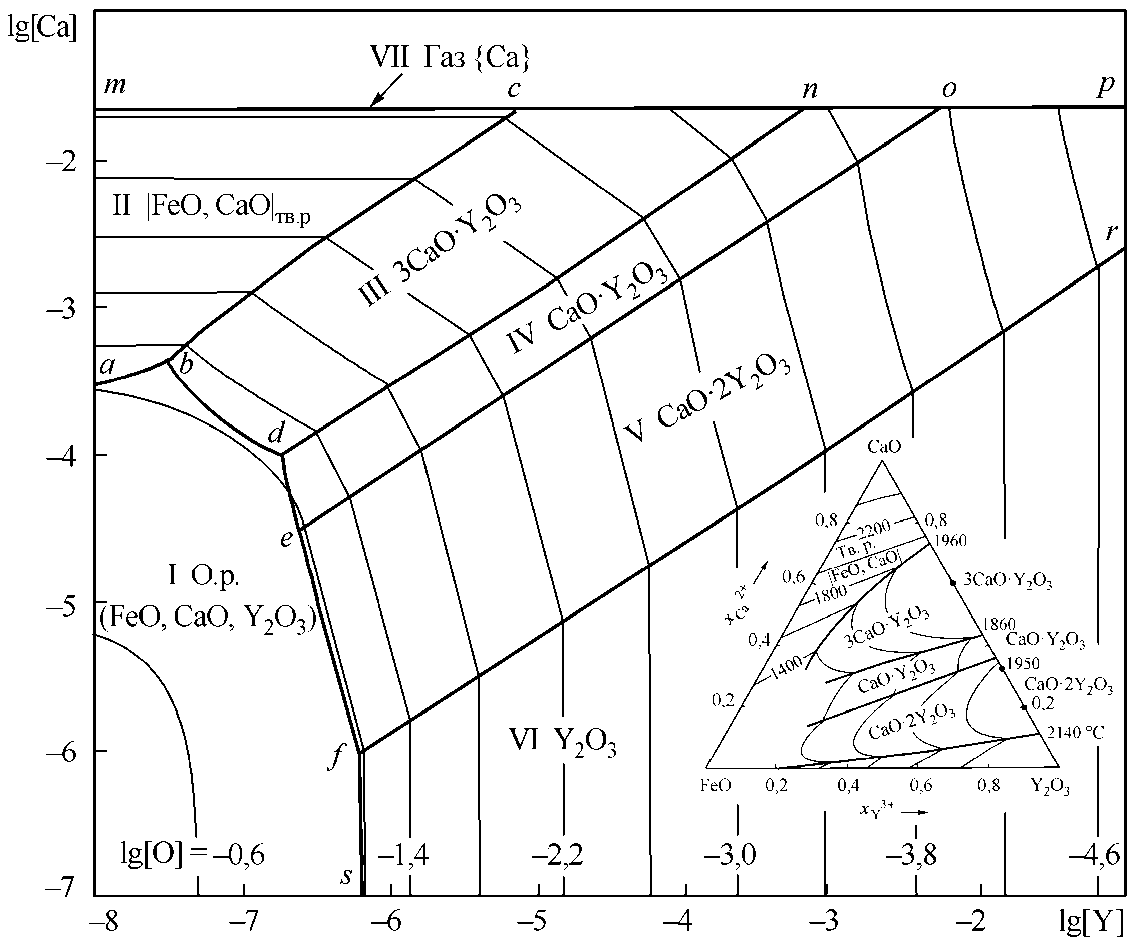
Фазы, образующиеся в жидком металле системы Fe–Y–Ca–O–C в качестве неметаллических включений представлены на рис. 2. На рис. 2, а приведено строение диаграммы FeO–CaO2–Y2O3, сопряженной с областью существования металлических расплавов. Так же на полях представлены составы металла, равновесного с обозначенными фазами. На контрастных линиях заданы составы металла, равновесного с двумя смежными оксидными фазами. Так на линии ab заданы составы металла, равновесного с оксидным расплавом (FeO, CaO, Y2O3) и твердыми растворами FeO в CaO, на линии bd заданы составы металла, равновесного с 3CaO·Y2O3 и с оксидным расплавом. На линии de задан состав металла, равновесного с CaO·Y2O3 и с оксидным расплавом, на линии ef – с CaO·2Y2O3 и с оксидным расплавом, на линии fs – с оксидным расплавом и Y2O3. В точках пересечения трех контрастных линий задан состав металла, равновесного с тремя оксидными фазами. Так, например, в точке f задан состав металла, равновесного с Y2O3, CaO·2Y2O3 и оксидным расплавом. В связи с тем, что кальций имеет высокую упругость пара, при избыточных количествах кальция в условиях закрытой плавки может уста- новиться равновесие с газовой фазой. Линия mcnop есть след от поверхности растворимости кальция в жидком металле, перпендикулярной плоскости рисунка, на которой заданы составы металла, равновесного с парами кальция. На линии mc заданы составы метала, равновесного с твердыми растворами оксидов и паром кальция, на линиях cn, no и op – с паром кальция и 3CaO·Y2O3, CaO·Y2O3 или CaO·2Y2O3 соответственно.
На рис. 2, б видно, что уже при содержании углерода 0,1 мас. % появляется область составов металла, равновесного с газовой фазой {CO, CO2} и примесью паров кальция. Это область IX. Кроме того, вдоль линии tcuhq определены составы металла, равновесного с парами кальция с примесью CO, CO 2 и смежными конденсированными оксидными фазами.
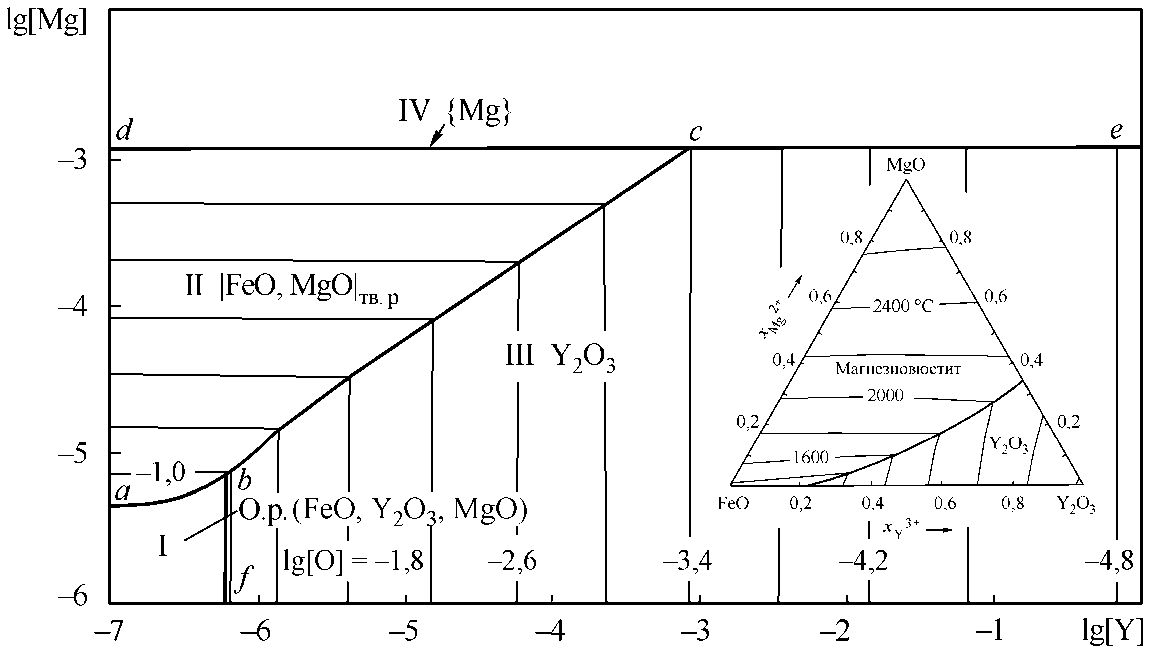
Сведений о наличии двойных или тройных соединений в оксидной системе FeO–MgO–Y2O3 не имеется. ПРКМ систем Fe–Mg–Y–O и Fe–Mg– Y–O–С приведены на рис. 3. Здесь же приведен и проект тройной оксидной диаграммы системы FeO–MgO–Y2O3. Видно, что MgO и FeO образуют непрерывный ряд твердых растворов, и в то же время Y 2 O 3 и FeO – взаимно нерастворимые вещества, и система FeO–Y2O3 где-то вблизи FeO имеет точку эвтектического превращения, как и система MgO–Y 2 O 3 [8]. Тонкими линиями на всех ПРКМ приведены изокислородные сечения.
б)
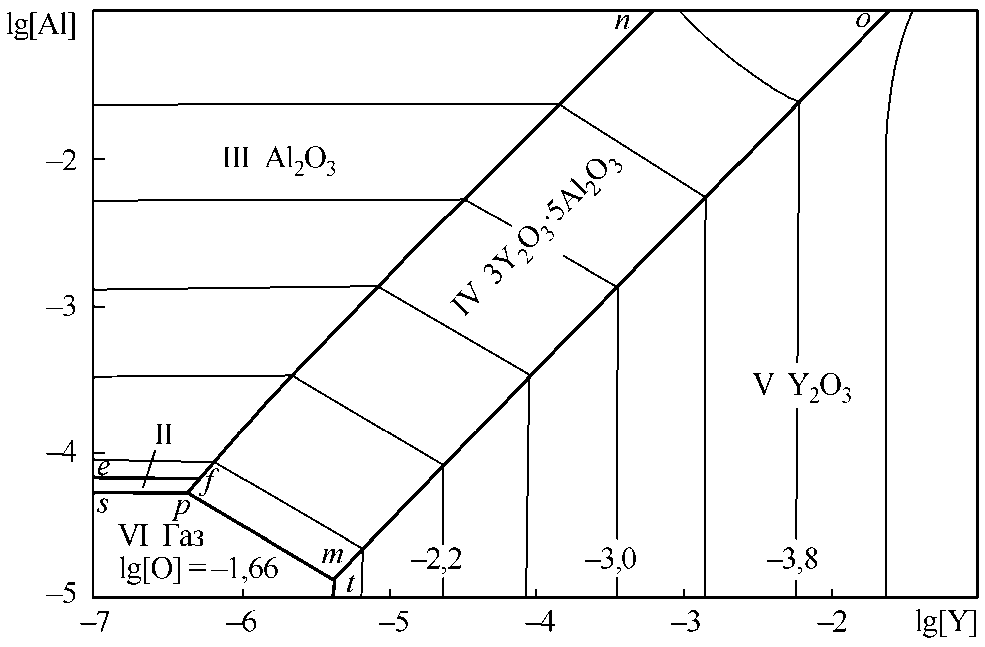
Рис. 1. ПРКМ системы Fe–Al–Y–O–С, Т = 1600 °С, Р общ = 1 атм: а) [C] = 0; б) [C] = 0,1 мас. %
а)
б)
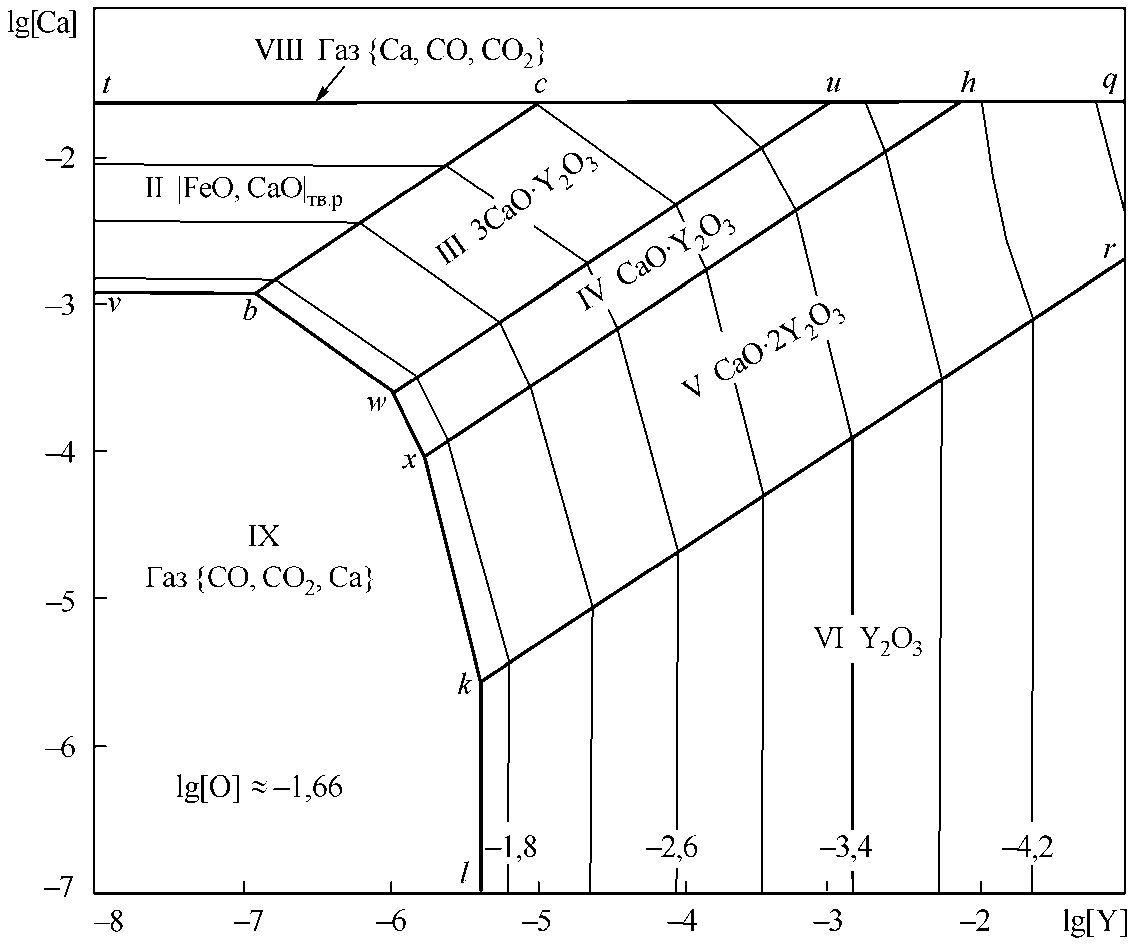
Рис. 2. ПРКМ системы Fe–Ca–Y–O–С, Т = 1600 °С, Р общ = 1 атм: а) [C] = 0; б) [C] = 0,1 мас. %
а)
б)
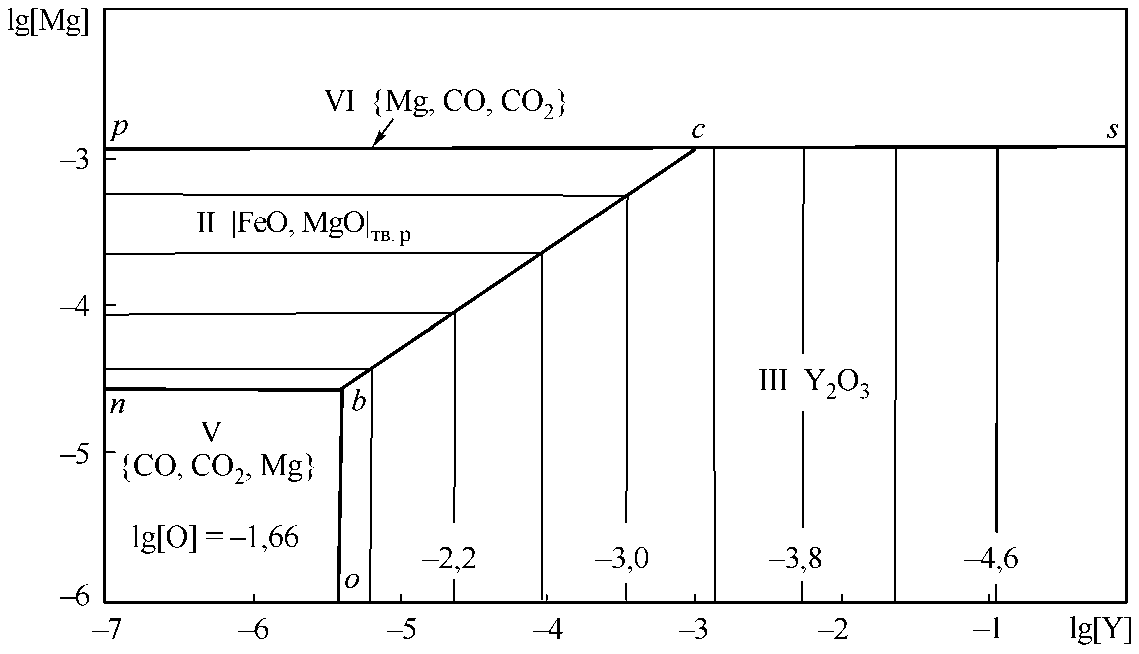
Рис. 3. ПРКМ системы Fe–Mg–Y–O–С, Т = 1600 °С, Р общ = 1 атм: а) [C] = 0; б) [C] = 0,1 мас. %
Из вида ПРКМ следует, что раскислительная способность иттрия в среднем на порядок выше раскислительной способности алюминия и на два порядка выше раскислительной способности кальция. Но, тем не менее, следует отметить, что раскисление алюминием и иттрием будет, скорее всего, комплексным. То же самое можно сказать о раскислении кальцием и иттрием. Большие поля составов металла, равновесных с алюминатами иттрия и соединениями иттрия с кальцием позволяют сделать это заключение.
Из вида ПРКМ Fe–Mg–Y–O–С можно сделать заключение о том, что раскисление иттрием и магнием носит альтернативный характер. Либо будут образовываться в качестве неметаллических включений твердые растворы на основе периклаза, либо оксиды иттрия. Раскислительная способность иттрия и магния практически одинакова.
Заключение
-
1. Впервые рассмотрены на основании термодинамического анализа фазовые равновесия, уста-
- навливающиеся в иттрийсодержащем стальном расплаве, раскисленном малыми добавками алюминия, кальция или магния.
-
2. Результаты термодинамических расчетов оформлены в виде диаграмм растворимости компонентов в металле, на которых приводится состав жидкого металла и указывается равновесная с ним оксидная фаза.
-
3. Из общего вида таких диаграмм раскисления иттрийсодержащего металла алюминием, кальцием или магнием следует ожидать, что раскисление стали алюминием и иттрием, кальцием и иттрием будет комплексным. Т.е. при тысячных долях процента компонентов в стали будут образовываться комплексные неметаллические включения. В случае если раскисление будет проводиться иттрием и магнием – это будет альтернативный процесс.
-
4. В целом раскисление высокоактивными элементами в реальном металле может иметь и более сложную картину, вследствие неравновес-ности процесса на начальных стадиях введения иттрия в жидкий металл.
Работа поддержана грантом РФФИ № 13-08-12167.
Список литературы Термодинамика процессов взаимодействия иттрия, кальция, магния и алюминия с кислородом в жидкой стали
- Химия. Справочное руководство/Пер. с нем. под ред. Ф.Г. Гаврюченкова, М.И. Курочкиной, А.А. Потехина, В.А. Рабиновича. -Л.: Химия, 1975. -576 с.
- Диаграммы состояния двойных металлических систем: справ. Т. 2. Кн. 2/Под ред. Н.П. Лякишева. -М.: Машиностроение, 2000. -448 с.
- Совершенствование литейных жаростойких хромоалюминиевых сталей микролегированием и модифицированием. -http://science-bsea.narod.ru/2009/mashin_2009/jamshinsky_sov.htm.
- Тарасюк, Л.И. Термодинамика раскисления железа иттрием/Л.И. Тарасюк, В.В. Морнева, Е.А. Казачков//Вест. Приазов. гос. техн. ун-та. Сер. «Технические науки». -2011. -№ 2 (23). -С. 33-39.
- Тарасюк, Л.И. Формирование неметаллических включений в сталях, модифицированных иттрием/Л.И. Тарасюк, В.В. Морнева, Е.А. Казачков//Вест. Приазов. гос. техн. ун-та. Сер. «Технические науки». -2011. -№ 2 (23). -С. 27-33.
- Применение редкоземельных металлов в металлургии. -http://www.urm.ru/ru/75-journal124-article64.
- Применение редкоземельных металлов в металлургии. -http://viam.ru/public/files/1988/1988-200121.pdf.
- Голубцов, В.А. Модифицирование стали для отливок/В.А. Голубцов, В.В. Лунев. -Челябинск; Запорожье: ЗНТУ, 2009. -356 с.
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. -М.: Издат. Дом МИСиС, 2009. -519 с.
- Михайлов, Г.Г. Термодинамическое моделирование фазовых равновесий с оксидными системами, содержащими РЗМ. Сообщение 2. Диаграммы состояния оксидных систем с Y2O3/Г.Г. Михайлов, Л.А. Макровец//Вестник ЮУрГУ. Серия «Металлургия». -2014. -Т. 14, № 4. -С. 5-10. DOI: DOI: 10.14529/met150401
- Bůžek, Z. Zakladni termodynamicke udaje o metalurgických reakciah/Z. Buzek//Hutnicke aktua¬lity. -1979. -Vol. 20, no. 1-2. -P. 3-111.
- Bůžek, Z. Vliv přechodných kovú na aktivitu a rozpustnost kysliku v železe při 1600 °C/Z. Buzek, M. Macoszek., J. Szlaver//Hutnicke listy. -1972. -Vol. XXVII, no. 8. -P. 547-557.
- Steelmaking Data Sourcebook. Revised Edition by The Japan Society for the Science. The 19th Committee on Steelmaking. New York et al., Gordon and Breach Science Publishers S.A., 1988. -325 p.
- Gloria, M. Inclusion Precepitation Diagram for the Fe-O-Ca-Al System/M. Gloria, S. Faurling, R. Ramalingam//Metall. Trans. B. -1980. -Vol. 11 (1). -P. 125-130 DOI: 10.1007/BF02657181
- Куликов, И.С. Раскисление металлов/И.С. Куликов -М.: Металлургия, 1975. -504 с.
- Туркдоган, Е.Т. Физическая химия высокотемпературных процессов: пер. с англ. -М.: Металлургия, 1985. -344 с.


