Токсичность йессотоксина в эксперименте in vivo
Автор: Багрянцева О.В., Гмошинский И.В., Евстратова А.Д., Трушина Э.Н., Мустафина О.К., Сото Х.С., Шипелин В.А., Шумакова А.А., Панова А.Д., Хотимченко С.А.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Экспериментальные модели и инструментальные исследования для оценки риска в гигиене и эпидемиологии
Статья в выпуске: 3 (23), 2018 года.
Бесплатный доступ
Йессотоксин (YTX) является полиэфиром. Известно более 90 производных йессотоксина. YTX исключен из группы диарейных токсинов, потому что, в отличие от окадаиковой кислоты, не вызывает диарею. Химическая структура YTX аналогична таковой бреветоксинов и сигаутоксинов, которые оказывают действие на работу кальций-натриевого насоса и трансмембранных ионных каналов. Следовательно, YTX способен оказывать влияние на работу всех органов и систем организма. Известно, что YTX является промотором апоптоза в ткани головного мозга. Среднелетальная доза ЛД50YTX и его аналогов в различных экспериментах, проведенных на мышах, составила от 100 до 500-750 мкг/кг. Безопасный уровень острого воздействия YTX (ARfD) составляет 25 μM/кг массы тела. В настоящее время установлены показатели токсичности для YTX и некоторых его аналогов, определены основные механизмы его действия, роль в качестве промотора апоптоза. Несмотря на растущее число данных о биологических эффектах, оказываемых YTX на теплокровный организм, точный механизм его действия в настоящее время неизвестен...
Йессотоксин, механизмы действия, биомаркеры, токсичность, оценка риска, допустимый уровень
Короткий адрес: https://sciup.org/142215894
IDR: 142215894 | УДК: 616-092.9: | DOI: 10.21668/health.risk/2018.3.12
Toxicity of yessotoxin in experiment in vivo
Yessotoxin (YTX) is a polyether. There are more than 90 known derivatives of yessotoxin. YTX was excluded from diarrhea toxins group as it, unlike okadaic acid, doesn't cause diarrhea. YTX chemical structure is similar to that of brevetoxins and ciguatoxins that influence functioning of calcium-sodium pump and trans-membrane ion channels. So, YTX can exert influence on functioning of all the organs and systems in a body. YTX is known to promote apoptosis in the cerebral tissues. Average lethal dose LD50 for YTX and its analogues varied from 100 µg/kg to 500-750 µg/kg; the figures were obtained in various experiments performed on mice. Safe YTX level for acute impact (acute reference dose) amounts to 25 μM/kg of body weight. Nowadays toxicity parameters for YTX and some of its analogues are determined; its basic action mechanisms and a role it plays in promoting apoptosis are well-known. In spite of more and more data on biological effects produced by YTX on a warm-blooded organism, experts are still unable to describe its action mechanisms precisely...
Текст научной статьи Токсичность йессотоксина в эксперименте in vivo
Йессотоксин (YTX) является полиэфиром, состоящим из 11 смежных эфирных колец, ненасыщенной боковой цепи и двух эфиров сульфата. Известно более 90 производных йессотоксина. Впервые выделен в 1986 г. в Японии из гребешков Patinopecten yessoensis . YTX продуцируется водорослями – динофлагеллятами Protoceratium reticu-latum и Gonyaulax spinifera . YTX исключен из группы диарейных токсинов (окадаиковая кислота и ее аналоги – DSP-токсины), потому что, в отличие от окадаиковой кислоты, не вызывает диареи. Однако YTX и его аналоги часто экстрагируются вместе с диарейными токсинами и дают положительные результаты в биологических тестах, проводимых на наличие диарейного яда моллюсков [1].
Химическая структура YTX аналогична таковой структуре бреветоксинов и сигаутоксинов, которые оказывают действие на работу кальций-натриевого насоса и трансмембранных ионных каналов. Механизм, приводящий к активации фософодиэстеразы с помощью йессотоксина, включает начальное увеличение кальция в цитозоле клетки, доступного для каль-цийзависимой фосфодиэстеразы I типа, с последующим снижением внутриклеточной концентрации циклического аденозинмонофосфата [2, 3].
YTX способствует активности каспаз 3 и 7 в HeLa-клетках. Он снижает порог проницаемости митохондриальных мембран в печени крыс; вызывает нарушение цитоскелета культуры клеток нейронов мозжечка и далее их апоптоз; способствует нарушению межклеточной адгезии, что, в свою очередь, может стать одной из возможных причин развития болезни Альцгеймера [4–7]; влияет на иммунную систему, способствуя повышению количества цитокинов, за счет повышения экспрессии кодирующих их генов [8]. YTX индуцирует митотическую катастрофу и генетические изменения, которые могут представлять интерес для контроля прогрессирования опухолевого процесса [9].
Среднелетальная доза ЛД50 YTX и его аналогов в различных экспериментах, проведенных на мышах, составила от 100 до 500–750 мкг/кг [6]. На наш взгляд, разница значений токсичности для различных видов йессотоксинов зависит от особенностей их химической структуры. Безопасный уровень острого воздействия YTX (ARfD) составляет 25 μM/кг массы тела. Данные о токсичности YTX для других видов животных практически отсутствуют [3, 6, 10]. Постановлением Европейского союза № 853/2004 в 2004 г. был установлен регламент безопасного содержания йессотоксинов в моллю- сках – 1 мг/кг [11]. Вместе с тем результаты проводимых анализов содержания йессотоксинов в мясе моллюсков показали, что ни в одном из исследованных образцов содержание йессотоксинов не превысило 3,75 мг эквивалентов йессотоксинов/кг мяса моллюсков [6]. На этом основании был установлен новый максимально допустимый уровень содержания йессотоксинов в моллюсках – 3,75 мг/кг [12].
Таким образом, в настоящее время установлены показатели токсичности для YTX и некоторых его аналогов, определены основные молекулы-мишени его действия, его роль в качестве промотора апоптоза, выявлен максимально допустимый уровень йессо-токсинов в моллюсках. Однако, несмотря на растущее число данных о биологических эффектах, оказываемых YTX на теплокровный организм, точный механизм его действия до сих пор неизвестен.
Целью настоящей работы явилось исследование токсичности YTX в экспериментах in vivo в дозировках ниже установленного безопасного уровня острого воздействия.
Материалы и методы. Эксперимент проведен на 72 крысах-самцах линии Wistar с исходной массой тела 100 ± 10 г. Крысы получены из питомника филиала «Столбовая» ФГБУН «Научный центр биомедицинских технологий» ФМБА России. Животные получали сухой сбалансированный корм производства фирмы ООО «Лабораторкорм» (Россия) в режиме неограниченного доступа. Крыс размещали по 2–3 особи в клетках из поликарбоната при 12/12-часовом режиме освещенности и температуре 21 ± 1 ° С. Все крысы были разделены методом случайной выборки на 12 групп численностью по 6 особей; исходная масса тела в группах не различалась ( p >0,1 ANOVA). Работу с животным проводили в соответствии с российскими требованиями к надлежащей лабораторной практике1.
В работе использовали препарат YTX производства фирмы National Research Council Canada (Канада) в виде метанольного раствора (содержание YTX 4,3 ц моль). Непосредственно перед проведением исследований метанол удаляли из препарата методом вакуумного выпаривания при температуре не выше +20 ° С в течение не более 4 часов. Сухой остаток перерастворяли в 96 % растворе этилового спирта по ГОСТ 5962–20132. Для получения рабочих разведений токсина аликвоты спиртового раствора YTX разбавляли стерильным апирогенным раствором 0,15 М NaCl с получением растворов концентрацией 2 μM/кг (группы № 2, 6, 10), 8 μM/кг (группы № 3, 7, 11) и 12 μM/кг (группы № 4, 8, 12),
1 моль YTX = 1187,32 г. Все испытуемые дозы – ниже установленного значения безопасного уровня острого воздействия YTX (ARfD) – 25 μM/кг массы тела.
Растворы, содержащие YTX, вводили крысам указанных групп однократно в дозах 1 мл/кг массы тела внутрибрюшинно. Животным контрольных групп (№ 1, 5, 9) вводили в том же количестве физиологический раствор.
Выведение животных из эксперимента осуществляли через 6 (группы № 1–4), 24 (группы № 5–8) и 168 (группы № 9–12) часов после введения препаратов окадаиковой кислоты путем декапитации под эфирной анестезией. Собирали кровь с антикоагулянтом (трикалиевая соль ЭДТА), отбирали образцы ткани мозга для определения апоптоза и содержания малонового диальдегида, глутатиона в печени крыс. Массу внутренних органов (печень, почки, селезенка, легкие, сердце, тимус, надпочечники, гонады, мозг) определяли на электронных весах с погрешностью ± 0,01 г.
Биохимические показатели сыворотки выявляли на биохимическом анализаторе Konelab 20i (Финляндия). Уровень содержания малонового диальдегида в мозге определяли оптическим методом с 2-тиобарбитуровой кислотой и измерением уровня хромогена с максимумом поглощения в красной области видимого спектра при длине волны 532 нм [13]. Содержание восстановленного глутатиона в печени крыс определяли спектрофотометрическим методом согласно [14].
Гематологические показатели определяли в цельной крови стандартными методами на гематологическом анализаторе Coulter AC TTM 5 diff OV (Beckman Coulter, США) с набором реагентов (Beckman Coulter, Франция). Апоптоз клеток мозга изучали на проточном цитофлуориметре FC 500 (Beckman Coulter International S.A., Австрия) с использованием технологии окрашивания нейронов головного мозга в суспензии флуоресцентными реагентами FITC-аннексином V и 7-аминоактиномици-ном (7-AAD) [15].
Статистическую обработку результатов проводили путем определения выборочного среднего, стандартной ошибки, вероятности принятия нуль-гипотезы о совпадении распределений сравниваемых выборок согласно критерию Стьюдента, Манна–Уитни и ANOVA. Различия признавали достоверными при уровне значимости р <0,05.
Результаты и их обсуждение. Введение YTX во всех указанных дозировках не вызвало признаков заболеваемости животных во всех опытных группах. Достоверного изменения массы тела животных, гонад, надпочечников, мозга не наблюдалось. Выявлено достоверное ( p <0,05) снижение массы селезенки, легких, тимуса (в % от массы тела) на протяжении всего времени проведения эксперимента. Наблюдалась тенденция к снижению массы сердца, почек и печени (рис. 1).
Определение гематологических показателей после введения YTX через 168 часов выявило снижение содержания лимфоцитов ( p <0,05) и тенденцию увеличения количества нейтрофилов в сыворотке крови подопытных животных. Выявлено, что введение токсина во всех испытываемых дозировках вызывало повышение содержания лейкоцитов на протяжении всего времени проведения эксперимента, что доказывается различием в полученных значениях для большинства экспериментальных групп с группой контроля ( р <0,05) (табл. 1).
Несмотря на то что изменения параметров состава крови не носили выраженного дозозависимого характера, полученные данные свидетельствуют о возможном негативном воздействии YET при его внутрибрюшинном введении в количествах, которые, согласно имеющимся сообщениям, не оказывают токсического воздействия на подопытных животных.
Уровень содержания мочевины в сыворотке крови при введении всех исследуемых доз снижался немонотонно, по сравнению с контрольными группами, на протяжении всего времени эксперимента. После 6 часов введения токсина наблюдалось повышение содержание креатинина, а после 168 часов – снижение этого показателя. Выявлена тенденция к снижению содержания общего белка во всех экспериментальных группах и аланинаминотрансферазы (АЛТ) в плазме крови у крыс после 6 и 24 часов введения токсина. Полученные данные указывают на влияние YET на обмен белков, преобладание катаболических процессов в организме теплокровных животных, индуцируемых токсином (табл. 2).
Через 6 и 24 часа часов после введения YTX наблюдалась тенденция к снижению содержания триглицеридов и достоверное повышение холестерина в сыворотке крови (табл. 2). Такая динамика свидетельствует о влиянии YTX на обмен липидов и возможную индукцию воспалительного процесса под воздействием токсина, что подтверждает имеющиеся данные о механизме действия YTX [5, 6].
Впервые выявлено достоверное ( p <0,05) дозозависимое увеличение содержания малонового диальдегида (МДА) в ткани мозга через 168 часов после введения YTX (рис. 2) и тенденция к увеличению содержания восстановленного глутатиона в тканях печени (рис. 3). Кроме того, показано достоверное ( p <0,1) дозозависимое увеличение количества нейронов головного мозга с ранним аппоптозом (с 2,3 % при введении 2 µ М/кг до 3,02 % клеток при введении 12 µ М/кг; контроль – 1,78 % от общего количества клеток) и снижение активности позднего апоптоза (с 0,367 % при введении 2 µ М/кг до 0,180 % клеток при введении 12 µ М/кг; контроль – 0,45 % от общего количества клеток), фиксируемое в течение всего периода наблюдений за животными (рис. 4).
Полученные сведения дополняют имеющиеся данные литературы, свидетельствующие о том, что YTX является индуктором процессов катаболизма,
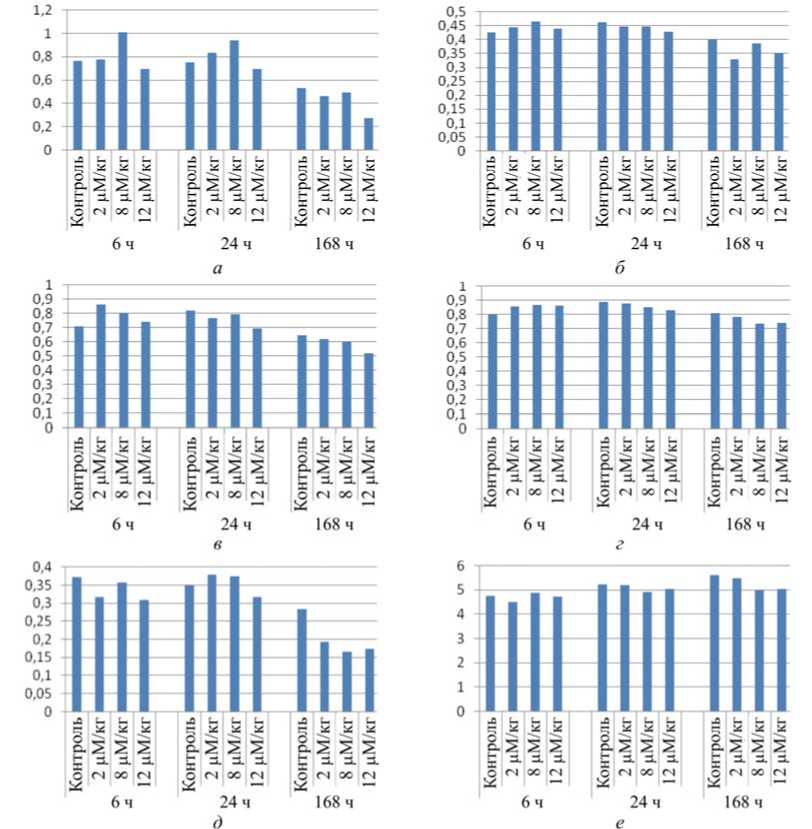
Рис. 1. Динамика изменения массы внутренних органов (в % от массы тела крыс). Ось абсцисс – доза и время введения YTX; ось ординат – вес органа в % от массы тела крыс. Число животных в каждой группе – 6: а – селезенка; б – сердце; в – легкие; г – почки; д – тимус; е – печень
Таблица 1
Гематологические показатели (эритроциты, лейкоциты), М ± m, крыс через 6, 24 и 148 ч после введения YTX (по 6 животных в каждой группе)
|
Группа |
Доза YTX, мкг/кг ( µ М/кг) |
Время после введения токсина, ч |
Среднее содержание Hb в эритроците, пг |
Средняя концентрация Hb в эритроците, г/л |
Лейкоциты, 10 9 /л |
Нейтрофилы, % |
Лимфоциты, % |
Моноциты, % |
|
1 |
Контроль |
6 |
20,2 ± 0,4 |
326,5 ± 1,3 |
8,9 ± 1,0 |
24,1 ± 2,3 |
61,8 ± 2,8 |
12,6 ± 1,6 |
|
2 |
2 |
20,4 ± 1,3 |
326,3 ± 1,8 |
14,0 ± 3,2 |
25,8 ± 3 |
63,7 ± 3,0 |
9,2 ± 0,8 |
|
|
3 |
8 |
21,0 ± 0,5 |
322,0 ± 3,4 |
10,0 ± 2,6 |
19,9 ± 2,8 |
65,8 ± 3,4 |
11,9 ± 0,6 |
|
|
4 |
12 |
19,5 ± 0,4* |
321,6 ± 2,8 |
10,7 ± 1,5* |
25,2 ± 1,8 |
62,6 ± 2,5 |
10,9 ± 0,8* |
|
|
5 |
Контроль |
24 |
19,7 ± 0,3 |
325,3 ± 2,4 |
11,2 ± 1,5 |
23,5 ± 3,0 |
60,8 ± 2,6 |
12,6 ± 1,3 |
|
6 |
2 |
20,7 ± 0,3 |
324,2 ± 3,6 |
13,9 ± 3,6* |
26,8 ± 4,6 |
60,4 ± 6,1 |
11,7 ± 1,7 |
|
|
7 |
8 |
20,8 ± 0,7 |
323,8 ± 3,1 |
13,3 ± 2,7* |
26,3 ± 4,6 |
61,6 ± 4,5 |
11,6 ± 0,7 |
|
|
8 |
12 |
20,3 ± 0,3 |
326,0 ± 3,7 |
10,5 ± 1,1 |
23,9 ± 3,0 |
62,6 ± 3,2 |
12,0 ± 1,3 |
|
|
9 |
Контроль |
168 |
19,5 ± 0,2 |
330,5 ± 3,6 |
8,4 ± 0,8 |
27,2 ± 2,3 |
57,6 ± 2,3** |
13,0 ± 1,9 |
|
10 |
2 |
19,7 ± 0,3 |
331,8 ± 2,0 |
10,3 ± 1,3* |
35,6 ± 2,6* |
50,7 ± 2,4** |
11,9 ± 1,2 |
|
|
11 |
8 |
20,1 ± 0,3 |
328,8 ± 2,7 |
13,7 ± 1,9* |
29,3 ± 4,7 |
59,2 ± 4,9** |
10,0 ± 1,4 |
|
|
12 |
12 |
19,4 ± 0,3 |
329,8 ± 2,2 |
6,4 ± 0,8 |
29,4 ± 2,1 |
54,8 ± 1,0** |
13,8 ± 1,9 |
П р и м е ч а н и е : * – различие с группой контроля для данного времени достоверно, p <0,05, Т -тест Стьюдента и/или критерий Манна–Уитни;
** – различие между группами (6 и 168 ч после введения YET) для данного критерия достоверно, p <0,05, Т- тест Стьюдента и/или критерий Манна–Уитни.
Таблица 2
Биохимические показатели плазмы крови крыс, М ± m , через 6, 24 и 168 ч после введения YTX (по 6 животных в каждой группе)
|
Группа |
Доза YTX, мкг/кг ( µ М/кг) |
Время после введения токсина, ч |
Холестерин, ммоль/л |
Триглицериды, ммоль/л |
АЛТ, ед/мл |
АСТ, ед/мл |
Белок общ, г/л |
Креатинин, мкмоль/л |
Мочевина ммоль/л |
Мочевая к-та, мкмоль/л |
|
1 |
Контроль |
6 |
1,29 ± 0,20 |
1,01 ± 0,21 |
103,26 ± 11,25 |
184,94 ± 19,49 |
62,59 ± 2,93 |
36,15 ± 0,85 |
9,93 ± 0,87 |
213,05 ± 13,48 |
|
2 |
2 |
2,29 ± 0,07* |
1,08 ± 0,10 |
146,42 ± 14,96* |
113,64 ± 41,35 |
58,58 ± 0,99 |
44,91 ± 1,24* |
6,28 ± 0,16* |
222,70 ± 21,37 |
|
|
3 |
8 |
2,22 ± 0,08* |
0,87 ± 0,10 |
153,35 ± 15,92* |
152,75 ± 59,19 |
56,87 ± 1,32* |
43,20 ± 3,55* |
5,66 ± 0,75* |
243,48 ± 24,27 |
|
|
4 |
12 |
1,96 ± 0,25* |
0,74 ± 0,11* |
140,95 ± 7,39* |
160,16 ± 42,13 |
59,54 ± 1,48 |
40,25 ± 0,75* |
5,95 ± 0,49* |
215,21 ± 29,85 |
|
|
5 |
Контроль |
24 |
1,41 + 0,16 |
1,01 ± 0,25 |
101,29 ± 9,04 |
182,80 ± 36,41 |
62,25 ± 3,78 |
37,66 ± 0,95 |
10,10 ± 1,25 |
195,11 ± 27,61 |
|
6 |
2 |
2,08 ± 0,15* |
0,76 ± 0,08* |
137,97 ± 16,01* |
300,23 ± 30,72 |
57,53 ± 1,20* |
36,36 ± 0,60 |
5,82 ± 0,17* |
108,47 ± 11,51 |
|
|
7 |
8 |
1,99 ± 0,11* |
0,89 ± 0,08 |
104,11 ± 7,05 |
240,16 ± 36,03 |
54,97 ± 1,54* |
37,76 ± 0,26 |
7,73 ± 0,30* |
171,84 ± 22,86 |
|
|
8 |
12 |
2,00 ± 0,17* |
0,81 ± 0,07 |
146,54 ± 19,2* |
203,70 ± 44,27 |
58,91 ± 1,16 |
40,65 ± 1,44* |
7,79 ± 0,31* |
191,54 ± 35,40 |
|
|
9 |
Контроль |
168 |
1,94 ± 0,19 |
0,79 ± 0,13 |
106,56 ± 12,33 |
280,39 ± 16,19 |
63,72 ± 3,92 |
42,35 ± 1,72 |
9,66 ± 0,51 |
183,68 ± 9,71 |
|
10 |
2 |
1,83 ± 0,09 |
0,71 ± 0,05 |
91,49 ± 8,58 |
206,67 ± 23,28 |
55,38 ± 0,97* |
34,40 ± 1,39* |
7,69 ± 0,59* |
174,08 ± 27,71 |
|
|
11 |
8 |
2,30 ± 0,14* |
0,82 ± 0,04 |
116,87 ± 14,46 |
187,33 ± 48,06 |
59,25 ± 3,04 |
35,32 ± 2,05* |
7,26 ± 0,55* |
167,79 ± 53,90 |
|
|
12 |
12 |
1,21 ± 0,04 |
1,24 ± 0,04 |
110,77 ± 8,21 |
86,57 ± 29,44 |
59,76 ± 1,79 |
36,76 ± 0,71* |
9,81 ± 0,62 |
198,33 ± 24,56 |
П р и м е ч а н и е : * – различие с группой контроля для данного времени достоверно, p <0,05, Т -тест Стьюдента и/или критерий Манна–Уитни.
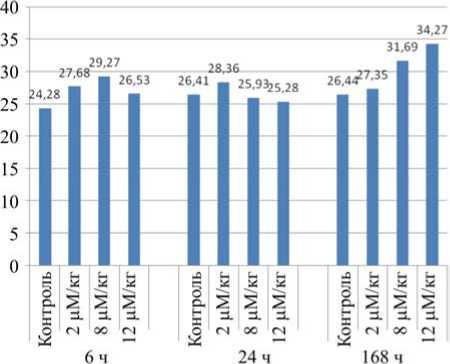
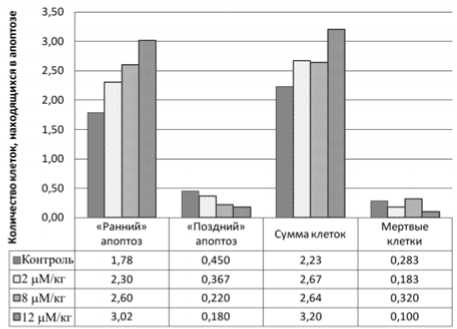
Рис. 4. Показатели апоптоза в ткани мозга (в % от общего количества нейронов в поле зрения) при введении YTX. Полученные значения количества клеток при «раннем» и «позднем» апоптозе достоверны и имеют разнонаправленный дозозависимый характер ( p <0,1)
Рис. 2. Содержание МДА в ткани мозга. Ось абсцисс – доза YTX; ось ординат – концентрация МДА в мозге, нмоль/г ткани. Число животных в каждой группе – 6
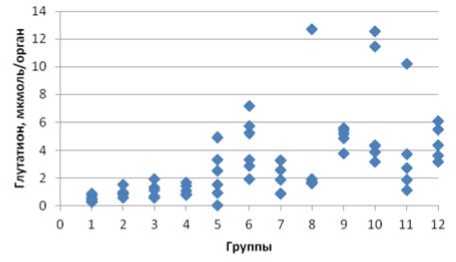
Рис. 3. Содержание восстановленного
глутатиона в печени крыс
выражающихся в активации свободнорадикального окисления и апотоза клеток головного мозга [3, 6, 10]. Впервые показано, что дозы YTX 2; 8 и 12 μM/кг могут оказывать токсическое воздействие на теплокровный организм.
Все испытуемые дозы ниже установленного значения безопасного уровня острого воздействия YTX ( ARfD = 25 μM/кг массы тела). Доза 2μM/кг соответствует допустимому уровню содержания токсина в моллюсках – 2,37 мг/кг. Полученные данные, а также данные, опубликованные в научной литературе о возможном токсическом действии YTX в дозах ниже ARfD , свидетельствуют о необоснованности увеличения максимально допустимого уровня содержания йессотоксинов в моллюсках с 1,0 до 3,75 мг/кг.
Выводы. Проведенные исследования показали наличие токсических эффектов йессотоксина при его внутрибрюшинном введении на протяжении всего времени проведения эксперимента при всех дозах – 2; 8 и 12 μM/кг. Все испытуемые дозы ниже установленного значения безопасного уровня
острого воздействия YTX (ARfD), равного 25 μM/кг массы тела. Данное действие проявлялось:
– в достоверном снижение массы селезенки, легких, тимуса (в % от массы тела) на протяжении всего времени проведения эксперимента, тенденции к снижению массы сердца, почек и печени;
– в усилении процессов катаболизма белков (снижение содержания белка, повышение количества креатинина, мочевой кислоты и АЛТ в плазме крови) и липидов (тенденция к снижению содержания триглицеридов и достоверное повышение холестерина в плазме крови) во всех экспериментальных группах;
– в усилении свободнорадикального окисления в головном мозге, выражающееся в дозозависимом росте показателей содержания малоново-
го диальдегида через 168 часов после введения токсина;
– в усилении процессов раннего апоптоза и снижении показателей позднего апоптоза в тканях головного мозга.
Полученные данные свидетельствуют о необходимости проведения дополнительных оценок рисков увеличения максимально допустимого уровня содержания йессотоксинов в моллюсках с 1,0 до 3,75 мг/кг.
Финансирование. Работа проведена за счет средств субсидии на выполнение государственного задания в рамках программы фундаментальных научных исследований (тема ФАНО России № 0529-2014-0044).
Список литературы Токсичность йессотоксина в эксперименте in vivo
- Yessotoxins, a Group of Marine Polyether Toxins: an Overview/В. Paz, А.Н. Daranas, М. Norte, P. Riobó, J.M. Franco, J.J. Fernández//Mar. Drugs. -2008. -Vol. 6. -P. 73-102 DOI: 10.3390/md20080005
- Yessotoxin, a novel phycotoxin, activates phosphodiesterase activity. Effect of yessotoxin on cAMP levels in human lymphocytes/A. Alfonso, L. de la Rosa, M.R. Vieytes, T. Yasumoto, L.M. Botana//Biochem. Pharmacol. -2003. -Vol. 65, № 2. -P. 193-208.
- Report of the Joint FAO/IOC/WHO ad hoc Expert Consultation on Biotoxins in Bivalve Molluscs. Oslo, Norway, 26-30 September 2004. Short Summary . -UNESCO, 2005. -8 p. -URL: http://unesdoc.unesco.org/images/0013/001394/139421e.pdf (дата обращения: 16.04.2018).
- Malagoli D., Ottaviani E. Yessotoxin affects fMLP-induced cell shape changes in Mytilus galloprovincialis immunocytes//Cell. Biol. Int. -2004. -Vol. 28, № 1. -P. 57-61.
- Alfonso A., Vieytes M.R., Botana L.M. Yessotoxin, a Promising Therapeutic Tool//Mar. Drugs. -2016. -Vol. 14. -P. 30 DOI: 10.3390/md14020030
- Marine biotoxins in shellfish -Yessotoxin group. Scientific Opinion of the Panel on Contaminants in the Food chain (Question No EFSA-Q-2006-065D) //The EFSA Journal. -2008. -Vol. 907. -P. 1-62. -URL: http://www.efsa.europa.eu/sites/default/files/scientific_output/files/main_documents/907.pdf (дата обращения: 16.04.2018).
- Franchini A., Malagoli D., Ottaviani E. Targets and Effects of Yessotoxin, Okadaic Acid and Palytoxin: A Differential Review//Mar. Drugs. -2010. -Vol. 8. -P. 658-677 DOI: 10.3390/md8030658
- Korsnes M.S Apoptotic events by yessotoxin in myoblast cell lines from rat and mouse//Toxicol. in vitro. -2006. -Vol. 20. -P. 1077-1087.
- Korsnes M.S., Korsnes R. Mitotic Catastrophe in BC3H1 Cells following Yessotoxin Exposure//Front. Cell. Dev. Biol. -2017. -Vol. 5, № 30. -18 p DOI: 10.3389/fcell.2017.00030
- Marine biotoxins. Food and Nutrition Paper (80). -Rome: Food and agriculture organization of the united nations, 2004. -287 p.
- Regulation (EC) No 853/2004 of the European Parliament and of the Council of 29 April 2004 //Official Journal of the European Union. -2004. -URL: https://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=OJ: L: 2004: 139: 0055: 0205: EN: PDF (дата обращения: 16.04.2018).
- Commission Regulation (EU) No 786/2013 of 16 August 2013 amending Annex III to Regulation (EC) No 853/2004 of the European Parliament and of the Council as regards the permitted limits of yessotoxins in live bivalve mollusks //Official Journal of the European Union. -2013. -URL: https://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=OJ: L: 2013: 220: 0014: 0014: EN: PDF (дата обращения: 16.04.2018).
- Ohkawa H., Ohishi N., Yagi K. Assay for lipid peroxides in animal tissues by thiobarbituric acid reaction//Anal. Biochem. -1979. -Vol. 95, № 2. -P. 351-358.
- Разыграев А.В. Метод определения глутатионпероксидазной активности с использованием пероксида водорода и 5,5'-дитиобис (2-нитробензойной кислоты)//Клинико-лабораторный консилиум. -2004. -№ 4. -С. 19-22.
- Биодоступность наночастиц оксида железа при использовании их в питании. Результаты экспериментов на крысах/Р.В. Распопов, Э.Н. Трушина, И.В. Гмошинский, С.А. Хотимченко//Вопросы питания. -2011. -Т. 80, № 3.-С. 25-30.


