Тотальное эндопротезирование при анкилозе височно-нижнечелюстного сустава
Автор: Епифанов С.А., Штемпель М.С., Зангиева О.Т., Федотов Р.Н., Высельцева Ю.В., Шомин Е.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.17, 2022 года.
Бесплатный доступ
Цель: оценить лечебные исходы, связанные с применением тотального эндопротезирования у пациентов с анкилозирующим поражением височно-нижнечелюстного сустава (ВНЧС). Материалы и методы: исследование включало в себя ретроспективный анализ данных и историй болезни пациентов с анкилозом ВНЧС, которым выполнено тотальное эндопротезирование в период с 2010 по 2018 гг. Критерии включения: 1) рентгенологическое подтверждение анкилоза, 2) ограничение открывания рта, 3) минимальный послеоперационный период не менее 12 месяцев, 4) применение индивидуально-изготавливаемого тотального эндопротеза ВНЧС. У каждого пациента оценивали количество предшествующих хирургических вмешательств в области поражённого ВНЧС (если таковые имели место), длительность послеоперационного периода до развития рецидива заболевания. Субъективную оценку состояния производили методом анкетирования по визуально-аналоговой шкале (ВАШ) (от 0 до 10) для показателей: 1) боль в области ВНЧС, 2) лицевая боль и головная боль, 3) функция ВНЧС, 4) диета (способность пережевывать твердую пищу), 5) дееспособность (субъективная оценка влияния тотального эндопротезирования ВНЧС на повседневную жизнедеятельность). Объективными методами исследования явились: оценка максимального межрезцового расстояния при максимальном открытии рта (ММР), оценка боковых движений нижней челюстью. Статистическая обработка проводилась с использованием непараметрических функций. Нами проведено обследование и лечение 32 пациентов (22 женщины, 10 мужчин) с 48 анкилозами ВНЧС (16 двухсторонних, 16 односторонних), средний возраст пациентов 39 лет (от 18 до 68 лет), 69% с 2 или более предшествующими операциями в области ВНЧС, и средним периодом наблюдения 24 месяца (от 12 до 84 месяца). Травма, как главная причина развития анкилоза зарегистрирована у 17 из 32 пациентов (53%). В результате хирургического лечения были достигнуты следующие результаты: средние показатели оценки боли в области ВНЧС до хирургического лечения - 8.0, после - 1.5; головной боли: до - 8, после - 3.5; лицевой боли: до - 8, после - 4.0; функции ВНЧС: до - 8.0, после - 2.5; способность пережевывать твердую пищу: до - 7.0, после - 3.0; дееспособность пациенты оценивали до операции как 7, после - 1.5. До хирургического лечения средний показатель ММР составил 14,5 мм (от 6.3, до 20 мм) и в послеоперационном периоде 35 мм (от 30, до 40 мм), соответственно. Средняя боковая экскурсия нижней челюсти улучшилась с 0.5 до 2.0 мм с левосторонним анкилозом внчс и с 1.0 до 1.3 мм с правой стороны. Все улучшения имели статистически значимые показатели (p function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Височно-нижнечелюстной сустав, внчс, анкилоз, тотальное эндопротезирование, артропластика
Короткий адрес: https://sciup.org/140293888
IDR: 140293888
Total temporomandibular joint replacement in TMJ ankylosis
Aim: to evaluate the results of the total temporomandibular joint replacement for patients with ankylosis of temporomandibular joint (TMJ). Methods and materials: the research includes the retrospective analysis of patients with tmj ankylosis and total tmj replacement from 2010 to 2018. Inclusion criteria: 1) Xray confirmation of ankylosis, 2) Restriction of mouth opening, 3) Post operation period more than 12 months, 4) Use of a custom-made total TMJ endoprosthesis. For each patient the number of previous surgical interventions in the affected TMJ was assessed (in case it happened) and the duration of the post operation period before the disease recurrance. Subjective assessment of the patient’s condition was made by the method of questioning the visual-analog scale (VAS) from 0 to 10 for the following parameters: 1) pain in the tMj, 2) facial pain and headaches, 3) TMJ function, 4) ability to chew solid food, 5) subjective impact assessment of the total TMJ endoprosthesis on life quality. The subjective assessment of the impact total MJ endoprosthesis has on day-to-day life. Objective methods of research consisted of an evaluation of the interstitial distance at maximum mouth opening (MOP) and an assessment of mandibula lateral movements. Non-parametric functions were used for statistical analysis. We examined and treated 32 patients (22 women, 10 men) with 48 TMJ ankyloses (16 bilateral, 16 unilateral), average age of patients was 39 years (spread from 18 to 68), 69% with 2 or more previous surgeries in the TMJ area, and the average observation period 24 months (spread from 12 to 84). Injury as the main cause of ankylosis was registered in 17 out of 32 cases (53%). As a result of surgical treatment, the following results were achieved: average subjective assessment of pain in the TMJ before surgical treatment-8.0, after - 1.5; headache: before - 8, after - 3.5; facial pain: before - 8, after - 4.0; TMJ functions: before - 8.0, after - 2.5; Ability to chew solid food: up to - 7.0, after - 3.0; patients assessed the legal capacity before the operation as 7, after - 1.5. Before the surgical treatment the average MR was 14.5 mm (spread from 6.3 to 20 mm) and in the postoperative period 35 mm (spread from 30 to 40 mm). The average lateral excursion of the lower jaw improved from 0.5 to 2.0 mm with left-sided ankylosis and from 1.0 to 1.3 mm on the right side. All improvements had statistically significant indicators (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Тотальное эндопротезирование при анкилозе височно-нижнечелюстного сустава
Анкилоз височно-нижнечелюстного сустава (ВНЧС) — это состояние, которое характеризуется костным, костнофиброзным, фиброзным сращением части или всей суставной поверхности головки мыщелкого отростка нижней челюсти с суставной ямкой височной кости, что проявляется нарушением жевания, речи, затрудняет соблюдение гигиены полости рта и других жизненно-важных функций, связанных с полноценным открыванием рта [1]. К развитию анкилоза может привести множество факторов, таких как травма, артриты, инфекционные заболевания, предшествующие хирургические вмешательства в области ВНЧС, врожденные деформации, идиопатические факторы и ятрогенные причины [2; 3]. Травма является наиболее частой причиной развития анкилозирурющего поражения ВНЧС [4].
Развитие анкилоза у пациентов с челюстно-лицевой деформацией может быть следствием нарушения окклюзии [5].
Диагноз анкилоза ВНЧС мы устанавливали на основании клинического и инструментального обследования, которое дополнительно включало компьютерную томографию (КТ), магнитно-резонансную томографию (МРТ), а также компьютерную обработку полученных данных.
Shawhney и др. и He и др. предложили рабочую классификацию анкилоза ВНЧС [6; 7], однако, она не нашла широкого распространения в нашей стране.
Основная цель лечения пациентов с анкилозом ВНЧС — вернуть пациенту нормальную его функцию со стабильным результатом, провести коррекцию челюстно-лицевой деформации, уменьшить болевой синдром и предотвратить возможное развитие рецидива анкилоза [8]. Многочисленные хирургические методики были предложены для устранения анкилоза ВНЧС: «щелевая артропластика», интерпозиционная артропластика и тотальное эндопротезирование ВНЧС [9]. Первоначально для интерпозиционной артропластики были использованы аутоткани, такие как хрящ, лоскут височной мышцы, кожножировой, жировой свободные лоскуты и др. Некоторые аллопластические материалы так же были использованы, однако сообщалось о большом количестве осложнений, связанных с их применением (в частности Proplast Teflon (Vitek, Houston, TX) и Silastic (Dow Corning, Midland, MO)) [10; 11].
Тотальная реконструкция ВНЧС может быть подразделена на аутогенную, такую как костохондральный трансплантат (КХТ) и грудиноключичный трансплантат (ГКТ) и аллопластическую [12; 13]. По данным литературы и нашим собственным наблюдениям использование КХТ связано с менее прогнозируемым результатом лечения больных и сопряжено с осложнениями, такими как реанкилоз, резорбция трансплантата, переломы, болевой синдром. ГКТ по своему строению более схож с мыщелковым отростком нижней челюсти, взятие трансплантата может быть выполнено с суставным диском, что обеспе- чивает лучшую функцию, однако, сохраняется высокий риск развития рецидива анкилоза [14].
Использование индивидуально-изготавливаемых или стандартных тотальных эндопротезов ВНЧС значительно сокращает время хирургического вмешательства, нет необходимости использовать донорские участки, пациент может в максимально короткое время вернуться к обычному ритму жизни, восстановив утраченные функции [15]. К недостаткам необходимо отнести их стоимость, износ материала, возможную несостоятельность эндопротеза (перелом, нестабильность фиксации и т.д.) [16]. L.Wolford и др. сообщили об успешном 5-летнем использовании тотального индивидуально-изготавлива-емого эндопротеза ВНЧС [17]. Mercuri и др. представили отчёт об успешном применении подобных эндопротезов с долгосрочным результатом в 9 и 14 лет [18; 19].
Нами использован протокол устранения анкилоза ВНЧС, предложенный L.Wolford в 1992 г.: 1) рассечение анкилозированных тканей сустава; 2) удаление разрастаний костной и соединительной тканей в области ВНЧС; 3) реконструкция ВНЧС с использованием индивиду-ально-изготавливаемого тотального эндопротеза ВНЧС; 4) использование свободного жирового графта, размещаемого вокруг суставной части эндопротеза; 5) выполнение корректирующей ортогнатической операции при наличии челюстно-лицевой деформации [20–22]. Базовый протокол может быть выполнен в 2 и более этапа, стадийность зависит от клинической картины заболевания.
Целью исследования стало изучение исходов лечения больных с анкилозом ВНЧС по предложенному протоколу в зависимости от: 1) пола и возраста, 2) субъективной оценки боли, восстановления функции, диеты, дееспособности; 3) объективных исследований функции ВНЧС; 4) оценки эффекта от предшествующих хирургических вмешательствах на ВНЧС; 5) оценки частоты реанкилозирования ВНЧС.
Материалы и методы
Исследование выполнено на основе анализа историй болезни пациентов, проходивших лечение в ФГБУ НМХЦ им. Н.И. Пирогова в период с 2010 по 2018 гг. по поводу анкилоза ВНЧС, которым выполнено тотальное эндопротезирование ВНЧС индивидуально-изготавли-ваемым имплантатом.
Критерии включения пациентов в исследование: 1) рентгенологическое подтверждение анкилоза ВНЧС, 2) ограничение открывания рта, 3) минимальный послеоперационный период не менее 12 месяцев, 4) применение индивидуально-изготавливаемого тотального эндопротеза ВНЧС. Критерии исключения: 1) неполное обследование пациента 2) наличие злокачественных новообразований головы и шеи, 3) ранее проведенная лучевая терапия.
У каждого пациента мы фиксировали количество предшествующих хирургических вмешательств перед тотальным эндопротезированием. Пациенты условно

разделены на группы: первая у которых выполнено 0–1 хирургическое вмешательство в области ВНЧС; вторая группа — 2–3; третья группа — 4 и более. Нами оценено шесть, на наш взгляд, наиболее важных показателей качества жизни в отношении состояния ВНЧС: боль в области ВНЧС, головная боль, лицевая боль, функция ВНЧС, диета (способность пережевывать твердую пищу), дееспособность. Самооценка выполнялась по психометрической шкале с градацией от 0 до 10.
Объективные исследования включали в себя измерения: межрезцового расстояния при максимальном открытии рта (ММР), латеральную экскурсию нижней челюсти влево (ЛЭЛ), латеральную экскурсию нижней челюсти вправо (ЛЭП). Всем пациентам до и после хирургического вмешательства выполнено КТ, в некоторых случаях исследование дополнено МРТ до хирургического вмешательства. Использование МРТ после эндопротезирования сопряжено с появлением большого количества артефактов, в связи с чем оно было ограниченно. Учитывая, что вероятность рецидива анкилоза с течением
Табл. 1. Наиболее распространенные тотальные эндопротезы ВНЧС, технические характеристики
Индивидуально-изготавливаемые тотальные эндопротезы ВНЧС (ИИТЭ ВНЧС) являются двухкомпонентными, состоят из имплантата мыщелкого отростка, изготавливаемого из титана, и имплантата суставной ямки височной кости из полиэтилена ультравысокой молекулярной массы (табл. 1).
Имплантат мыщелкого отростка крепится к ветви нижней челюсти 5–7 бикортикальными винтами диаметром от 2 до 2,7 мм. Имплантат суставной ямки крепится к скуловому отростку височной кости 3–5 винтами диаметром 2 мм. Процесс производства имплантатов, а также используемые материалы аналогичны применяемым при протезировании тазобедренных и коленных суставов и являются на сегодняшний день «золотым стандартом» в травматологии и ортопедии.
Технологический цикл производства основан на обработке DICOM данных пациента, получаемых при КТ с последующим моделированием в специальных программах и получением виртуальной 3D модели имплантатов и костей лицевого скелета. В зависимости от клинической картины заболевания в своей практике мы использовали аналоговое, цифровое и комбинированный вид моделирования тотальных эндопротезов. Аналоговое моделирование включало в себя первоначальное изготовление стереолитографических моделей с последующим восковым моделированием имплантатов. Однако этот метод сопряжён с множеством недостатков, таких как неточности при сканировании восковых моделей, их усадка, возможная деформация при транспортировке, длительность производства. С 2014 г. мы активно применяем только цифровое моделирование (Рис. 1, 2). Эта технология позволила нам в значительной степени
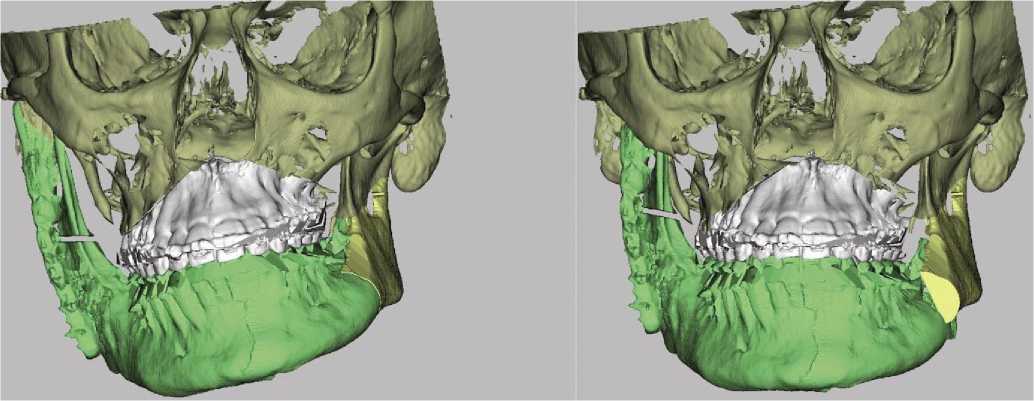
Рис. 1. Компьютерное моделирование ортогнатической операции.
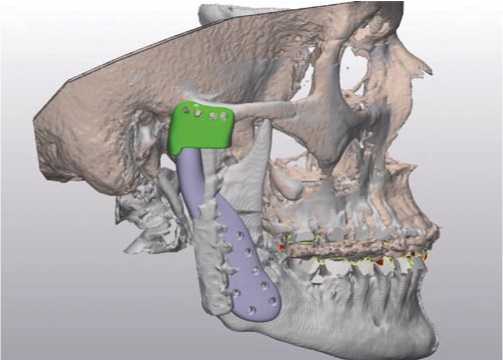
Рис. 2. Компьютерное моделирование индивидуального имплантата правого ВНЧС.
сократить время необходимое на производство ИИЭ ВНЧС с 21 до 7 суток. С 2015 г. в качестве технологии производства имплантата мыщелкого отростка мы используем 3D печать из порошкового титана.
Отличительной особенностью этой технологии является высокая точность производства, позволяющая воспроизводить контактную поверхность имплантата мыщелкого отростка в точности по рельефу поверхности нижней челюсти. Это позволяет уменьшить количество возможных ошибок, связанных с неточностью позиционирования имплантата во время хирургического вмешательства.
Протокол хирургического вмешательства
В доступной литературе и в нашей практике мы используем два базовых протокола хирургического лечения пациентов с анкилозом ВНЧС: 1-этапный и 2-х этапный.
2-х этапный протокол включает в себя: 1) 1-й хирургический этап: рассечение анкилозированного сустава, удаление трансформированной и реактивно-изменённой костной ткани, подготовка протезного ложа суставной впадины, имплантация временного аллогенного материала (силикон, акрил, костный цемент) или свободного жирового трансплантата с применением или без межчелюстной фиксации; 2) КТ челюстей и основания черепа; 3) моделирование имплантата с использованием специальных программ с участием хирурга (расстояние от резецированного участка мыщелкого отростка до суставной впадины должно быть не менее 20 мм); 4) производство имплантата мыщелкого отростка и суставной ямки на сертифицированном производстве; 5) 2-й хирургический этап: имплантация тотального эндопротеза. 2-й этап хирургического вмешательства может быть дополнен использованием свободного жирового аутотрансплантата, который необходимо разместить вокруг шейки имплантата, а также проведением ортогнатических или корректирующих операций. В нашей практике
2-х этапный протокол мы использовали у пациентов со злокачественными новообразованиями (ЗНО) головы и шеи, которым выполнено хирургическое лечение по поводу ЗНО, проведена лучевая терапия, антирезорб-тивная терапия, которые не вошли в это клиническое исследование.
1 этапный протокол включает в себя: 1) КТ челюстей и основания черепа; 2) моделирование предстоящего хирургического вмешательства и имплантата с использованием специальных компьтерных программ с участием хирурга (расстояние от резецированного участка мыщелкого отростка до суставной впадины должно быть не менее 20 мм); 3) изготовление имплантата мыщелкого отростка и суставной ямки на сертифицированном производстве; 4) рассечение анкилозированного сустава, удаление трансформированной и реактивно-изменённой костной ткани, подготовка протезного ложа суставной впадины, имплантация тотального эндопротеза. Хирургический этап так же как и при 2-х этапном протоколе может быть дополнен дополнительными хирургическими вмешательствами.
Техника хирургического вмешательства
Нами использованы базовые хирургические доступы к анкилозированым тканям ВНЧС через внутриушной (предушный) и окаймляющий угол нижней челюсти. Этапы хирургического вмешательства: 1) унилатеральное или билатеральное рассечение анкилозированных структур сустава, удаление мыщелкого отростка, удаление гете-ротопическиой и реактивно-измененной костной ткани в области суставной ямки, скулового отростка височной кости и прилегающих областей; 2) короноидэктомия через внутриушной (предушный) хирургические доступы при его реактивной гипертрофии, увеличении длины или вовлечении в гетеротопическую костную трансформацию; 3) позиционирование нижней челюсти в физиологическое положение, при необходимости может быть выполнена сагиттальная остеотомия с противоположной стороны с временной стабилизацией промежуточным сплинтом с жесткой фиксацией; 4) реконструкция с использованием ИИТЭ ВНЧС; 5) выполнение дополнительных хирургических процедур (аутотрансплантация жирового графта вокруг суставной части эндопротеза, ортогнатические операции и т.д.).
Результаты
Нами проведено обследование и лечение 32 пациентов (22 женщины и 10 мужчин) с 48 анкилозами ВНЧС (16 билатеральных, 16 односторонних), средний возраст пациентов составил 39 лет (от 18 до 68 лет). Средний период послеоперационного наблюдения составил 29,5 месяцев (от 12 до 84 месяцев) (табл. 2).
Травма как основная причина развития анкилоза зарегистрирована у 17 пациентов из 32 (53%) (табл. 3).
Средний показатель боли в области ВНЧС до хирургического лечения составил 8.0, после операции он
Табл. 2. Распределение по возрасту и полу
|
Количество пациентов |
Двухсторонний анкилоз суставов (оперированных суставов) |
Односторонний анкилоз |
Средний возраст начала заболевания ВНЧС (от и до) |
Средний возраст на момент хирургического вмешательства |
Мужчин/ Женщин |
Число предшествующих хирургических вмешательств на пациента 0-1 /2-3/ 4 или более |
Средний период послеоперационного наблюдения месяцев (от и до) |
|
32 |
16 (32) |
16 |
20 (13,26) |
39 |
10/22 |
10/6/16 |
29.5 (12, 84) |
Табл. 3. Этиологические причины развития анкилоза (n = 32)
Ни у одного пациента не зарегистрировано развитие реанкилоза (Рис. 3).
Послеоперационное обследование выполнено в период от 12 до 84 месяцев. Статистически значимых различий не отмечено. Результаты представленные в обоих группах сопоставимы и имеют положительный результат.
Десять пациентов (31%) имели 0–1 предшествующее хирургическое вмешательство в области ВНЧС, 6 паци-
Табл. 4. Измерения показателей до хирургического вмешательства (Гр1) и в отдаленный период (Гр2) (n = 32). Первые шесть измерений выполнены по шкале от 0 до 10, в скобках указаны величины от и до
|
Гр 1 |
Гр 2 |
р |
|
|
Боль в области ВНЧС |
8 (4.3, 9.0) |
1.5 (0, 7) |
<0.001 |
|
Головная боль |
8 (4, 9) |
3.5 (0, 7) |
<0.001 |
|
Лицевая боль |
8 (4, 9) |
4 (0, 7) |
<0.001 |
|
Функция сустава |
8 (7, 9) |
2.5 (1, 6.5) |
<0.001 |
|
Диета (способность пережевывать твердую пищу) |
7 (5, 8) |
3 (0, 6) |
<0.001 |
|
Дееспособность |
7 (4, 8) |
1.5 (0, 7) |
<0.001 |
|
Межрезцовое расстояние при максимальном открытии рта (мм) МР |
14.5 (6.3, 20.3) |
32 (30, 40) |
<0.001 |
|
Боковое выдвижение нижней челюсти влево (мм) |
0.5 (0, 2.5) |
2 (1, 3) |
p<0.05 |
|
Боковое выдвижение нижней челюсти вправо (мм) |
1 (0, 1.9) |
1.3 (1, 2) |
p<0.05 |
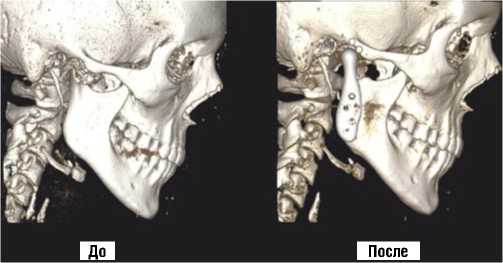
Рис. 3. Компьютерная томограмма пациента до и через 36 месяцев после тотального эндопротезирования правого ВНЧС.
ентов (8%) — от 2 до 3 и 16 пациентов (50%) имели 4 и более хирургических вмешательств. Мы не обнаружили статистически значимых различий между двумя группами пациентов у которых было 2–3 и 4 и более предшествующих хирургических вмешательств в области ВНЧС. Более выраженные изменения мы наблюдали в подгруппе где у пациентов выполнено 2 и более хирургических вмешательств.
Осложнения после хирургических вмешательств
Шесть пациентов (19%) имели осложнения, потребовавшие дополнительных хирургических вмешательств — образование гетеротопической костной ткани (но без анкилозирования) и появление боли в области оперированного ВНЧС в период более чем 2 года после хирургического вмешательства, потребовавшая вторичного удаления гетеротопической костной ткани и использования свободного жирового транстплантата вокруг эндопротеза (Рис. 4).
У одного пациента (3%) развилась одностороннее инфекционное поражение в области ВНЧС через 2 недели после хирургического вмешательства. Пациент был успешно вылечен консервативно по протоколу L. Wolford (протокол ведения пациентов с перипротезной инфекцией) [23].
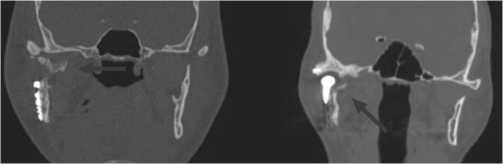
Рис. 4. Осложнение хирургического лечения, образование гетеротопической костной ткани вокруг эндопротеза (отмечено стрелкой).
У одного пациента (3%) зарегистрирован синдром Фрей на стороне хиргического вмешательства. Проявления синдрома разрешились в течение 3 месяцев, в дальнейшем пациент имел стабильный результат в течение 4,5 лет.
У шестнадцати (50%) пациентов был использован имплантат мыщелкого отростка заготавливаемый методом машинного фрезерования, у 16 (50%) — изготовлен методом 3D-печати.
Один пациент (3%) имел 4 предшествующих неудачных хирургических вмешательств в области ВНЧС, направленных на устранение анкилоза. Однако в послеоперационном периоде через 3 года мы наблюдали рецидив ограничения открывания рта за счёт выраженной гипертрофии венечного отростка и его контакта со скуловой дугой. Мы не обнаружили у него развития гетеротопической костной ткани вокруг эндопротеза. В качестве лечения была выполнена внутриротовая резекция гипертрофированного участка венечного отростка с аутотрансплантацией свободного жирового трансплантата. Послеоперационное наблюдение в течении 12 месяцев показало отсутствие признаков рецидива заболевания.
Обсуждения
Цель представленного исследования — оценка лечебных исходов у пациентов, пролеченных по поводу анкилоза ВНЧС с использованием тотального эндопротезирования. Нами прооперировано 48 анкилозированных ВНЧС у 32 пациентов (16 односторонних и 16 двухсторонних) со средним периодом наблюдения 29,5 месяцев, признаков развития рецидива анкилоза не отмечено. У 6 пациентов в послеоперационном периоде зарегистрировано развитие гетеротопической костной ткани в области оперированного ВНЧС без признаков ан-килозирования, которые зарегистрированы через 2 года и позднее после тотального эндопротезирования. Средний показател ММР улучшился с 14.5 мм до хирургического лечения до 32 мм после. Все субъективные показатели до и после хирургии продемонстрировали статистически значимое улучшение.
В настоящее время в зарубежной литературе представлено большое количество вариантов лечения пациентов с анкилозом ВНЧС. Надежность и успех хирургических вмешательств напрямую зависит от их количества, наличия послеоперационных рубцов, степени повреждения окружающих сустав тканей и устранения боли связанной с патологией ВНЧС.
Заключение
В заключении необходимо отметить, что, исходя из данных проведённого ретроспективного исследования, хирургическое лечение пациентов с анкилозом ВНЧС в одну хирургическую стадию с использованием индивиду-ально-изготавливаемого тотального эндопротеза, трансплантации аутожировой ткани является безопасным и предсказуемым. Однако, большинство хирургов могут придерживаться лечения в 2 стадии с первоначальным устранением анкилоза, удалением гетеротопической костной ткани и последующим отсроченным восстановлением сустава с помощью тотального эндопротеза.
Т.о. методика хирургического лечения пациентов с анкилозом ВНЧС с использованием индивидуально-из-готавливаемых тотальных эндопротезов ВНЧС и жирового аутографта является методикой выбора при данной патологии и может быть отнесена к протоколу ведения пациентов с этой нозологической группой.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Тотальное эндопротезирование при анкилозе височно-нижнечелюстного сустава
- Епифанов С.А. Заболевания височно-нижнечелюстного сустава — междисциплинарная проблема: переосмысление устоявшихся понятий в практике врача — челюстно-лицевого хирурга // Вестник Национального медико-хирургического Центра им. Н.И. Пирогова. — 2020. — T.15. — №3. — Часть 2. — С. 102-105. [Epifanov SA. Disorders of the temporomandibular joint — it's an interdisciplinary problem: rethinking established concepts in the practice of a maxillofacial surgeon. Vestnik Natsionalnogo mediko-khirurgicheskogo Tsentra im. N.I. Pirogova. 2020; 15(3 part 2): 102-105 (In Russ).] doi: 10.25881/BPNMSC.2020.57.96.019.
- Roychoudhury A, Parkash H, Trikha A. Functional restoration by gap arthroplasty in temporomandibular joint ankylosis: A report of 50 cases. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 1999; 87(2): 166-9. doi: 10.1016/s1079-2104(99)70267-2.
- Erol B, Tanrikulu R, GoANrgun B: A clinical study on ankylosis of the temporomandibular joint. J Craniomaxillofac Surg. 2006; 34(2): 100-6. doi: 10.1016/j.jcms.2005.07.008.
- Topazian RG: Etiology of ankylosis of temporomandibular joint: Analysis of 44 cases. J Oral Surg Anesth Hosp Dent Serg. 2008; 12(2): 61-6. doi: 10.1007/s10006-008-0103-y.
- Miyamoto H, Kurita K, Ogi N, Ishimaru JI, Goss A. The role of the disk in sheep temporomandibular joint ankylosis. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 1999; 88(2): 151-8. doi: 10.1016/s1079-2104(99) 70109-5.
- Sawhney CP. Bony ankylosis of the temporomandibular joint: Follow-up of 70 patients treated with arthroplasty and acrylic spacer interposition. Plast Reconstr Surg. 1986; 77(1): 29-40.
- He D, Yang C, Chen M, Zhang X, et.al. Traunatic Temporomandibular joint ankylosis: Our classification and treatment experience. J Oral Maxillofac Surg. 2011; 69(6): 1600-7. doi: 10.1016/j.joms.2010.07.070.
- Епифанов С.А., Поляков А.П., Скуредин В.Д. Протезирование ви-сочно-нижнечелюстного сустава // Вестник Национального медико-хирургического Центра им. Н.И. Пирогова. — 2014. — Т.9. — №4. — С. 17-22. [Epiphanov SA, Poliakov AP, Skuredin VD. Tmj prosthesis. Vestnik Natsionalnogo mediko-khirurgicheskogo Tsentra im. N.I. Pirogova. 2014; 9(4): 17-22. (In Russ).]
- Епифанов С.А., Скуредин В.Д. Эволюция тотального эндопротезирования височно-нижнечелюстного сустава // Вестник Национального медико-хирургического центра им. Н.И. Пирогова. — 2018. — T.13. — №2. —
- С. 141-145. [Epiphanov SA, Skuredin VD. The evolution of total endoprosthesis of the temporo-mandibular joint. Vestnik Natsionalnogo mediko-khirurgic-heskogo Tsentra im. N.I. Pirogova. 2018; 13(2): 141-145. (In Russ).]
- Wolford LM, Henry CH, Nikaein A, Newman JT, Namey TC: The Temporomandibular Joint Alloplastic Implant Problem. In Sessle BJ, Bryant PS, and Dionne RA, (Editors), Temporomandibular Disorders and Related Pain Conditions, IASP Press, Seattle. WA. 1995. pp.443-447.
- Henry CH, Wolford LM: Treatment Outcomes for TMJ Reconstruction After Proplast-Teflon Implant Failure. J Oral Maxillofac Surg. 1993; 51(4): 352-8. doi:10.1016/s0278-2391 (10)80343-x.
- Matukas VJ, Szvmela VF, Schmidt JF: Surgical treatment of bony ankylosis in a child using a composite cartilage-bone iliac crest graft. J oral Surg. 1980; 38(12): 903-5.
- Macintosh RB, Henny FA: A spectrum of application of autogenous cos-tochondral grafts. J Maxillofac Surg. 1977; 5(4): 257-67. doi: 10.1016/ s0301-0503(77)80120-3.
- Wolford LM, Cottrell DA, Henry CH: Sternoclavicular grafts for temporomandibular joint reconstruction. J Oral Maxillofac Surg. 1994; 52(2): 119-28. doi: 10.1016/0278-2391(94)90391-3.
- Epifanov S, Ruidel D. Total temporomandibular joint replacement with use of custom 3-D printed TMJ prosthetics // Craniomaxillofacial Trauma & Reconstruction. 2020; 13(3): 19.
- Loveless TP, Bjornland T, Dodson TB, Keith DA. Efficacy of temporomandibular joint ankylosis surgical treatment. J Oral Maxillofac Surg. 2010; 68(6): 1276-82. doi: 10.1016/j.joms.2009.10.014.
- Wolford LM, Pitta MC, Reiche-Fischel O, Franco PF: TMJ Concepts/Techm-edica custom- made TMJ total joint prosthesis: 5-year follow-up study. Int J Oral Maxillofac Surg. 2003; 32(3): 268-74. doi: 10.1054/ijom.2002.0350.
- Mercuri LG, Wolford LM, Sanders B, White RD, Giobbie-Hurder A. Long-term follow-up of the CAD/CAM patient fitted total temporomandibular joint reconstruction system. J Oral Maxillofac Surg. 2002; 60(12): 1440-8. doi: 10.1053/joms.2002.36103.
- Mercuri LG, Edibam NR, Giobbie-Hurder: Fourteen-year follow-up of a patient-fitted total temporomandibular joint reconstruction system. J Oral Maxillofac Surg. 2007; 65(6): 1140-8. doi: 10.1016/j.joms.2006.10.006.
- Wolford LM, Morales-Ryan CA, Garcia-Morales P, Cassano DS. Autologous fat grafts placed around temporomandibular joint (TMJ) total joint prostheses to prevent heterotopic bone. Proc (Bayl Univ Med Cent). 2008; 21(3): 248-54. doi: 10.1080/08998280.2008.11928404.
- Wolford LM, Cassano DS: Autologous Fat Grafts Around Temporomandibular Joint (TMJ) Total Joint Prostheses to Prevent Heterotopic Bone. In M.A. Shiffman (Ed.) Autologous Fat Transfer. Springer-Verlag Berlin Heidelberg. 2010. pp. 361-382.
- Mercuri LG, Ali FA, Woolson R. Outcomes of total alloplastic replacement with periarticular autogenous fat grafting for management of reankylosis of the temporomandibular joint. J Oral Maxillofac Surg. 2008; 66(9): 1794-803. doi: 10.1016/j.joms.2008.04.004.
- Wolford LM, Rodrigues DB, McPhillips A: Management of the Infected Temporomandibular Joint Total Joint Prosthesis. J Oral Maxillofac Surg. 2010; 68(11): 2810-23. doi: 10.1016/j.joms.2010.05.089.


