Трансхиатальная лапароскопическая энуклеация лейомиомы нижнегрудного отдела пищевода
Автор: Камалов А.К., Рябов А.Б., Хомяков В.М., Волченко Н.Н., Колобаев И.В., Кострыгин А.К., Соболев Д.Д., Уткина А.Б., Аксенов С.А., Макурина М.П.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 6 т.21, 2022 года.
Бесплатный доступ
Актуальность. Мезенхимальные опухоли составляют 2 % от всех новообразований пищевода, из них на долю лейомиом приходится до 80 %, которые преимущественно локализуются в нижней трети пищевода. Хирургический метод является основным в лечении данной нозологии. Из-за низкой встречаемости отсутствуют единые подходы к выбору хирургического объема и доступа. Малоинвазивные методики имеют преимущества перед открытыми доступами. Однако целый ряд факторов влияет на принятие решения: размер, локализация и расположение опухоли по окружности пищевода. При небольших новообразованиях с интрамуральной формой роста возможно выполнение эндоскопической резекции. При больших и протяженных лейомиомах показана операция Льюиса. В остальных случаях энуклеация опухоли является золотым стандартом лечения. Вопрос малоинвазивного хирургического доступа является актуальным. При опухолях, расположенных в нижнегрудном отделе пищевода ближе к пищеводно-желудочному переходу, торакоскопический доступ имеет ограничения. В этой связи лапароскопический доступ с возможностью трансхиатальной мобилизации пищевода обеспечивает адекватную возможность для энуклеации опухоли. Описание клинического случая. Нами выполнена лапароскопическая трансхиатальная энуклеация опухоли пищевода у пациентки 47 лет, с лейомиомой нижнегрудного отдела пищевода. Операция выполнена в объеме R0. Период наблюдения составил 12 мес, без признаков рецидива заболевания. Заключение. Данная методика, на наш взгляд, полностью оправдана, при тщательном отборе пациентов и соблюдении всех правил онкохирургии. Лапароскопический доступ с трансхиатальной мобилизацией пищевода обеспечивает хорошую возможность для выполнения энуклеации мезенхимальных опухолей, локализованных в нижней трети грудного отдела, на уровне наддиафрагмального и абдоминального сегмента
Лапароскопическая трансхиатальная энуклеация, лейомиома пищевода, хирургическое лечение
Короткий адрес: https://sciup.org/140296690
IDR: 140296690 | УДК: 616.329-006.363.03-089 | DOI: 10.21294/1814-4861-2022-21-6-170-176
Transhiatal laparoscopic enucleation of lower thoracic esophageal leiomyoma
The purpose of the study. Mesenchymal tumors of the esophagus comprise 2 % of all esophageal tumors. Leiomyosarcoma is the most common mesenchymal tumor in the esophagus (up to 80 %). it is located in the lower third of the esophagus. The main treatment modality of leiomyosarcoma is surgery. Due to the low frequency of occurrence, there are no unified approaches to the choice of surgical volume and access. Minimally invasive techniques have advantages over open approaches. However, final treatment approach depends on many factors: localization and location of the tumor around the circumference of the esophagus, as well as size. Endoscopic resection is feasible for small tumors with an intramural growth. in case of large leiomyomas, Lewis operation should be performed. in all other cases, tumor enucleation is the gold standard of treatment. The issue of minimally invasive surgical access is relevant. Thoracoscopic access has limitations for tumors located in the lower thoracic esophagus closer to the esophageal-gastric junction. in this regard, a laparoscopic approach with the possibility of transhiatal mobilization of the esophagus provides an adequate opportunity for tumor enucleation. Clinical case description. We hereby report our case study in which we employ the use of laparoscopic transhiatal enucleation to remove leiomyoma of the lower thoracic part of the esophagus. A 47-year-old female presented to P.A. Herzen Moscow Oncology Research institute with complaints of pain in the epigastrium, discomfort behind the sternum when taking solid food. R0 resection was performed. During the one year follow-up period no sign of disease recurrence was observed. Conclusion. This approach, in our opinion, is fully justified, with careful selection of patients and compliance with guidelines of cancer surgery. Laparoscopic approach with transhiatal mobilization of the esophagus provides a good opportunity to perform the enucleation of mesenchymal tumors localized in the lower third of the thoracic region, at the level of the supraphrenic and abdominal segments.
Текст научной статьи Трансхиатальная лапароскопическая энуклеация лейомиомы нижнегрудного отдела пищевода
Мезенхимальные опухоли составляют 2 % от всех новообразований пищевода [1], из них на долю лейомиом приходится до 80 % [2], которые преимущественно локализуются в нижней трети пищевода (до 81 %) [3, 4]. Хирургический метод является основным в лечении данной нозологии. Как правило, мезенхимальные новообразования протекают бессимптомно, а клинические симптомы появляются, когда опухоль достигает больших размеров. Одни из первых жалоб, которые предъявляют пациенты, – это чувство инородного тела за грудинной, затруднение глотания пищи, а также, при наличии изъязвления слизистой оболочки пищевода, возможны желудочно-кишечные кровотечения (ЖКК) [3–5].
Основными методами диагностики являются компьютерная томография и эндосонография, позволяющие определить до операции локализацию опухоли в пищеводе, размер, характер роста и строение. Анализ данных с достаточно высокой степенью информативности позволяет сформулировать диагноз [6].
При планировании органосохраняющего лечения морфологическая верификация не обязательна, так как по малым образцам сложно дифференцировать лейомиому от гастроинтестинальной стромальной опухоли [7, 8]. Кроме того, вследствие воспаления в месте биопсии развивается фиброз, который затрудняет энуклеацию опухоли без вскрытия просвета пищевода. Однако при планировании неадъювантного противоопухолевого лечения морфологическая верификация обязательна.
В связи с низкой частотой встречаемости данной категории опухолей отсутствуют единые подходы к выбору хирургического доступа. Малоинвазивные методики имеют преимущества перед открытыми доступами. Однако целый ряд факторов влияет на принятие решения: локализация опухоли в нижнегрудном отделе пищевода, расположение опухоли по окружности пищевода, а также размер лейомиомы.
При небольших новообразованиях (до 4 см) с интрамуральной формой роста возможно выполнение эндоскопической туннельной резекции
[3, 6]. При больших и протяженных лейомиомах показана операция Льюиса. В остальных случаях эндохирургическая энуклеация опухоли является золотым стандартом лечения [9]. Вопрос выбора малоинвазивного хирургического доступа является актуальным. При опухолях, расположенных в нижнегрудном отделе пищевода ближе к пищеводножелудочному переходу, торакоскопический доступ имеет ограничения. В этой связи лапароскопический доступ с возможностью трансхиатальной мобилизации пищевода обеспечивает адекватную возможность для энуклеации опухоли. В подтверждение этого приводим клиническое наблюдение.
Описание клинического случая
Пациентка С., 47 лет, обратилась в МНИОИ им. П.А. Герцена с жалобами на боли в эпигастрии, дискомфорт за грудиной при приеме твердой пищи. По данным ЭГДС с эндосонографией на уровне 35,5 см от резцов, по задней полуокружности визуализирована проксимальная граница субэпителиального образования пищевода, занимающая на этом уровне половину окружности. Дистальнее опухоль переходила на левую и переднюю стенки (до уровня 37 см от резцов), занимая 3/4 окружности, нависая над кардиоэзофагеальным переходом. При инструментальной пальпации опухоль имела мягкую консистенцию. Просвет пищевода сужен не более чем на 1/4. При эндосонографии с датчиком 20 МГц и эхоэндоскопом 6 МГц подтверждено, что образование являлось единым, охватывало циркулярно просвет пищевода на 3/4, анэхогенно, имело гиперэхогенные септы, располагалось в подслизистом слое (рис. 1). По данным СКТ с внутривенным контрастированием – в заднем средостении определялось образование округлой формы с относительно четкими контурами, поперечными размерами 38×36 мм, вертикальным – 52 мм, накапливавшее контрастный препарат в пределах 15HU, на фоне которого прослеживалась слизистая оболочка пищевода и его просвет с газом, без признаков инвазивного роста (рис. 2). Учитывая данные исследования, клинически был выставлен диагноз мезенхимальная опухоль.
29.06.2021 пациентке выполнена лапароскопическая трансхиатальная энуклеация опухоли пищевода. Положение пациентки на операционном столе на спине с разведенными ногами. Под камеру в области пупочного кольца установлен 11-мм троакар. По параректальной линии на уровне пупка установлено 2 5-мм порта справа и слева. Дополнительно было установлено 2 10-мм порта на уровне реберной дуги соответственно (рис. 3). После ревизии была мобилизована левая доля печени рассечением венечной и треугольной связок. Затем была рассечена желудочно-диафрагмальная связка и выполнена сагиттальная диафрагмото-мия. Рассечена правая ножка диафрагмы. Далее произведена мобилизация кардиального отдела
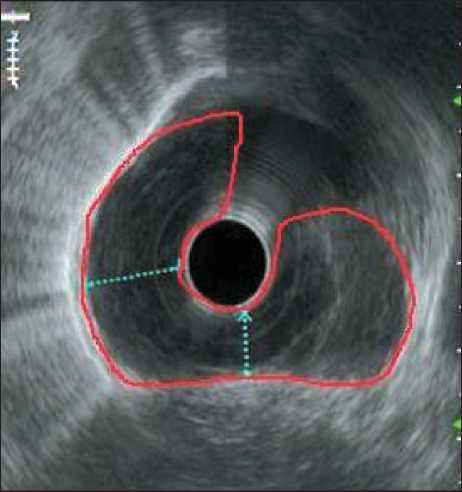
Рис. 1. Эндосонография. Границы опухоли отмечены красной линией
Fig. 1. Endosonography. The borders of the tumor are marked with a red line
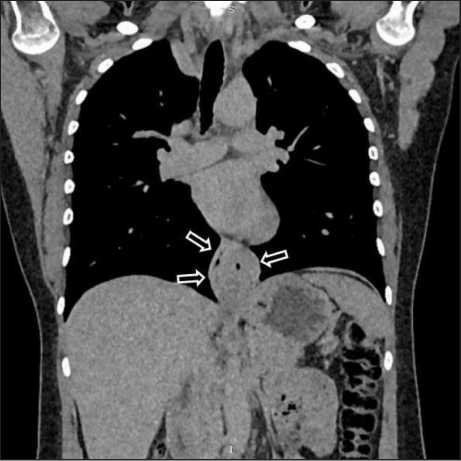
Рис. 2. КТ органов грудной клетки. Опухоль пищевода отмечена стрелками
Fig. 2. CT-scan of the chest. Tumor of the esophagus is marked with arrows
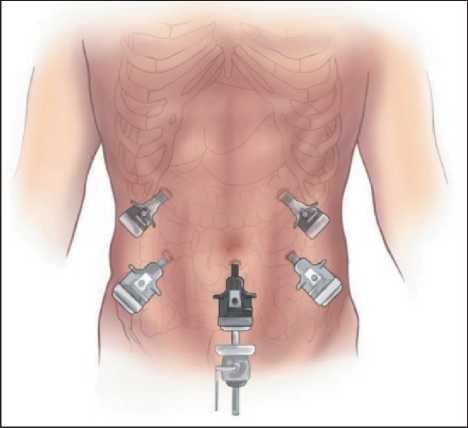
Рис. 3. Схематичное расположение портов
Fig. 3. Schematic diagram of ports
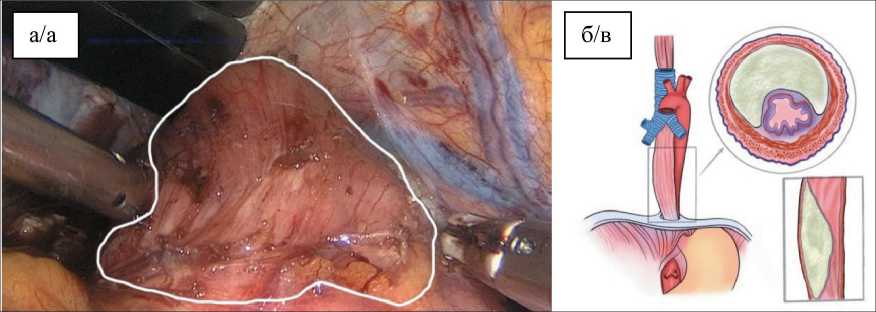
Рис. 4. Мобилизована н/3 пищевода и зона КЭП с опухолью:
а – интраоперационная фотография (выделена белой линией); б – схематичное изображение Fig. 4. Low third of the esophagus and zone of cardioesophageal junction (CEJ) with tumor were mobilized: a – intraoperative photograph (white line), b – schematic image
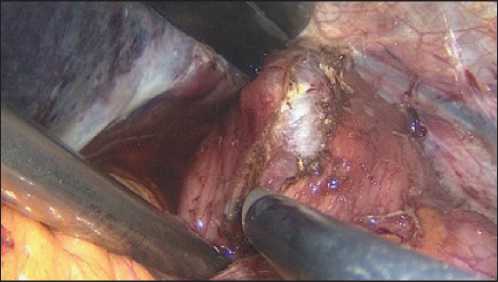
Рис. 5. Рассечение мышечного слоя пищевода
Fig. 5. Dissection of the muscular layer of the esophagus
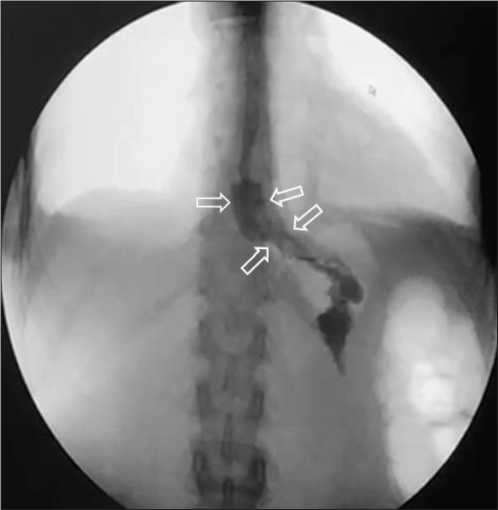
Рис. 6. Рентгеноскопия с пероральным контрастированием н/3 пищевода и КЭП после операции
Fig. 6. Radioscopy with oral contrast of the low third of the esophagus and CEJ after surgery
При морфологическом исследовании – опухоль построена из разнонаправленных пучков, образованных веретеновидными клетками, с эозинофильной цитоплазмой, сигароподобными вытянутыми ядрами. Опухоль четко ограничена от окружающей жировой клетчатки. Митотическая активность в опухоли не выражена. По результатам иммуногистохимического (ИГХ) исследования – положительная экспрессия в опухолевых клетках: SMA, Desmin. Отрицательная экспрессия: CD117, CD34, DOG1. ИГХ картина соответствует лейомиоме пищевода.
С учетом радикальности хирургического вмешательства и морфологии опухоли дополнительное противоопухолевое лечение не показано, рекомендовано динамическое наблюдение. Срок наблюдения – 12 мес. По результатам контрольного обследования данных за рецидив заболевания не выявлено. Жалоб пациентка не предъявляет.
Обсуждение
При лейомиомах пищевода хирургическое лечение в объеме энуклеации опухоли показано в случае симптомного течения заболевания, быстром темпе роста или при размерах опухоли более 3 см [6, 10]. Если не планируется неоадъювантная терапия, то морфологическая верификация не обязательна, поскольку это не меняет тактику лечения [11]. Обязательными требованиями к органосохраняющему хирургическому лечению являются радикальное удаление опухоли без повреждения ее капсулы, блуждающих нервов и попытка сохранения слизистой оболочки пищевода.
В настоящее время имеется большой арсенал хирургических доступов и методик при мезен-хиамальных опухолях пищевода. С развитием малоинвазивной хирургии в последнее время все реже и реже стал применяться открытый доступ. В основном открытая хирургия используется при местнораспространенных опухолях, когда выполняется операция Льюиса. Применение эндоскопических методов удаления опухоли имеет ряд ограничений, это небольшие опухоли до 3–4 см в диаметре, с четкими ровными контурами, которые располагаются в подслизистом слое. В данном клиническом примере применение метода туннельной резекции было невозможно из-за того, что опухоль циркулярно охватывала весь пищевод.
В классических случаях опухоли верхне- и среднегрудного отделов пищевода удаляются торакоскопическим доступом справа. При нижнегрудной локализации выбор доступа определен
Список литературы Трансхиатальная лапароскопическая энуклеация лейомиомы нижнегрудного отдела пищевода
- Sanchez-Garcia Ramos E., Cortes R., de Leon A.R., ContrerasJimenez E., Rodríguez-Quintero J.H., Morales-Maza J., Aguilar-Frasco J., Irigoyen A., Reyes F., Alfaro-Goldaracena A. Esophageal schwannomas: A rarity beneath benign esophageal tumors a case report. Int J Surg Case Rep. 2019; 58: 220-3. https://doi.org/10.1016/j.ijscr.2019.03.038.
- Kitada M., Matsuda Y., Hayashi S., Ishibashi K., Oikawa K., Miyokawa N. Esophageal schwannoma: a case report. World J Surg Oncol. 2013; 11: 253. https://doi.org/10.1186/1477-7819-11-253.
- Pence K., Correa A.M., Chan E., Khaitan P., Hofstetter W., Kim M.P. Management of esophageal gastrointestinal stromal tumor: review of one hundred seven patients. Dis Esophagus. 2017; 30(12): 1-5. https://doi.org/10.1093/dote/dox064.
- Jesić R., Randjelović T., Gerzić Z., Zdravković Dj., Krstić M., Milinić N., Pavlović A., Svejić T., Bulajić M. [Leiomyoma of the esophagus. Case report]. Srp Arh Celok Lek. 1997; 125(3-4): 113-5.
- Kobayashi N., Kikuchi S., Shimao H., Hiki Y., Kakita A., Mitomi H., Ohbu M. Benign esophageal schwannoma: report of a case. Surg Today. 2000; 30(6): 526-9. https://doi.org/10.1007/s005950070120.
- Wang G.X., Yu G., Xiang Y.L., Miu Y.D., Wang H.G., Xu M.D. Submucosal tunneling endoscopic resection for large symptomatic submucosal tumors of the esophagus: A clinical analysis of 24 cases. Turk J Gastroenterol. 2020; 31(1): 42-8. https://doi.org/10.5152/tjg.2020.19062.
- Rösch T., Kapfer B., Will U., Baronius W., Strobel M., Lorenz R., Ulm K.; German EUS Club. Endoscopic ultrasonography. Accuracy of endoscopic ultrasonography in upper gastrointestinal submucosal lesions: a prospective multicenter study. Scand J Gastroenterol. 2002; 37(7): 856-62.
- Dumonceau J.M., Deprez P.H., Jenssen C., Iglesias-Garcia J., Larghi A., Vanbiervliet G., Aithal G.P., Arcidiacono P.G., Bastos P., Car-rara S., Czakó L., Fernández-Esparrach G., Fockens P., Ginès À., Havre R.F., Hassan C., Vilmann P., van Hooft J.E., Polkowski M. Indications, results, and clinical impact of endoscopic ultrasound (EUS)-guided sampling in gastroenterology: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline - Updated January 2017. Endoscopy. 2017; 49(7): 695-714. https://doi.org/10.1055/s-0043-109021.
- Mujawar P., Pawar T., Chavan R.N. Video Assisted Thoracoscopic Surgical Enucleation of a Giant Esophageal Leiomyoma Presenting with Persistent Cough. Case Rep Surg. 2016. https://doi.org/10.1155/2016/7453259.
- Milito P., Asti E., Aiolf A., Zanghi S., Siboni S., Bonavina L. Clinical Outcomes of Minimally Invasive Enucleation of Leiomyoma of the Esophagus and Esophagogastric Junction. J Gastrointest Surg. 2020; 24(3): 499-504. https://doi.org/10.1007/s11605-019-04210-3.
- Andrási L., Szepes Z., Tiszlavicz L., Lázár G., Paszt A. Complete laparoscopic-transhiatal removal of duplex benign oesophageal tumour: case report and review of literature. BMC Gastroenterol. 2021; 21(1): 47. https://doi.org/10.1186/s12876-021-01625-8.
- Asti E., Siboni S., Sironi A., Barbieri L., Bonavina L. Minimally invasive surgery for submucosal benign esophageal tumors: indications, preoperative investigations, patient selection, and clinical outcomes. Ann Laparosc Endosc Surg. 2019; 4. https://doi.org/10.21037/ales.2019.06.13.
- Thakut G., Murchite S.A., Kulkarni R.M., Gaikwad V.V. Leiomyoma of esophagus-A case report. Int J Surg Case Rep. 2020; 76: 285-287. https://doi.org/10.1016/j.ijscr.2020.09.142.


