Трансоральный преднижнечелюстной видеоассистированный доступ к щитовидной железе в эксперименте
Автор: Шулутко А.М., Семиков В.И., Гряэнов С.Е., Сердюк А.А., Горбачева О.Ю.
Журнал: Московский хирургический журнал @mossj
Рубрика: Экспериментальные и лабораторные исследования
Статья в выпуске: 1 (35), 2014 года.
Бесплатный доступ
В рамках такого перспективного направления в малоинвазивной хирургии, как NOTES, абсолютно оправданным становится поиск новых оперативных подходов к щитовидной и паращитовидным железам. В статье представлены первые наблюдения и результаты, полученные в ходе разработки трансорального преднижнечелюстного видеоассистированного безгазового доступа и вмешательства на щитовидной железе в эксперименте на 10 человеческих трупах. Лейтмотивом работы на данном этапе можно считать то, что предлагаемый доступ вполне осуществим в клинической практике со стороны хирургической техники и оборудования, а также оправдан как достаточно малотравматичный доступ с хорошим косметическим результатом, однако требует дальнейшего изучения.
Эндоскопическая тиреоидэктомия, трансоральный доступ
Короткий адрес: https://sciup.org/142211135
IDR: 142211135 | УДК: 616-089;
Текст научной статьи Трансоральный преднижнечелюстной видеоассистированный доступ к щитовидной железе в эксперименте
Повсеместное стремление к минимально инвазивным вмешательствам – неизбежный процесс эволюции хирургической практики. Эндоскопические технологии, активно применяемые во всех областях хирургии, позволили по новому взглянуть и на подходы к тиреоидной хирургии. В первую очередь это касается минимизации операционной травмы, уменьшения или полного исключения косметического дефекта на шее больного. Первые экспериментальные разработки альтернативных доступов к щитовидной и паращитовидным железам выполнены в конце 90-х годов на животных [1–3]. В 1996 году М. Gagner впервые описал эндоскопическое субтотальное удаление паращитовидных желез у больного гиперпаратиреозом [4], а C.S.G. Huscher в том же году через боковой шейный доступ эндоскопически удалил правую долю щитовидной железы [5]. В последующие годы интерес к эндовидеохирургическим вмешательствам на щитовидной железе только возрастал. Разработаны различные варианты отдаленных доступов, позволяющие избежать кожного разреза на шее, – подмышечный, параареолярный, грудной, поднижнечелюстной, комбинированные методы, при которых рабочее пространство создается посредством инсуфляции СО2 или методом лифтинга кожного лоскута [6–12]. Отдельной строкой можно упомянуть о робот-ассистированных операциях [13, 14].
Наряду с эндоскопическими вмешательствами, так или иначе выполняемыми через разрезы на коже, новой ветвью развития малоинвазивной хирургии в последние годы становится NOTES (Natural Orifice Transluminal Endoscopic Surgery) [15, 16]. Непосредственная близость органов шеи к ротовому отверстию делает это направление перспективным в отношении хирургии щитовидной и паращитовидных желез. Впервые трансоральная видеоассистированная тиреоидэктомия (TOVAT) выполнена К. Witzel с соавт. в 2007 году на свиньях [17], а в 2009 году Т. Benhidjeb с соавт. сообщили о первых экспериментальных работах на человеческих трупах [18]. В этих исследованиях доступ к переднему отделу шеи осуществлялся через дно полости рта с созданием рабочего пространства путем инсуфляции СО2.
В клинической практике трансоральный подъязычный доступ к щитовидной железе впервые осуществлен Т. Wilhelm и А. Metzig в 2009 году. Методика получила название ЕMIT (Endoscopic Minimally Invasive Thyroidectomy) и была выполнена у 8 пациентов [19]. В 2012 году группа японских хирургов под руководством А. Nakajo сообщила о результатах применения в клинической практике новой техники трансоральной эндоскопической тиреоидэктомии, получившей аббревиатуру TOVANS (Transoral Videoassisted Neck Surgery), отличием которой стали предниж-нечелюстной доступ в преддверии рта и создание рабочего пространства на передней поверхности шеи методом лифтинга, без инсуфляции СО2 [20].
В нашей стране также имеется ряд работ, посвященных миниинвазивным эндовидеохирургическим вмешательствам на щитовидной и паращитовидных железах [21–25], в том числе и экспериментальная работа по трансоральному подъязычному доступу на человеческих трупах [26].
У всех вышеизложенных методик можно отметить одно значимое преимущество перед традиционным доступом Т. Кохера – высокий косметический результат операции. Однако для адекватной оценки эффективности хирургического вмешательства необходимо учитывать и такие параметры, как травматичность, продолжительность вмешательства, качество жизни пациента в послеоперационном периоде, стресс-реакция организма и др. Исследования в этой области свидетельствуют о том, что по ряду основных параметров эндоскопические вмешательства из отдаленных доступов на щитовидной и паращитовидных железах существенно не отличаются от традиционной операции [27–29].
С нашей точки зрения, наибольшего интереса заслуживает трансоральный доступ, разработанный японскими хирургами [20]. Он эстетичен, малотравматичен, не требует инсуфляции СО2 и специального оборудования. Однако сопряжен с определенными техническими трудностями, обусловленными пространственным соотношением инструментов. Расположенные практически параллельно, инструменты «конфликтуют» друг с другом и между ними невозможно создание эффективной триангуляции. Это приводит к неудобству выполнения операции, увеличению времени вмешательства и требует либо определенного навыка, либо инструментов с изогнутой рабочей частью.
Нашей целью явилась разработка и хирургическое обоснование трансорального преднижнечелюстного ви-деоассистированного безгазового доступа к щитовидной железе, модифицированного установкой дополнительного рабочего инструмента через прокол на боковой поверхности шеи.
Материалы и методы
В период с октября по декабрь 2013 г. отработка техники доступа и вмешательства на щитовидной железе выполнена на 10 человеческих трупах обоих полов в возрасте 54–82 лет. У всех объектов время смерти не превышало период 24 часов до начала эксперимента и отсутствовали какие-либо повреждения или патологические процессы в полости рта и в области шеи.
На первых 3 анатомических объектах нами была отработана исключительно техника доступа, включающая в себя разрез в преддверии рта, создание подкожного туннеля и рабочего пространства на передней поверхности шеи методом лифтинга. На следующих 7 объектах помимо доступа выполняли вмешательство на щитовидной железе, ограниченное в 6 случаях гемитиреоидэктомией и в 1 случае выполнена тиреоидэктомия. С целью топографической ориентации, у 4 объектов перед трансоральным доступом мы выполняли разрез на шее по Кохеру с препарированием доли щитовидной железы и маркировкой цветными нитями анатомически важных структур – верхней и нижней щитовидных артерий, вены среднего сплетения и возвратного гортанного нерва. Все препараты извлекали через разрез в преддверии рта. В одном из восьми удаленных препаратов было обнаружено узловое образование диаметром 2 см.
Оборудование, используемое в нашей работе, представлено видеокамерой и осветителем (Электрон, Россия), монитором (Izumi, Россия), лапароскопическим эндоскопом диаметром 10 мм с прямой оптикой и набором стандартных лапароскопических инструментов диаметром 5 мм (Endopath, Ethicon Endo-surgery, Germany). Коагуляцию при диссекции тканей и пересечении сосудов в эксперименте не проводили в связи с отсутствием необходимости. В клинической практике с этой целью предполагается использование ультразвукового скальпеля Harmonic.
Для имитации эндотрахеального наркоза в трахею объекта через рот вводили интубационную трубку, которую фиксировали к щеке пластырем. Оперирующий хирург с ассистентом располагались в изголовье объекта. Последний лежит на спине с запрокинутой головой и открытым ртом. Нижнюю губу оттягивали кпереди мягким зажимом и выполняли разрез слизистой оболочки длиной около 2 см в преддверии полости рта, в центре между нижней губой и десной (рис. 1). Под контролем зрения частично рассекали и латерально раздвигали пучки подбородочной мышцы, продвигаясь к подбородочному выступу, а затем, огибая выступ, проникали под подкожную мышцу шеи, рассекая ее в том месте, где она прикрепляется к нижнему краю нижней челюсти (рис. 2).
На данном этапе нами уделено внимание такой анатомической характеристике, как форма базальной дуги нижней челюсти. Согласно типовым различиям в строении нижней челюсти, различают длинную и узкую базальную дугу, короткую, широкую и промежуточную форму [30]. При двух последних вариантах вышеописанный этап не представляет каких либо трудностей. При длинной и узкой форме (выступающий подбородок), за счет острого угла между наружной
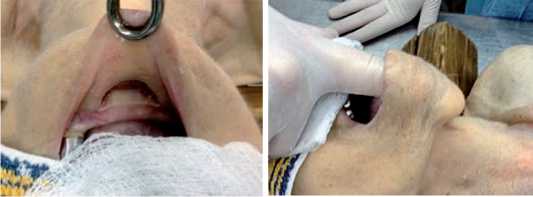
Рис. 1. Разрез в преддверии Рис. 2. Создание подкожного полости рта туннеля поверхностью тела нижней челюсти и подподбородочной областью, проникновение в подподбородочный треугольник занимает больше времени.
Далее, тупым и острым путем, используя диссектор и ножницы, под контролем эндоскопа отслаивали подкожную мышцу шеи в краниокаудальном направлении по срединной линии от подбородочного выступа до яремной вырезки и в латеральном направлении до медиального края грудиноключично-сосцевидной мышцы (рис. 3). В случае гемитиреоидэктомии отслойку производили монолатерально, в случае тиреоидэктомии – билатерально. В процессе отслойки, на уровне верхнего края щитовидного хряща горизонтально чрезкожно под подкожной мышцей шеи проводили первую спицу Киршнера, при тракции за которую создавали достаточный обзор для дальнейшей отслойки (рис. 4). На уровне перстневидного хряща аналогично первой проводили вторую спицу Киршнера. Спицы фиксировали в скобах Киршнера, которые подтягивали кпереди, достигая необходимого рабочего пространства, и фиксировали на L-образной операционной дуге. Созданная таким образом полость ограничена сверху подкожной мышцей шеи, а дно представлено передней поверхностью трахеи, грудино-подъязычной и грудино-щитовидной мышцами (рис. 5). На стороне, противоположной от оперируемой доли щитовидной железы, в точке входа (или выхода) второй спицы Киршнера, на переднебоковой поверхности шеи через прокол кожи устанавливали 5-мм троакар для рабочего инструмента (рис. 6).
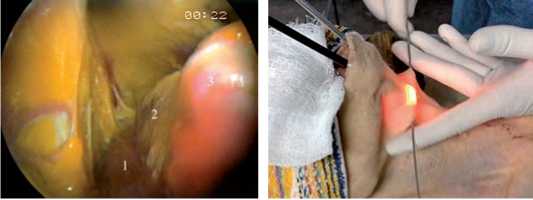
Рис. 3. Создание туннеля под подкожной мышцей шеи:
1 – грудино-подъязычная мышца;
2 – трахея; 3 – щитовидный хрящ
Рис. 4. Проведение спицы Киршнера
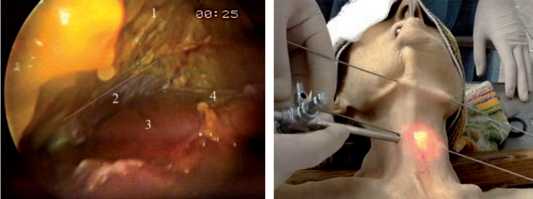
Рис. 5. Рабочее пространство:
1 – подкожная мышца шеи;
2 – медиальный край грудиноключично-сосцевидной мышцы;
3 – грудино-подъязычная и грудино-щитовидная мышцы; 4 – трахея
Рис. 6. Установка троакара на шее
Установка троакара на шее позволяет создать эффективный угол между браншами инструментов, равный практически 90°. Грудино-подъязычную и грудино-щитовидную мышцы, прикрывающие долю щитовидной железы, отводили кпереди и латерально и фиксировали к стенке рабочей полости прошиванием через кожу. После диссекции от трахеи пересекали перешеек щитовидной железы и приступали к мобилизации доли. Осуществляя переднекаудальную тракцию доли зажимом, установленным через троакар на шее, выделяли верхний полюс и пересекали верхние щитовидные сосуды (рис. 7). Подтягивая долю медиально, выделяли боковую поверхность и пересекали вену среднего сплетения. При этом становилась доступной осмотру боковая поверхность трахеи, где находили возвратный гортанный нерв (рис. 8). После этого мобилизовали нижний полюс (рис. 9). После пересечения нижних щитовидных сосудов долю удаляли через разрез в преддверии полости рта. К ложу удаленной доли проводили трубчатый дренаж по Редону через троакар на шее. Троакар и спицы Киршнера удаляли. Разрез в преддверии рта зашивали наглухо. Область оперативного вмешательства, расположение рабочих инструментов, эндоскопа и спиц представлены на схеме (рис. 10).
Результаты
В ходе экспериментальной работы нами достигнуто практическое понимание того, что трансоральный предниж-нечелюстной видеоассистированный безгазовый доступ к щитовидной железе выполним в клинической практике как технически, так и с точки зрения анатомо-топографических k 00:54
t r

Рис. 7. Мобилизация верхнего полюса левой доли:
1 – левая доля щитовидной железы; 2 – верхний полюс доли;
3 – верхняя щитовидная артерия;
4 – грудино-подъязычная мышца, фиксированная к коже
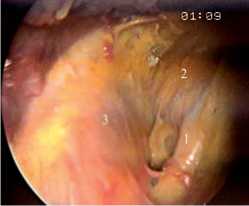
Рис. 8. Боковая поверхность трахеи, место локализации ВГН (левая доля отведена медиально): 1 – возвратный гортанный нерв;
2 – трахея; 3 – сонная артерия
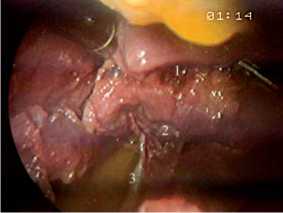
Рис. 9. Мобилизация нижнего полюса левой доли:
1 – левая доля щитовидной железы; 2 – нижний полюс доли;
3 – нижняя щитовидная артерия
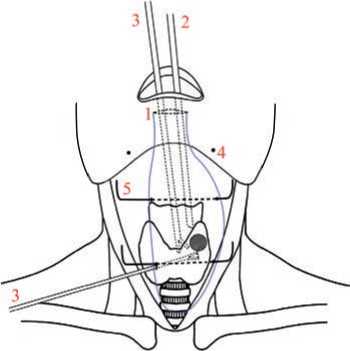
Рис. 10. Схема операции:
1 – разрез в преддверии полости рта; 2 – эндоскоп; 3 – рабочий инструмент; 4 – точка выхода подбородочного нерва; 5 – спица Киршнера Синей линией очерчена область отслойки кожного лоскута (рабочее пространство)
особенностей. Вмешательство на щитовидной железе так же технически выполнимо из предлагаемого доступа. При этом дополнительный рабочий инструмент, установленный через троакар на шее, создает оптимальные условия для манипулирования, тракции и диссекции в рабочей области.
Из 10 проведенных операций 3 выполнены в условиях, максимально приближенных к реальным, без предварительного разреза на коже и маркировки основных структур. Время, затраченное на гемитиреоидэктомию, в этих случаях составило 102 мин., 91 мин., и 75 мин. соответственно.
Краниокаудальный ракурс обзора рабочей зоны достаточен для определения всех важных анатомических структур – верхних и нижних щитовидных сосудов, возвратного гортанного нерва. В 4 случаях с предварительной маркировкой цветными нитями все структуры были определены через эндоскоп с прямой оптикой. У объектов без маркировки во всех случаях были доступны обзору верхние и нижние щитовидные сосуды, в 2 случаях – возвратный гортанный нерв. В дальнейшем, мы считаем целесообразным использовать угловую оптику (30°), поскольку при этом возможно создание лучшего угла обзора боковой поверхности трахеи и места локализации возвратного гортанного нерва.
Применение доступа в клинической практике потребует эффективной коагуляции в силу хорошего кровоснабжения тканей шеи и щитовидной железы, что, на наш взгляд, может быть достигнуто использованием ультразвукового скальпеля Harmonic. Однако мы не исключаем возможности клипирования основных сосудов и использования биполярной коагуляции.
Доступ можно считать малотравматичным, поскольку отслойка кожного лоскута производится на меньшей площади по сравнению, например с параареолярным и подмы- шечным доступами. Мышечные структуры также подвергаются минимальной травме – частично надсекаются пучки подбородочной мышцы и платизмы в области подбородочного выступа. Создание рабочего пространства осуществляется путем эндолифтинга и не требует инсуфляции CO2, что исключает возможные осложнения в виде эмфиземы шеи и средостения, эмболии сосудов. В клинической практике стоит ожидать нарушение чувствительности в подбородочной области и отек передней области шеи. В статье А. Nakajo с соавт. приведены данные об уменьшении отека в течении нескольких дней и восстановлении чувствительности в подбородочной области в течении 6 мес. после операции [20].
Двухсантиметровый разрез в преддверии полости рта мы считаем вполне достаточным для удаления препарата с размером узлового образования 2–3 см. При этом не исключаем возможности интракорпорального фрагментирования и удаления препарата в контейнере.
Доступ предполагает хороший косметический результат операции. Повреждения кожных покровов на передней поверхности шеи ограничиваются проколом для 5 мм троакара (в будущем возможно использование 3 мм инструмента) и точечными проколами от спиц и фиксирующих лигатур. Порт на шее, помимо прочего, служит и для выведения дренажной трубки с целью контроля гемостаза в послеоперационном периоде.
Немаловажным фактом является то, что вмешательство на щитовидной железе из предлагаемого доступа выполнимо с использованием стандартных лапароскопических инструментов и оборудования. Нет необходимости в специальных ранорасширителях и инструментах, эндолифтинг осуществляется с использованием стандартных спиц и скоб Киршнера.
Заключение
Оценивая альтернативные хирургические доступы к щитовидной и паращитовидным железам, очевидным становится тот факт, что все они направлены на уменьшение или исключение косметического дефекта на шее пациента, а в ряде случаев и уменьшение операционной травмы по сравнению с традиционным доступом. Однако по отношению друг к другу обладают как преимуществами, так и недостатками. В рамках такого перспективного направления в хирургии, как NOTES, предлагаемый трансоральный преднижнечелюстной видеоассистированный безгазовый доступ может занять свою нишу и стать методом выбора у определенной категории пациентов с заболеваниями щитовидной и паращитовидных желез. Особенности вмешательства требуют более скрупулезной оценки анатомотопографических критериев, влияющих на выполнимость метода, и продолжения отработки техники на трупах перед внедрением доступа в клиническую практику.
Список литературы Трансоральный преднижнечелюстной видеоассистированный доступ к щитовидной железе в эксперименте
- Brunt L.M., Jones D.B., Wu J.S. et al. Experimental development of an endoscopic approach to neck exploration and parathyroidectomy//Surgery. 1997. Vol. 122. P. 893-901.
- Kanauchi H., Yamasaki K., Ogawa T. et al. Endoscopic thyroidectomy in a porcine//Endocr. J. 1998. Vol. 45, № 1 P. 135-136.
- Jones D.B., Quasebarth M.A., Brunt L.M. Videoendoscopic thyroidectomy: experimental development of a new technique//Surg. Laparosc. Endosc. Percutan. Tech. 1999. Vol. 9, № 3 P. 167-170.
- Gagner M. Endoscopic subtotal parathyroidectomy in patients with primary hyperparathyroidism//Br. J. Surg. 1996. Vol. 83. P. 875.
- Huscher CSG., Chiodini S., Napolitano C. et al. Endoscopic right thyroid lobectomy//Surg. Endosc. 1997. Vol. 11, № 8. P. 877.
- Yeung G.H. Endoscopic surgery of the neck: a new frontier//Surg. Laparosc. Endosc. 1998. Vol. 8. P. 227-232.
- Miccoli P., Berti P., Raffaelli M. et al. Minimally invasive video-assisted thyroidectomy//Am. J. Surg. 2001. Vol. 181. P. 567-570.
- Ohgami M., Ishii S., Arisawa Y. et al. Scarless endoscopic thyroidectomy: breast approach for better cosmetics//Surg. Laparosc. Endosc. Percutan. Tech. 2000. Vol. 10, № 1. P. 1-4.
- Ikeda Y., Takami H., Sasaki Y. et al. Endoscopic neck surgery by the axillary approach//J. Am. Coll. Surg. 2000. Vol. 191. P. 336-340.
- Shimazu K., Shiba E., Tamaki Y. et al. Endoscopic thyroid surgery through the axillo-bilateral-breast approach//Surg. Laparosc. Endosc. Percutan. Tech. 2003. Vol. 13, №3. P. 196-201.
- Yamashita H., Watanabe S., Koike E., Ohshima A., Uchino S., Kuroki S. et al. Video-assisted thyroid lobectomy through a small wound in the submandibular area//Am. J. Surg. 2002. Vol. 183. P. 286289.
- Shimazu K., Kitagawa W., Akasu H., Tanaka S. Video-assisted endoscopic endocrine neck surgery with a benefit of cosmesis: a new technique using a totally gasless anterior neck skin lifting method//J. Nippon. Med. Sch. 2002. Vol. 69, №1. P. 2-3.
- Kang S.W., Lee C.H., Lee S.H., Lee K.Y., Jeong J.J., Lee Y.S., Nam K.H., Chang H.S., Chung W.Y., Park C.S. Robotic thyroid Surgery using a gasless, transaxillary approach and the da Vinci S system: the operative outcomes of 338 consecutive patients//Surgery. 2009. Vol. 146. P. 1048-1055.
- Lee K.E., Rao J., Youn Y.K., Endoscopic thyroidectomy with the da Vinci robotic system using the bilateral axillary breast approach (BABA. technique: our initial experience//Surg. Laparosc. Endosc. Percutan. Tech. 2009. Vol. 19. P. 71-75.
- ASGE/SAGES Working Group on Natural Orifice Translumenal Endoscopic Surgery White Paper October 2005//Gastrointest. Endosc. 2006. Vol. 63. P. 199-203.
- Forgione, Antonello, Zorron, Ricardo. NOTES: Basic and advanced surgical applications outside of the urological field//Archivos Espanoles de Urologia. 2012. Vol. 65, №3. P. 423-433.
- Witzel K., Rahden BHA., Kaminski C., Stein H.J. Transoral access for endoscopic thyroid resection//Surg. Endsoc. 2008. Vol. 22. P. 1871-1875.
- Benhidjeb T., Wilhelm T., Harlaar J., Kleinrensink G.J., Schneider T.A., Stark M. Natural orifice surgery on thyroid gland: totally transoral video-assisted thyroidectomy (TOVAT.: report of first experimental results of a new surgical method//Surg. Endosc. 2009. Vol. 23. P. 1119-1120.
- Wilhelm T., Metzig A. Endoscopic Minimally Invasive Thyroidectomy (eMIT.: A Prospective Proof-of-Concept Study in Humans//World J. Surg. 2011. Vol. 35 P. 543-551.
- Nakajo А., Arima H., Hirata M., Mizoguchi T., Kijima Y., Mori S., Ishigami S., Ueno S., Yoshinaka H., Natsugoe S. Trans-Oral Video-Assisted Neck Surgery (TOVANS. A new transoral technique of endoscopic thyroidectomy with gasless premandible approach//Surg. Endosc. 2012. DOI 10.1007/s00464-012-2588-6.
- Егиев В.Н. с соавт. Проблемы и перспективы эндовидеохирургических вмешательств при узловых образованиях щитовидной железы//Хирургия. 2004. №6. С. 59-62.
- Емельянов С.И., Хатьков И.Е., Кумахов Р.Б. Малоинвазивные технологии в лечении узловых новообразований щитовидной железы//Эндоскопическая хирургия. 2002. №4. С. 42-45.
- Колосюк В.А., Романчишен А.Ф. Эндовидеохирургия щитовидной и паращитовидных желез//Вестник хирургии. 2004. №163. С. 97-99.
- Цуканов Ю.Т., Цуканов А.Ю. Варианты и результаты эндоскопической хирургии щитовидной железы//Эндоскопическая хирургия. 2006. №2. С. 149.
- Решетов И.В., Чиссов В.И. Опыт применения видеоассистированных технологий в хирургии щитовидной железы//Эндоскопическая хирургия. 2004. №1. С. 137.
- Сиркис М.А. Анатомо-хирургическое обоснование трансорального доступа к щитовидной и паращитовидным железам (экспериментальное исследование. Дис..кан. мед. наук. Санкт-Петербург, 2011.
- Chen X., Peng B., Gong R., Wang L., Liao B., Li C. Meta analysis. Endoscopic thyroidectomy: an evidence-based research on feasibility, safety and clinical effectiveness//Chin. Med. J. 2008. Vol. 121, № 20. P. 2088-2094.
- Cui W., Zuo F., Chen G., et al. The trauma and stress reaction following endoscopic thyroidectomy//Journal of laparoscopic surgery. 2011. Vol. 8. P. 608-610.
- Lombardi C.P., Raffaelli M., Princi P., Lulli P., Rossi E.D., Fadda G., Bellantone R. Safety of video-assisted thyroidectomy versus conventional surgery//Head Neck. 2005. Vol. 27, № 1. P. 58-64.
- Анатомия человека: учебник для стоматологических факультетов медицинских вузов./Под ред. Колесникова Л.Л., 4-е изд., перераб. и доп. 2010. 816 с.


