Трифенилсурьма и пентафенилсурьма - исходные соединения в синтезе фенильных производных пятивалентной сурьмы. Строение трифенилсурьмы, бис(3,4-дифторбензоато)трифенилсурьмы и карбоната тетрафенилсурьмы
Автор: Ефремов Андрей Николаевич, Шарутин Владимир Викторович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия элементоорганических соединений
Статья в выпуске: 2 т.14, 2022 года.
Бесплатный доступ
В настоящей работе уточнено строение трифенилсурьмы (1). Взаимодействием эквимолярных количеств сольвата пентафенилсурьмы (Ph5Sb∙0,5PhH) (2) с 3,4-дифторбензойной кислотой в бензоле получена и структурно охарактеризована бис(3,4-дифторбензоато)трифенилсурьма Ph3Sb[OC(O)C6H3F2-3,4]2 (3). А также уточнено строение триклинной модификации карбоната тетрафенилсурьмы (4). По данным рентгеноструктурного анализа, проведенного при 293 К на автоматическом четырехкружном дифрактометре D8 Quest Bruker (двухкоординатный CCD - детектор, Мо Kα-излучение, λ = 0,71073 Å, графитовый монохроматор), кристаллы характеризуются: C36H30Sb2 (1), M 706,10; сингония триклинная, группа симметрии Р1 ; параметры ячейки: a = 10,941(11), b = 11,825(16), c = 13,747(13) Å; a = 102,57(5)°, β = 104,22(5)°, g = 108,35(6)°; V = 1550(3) Å3; Z = 2; размер кристалла 0,5 × 0,44 × 0,11 мм; интервалы индексов отражений -13 ≤ h ≤ 14, -15 ≤ k ≤ 15, -17 ≤ l ≤ 17; всего отражений 37455; независимых отражений 6837; Rint 0,0252; GOOF 1,121; R1 = 0,0257, wR2 = 0,0605; остаточная электронная плотность -0,84/0,23 e/Å3; C32H21O4F4Sb (3), M 667,24; сингония моноклинная, группа симметрии С2/с; параметры ячейки: a = 12,652(5), b = 22,466(10), c = 11,561(5) Å; β = 120,027(15)°; V = 2845(2) Å3; Z = 4; размер кристалла 0,5×0,45×0,12 мм; интервалы индексов отражений -16 ≤ h ≤ 16, -28 ≤ k ≤ 28, -14 ≤ l ≤ 14; всего отражений 27275; независимых отражений 3163; Rint 0,029; GOOF 1,107; R1 = 0,0372, wR2 = 0,1058; остаточная электронная плотность 1,61/-0,53 e/Å3; C49H40O3Sb2 (4), M 920,31; сингония триклинная, группа симметрии Р1 ; параметры ячейки: a = 10,093(4), b = 13,994(5), c = 15,665(6) Å; a = 73,917(15)°, β = 79,76(2)°, g = 74,312(15)°; V = 2034,0(13) Å3; Z = 2; размер кристалла 0,26 × 0,22 × 0,05 мм; интервалы индексов отражений -12 ≤ h ≤ 12, -17 ≤ k ≤ 17, -20 ≤ l ≤ 20; всего отражений 50553; независимых отражений 9006; Rint 0,0333; GOOF 1,066; R1 = 0,0239, wR2 = 0,0522; остаточная электронная плотность -0,43/0,77 e/Å3. Атомы сурьмы в 3 имеют искаженную тригонально-бипирамидальную координацию с атомами кислорода в аксиальных положениях (угол OSbO - 174,13(12)°, расстояния Sb-С и Sb-O составляют 2,101(3)-2,118(4) Å и 2,118(3) Å). Структурная организация в кристаллах 3 и 4 обусловлена слабыми межмолекулярными контактами типа О···Н-C 2,49 и 2,56 Å соответственно. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2117872 для 1, № 2121388 для 3, № 2121833 для 4; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Сольват, пентафенилсурьма, бензол, бис(3, 4-дифторбензоато)трифенилсурьма, синтез, строение, трифенилсурьма, карбонат тетрафенилсурьмы, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147237503
IDR: 147237503 | УДК: 546.865+547.47+548.312.5
Triphenylantimony and pentaphenylantimony as initial compounds in the synthesis of pentavalent antimony phenyl derivatives. Structure of triphenylantimony, bis(3,4-difluorobenzoato)triphenylantimony and tetraphenylantimony carbonate
In this work, the structure of triphenylantimony (1) has been clarified. By the interaction of equimolar amounts of pentaphenylantimony solvate (Ph5Sb∙0.5PhH, 2) with 3,4-difluorobenzoic acid in benzene Bis(3,4-difluorobenzoato)triphenylantimony Ph3Sb[OC(O)C6H3F2-3,4]2 (3) has been obtained for structural characterization. The structure of the triclinic modification of tetraphenylantimony carbonate (4) has also been clarified. According to the data of X-ray diffraction analysis carried out at 293 K on an automatic four-circle D8 Quest Bruker diffractometer (two-coordinate CCD detector, MoKα radiation, λ = 0.71073 Å, graphite monochromator), the crystals are characterized as follows: C36H30Sb2 (1), M 706.10; triclinic system, space group Р1 ; cell parameters: a = 10.941(11), b = 11.825(16), c = 13.747(13) Å; a = 102.57(5)°, β = 104.22(5)°, g = 108.35(6)°; V = 1550(3) Å3; Z = 2; crystal size 0.5×0.44×0.11 mm; index ranges -13 ≤ h ≤ 14, -15 ≤ k ≤ 15, -17 ≤ l ≤ 17; reflections collected 37455; independent reflections 6837; Rint 0.0252; GOOF 1.121; R1 = 0.0257, wR2 = 0.0605; the largest diff. peak/hole 0,23 /-0,84 e/Å3; C32H21O4F4Sb (3), M 667.24; monoclinic system, space group С2/с; cell parameters: a = 12.652(5), b = 22.466(10), c = 11.561(5) Å; β = 120.027(15)°; V = 2845(2) Å3; Z = 4; crystal size 0.5×0.45×0.12 mm; index ranges -16 ≤ h ≤ 16, -28 ≤ k ≤ 28, -14 ≤ l ≤ 14; reflections collected 27275; independent reflections 3163; Rint 0.029; GOOF 1.107; R1 = 0.0372, wR2 = 0.1058; the largest diff. peak/hole 1.61/-0.53 e/Å3; C49H40O3Sb2 (4), M 920.31; triclinic system, space group Р1 ; cell parameters: a = 10.093(4), b = 13.994(5), c = 15.665(6) Å; a = 73.917(15)°, β = 79.76(2)°, g = 74.312(15)°; V = 2034.0(13) Å3; Z = 2; crystal size 0.26×0.22×0.05 mm; index ranges -12 ≤ h ≤ 12, -17 ≤ k ≤ 17, -20 ≤ l ≤ 20; reflections collected 50553; independent reflections 9006; Rint 0.0333; GOOF 1.066; R1 = 0.0239, wR2 = 0.0522; the largest diff. peak/hole 0.77/-0.43 e/Å3. The antimony atoms in 3 have a distorted trigonal-bipyramidal coordination with the oxygen atoms in axial positions (the OSbO angle is 174.13(12)°, the Sb-C and Sb-O distances are 2.101(3)-2.118(4) Å and 2.118(3) Å). The structural organization in crystals 3 and 4 is due to weak intermolecular contacts of the О···Н-C type, 2.49 and 2.56 Å, respectively. Complete tables of atom coordinates, bond lengths and valence angles are deposited at the Cambridge Crystallographic Data Center (No. 2117872 for 1, No. 2121388 for 3, No. 2121833 for 4; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Текст научной статьи Трифенилсурьма и пентафенилсурьма - исходные соединения в синтезе фенильных производных пятивалентной сурьмы. Строение трифенилсурьмы, бис(3,4-дифторбензоато)трифенилсурьмы и карбоната тетрафенилсурьмы
В основе одного из эффективных способов синтеза соединений пятивалентной сурьмы лежит реакция окислительного присоединения, когда из триарильных соединений сурьмы, кислоты НХ и пероксида получают арильные производные пятивалентной сурьмы Ar 3 SbX 2 . Указанная реакция впервые была осуществлена на примере синтеза диацетата трифенилсурьмы из трифенил-сурьмы, уксусной кислоты и пероксида водорода [1]. Именно по этой схеме были синтезированы дикарбоксилаты трифенилсурьмы [2], диоксиматы трифенилсурьмы [3] и другие производные пятивалентной сурьмы общей формулы Ph 3 SbX 2 [4].
Строение базового реагента для получения фенильных производных пятивалентной сурьмы ранее изучалось [5], однако только в настоящей работе удалось выполнить наиболее точное ис- следование особенностей структуры трифенилсурьмы (1). По данным рентгеноструктурного анализа, атомы сурьмы в двух кристаллографически независимых молекулах трифенилсурьмы имеют тетрагональную координацию с атомами углерода фенильных заместителей и неподеленной электронной парой в вершинах тетраэдра (рис. 1, табл. 1). Длины связей Sb–C и величины углов CSbC равны 2,148(3)-2,166(3) А и 95,12(13)°-97,87(11)° соответственно.
Рис. 1. Строение соединения 1
Не менее важным соединением в химии фенильных производных сурьмы является пента-фенилсурьма ( 2 ), синтез которой впервые был описан в 1952 году [6], а особенности ее строения – несколько позже [7–10]. Известно, что пентафенилсурьма является прекурсором для получения многочисленных фенильных производных пятивалентной сурьмы [4]. Как правило, одноосновные карбоновые кислоты легко отщепляют одну фенильную группу в 2 [11–15] с образованием карбоксилатов тетрафенилсурьмы, которые, в свою очередь, образуют с кислотами аддукты Ph4SbOC(O)R∙HOC(O)R [16]. Реакции дикарбоновых кислот в зависимости от соотношения исходных реагентов могут сопровождаться замещением одного или двух активных атомов водорода в карбоксильных группах [17–19].
Показано, что взаимодействие диоксима метилендициклопентанона-2,2’ с пентафенилсурь-мой в жестких условиях (90 ° С, 5 ч) при мольном соотношении исходных реагентов 1:2 соответственно приводит к образованию макроциклического сурьмаорганического соединения - бис -р, - [(метилендициклопентанон-2,2’-диоксимато)трифенилсурьмы], в молекулах которого симметричные диоксимные радикалы чередуются со структурными блоками трифенилсурьмы [20].
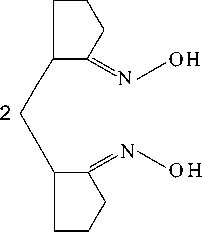
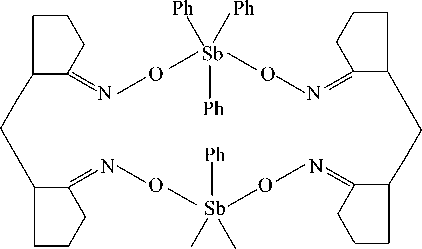
Ph Ph
В настоящей работе описан подобный случай отщепления 3,4-дифторбензойной кислотой двух фенильных заместителей от пентафенилсурьмы с образованием бис (3,4-дифторбензоато)трифенилсурьмы. Несмотря на эквимолярное соотношение исходных реагентов, продуктом реакции являлась бис (3,4-дифторбензоато)трифенилсурьма ( 3 ).
Ph 5 Sb + 2 HOC(O)C 6 H 3 F 2 -3,4 ^ Ph 3 Sb[OC(O)C 6 H 3 F 2 -3,4] 2 + 2 PhH
В ИК-спектре соединения 3 наблюдается полоса поглощения средней интенсивности валентных колебаний связей Sb–C при 428 см–1. Наличие карбонильной группы характеризуется присутствием полосы поглощения валентных колебаний связи С=О сильной интенсивности при 1634 см–1. Полосы поглощения, характеризующие колебания ν(С–О) в карбоксилатных лигандах, наблюдаются при 1333 см–1. ИК-спектр соединения 3 также содержит характерные полосы валентных колебаний углеродного скелета ароматических фрагментов: 1508, 1481, 1425 см–1. Валентным колебаниям связей C Ar –H отвечает полоса поглощения средней интенсивности при 3022 см–1, внеплоскостным деформационным колебаниям этих же связей – полосы при 823, 794 и 758 см–1, плоскостным деформационным колебаниям – полосы при 1113, 1065 и 1022 см–1 [21–23].
По данным РСА, в центросимметричных молекулах соединения 3 атомы сурьмы имеют искаженную тригонально-бипирамидальную координацию с атомами кислорода карбоксилатных лигандов в аксиальных положениях (рис. 3).
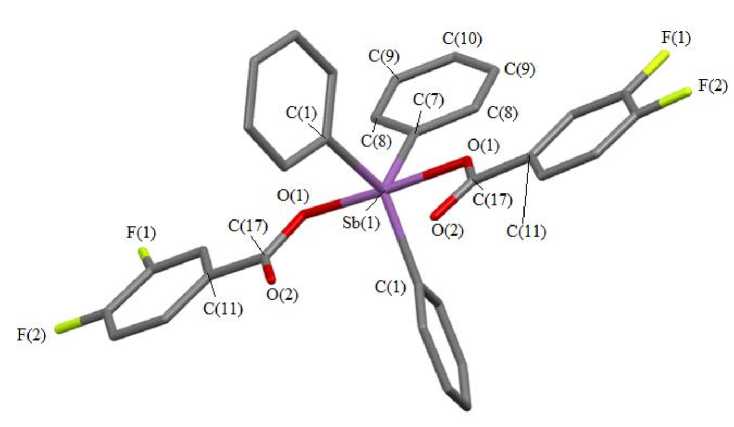
Рис. 2. Строение соединения 3 (атомы водорода не показаны)
Сумма углов CSbC в экваториальной плоскости молекулы составляет 359,96(11)°, аксиальный угол OSbO равен 174,13(12)°, атом сурьмы не выходит из экваториальной плоскости. Конформация арильных лигандов по отношению к экваториальной плоскости [С 3 ] пропеллерная. Двугранные углы между плоскостями бензольных колец и экваториальной плоскостью составляют 20,20° [C(1)–C(6)], 78,01° [C(7)–C(10)]. Длины связей Sb–C имеют близкие значения: 2,101(3), 2,118(4) Å, а расстояния Sb–O (2,118(3) Å) соизмеримы с ковалентными длинами связей Sb–O (2,05 Å [24]). Плоскости карбоксильных групп практически компланарны (угол между ними составляет 5,24 ° ), а карбоксилатные лиганды в молекулах 3 расположены таким образом, что внутримолекулярные контакты Sb—O(=C) формируются внутри наибольшего экваториального угла СSbC (137,6(2) ° ), что характерно для большинства структурно охарактеризованных дикарбоксилатов триарилсурьмы [5]. Бидентатные карбоксилатные лиганды координируют на атом металла симметрично, при этом внутримолекулярные расстояния Sb—O(=C) равны 3,014(5) А, что меньше суммы ван-дер-ваальсовых радиусов атомов Sb и O (3,58 Å [25]).
Пентафенилсурьма способна реагировать с кислородом [26] и углекислым газом [27]. Выделенный в последней работе карбонат бис(тетрафенилсурьмы) способен реагировать с солями тетрафенилстибония, присоединяя еще один катион за счет изменения структурной функции карбонатной группы с μ2-хелатно-мостиковой на μ3-мостиковую, с образованием ионных комплексов с трис(тетрафенилстибокси)метилий-катионом [28]. Так, при кристаллизации продуктов реакций пентафенилсурьмы с 2,4-динитробензолсульфоновой кислотой из смеси бензол–октан на воздухе наряду с целевым продуктом – 2,4-динитробензолсульфонатом тетрафенилсурьмы – с выходом 32 % выделен сольват ионного комплекса сурьмы с трехкоординированным атомом углерода в катионе [(Ph4SbO)3C]+[OSO2C6H3(NO2)2-2,4]– ⋅ 3PhH. Катион имеет практически плоский цен- тральный фрагмент СO3Sb3. Углы ОСО и COSb близки к 120°, связи C–O изменяются в интервале 1,277(4)–1,290(3) Å, расстояния Sb–O [2,266(2)–2,299(2) Å] превышают сумму ковалентных радиусов атомов сурьмы и кислорода. Минорным продуктом реакции является карбонат бис(тетрафенилсурьмы) (4), из которого, как полагают авторы, и образуется ионный комплекс, поэтому интересно было изучить структуру карбоната тетрафенилсурьмы более тщательно.
В настоящей работе уточнена структура триклинной модификации карбоната тетрафенил-сурьмы 4 , которая ранее была установлена с точностью R = 4,9 % в работе [29]. Результаты нашего исследования кристалла 4 были более точными (R = 3,7 %), чем в работе [28]. Координационные полиэдры двух атомов сурьмы в 4 различны: один из атомов сурьмы имеет тригонально-бипирамидальное окружение (OSbC акс 176,38(8)°), другой – искаженное октаэдрическое ( транс углы CSbО 154,59(8), 157,47(8)° (рис. 3).
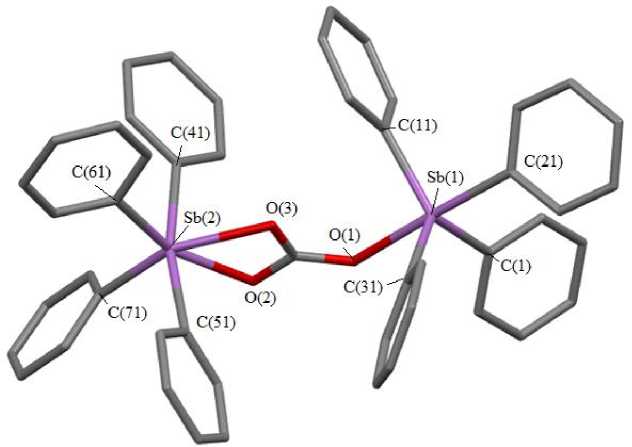
Рис. 3. Строение соединения 4 (атомы водорода не показаны)
Интервалы изменения длин связей Sb–C в структуре 4 составляют 2,0992(15)–2,634(2) Å, а расстояния Sb–О равны 2,1844(17)–2,3104(17) Å, что больше суммы ковалентных радиусов указанных элементов [27]. Длины связей C–O в карбонатных группах составляют 1,281(3); 1,277(3); 1,296(3) Å, при этом более короткой связи Sb–О соответствует более длинная связь С–О.
Экспериментальная часть
Сольват пентафенилсурьмы с бензолом Ph 5 Sb∙½PhH (2). После перекристаллизации пен-тафенилсурьмы из бензола получили бесцветные кристаллы с т. разл. 135,5 °С. Найдено: C 72,41; H 5,19. C 32 H 21 O 4 F 4 Sb. Вычислено: C 72,49; H 5,13.
Синтез бис (3,4-дифторбензоато)трифенилсурьмы Ph 3 Sb[OC(O)C 6 H 3 F 2 -3,4] 2 (3) . Смесь 0,150 г (0,27 ммоль) сольвата пентафенилсурьмы с бензолом и 0,043 г (0,27 ммоль) 3,4-дифторбензойной кислоты в 10 мл бензола нагревали 5 минут при 80 С, охлаждали до комнатной температуры и добавляли 2 мл октана. Через 24 ч выделяли 0,06 г (41 %) бесцветных кристаллов 3 с т. разл. 134 °С. ИК-спектр ( ν , см–1): 3022, 2953, 1634, 1599, 1508, 1481, 1425, 1333, 1273, 1227, 1200, 1113, 1065, 1023, 997, 937, 901, 839, 802, 779, 770, 733, 692, 638,546, 489, 451, 428. Найдено: C 57,37; H 3,21. C 32 H 21 O 4 F 4 Sb. Вычислено: C 57,55; H 3,15.
Элементный анализ на C и H выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter (рис. 4).
ИК-спектр соединения 3 записывали на ИК-Фурье спектрометре Shimadzu IRAffinity-1S в таблетке KBr в области 4000–400 см–1.
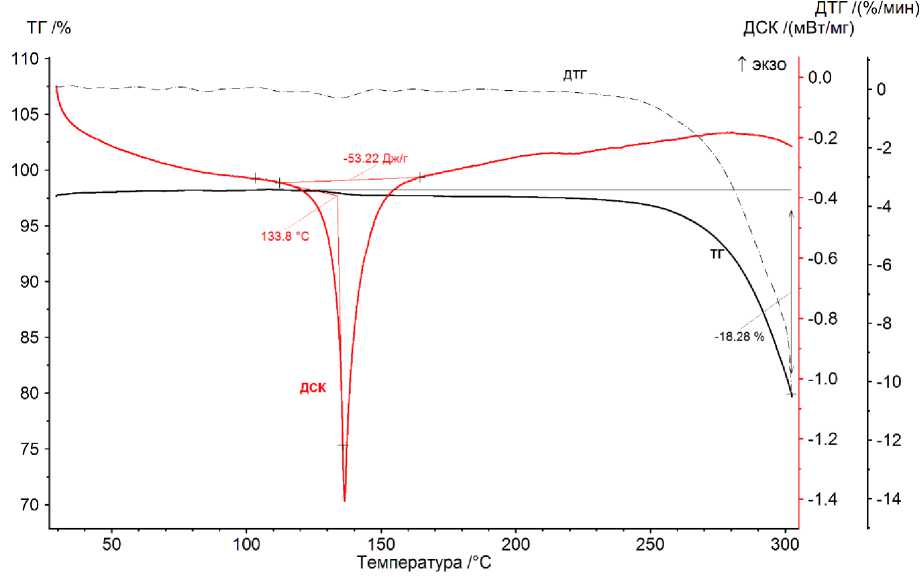
Рис. 4. Кривые ДТГ и ДСК для образца 3
Рентгеноструктурный анализ ( РСА ) кристаллов проведен на автоматическом четырехкружном дифрактометре D8 QUEST фирмы Bruker (Mo K α -излучение, λ = 0,71073 Å, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены с помощью программ SMART и SAINT-Plus [30]. Все расчеты по определению и уточнению структур выполнены с помощью программ SHELXL/PC [31], OLEX2 [32]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника ( U изо (H) = 1,2 U экв (C)). Кристаллографические данные и результаты уточнения структур приведены в табл. 1, геометрические характеристики координационного полиэдра атома сурьмы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1, 3, 4
|
Параметр |
1 |
3 |
4 |
|
Формула |
C 36 H 30 Sb 2 |
C 32 H 21 O 4 F 4 Sb |
C 49 H 40 O 3 Sb 2 |
|
М |
706,10 |
667,24 |
920,31 |
|
Т , К |
293 |
293 |
293 |
|
Сингония |
Триклинная |
Моноклинная |
Триклинная |
|
Пр. группа |
P 1 |
C2/c |
P 1 |
|
a , Å |
10,941(11) |
12,652(5) |
10,093(4) |
|
b, Å |
11,825(16) |
22,466(10) |
13,994(5) |
|
c, Å |
13,747(13) |
11,561(5) |
15,665(6) |
|
α ,º |
102,57(5) |
90,00 |
73,917(15) |
|
β,º |
104,22(5) |
120,027(15) |
79,76(2) |
|
γ ,º |
108,35(6) |
90,00 |
74,312(15) |
|
V , Å3 |
1550(3) |
2845(2) |
2034,0(13) |
|
Z |
2 |
4 |
2 |
|
ρ (выч.), г/см3 |
1,513 |
1,558 |
1,503 |
|
µ , мм–1 |
1,764 |
1,032 |
1,369 |
|
F (000) |
696,0 |
1328,0 |
920,0 |
Окончание табл. 1
|
Параметр |
1 |
3 |
4 |
|
Размер кристалла, мм |
0,5 × 0,44 × 0,11 |
0,5 × 0,45 × 0,12 |
0,26 × 0,22 × 0,05 |
|
Область сбора данных по 2 θ , град. |
5,74–54,42 |
6,6–54,32 |
5,802–54,44 |
|
Интервалы индексов отражений |
–13 ≤ h ≤ 14, –15 ≤ k ≤ 15, –17 ≤ l ≤ 17 |
–16 ≤ h ≤ 16, –28 ≤ k ≤ 28, –14 ≤ l ≤ 14 |
–12 ≤ h ≤ 12, –17 ≤ k ≤ 17, –20 ≤ l ≤ 20 |
|
Измерено отражений |
37455 |
27275 |
50553 |
|
Независимых отражений |
6837 |
3163 |
9006 |
|
R int |
0,0252 |
0,0291 |
0,0333 |
|
Переменных уточнения |
343 |
187 |
477 |
|
GOOF |
1,121 |
1,107 |
1,066 |
|
R -факторы по F 2 > 2 σ ( F 2) |
R 1 = 0,0257, wR 2 = 0,0605 |
R 1 = 0,0372, wR 2 = 0,1058 |
R 1 = 0,0239, wR 2 = 0,0522 |
|
R -факторы по всем oтражениям |
R 1 = 0,0330, wR 2 = 0,0652 |
R 1 = 0,0425, wR 2 = 0,1124 |
R 1 = 0,0349, wR 2 = 0,0572 |
|
Остаточная электронная плотность (min/max), e/A3 |
–0,84/0,23 |
–0,53/1,61 |
–0,43/0,77 |
Таблица 2
|
Связь |
d , Å |
Угол |
ω , град. |
|
1 |
|||
|
Sb(1)–С(1) |
2,163(3) |
С(11)Sb(1)С(1) |
95,87(11) |
|
Sb(1)–С(11) |
2,155(3) |
C(11)Sb(1)C(21) |
95,55(11) |
|
Sb(1)–С(21) |
2,158(4) |
C(21)Sb(1)C(1) |
97,46(14) |
|
Sb(2)–С(51) |
2,148(3) |
C(51)Sb(2)C(31) |
97,65(12) |
|
Sb(2)–С(31) |
2,165(3) |
C(51)Sb(2)С(41) |
95,12(13) |
|
Sb(2)–С(41) |
2,166(3) |
C(31)Sb(2)С(41) |
95,43(12) |
|
3 |
|||
|
Sb(1)–O(1) |
2,118(3) |
O(1)Sb(1)O(11) |
174,13(12) |
|
Sb(1)–O(11) |
2,118(3) |
C(11)Sb(1)C(7) |
111,18(11) |
|
Sb(1)–С(7) |
2,118(4) |
C(1)Sb(1)С(7) |
111,18(11) |
|
Sb(1)–С(1) |
2,101(3) |
C(11)Sb(1)С(1) |
137,6(2) |
|
Sb(1)∙∙∙O(2) |
3,014(5) |
C(1)Sb(1)O(11) |
91,87(13) |
|
Преобразования симметрии: 12- X , +y, 3/2-z |
|||
|
4 |
|||
|
Sb(1)–C(31) |
2,117(3) |
C(31)Sb(1)C(1) |
115,22(11) |
|
Sb(1)–O(1) |
2,2505(17) |
C(11)Sb(1)C(1) |
116,55(9) |
|
Sb(1)–C(1) |
2,119(2) |
C(21)Sb(1)O(1) |
176,38(8) |
|
Sb(1)–С(11) |
2,0992(15) |
C(51)Sb(2)С(41) |
167,09(9) |
|
Sb(1)–С(21) |
2,168(3) |
C(71)Sb(2)O(3) |
154,59(8) |
|
Sb(2)–O(3) |
2,3104(17) |
C(71)Sb(2)C(7) |
125,66(8) |
|
Sb(2)–O(2) |
2,1844(17) |
C(61)Sb(2)O(2) |
157,47(8) |
|
Sb(2)–C(51) |
2,169(2) |
C(61)Sb(2)C(51) |
92,76(10) |
|
Sb(2)–C(71) |
2,162(2) |
C(61)Sb(2)C(71) |
106,18(10) |
|
Sb(2)–C(7) |
2,634(2) |
C(61)Sb(2)C(7) |
128,14(9) |
|
Sb(2)–С(61) |
2,162(3) |
C(61)Sb(2)С(41) |
91,79(10) |
|
Sb(2)–С(41) |
2,173(2) |
C(41)Sb(2)С(7) |
84,92(8) |
Длины связей и валентные углы в соединениях 1, 3 , 4
Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2117872 для 1, 2121388 для 3, 2121833 для 4; ; .
Выводы
Взаимодействием эквимолярных количеств сольвата пентафенилсурьмы (Ph5Sb∙0,5PhH) с 3,4-дифторбензойной кислотой в бензоле получена и структурно охарактеризована бис (3,4-дифторбензоато)трифенилсурьма Ph 3 Sb[OC(O)C 6 H 3 F 2 -3,4] 2 . Уточнено строение трифенилсурьмы и триклинной модификации карбоната тетрафенилсурьмы.
Финансирование работы
Работа выполнена при финансовой поддержке РФФИ в рамках научного проекта № 20-3390099.
Список литературы Трифенилсурьма и пентафенилсурьма - исходные соединения в синтезе фенильных производных пятивалентной сурьмы. Строение трифенилсурьмы, бис(3,4-дифторбензоато)трифенилсурьмы и карбоната тетрафенилсурьмы
- Improved Methods for the Sinthesis of Antimony Triacetate, Triphenylantimonyldiacetate and Pentaphenylantimony / T.C. Thepe, R.J. Garascia, M.A. Selvoski et al. // Ohio J. Sci. - 1977. - V. 77, № 3. - P. 134-135.
- Синтез и строение бис(1-адамантанкарбоксилото)трифенилсурьмы / В.В. Шарутин, О.К. Шарутина, А.П. Пакусина и др. // Журн. неорг. химии. - 2008. - Т. 53, № 8. - С. 1335-1341.
- Шарутин, В.В. Синтез и строение салицилальдоксиматов тетра- и трифенилсурьмы / В.В. Шарутин, О.К. Шарутина, О.В. Молокова // Журн. неорг. химии. - 2012. - Т. 57, № 6. - С. 902.
- Шарутин, В.В. Синтез, реакции и строение арильных соединений пятивалентной сурьмы / B.В. Шарутин, А.И. Поддельский, О.К. Шарутина // Коорд. химия. - 2020. - Т. 46, № 10. - C. 579-648. DOI: 10.31857/S0132344X20100011.
- Cambridge Crystallografic Datebase. Release 2020. Cambridge. deposit@ccdc.cam.ac.uk; http: //www .ccdc.cam.ac.uk
- Wittig, G. Pentaphenyl-arsen und Pentaphenyl-antimon / G. Wittig, K. Clauss // Europ. J. Org. Chem. - 1952. - Bd. 577. - S. 26-39. DOI:10.1002/JLAC.19525770104.
- Wheatley, P.J. An X-ray Diffraction Determination of the Crystal and Molecular Structure of Pentaphenylantimony / P.J. Wheatley // J. Chem. Soc. - 1964. - № 718. - P. 3718-3723. DOI: 10.1039/JR9640003718.
- Beauchamp, A.L. A Reinvestigation of the Crystal and Molecular Structure of Pentaphenylantimony / A.L. Beauchamp, M.J. Bennett, F.A. Cotton // J. Am. Chem. Soc. - 1968. - V. 90. - P. 66756680. DOI: 10.1021/ja01026a020.
- Brabant, C. Structure Crystalline du Pentaphenylantimone Dans le Solvate Cycljhexanique (C6H5)5Sb • У C6H12 / C. Brabant, B. Blanck, A.L. Beauchamp // J. Organomet. Chem. - 1974. -V. 82. - P. 231-234. DOI: 10.1016/S0022-328X(00)90360-7.
- Geometry of Pentaphenylantiminy in Solution: Support for a Trigonal Bipyramidal Assignment from X-ray Absorption Spectroscopy and Vibrational Spectroscopic Data / B. Lindquist-Kleissler, M. Weng, P. Le Magueres et al. // Inorg. Chem. - 2021. - V. 60. - P. 8566-8574. DOI: 10.1021/acs.inorgchem.1c00496.
- Синтез и строение 1-адамантанкарбоксилата тетрафенилсурьмы и бис(1- адамантанкар-боксилата) трифенилсурьмы / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журн. общ. химии. - 2009. - Т. 79, №. 10. - С. 1636-1643.
- Шарутин, В.В. Синтез и строение N-бензоилглицината тетрафенилсурьмы. / B.В. Шарутин, О.К. Шарутина, К.А. Хныкина // Журн. неорган. химии. - 2016. - Т. 61, № 2. - C. 192-194. DOI: 10.7868/S0044457X16020197.
- Шарутин, В.В. Синтез и строение фенилпропионатов тетра- и трифенилсурьмы / B.В. Шарутин, О.К. Шарутина, А.Р. Котляров // Журн. неорган. химии. - 2015. - Т. 60, № 4. - C. 525-528. DOI: 10.7868/S0044457X15040236.
- Шарутин, В.В. Синтез и строение 4-оксибензоатов тетра- и трифенилсурьмы / B.В. Шарутин, О.К. Шарутина, В.С. Сенчурин // Журн. неорган. химии. - 2014. - Т. 59, № 9. - C. 1182-1186. DOI: 10.7868/S0044457X14090189.
- Синтез и строение кислого фталата тетрафенилсурьмы / В.В. Шарутин, О.К. Шарутина, И.Г. Мельникова и др. // Изв. РАН. Сер. хим. - 1996. - № 8. - С. 2082-2085.
- Синтез и строение аддуктов нитрата тетрафенилсурьмы с азотной кислотой и ацетата тетрафенилсурьмы с уксусной кислотой / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина и др. // Журн. неорган. химии. - 2008. - Т. 53, № 7. - С. 1194-1198.
- Шарутин, В.В. Синтез и строение кислого малоната татрафенилсурьмы / В.В. Шарутин, В.С. Сенчурин, О.К. Шарутина // Журн. неорг. химии. - 2014. - Т. 59, № 2. - С. 247. DOI: 10.7868/S0044457X14020184.
- Шарутин, В.В. Синтез и строение сукцината, малата и тартрата бис(тетрафенилсурьмы) / В.В. Шарутин, О.К. Шарутина // Коорд. химия. - 2014. - Т. 40, № 9. - С. 559. DOI: 10.7868/S0132344X14090072.
- Sharutin, V.V. Interaction of Pentaphenylantimony with Acetylenedicarboxylic Acid. Molecular Structure of Bis(tetraphenylantimony) Acetylenedicarboxilate / V.V. Sharutin, O.K. Sharutina, Yu.O. Gubanova // Вестник ЮУрГУ. Серия «Химия». - 2015. - Т. 7, № 4. - С. 17-22. DOI: 10.14529/chem150403
- Cnm^ и строение бис-ц-[(метилендициклопентанон-2,2'-диоксимато)трифенилсурьмы] / B.В. Шарутин, О.В. Молокова, О.К. Шарутина и др. // Коорд. химия. - 2005. - Т. 31, № 3. - C.172-176.
- Тарасевич, Б.Н. ИК-спектры основных классов органических соединений / Б.Н. Тарасевич. - М.: МГУ, 2012. - 54 с.
- Инфракрасная спектроскопия органических и природных соединений: учебное пособие / А.В. Васильев, Е В. Гриненко, А О. Щукин и др. - СПб.: СПбГЛТА, 2007. - 54 с.
- Spectral Database for Organic Compounds, SDBS. Release 2021. National Institute of Advanced Industrial Science and Technology.
- Covalent Radii Revisited / B. Cordero, V. Gómez, A.E. Platero-Prats et al. // Dalton Trans. -2008. - V. 21. - P. 2832-2838. DOI: 10.1039/B801115J.
- Consistent van der Waals Radii for the Whole Main Group / M. Mantina, A.C. Chamberlin, R. Valero et al. // J. Phys. Chem. A. - 2009. - V. 113, № 19. - P. 5806-5812. DOI: 10.1021/jp8111556.
- Синтез, строение и реакции ц-оксо-бис(тетрафенилсурьмы) / В.В. Шарутин, О.К. Шарутина, В.С. Сенчурин и др. // Коорд. химия. - 2001. - Т. 27, № 9. - C. 710-716.
- Карбонат тетрафенилсурьмы. Синтез и строение / В.В. Шарутин, О.К. Шарутина, Т.П. Платонова и др. // Журн. общ. химии. - 2001. - Т. 71, № 10. - С. 1637-1640.
- Шарутин, В.В. Арильные сурьмаорганические производные трехкоординированного углерода / В.В. Шарутин, О.К. Шарутина, А.Н. Ефремов // Журн. неорган. химии. - 2020. - Т. 65, № 1. - С. 49-55. DOI: 10.31857/S0044457X20010158.
- Ferguson, G. The Crystal and Molecular Structure of ^-Carbonato-bis(tetraphenylantimony): a System Containing Penta- and Hexacoordinated Antimony / G. Ferguson, D.M. Hawley // Acta Cryst. -1974. - V. 30. - P. 103-111. DOI: 10.1107/S0567740874002299.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- OLEX2: Complete Structure Solution, Refinement and Analysis Program / O.V. Dolomanov, L.J. Bourhis, R.J. Gildea et al. // J. Appl. Cryst. - 2009. - V. 42. - P. 339-341. DOI: 10.1107/S0021889808042726.


