Ультразвуковые признаки для диагностики и оценки эффективности медикаментозного лечения сочетанных пролиферативных заболеваний матки
Автор: Кедрова Анна Генриховна, Леваков Сергей Александрович, Нечаева Ольга Евгеньевна, Тазитдинов Ренат Халлилович, Челнокова Наталья Николаевна
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 3 (19), 2014 года.
Бесплатный доступ
В статье изложены вопросы ультразвуковой диагностики доброкачественных пролиферативных заболеваний матки, особенности при их сочетании и изменениях, возникающих на фоне медикаментозного лечения диеногестом. Анализ ультразвуковых особенностей матки при сочетании нескольких доброкачественных заболеваний (миомы матки, внутреннего эндометриоза и гиперплазии эндометрия) дал возможность выделить характерные изменения, возникающие в ответ на лечение диеногестом. Полученные ультразвуковые критерии медикаментозного эффекта - гомогенность миометрия, четкие контуры миоматозного узла с усилением его эхогенности, уменьшение М-эха, его равномерность, средняя эхогенность с четкостью границы мио- и эндометрия, снижение локального кровотока в измененных участках, могут быть использованы для выбора безоперационной тактики ведения пациенток. В тоже время, при сохранении гетерогенности миометрия, «синдрома частокола» и «размытости границ» требуется хирургическое лечение или эмболизация маточных артерий (ЭМА).
Ультразвуковые критерии заболеваний матки, миома матки, гиперплазия эндометрия, внутренний эндометриоз, диеногест
Короткий адрес: https://sciup.org/14338493
IDR: 14338493
Ultrasound criteria for diagnosis and monitoring of drug therapy of combined proliferative diseases of the uterus
The aim of the paper was to evaluate the diagnostic accuracy of transvaginal tenderness-guided ultrasonography in the identification of location of genital endometriosis, endometrial hyperplasia and uterine fibroids before and after treatment dienogest. It is a selective progestin for the treatment of endometriosis. Adenomyosis was diagnosed when a poorly defined area of abnormal echo-texture (decreased or increased echogenicity, heterogeneous echotexture, myometrial cysts) presented in myometrium. Typical ultrasonic changes of efficacy were: homogeneity of myometrium; clear and intense contours of uterine fibroid with increased echogenicity; reduction of the echogenic endometrial stripe with the average echogenicity and clear lines of myo- and endometrium with a reduction in local blood. These criteria can be used to select non-surgical management of patients. In cases where a poorly defined area of abnormal echotexture (decreased or increased echogenicity, heterogeneous echotexture, myometrial cysts) did not change the surgery or the embolization of artery uterine is required. The preferred imaging modality for the evaluation of uterine on therapeutic alternatives to hysterectomy and myomectomy is transvaginal ultrasonography.
Текст научной статьи Ультразвуковые признаки для диагностики и оценки эффективности медикаментозного лечения сочетанных пролиферативных заболеваний матки
Современная тенденция к увеличению гормонозависимых заболеваний органов женской репродуктивной системы (ОЖРС) обуславливает поиск новых эффективных алгоритмов ранней диагностики начальных форм эндометриоза, гиперплазии эндометрия и миомы матки, так как именно сочетанная патология требует ранней терапии и индивидуального подхода к больной, из-за частого развития гормо-норезистентности в процессе лечения. Дать точную эпидемиологическую оценку доброкачественной пролиферативной патологии матки достаточно сложно, из-за применения нескольких диагностических характеристик и классификаций, приводящих к большой статистической разнице при оценке заболеваемости. Так, эндометриоз наблюдается у 10-60% женщин репродуктивного возраста, а одна треть из них имеет дополнительно и миому матки [1]. По данным работ Сидоровой И.С. и Гуриева Т.Д., использующих морфологические характеристики диагноза, сочетание миомы матки с аденомиозом в клинике оперативной гинекологии встречается в 49% наблюдений [2]. При этом дооперационные методы диагностики демонстрировали данную сочетанную патологию у 60% больных [3, 4]. Патогенез аденомиоза, миомы матки и гиперплазии эндометрия часто одинаковый и имеет схожие факторы риска: гиперэстрогенный фон (изменение в составе эстрогенных метаболитов); нарушение углеводного обмена; поздний репродуктивный возраст; генетические предпосылки; внутрима-точные хирургические вмешательства; повышенный уровень фолликулостимулирующего гормона (ФСГ) и/или пролактина (ПРЛ); изменения в рецепторной активности тканей-мишеней; неблагоприятное воздействие внешних факторов среды (курение, стресс, депрессия) [5]. У большей половины таких пациенток вышеназванные заболевания матки вызывают обильные кровотечения и интенсивный болевой дискомфорт (боли в спине или в низу живота). Лечение для них включает инвазивные хирургические процедуры (абдоминальная или лапароскопическая гистерэктомии или миомэктомии), малоинвазивные методы (гистероскопическая миомэктомия, эмболизация маточных артерий) или консервативную альтернативу – фармакологические варианты. В идеале, выбор лечения должен быть оптимально адаптирован для каждого пациента, в зависимости от типа и локализации миомы, распро- страненности эндометриоза и симптомов, беспокоящих женщину. Несмотря на достигнутые успехи в лечении каждой отдельно взятой патологии матки, сочетание миомы, аденомиоза и/или гиперплазии создает значительные трудности, так как понимание биологических основ развития сочетанной пролиферативной патологии матки до сих пор не имеет концептуальной обоснованности. Выполненные работы часто носят дискуссионный характер, а применяемые в них диагностические термины имеют авторские трактовки и различаются даже по патоморфологическим критериям [6]. В России официально принята Международная классификации болезней 10-го пересмотра (МКБ-10), согласно которой аденомиоз – это эндометриоз матки (N80.0), а миома матки характеризуется в зависимости от локализации доминантного узла: подслизистая (D25.00), интрамуральная (D25.01), субсерозная (D25.02), и не-уточненная (D25.09). Гиперпластические болезни эндометрия (ГПЭ) различаются по вариантам гиперплазии (N84.0; N85.0; N85.1) и локализации полипа [7]. В МКБ 10 не предусмотрена классификация сочетанной патологии матки, что затрудняет диагностику, статистический анализ и процесс лечения. При этом, современные методы визуализации органов малого таза (УЗТ, КТ, МРТ) имеют высокую чувствительность – 80-96%, хотя не всегда специфичны (40-60%), что может приводить к ошибочной диагностике [8-10].
В этой связи, цель нашего анализа – выявить совокупность клинических и ультразвуковых признаков, свойственных сочетанию миомы матки, аденомиоза и гиперплазии эндометрия, а также проследить их изменения в процессе лекарственной терапии для выработки критериев оценки эффективности.
Материалы и методы
При ежегодной диспансеризации женщин мы выделили 84 пациентки с УЗИ-признаками аденомиоза, миомы матки и/или утолщенным эндометрием. При этом мы применяли общепринятые ультразвуковые критерии (табл. 1.), рекомендуемые для скрининга диагностики пролиферативных доброкачественных заболеваний матки [11-13].
Ультразвуковые исследования были выполнены с использованием вагинального датчика для цветного допплеровского изображения и спектрального анализа (Асuson Seguoia 512,
Таблица 1
|
Наименование |
Аденомиоз + миома матки N = 49(58,3%) |
Аденомиоз+ гиперплазия эндометрия N =23 (27,4%) |
Аденомиоз + миома+ гиперплазия эндометрия N=12(14,3%) |
|
Матка размеры |
|||
|
Не увеличена |
0 |
2 |
0 |
|
Увеличена 6-7 недель |
34 |
16 |
1 |
|
Увеличена 10-12 недель |
14 |
5 |
9 |
|
Увеличена >12 недель |
1 |
0 |
2 |
|
Матка контуры |
|||
|
Бугристые |
18 |
0 |
4 |
|
Неровные |
31 |
7 |
8 |
|
Ровные |
0 |
16 |
0 |
|
Матка узлы |
|||
|
Множественные |
15 |
0 |
3 |
|
Единичный |
34 |
0 |
9 |
|
Субмукозный узел |
5 |
0 |
2 |
|
Субсерозный узел |
7 |
0 |
4 |
|
Интерстициальный |
37 |
0 |
6 |
|
Нет |
0 |
23 |
0 |
|
Полость матки |
|||
|
Расширена равномерно |
0 |
8 |
0 |
|
Расширена неравн омерно |
4 |
3 |
3 |
|
Расширена, есть жидкость |
2 |
3 |
1 |
|
Не определяется |
6 |
0 |
0 |
|
Контур деформирован или оттеснен узлом |
37 |
0 |
2 |
|
Толщина эндометрия не соответствует фазе цикла, эхоструктура неоднородная |
0 |
17 |
6 |
|
Миометрий |
|||
|
Неравномерной утолщен |
42 |
5 |
4 |
|
Диффузно неоднородный, преобладают: - "пятнистые" участки с отражениями пониженной интенсивности; - линейные отражения повышенной интенсивности |
7 5 2 |
18 И 7 |
8 5 3 |
|
Патологияп |
эидатков или смежных тканей |
||
|
Яичники с небольшими кистозными включениями |
2 |
2 |
0 |
|
Утолщение крестцово-маточных связок |
5 |
1 |
4 |
|
другие |
4 |
1 |
0 |
|
нет |
38 |
19 |
8 |
Ультразвуковые характеристики изображений матки в зависимости от выявленной патологии
Voluson 730 pro, Toshiba). Все обследования были сделаны одним и тем же врачом по единому протоколу, куда вносились данные при первичном и повторных осмотрах.
При осмотре в режиме «серой шкалы» оценивали: размеры и контуры матки, толщину, структуру, границы миометрия и эндометрия; положение срединного М-эха; отдельно описывали все узловые образования – их размеры, локализацию, границы, структуру. Дополнительно производилось цветовое допплеровское картирование всех описанных структур и области сосудистых пучков матки с обеих сторон, с последующей допплерометрией в зонах аномальной васкуляризации. Максимальная скорость кровотока и индекс резистентности (ИР) были измерены с учетом максимальной толщины эндометрия, миометрия и локализации узлов миомы. При наличии нескольких узлов производили измерения каждого в отдельности, но с акцентом на доминантный, самый крупный узел. Он измерялся по трем наибольшим размерам (A, B и C в двух плоскостях и приблизительно перпендикулярно к осям: Х, Y и Z. Объем матки рассчитывали по формуле объема эллипсоида:
0,523 х А х В х С
При ультразвуковых признаках патологии эндометрия нами выполнялась аспирационная биопсия эндометрия или амбулаторная гистероскопия с забором материала на цитологическое и/ или гистологическое исследование. Все диагностические процедуры выполняли на первичном этапе постановки диагноза, а также в процессе лечения, с интервалом каждые 10-12 нед. Во время контрольных визитов, мы акцентировали внимание на динамических изменениях клинических симптомов, таких как: интенсивность маточного кровотечения, выраженность болевого синдрома, общее самочувствие, которые соотносили с данными гинекологического осмотра и ультразвуковыми характеристиками. Для сравнительного анализа полученные данные вносились в таблицы-кодификатор.
Результаты
Средний возраст пациенток выбранной группы составил 37,5±4,6 лет.
По данным гинекологического осмотра и ультразвукового исследования (УЗИ) почти все отобранные пациентки имели увеличенные размеры матки. По результатам, представлен- ным в таблице 2, можно заключить, что неровность контуров матки была больше характерна при сочетании миомы и аденомиоза, при этом визуализировалась гетерогенная структура миометрия во всех отделах, а его неравномерное утолщение было связано, как с миоматозным узлом, так и с аденомиозом.
Необходимо отметить, что типичные для аденомиоза признаки лучше визуализировались при расположении узлов субсерозно, чем при интерстициальной локализации, а также при небольших размерах узлов – до 2,5 см. У двух женщин, имеющих несколько сливных узлов, размер которых достигал 6-7 см, а размеры матки соответствовали 13 нед. беременности, миометрий не имел расширенных границ, но в его структуре прослеживались гипо- и гиперэхогенные включения от 0,2 до 0,4см.
При сочетании аденомиоза и гиперплазии эндометрия более характерно: ярко выраженое ги-поэхогенное, утолщенное М-Эхо, неравномерной толщины (от 1 до 2,3 см), часто неоднородной структуры за счет аэхогенных единичных или множественных аваскулярных включений от 0,1 до 0,7 см (рис. 1), при этом наблюдалась очень нечеткая и размытая граница между эндо- и миометрием, что зачастую искажало ультразвуковую картину патологии эндометрия, увеличивая его толщину. Допплерометрические показатели кровотока в маточной артерии при аденомиозе и гиперплазии эндометрия часто имели индекс резистентности > 0,6, а кровоток внутреннего слоя миометрия, граничащего с эндометрием, характеризовался высокой плотностью сосудов, «цветовых локусов», расположенных хаотично.
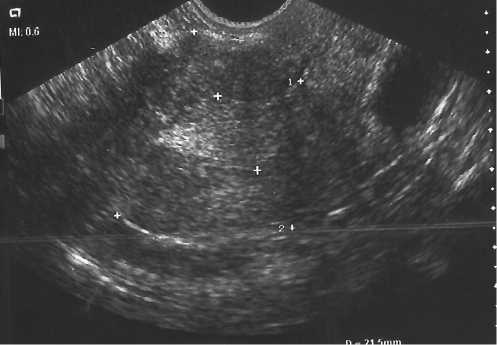
Рис. 1. Внутренний эндометриоз и гиперплазия эндометрия. Матка «шарообразной» формы, миометрий неоднородной структуры, М-эхо 22 мм, отсутствует четкая граница между мио-и эндометрием, зона «эндометрий-миометрий» неравномерно утолщена и неоднородна.
Таблица 2
Ультразвуковые особенности эндометрия, при признаках аденомиоза
|
Гистологический диагноз биопсии эндометрия |
Число больных N=35 |
Характерные ультразвуковые признаки |
|
Простая гиперплазия эндометрия |
12 |
ТЭ до 21 мм, эндометрий неоднородной структуры, в основном повышенной эхогенности с мелкими аэхогенными включениями, частично определяется кровоток в спиральных артериях с широким диапазоном значений от 4,3 до 6,8 см/сек, в зависимости от выраженности аденомиоза, индекс резистентности высокий 0,64-0,86 |
|
Полип эндометрия |
4 |
Локальные изменения эндометрия, повышенной эхогенности, с четким контуром, ТЭ до 17мм, единичный локальный кровоток, иногда трудно дифференцировать с субмукозным узлом миомы, особенно при небольших размерах и сгустками крови |
|
Эндометрий секреторной фазы с признаками хронического эндометрита |
9 |
ТЭ 7-15мм, М-эхо гиперэхогенное, без аэхогенных включений, по базальному слою эндометрия визуализируются стенки сосудов по типу «рельсов». ЦДК, индекс резистентности и скорость кровотока были повышены, как при аденомиозе. |
|
Эндометрий ановуляторного цикла |
10 |
ТЭ 5-7мм, структура неоднородная, нечеткие границы эндометрия и миометрия, трехслойность отсутствует, кровоток в спиральных артериях не визуализировался, индекс резистентности 0,49-0,53 |
В случаях сочетания миомы матки и внутреннего эндометриоза форма матки, при отсутствии доминантного узла лейомиомы, чаще приближалась к «шарообразной», характерной для аденомиоза, но при крупных узлах (более 2,5 см), ее форма всегда была неправильной и бугристой, при этом кровоток имел периферическую картину, с локализацией сосудов, как бы по «капсуле» узла (рис. 2а).
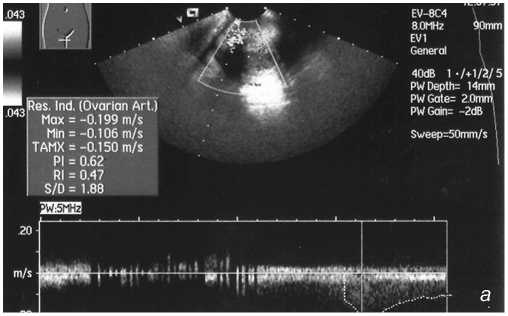
Рис. 2а. Миома матки в сочетании с аденомиозом: периферический кровоток, с локализацией сосудов по «капсуле» узла.
Структура миометрия во всех случаях была неоднородной, «сетчатой» или «ячеистой», хотя симптом «частокола» появлялся лишь при значительно утолщенном миометрии, при 2-3 степени внутреннего эндометриоза (рис. 2б). Из до-
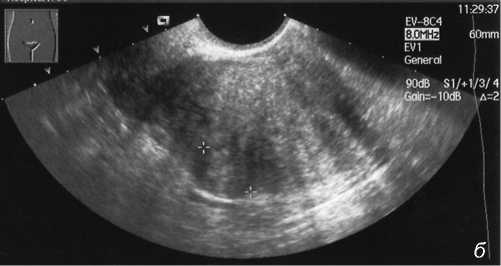
Рис. 2б. Выраженный аденомиоз и миома матки. В неравномерно расширенном миометрии визуализируется эффект «частокола».
полнительной информации об особенностях васкуляризации матки при сочетании миомы матки и аденомиоза необходимо отметить, что индекс резистентности был около 0,5, при высо- кой скорости кровотока. Обращает на себя внимание, что среди обследованных женщин у 6 больных были обнаружены тромбы в венах параметрия (рис. 2в), что может являться косвенным свидетельством о нарушении кровотока в матке.
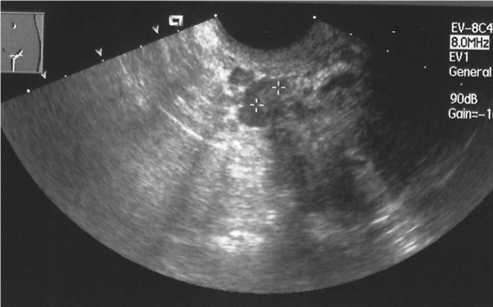
Рис. 2в. Миома матки (интерстициальный узел размерами до 1.8 см) в сочетании с внутренним эндометриозом. В одной из вен параметрия справа визуализируется образование повышенной эхогенности, размерами до 1см, определяется пристеночный обходной кровоток – тромб в вене параметрия.
Основные ультразвуковые характеристики, отмеченные при исследовании и представленные в таблицах 1 и 2, использовались нами в качестве основных критериев и для оценки эффективности проводимой терапии. При этом особое внимание мы обращали на изменение эхоструктуры, контуры и формы матки и узлов лейомиомы.
В целях объективизации сведений об изменении степени васкуляризации матки у части больных мы пользовались методиками УЗ-ан-гиографии и проводили построение гистограмм отдельно выбранных областей, применяя амплитудную оценку акустических параметров отраженных эхогафических сигналов, выраженных в децибелах.
В результате динамического наблюдения, при контрольных исследованиях, после лечения диеногестом 2 мг/сутки, в течении 12 нед, ультразвуковая картина изменялась положительно у 67 (79,8%) пациенток. В целом, к положительным динамическим изменениям на фоне лечения, мы относили случаи, когда матка принимала удлиненно-вытянутую форму (рис. 3 а, б), миометрий становился гомогенной структуры, хорошо и четко визуализировались границы миоматозного узла и прослеживалась четкая граница между мио- и эндометрием (рис. 4а). У части больных появлялся эффект «латеральных теней» из-за нарастающей плотности миоматозного узла (рис. 4б).
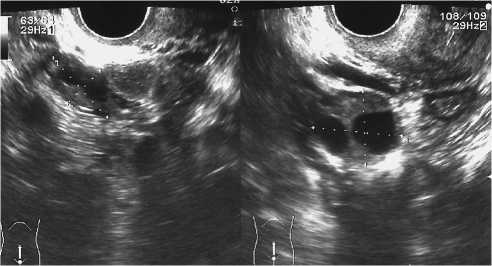
Рис. 3а. Узловой аденомиоз до начала лечения диеногестом
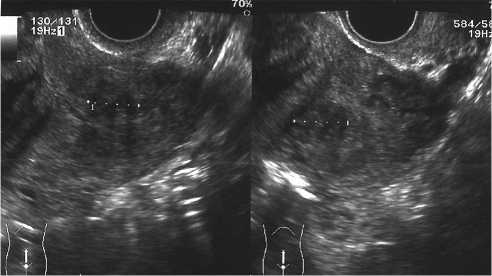
Рис. 3б. Узловой аденомиоз после 16 нед. лечения диеногестом
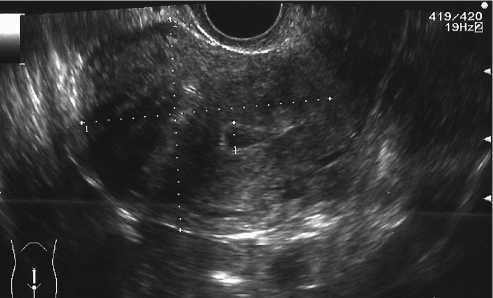
Рис. 4а. Положительный эффект от медикаментозного лечения внутреннего эндометриоза и миомы матки. Матка принимает удлиненно-вытянутую форму, миометрий гомогенной структуры, границы миоматозного узла четко визуализируются, прослеживается четкая граница между мио- и эндометрием.
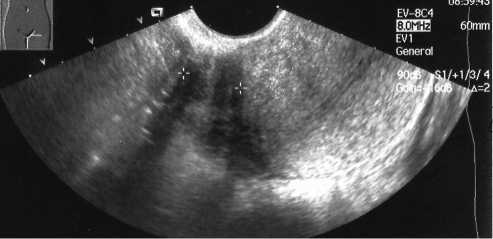
Рис. 4б. Положительный эффект от медикаментозного лечении внутреннего эндометриоза и миомы матки. Границы миоматозного узла становятся четкими, появляется эффект «латеральных теней».
Таблица 3
|
Наименование |
До лечения диеногестом 2 мг N =84(100%) |
|
Матка размеры |
|
|
Не изменились |
20 (23,8%) |
|
Уменьшились незначительно < 2см |
47 (56%) |
|
Уменьшились значительно > 2см |
8 (9,5%) |
|
Увеличились |
9 (10,7%) |
|
Матка контуры и форма |
|
|
Не изменились |
32 (38,1%) |
|
Изменились, контуры выровнялись |
И (13,1%) |
|
Изменились, форма матки вытянулась |
41 (48,9%) |
|
Состояние узловых образований в матке (% для I и III группы больных с наличием узлов миомы N=61) |
|
|
Появилась четкость контуров узлов, Повысилась эхогенность узла, однородность |
26 (42,6%) |
|
Уменьшились размеры узлов |
8 (13,2%) |
|
Увеличились размеры узлов |
9 (14,7%) |
|
Появились кистозные деформации в узле |
4 (6,5%) |
|
Узлы без динамики |
12(19,7%) |
|
Состояние эндометрия (% для группы больных II-III с начальными признаками гиперплазии эндометрия N= 35) |
|
|
Нет динамических изменений |
0 |
|
Уменьшение толщины М-эха |
15 |
|
Эндометрий линейный |
12 |
|
Изменение эхогенности |
8 |
|
Структура миометрия |
|
|
Без существенной динамики |
17(20,2%) |
|
Уменьшение плотности линейных страт, изменение в сторону гомогенности, из них появилась равномерность толщины миометрия |
67 (79,8%) 12 |
|
Патология придатков матки или смежных тканей |
|
|
Уменьшились кистозные включения в яичниках |
2 |
|
Без динамики |
9 |
Динамические ультразвуковые изменения в матке при приеме диеногеста
Основные ультразвуковые эффекты, полученные во время динамического наблюдения за больными, представлены в таблице 3.
В случаях положительного эффекта лекарственной терапии матка уменьшалась в размерах, в среднем на 1-1,5 см (максимально – на 4 см) и ее форма становилась удлиненно-вытянутой. В миометрии интенсивность гетерогенных включений снижалась, уходила «ячеистость» и «сетчатость» при внутреннем эндометриозе I-II степени, но симптом «частокола» оставался при аденомиозе (рис. 5а), возможно за счет фиброзно-склеротических изменений, которые мало чувствительны к гормонотерапии. Измеряемый и вычисленный объем доминирующего узла, по сравнению с исходным, в большинстве наблюдений не изменялся, лишь у 8 (13,2%) женщин были отмечены уменьшения объема узлов от 85 мм3 (56-111) до 46 мм3 (34-74), а у 9 (14,7%) пациенток зафиксировано увеличение объема узлов от 35 мм3 до 68 мм3.
Ультразвуковые признаки лечебного эффек-
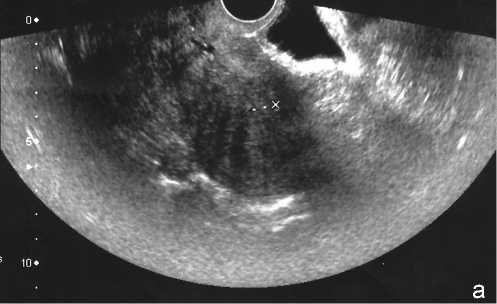
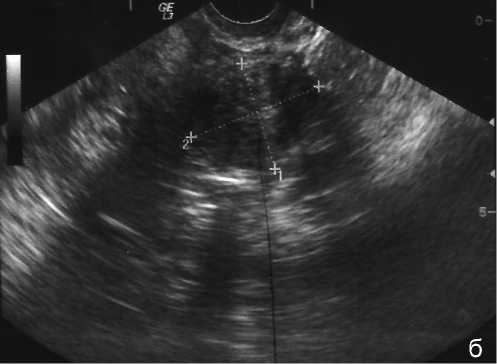
Рис. 5а. Эффект от медикаментозного лечения не получен. «Синдром частокола» остается после 12 нед. лечения диеногес-том 2мг/сутки.
Рис. 5б. Эффект от медикаментозного лечения не получен. Структура узла миомы не изменилась в динамике и синдром «частокола» остается.
та, такие как: гомогенность миометрия, четкие контуры миоматозного узла с усилением его эхогенности, уменьшение М-эха, его равномерность, средняя эхогенность с четкостью границы мио- и эндометрия, почти всегда коррелировали с данными снижения локального кровотока в измененных участках. При этом существенных различий в показателях и распределении кровотока по крупным сосудам мы не зарегистрировали.
В случаях отсутствия эффекта от лечения картина гетерогенного миометрия оставалась без динамики, не изменялась картина «синдрома частокола» (рис. 5а), границы оставались размытыми и эхогенность миоматозных узлов не изменялась (рис. 5б).
Обсуждение
Согласно утверждению экспертов Американского общества по репродуктивной медицине (ASRM), «эндометриоз следует рассматривать, как длительно протекающее заболевание, которое требует разработки плана долговременного ведения пациентки с целью максимального использования медикаментозного лечения и исключения повторных хирургических вмешательств» [14]. Однако до настоящего времени ни одна из предложенных стратегий лечения эндометриоза не привела к полному излечению и не позволила избежать рецидивов заболевания. Вследствие множественных поли-системных нарушений, лежащих в основе патогенеза болезни, лечение сочетанной патологии матки составляет крайне деликатную задачу, часто требуя индивидуального подбора терапии под многократным динамическим контролем. При этом четких ультразвуковых критериев медикаментозного эффекта до сих пор нет. Наше исследование показало, что ультразвуковые характеристики могут служить хорошим ориентиром для этой цели, позволяя контролировать изменения, происходящие на фоне эмпирически подобранной терапии, с учетом гормональной зависимости нескольких пролиферативных заболеваний матки. Ранее показанная высокая диагностическая ценность трансвагинального ультразвукового исследования для диагностики аденомиоза, составляющая 80,8% [15], была нами подтверждена и для сочетания внутреннего эндометриоза с миомой и гиперплазией эндометрия.
Анализ, полученных данных показал, что основные ультразвуковые критерии внутреннего эндометриоза – наличие включений пониженной эхогенности при утолщении миометрия, вызванные гладкомышечной гиперплазией, гетеротопией и склерозом сосудов, имеют крайне вариабельную сонографическую картину, особенно в случаях сочетания нескольких нозологий. Измененные области в миометрии, при сочетанной патологии матки, крайне неоднородны: от малых, точечных включений до выраженных «линейных страт» и кистозных полостей, за счет участков склероза, расширенных желез или геморрагических очагов. Миома матки, гиперплазия эндометрия и внутренний эндометриоз, взаимодействуя, часто искажают или «смазывают» ультразвуковую картину друг друга, приводя к ошибочной диагностике. В этой связи общепринятые ультразвуковые признаки каждой отдельной нозологии матки нельзя считать достаточными и в полной мере объективными при их сочетании. Наиболее частыми и объективными изменениями при сочетанной патологии матки можно считать контурные аномалии границ разных тканей. Например, гиперплазия эндометрия, как ультразвуковое увеличенное и неоднородное М-эхо, несоответствующее фазе менструального цикла, при аденомиозе является необъективным критерием, так как отсутствует четкая граница между мио- и эндометрием, а зона «эндометрий-миометрий» почти всегда неравномерно утолщена и неоднородна (рис. 1).
Такая картина может имитировать ложное утолщение М-эха и для точной диагностики требует высокой квалификации врача, проводящего исследование. Неоднозначна и дифференциальная диагностика с хроническим эндометритом (рис. 6 а), который также встречается при внутреннем эндометриозе.
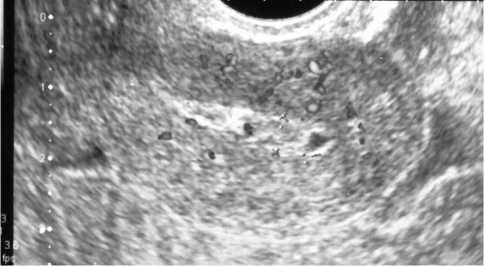
Рис. 6а. Внутренний эндометриоз и хронический эндометрит. Миометрий неоднородной структуры с неоднородными фокусами кровотока. М-эхо 52 мм, прослеживается четкая граница между мио- и эндометрием, зона «эндометрий-миометрий» однородная, полость расширена с гиперэхогенными включениями (синехии) и сгустками крови.
Особое внимание необходимо обращать на пациенток с признаками очаговой гиперплазии на фоне атрофичного эндометрия (рис. 6 б), которые не имеют выраженной клиники кровотечений и кровомазания, но, с учетом онкологической настороженности, требуют биопсии эндометрия.
ЦДК и допплерометрия во многих случаях позволяют проводить дифференциальную диагностику между узловой формой аденомиоза и узлами миомы матки. Так, если при миоме матки чаще имел место периферический кровоток, с локализацией сосудов по «капсуле» узла (рис. 2а), то для аденомиоза был характерен центральный тип кровотока, в виде «впрыска», а «капсула» с сосудами отсутствовала (рис. 3а). Уменьшение объема матки, изменение ее формы от «шарообразной» к «нормально вытянутой» и появление гомогенности структуры, при отсутствии динамического утолщения эндометрия может трактоваться как положительная динамика в ответ на лечение (рис 3 а, б). Сохра-
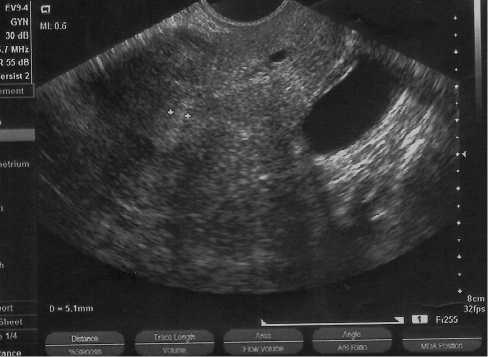
Рис. 6б. Внутренний эндометриоз и очаговая гиперплазия эндометрия. Матка «шарообразной» формы, миометрий неоднородной структуры, М-эхо 5 мм, граница между мио- и эндометрием нечеткая, в области дна эхогенное включение 155х11,8мм.
няющиеся выраженные изменения в структуре матки, несмотря на проводимое лечение, дают возможность расценивать данную ситуацию как прогностически неблагоприятную и даже рекомендовать оперативное лечение. Однако для определения конкретных ультразвуковых критериев, характеризующих положительную динамику лечения или, напротив, усиление пролиферации и активного прогрессирования болезни, необходимо дополнительное исследование с сопоставлением ультразвуковых и морфологических заключений.
Выводы
Ультразвуковой метод диагностики может являться одним из критериев оценки эффективности медикаментозного лечения у женщин с сочетанной патологией матки. Для более точной объективизации эффекта от лечения необходимо сопоставлять клинические данные с ультразвуковыми критериями. Например, выраженность болевого синдрома, интенсивность кровянистых выделений и динамику ультразвуковых характеристик: изменение объема матки и доминантного узла миомы, структуры миометрия и эндометрия, их толщину и эхогенность. Также необходимо мониторировать индекс периферического сопротивления и степень васкуляризации патологических очагов. Отсутствие динамики вышеописанных показателей, по нашему мнению, свидетельствует о неэффективности проводимой медикаментозной терапии и требует тактики оперативного лечения или эмболизации маточных артерий (ЭМА).
Список литературы Ультразвуковые признаки для диагностики и оценки эффективности медикаментозного лечения сочетанных пролиферативных заболеваний матки
- Parazzini F, Mais V, Cipriani S. GISE. Determinants of adenomyosis in women who underwent hysterectomy for benign gynecological conditions: results from a prospective multicentric study in Italy. Eur J Obstet Gynecol Reprod Biol 2009; 143:103-106.
- Гуриев Т.Д., Сидорова И.С., Унанян А.Л. Сочетание миомы матки и аденомиоза. Пособие для врачей. М.: Медицинское информационное агентство. 2012. С. 34.
- Taran FA, Weaver AL, Coddington CC. Characteristics indicating adenomyosis coexisting with leiomyomas: a case-control study. Hum Reprod. 2010 May;25(5):1177-82.
- Stewart EA, Strauss JF. Disorders of the uterus: leiomyomas, adenomyosis, endometrial polyps, abnormal uterine bleeding, intrauterine adhesions and painful menses. In: Yen and Jaffe's Reproductive Endocrinology. Barbieri RL, Strauss JF, eds. 2004; 5th edn. Philadelphia: Elsevier. 713-34.
- Brosens I, Puttemans P, Benagiano G. Endometriosis: a life cycle approach? Am J Obstet Gynecol. 2013 Mar 15. pii: S0002-9378(13) 00263-9.: 10.1016/j.ajog.2013.03.009
- Gordts S, Brosens JJ, Fusi L. Uterine adenomyosis: a need for uniform terminology and consensus classification. Reprod Biomed Online. 2008 Aug;17(2):244-8.
- Пособие по освоению Международной статистической классификации болезней и проблем, связанных со здоровьем (десятый пересмотр). Для врачей и специалистов по статистике. Спб.: 1998.
- Ascher SM, Jha RC, Reinhold C. Benign myometrial conditions: leiomyomas and adenomyosis. Top Magn Reson Imaging. 2003 Aug; 14(4):281-304.
- Tamai K, Koyama T, Umeoka S. Spectrum of MR features in adenomyosis. Best Pract Res Clin Obstet Gynaecol. 2006 Aug;20(4):583-602.
- Мерц Э. Ультразвуковая диагностика в акушерстве и гинекологии. Том 2. Гинекология. Пособие для врачей. М.: Медпресс Информ. 2011, стр.256-260.
- Стрижаков А.Н., Давыдов А.И., Пашков В.М., и соавт. Доброкачественные заболевания матки. Пособие для врачей. М.: Гэотар-Медиа. 2011, стр.69-72.
- Зыкин Б.И. Стандартизация ультразвуковых исследований в гинекологии. Дис... докт. мед. наук М.: 2002.
- Медведев М.В., Хохолин B.Л. Ультразвуковое исследование матки. Клиническое руководство по ультразвуковой диагностике. Под ред. Митькова В.В., Медведева М.В. М.: Видар, 1997, Т3, с. 76-119.
- Practice Committee of American Society of Reproductive Medicine (ASRM), 2008
- Kepkep K, Tuncay YA, G`ynhmer G. Trans-vaginal sonography in the diagnosis of adenomyosis: which findings are most accurate? Ultrasound Obstet Gynecol. 2007 Sep;30(3):341-5.


