Усовершенствование технологии культивирования вирусов парагриппа-3 и инфекционного ринотрахеита для изготовления ассоциированных вакцин КРС
Автор: Каримуллина И.Г., Гумеров В.Г., Яруллин А.И., Мухаммадиев Р.С., Мингалеев Д.Н., Сорокина Д.А.
Статья в выпуске: 3 т.259, 2024 года.
Бесплатный доступ
Представлены сравнительные результаты исследований стационарного и роллерного культивирования вирусов инфекционного ринотрахеита (ИРТ) и парагриппа-3 (ПГ-3) на перевиваемых линиях культуры клеток МДВК (почка теленка) и ТР (трахея эмбриона коровы). Показано, что максимальный титр инфекционной активности исследуемых вирусов достигался при роллерном способе культивирования: для ИРТ на культуре клеток МДВК при использовании среды Игла МЭМ с добавлением 1 % глутамина, для ПГ-3 − на культуре клеток ТР с использованием среды, состоящей из 50 % ГЛА, 40 %, Игла МЭМ и 10 % среды 199. При этом инфекционная активность вирусов составила соответственно 7,9-8,3 lg ТЦД50/мл и 7,2-8,5 lg ТЦД50/мл.
Культура клеток, инфекционный ринотрахеит, парагрипп-3, крупный рогатый скот (КРС)
Короткий адрес: https://sciup.org/142242518
IDR: 142242518 | УДК: 619:57.085.23:578.825:578.831 | DOI: 10.31588/2413_4201_1883_3_259_78
Improvement of the technology of culturing the viruses of paragrip-3 and infectious rhinotracheitis for the manufacture of an associated vaccine cattle
Comparative results of the assessment of stationary and roller cultivation of infectious rhinotracheitis (IRT) and parainfluenza-3 (PG-3) viruses on continuous cell culture lines of MDVK and TR are presented. It was shown that the maximum titer of the infectious activity of the studied viruses was achieved with the roller method of cultivation: for IRT on a MDVK cell culture using Eagle's medium MEM with the addition of up to 1 % glutamine, for PG-3 - on a TR cell culture using a medium consisting of 50 % HLA, 40 %, Needle MEM and 10 % medium 199. In this case, the infectious activity of the viruses was 7.9-8.3 lg TCID50/ml and 7.2-8.5 lg TCID50/ml, respectively.
Текст научной статьи Усовершенствование технологии культивирования вирусов парагриппа-3 и инфекционного ринотрахеита для изготовления ассоциированных вакцин КРС
Массовое выращивание вирусов животных в культуре клеток представляет собой центральное звено любого технологического процесса, основанного на использование клеток животных, и прежде всего производство вирусных препаратов [8]. Данная стадия обуславливает массу и качество клеток и, как следствие, технологию получения вирусного сырья. Выбор подхода выращивания вируса в существенной мере связан со способностью клеток размножаться на поверхности плотного субстрата или суспензии [6, 12].
Несмотря на последние достижения в развитии клеточной биотехнологии, получение вирусного сырья на перевиваемых линиях клеток для противовирусных препаратов к настоящему времени испытывает определенные трудности [6]. Широко распространенный способ пристеночного культивирования клеток в матрасах в связи с малой производительностью и большой трудоемкостью малопригоден для промышленного применения [4-7]. На сегодняшний день самым эффективным способом получения в больших объемах вирусной биомассы для изготовления биопрепаратов является использование суспензионной культуры клеток [8]. К высокопродуктивному суспензионному выращиванию приспособлено несколько клеточных линий животных (ВНК-21/13,
ПТП, ППК-66Б), спектр чувствительности которых весьма специфичен, поэтому они не всегда удовлетворяют имеющиеся требования [1, 6].
Последующие исследования были направлены на поиск способов получения вирусной суспензии, выращенных на микроносителях, позволяющие получать вирусную суспензию в короткие сроки, в больших объемах и с высокой инфекционной активностью [13]. Тем не менее, культивирование клеток на микроносителях обусловлено необходимостью использования весьма сложных методов пересева клеток, контроля за их ростом, подготовки носителей и освобождения от последних псевдосуспензии [1]. Все это снижает общую рентабельность производства, несмотря на незначительное повышение конечной плотности популяции клеток. В этом плане наиболее универсальным является роллерный способ выращивания клеток в круговом монослое. Однако он требует детальной отработки режимов выращивания для конкретных клеточных линий с целью обеспечения максимальной реализации их ростового потенциала [1, 3, 4, 6, 9, 11].
Цель исследования – изыскание наиболее эффективной технологии выращивания культур клеток для получения биомассы вирусов ПГ-3 и ИРТ с высокой инфекционной активностью.
Материал и методы исследований. Для создания ассоциированных вакцин, в состав которых входят антигены ПГ-3 и ИРТ КРС, требовалось, в первую очередь, изучить чувствительность первичных и перевиваемых линий культур клеток к штаммам «ТК-А (ВИЭВ)-В2» вируса ИРТ и «ПТК-45/86» вируса ПГ-3, полученных из государственной коллекции микроорганизмов ФГБНУ «ФЦТРБ-ВНИВИ». В предварительных опытах по выбору культуры клеток было установлено, что наиболее перспективными для репродукции указанных вакцинных штаммов вирусов являются перевиваемые клетки почки (МДВК) и трахеи (ТР) эмбриона коровы.
В экспериментах по отработке оптимального метода выращивания вирусов ИРТ и ПГ-3 КРС исследованы следующие параметры: время формирования получаемого монослоя, начальная посевная концентрация клеток, доза заражения, сроки проявления максимального цитопатического действия, состав питательной среды. Репродукцию штаммов вирусов проводили с применением перевиваемых линий культур клеток МДВК и ТР стационарным и роллерным методами. При этом осуществляли учет коэффициента заполнения роллерных бутылей, скорости их вращения, рН среды и температуры культивирования, продолжительности выращивания, количества пассажей клеток и вирусов.
При выращивании культур клеток животных в качестве ростовой среды применяли следующие питательные среды: ГЛА, 199, Игла MEM с внесением 1 % L-глютамина, 10 % сыворотки крови КРС и гентамицина в концентрации 50 мкг/мл. Для поддержания культур клеток после заражения использовали вышеуказанные среды без сыворотки. Для культивирования клеток и вирусов использовали матрасы объемом 1500 мл (стационарное выращивание) и бутыли объемом 2500 мл «типа четверть» (роллерное культивирование на промышленной установке). После каждого опыта инфекционную активность вирусной биомассы определяли методом микротитрации на 96-луночных планшетах, культуры клеток инкубировали в инкубаторе во влажной атмосфере с концентрацией СО 2 5 % в течение 48-96 ч (в зависимости от репродукции вирусов). Инфекционный титр вирусов рассчитывали методом Рида и Менча. Контроль культуры клеток и штаммов вирусов ИРТ и ПГ-3 на возможную контаминацию микоплазмами осуществляли высевом их на бульон, используя триптический перевар сердца КРС.
Результат исследований . В таблице 1 представлены результаты исследований по установлению оптимальных условий получения высокоактивной биомассы штаммов вирусов ИРТ и ПГ-3 КРС с целью изготовления ассоциированной вакцины.
Таблица 1 – Параметры, влияющие на накопление вирусов, при различных способах культивирования
|
Способ культивирования |
Концентрация клеток при посеве, тыс/см3 |
Время формирования получаемого монослоя, сут. |
Доза вируса для заражения, ТЦД 50 /мл на клетку |
Время выращивания вируса, час. |
|
Штамм вируса «ПТК-45/86» ПГ-3 на культуре клеток ТР |
||||
|
Стационарный |
110-120 |
2-3 |
0,2-0,4 |
96-110 |
|
Роллерный |
110-120 |
2-3 |
0,4-0,8 |
96-110 |
|
Штамм вируса «ТК-А (ВИЭВ)-В2» ИРТ на культуре клеток МДВК |
||||
|
Стационарный |
110-120 |
2-3 |
0,2-0,3 |
48-60 |
|
Роллерный |
110-120 |
2-3 |
0,3-0,5 |
48-64 |
Максимальный титр инфекционной активности исследуемых вирусов достигался методом роллерного культивирования и для вируса ПГ-3 составил 7,9-8,3 lg ТЦД50/мл и для вируса ИРТ – 7,2-8,5 lg ТЦД50/мл (Рисунок 1). При этом вирусы репродуцировали с коэффициентом заполнения сосудов 0,170,19 и скорости их вращения 10-11 об/ч. Для инфицирования клеточного монослоя использовали вирус ПГ-3 в дозе 0,6±0,2 ТЦД50/мл на клетку и вирус ИРТ - 0,4±0,1 ТЦД50/мл на клетку.
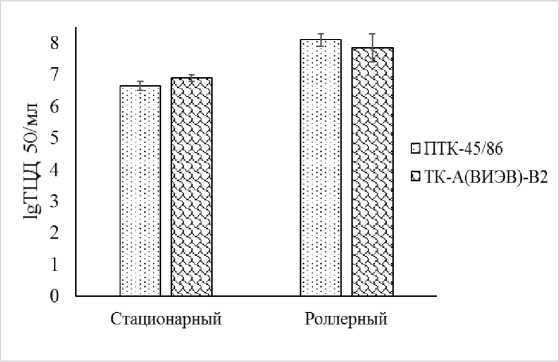
Рисунок 1 – Инфекционная активность штаммов вирусов ПГ-3 и ИРТ КРС при различных способах выращивания
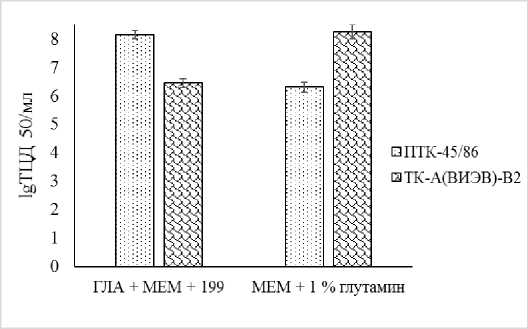
Рисунок 2 – Влияние состава питательной среды на репродукцию штаммов вирусов ПГ-3 и ИРТ КРС
Основными параметрами, которые определяют уровень накопления вирусов в монослое клеток, являются концентрация водородных ионов (рН) и температура культивирования. Наши исследования показали хорошую репродукцию вирусов ПГ-3 и ИРТ при температуре 37±0,5 ˚С и рН 7,2±0,2. При более низких или высоких значениях рН (5,0 и 9,0) и температуры (35 и 39 ˚С) активность вирусов была ниже на 0,3-1,24 lg ТЦД 50 /мл.
На жизнеспособность клеток линии ТР и выращивание в ней вируса ПГ-3 существенное влияние оказывал состав питательной среды (Рисунок 2).
Применение поддерживающей питательной среды, состоящей из 10 % среды 199,40 % Игла МЭМ и 50 % ГЛА, в культуре клеток линии ТР увеличивало урожайность вируса ПГ-3 до 8,0-8,3 lg ТЦД 50/мл, в то время как поддерживающая среда Игла МЭМ с добавлением 1% глутамина в культуре клеток МДВК не обеспечивало накопление титра вируса ПГ-3 на достаточно высоком уровне. При репродукции вируса ИРТ на культуре клеток МДВК с поддерживающей средой Игла МЭМ и добавлением 1 % глутамина наблюдали повышение инфекционного титра до 8,08,5 lg ТЦД 50/мл. Следует отметить, что замена вышеуказанной среды на смешанную среду (50 % ГЛА, 40 % Игла МЭМ и 10 % среды 199) снижала инфекционную активность на 1,35±0,15 lg ТЦД 50/мл.
Следует отметить, что присутствие в питательных средах смеси антибиотиков (пенициллина и стрептомицина) в рекомендуемой дозе предотвращало контаминацию культур клеток бактериальной микрофлоры и не оказывало влияния на конечный титр вирусов.
Заключение. Результаты изучения условий роллерного культивирования перевиваемых линий клеток МДВК и ТР, которые отобраны по признакам высокой чувствительности и репродуцирующей способности к штаммам вирусам ИРТ и ПГ-3, позволяют получить высокоактивные антигены для возможности конструирования ассоциированной вакцины.
Список литературы Усовершенствование технологии культивирования вирусов парагриппа-3 и инфекционного ринотрахеита для изготовления ассоциированных вакцин КРС
- Бабак, В. А. Оптимальные режимы культивирования линии клеток ВНК-21 (С-13) / В. А. Бабак, Ю. В. Ломако, А. А. Гусев [и др.] // Ученые записки учреждения образования Витебская ордена Знак почета государственная академия ветеринарной медицины. – 2011. – Т. 47. – № 2-1. – С. 7-11.
- Гумеров, В. Г. Факторы, влияющие на репродукцию вирусов в культуре клеток / И. Г. Каримуллина, А. К. Галиуллин, Э. М. Плотникова [и др.] // Ученые записки Казанской государственной академии ветеринарной медицины им. Н.Э. Баумана. – 2018. – Т. 234. – № 2. – С. 83-86.
- Демидчик, Г. А. Технология выращивания вакцинного штамма ТК-А вируса ИРТ КРС для изготовления инактивированной вакцины / Г. А. Демидчик // Ветеринария. Реферативный журнал. – 1999. – № 1. – С. 41.
- Закутский, Н. И. Разработка и совершенствование технологии изготовления инактивированной вакцины против инфекционного ринотрахеита крупного рогатого скота: дис. на соиск. учен. степ. канд. вет. наук: 06.02.02 / Закутский Николай Иванович; Всероссийский научно-исследовательский институт ветеринарной вирусологии и микробиологии РАСХН. − Покров, 1998. – 311 с.
- Закутский, Н. И. Технология выращивания вакцин штамма ТК-А вируса ИРТ КРС для изготовления инактивированной вакцины / Н. И. Закутский // Ветеринария. – 1997. – № 2. – С. 23-25.
- Каримуллина, И. Г. Оптимизация технологии культивирования вирусов парагриппа-3, инфекционного ринотрахеита и хламидий при разработке ассоциированной вакцины: дис. на соиск. учен. степ. канд. биол. наук: 03.00.07 / Каримуллина Ильсияр Габделгазизовна; Всеросс. науч.-исслед. вет. ин-т. – Казань, 2004. – 133 с.
- Каримуллина, И. Г. Исследование репродуктивных свойств вирусов инфекционного ринотрахеита и парагриппа-3 крупного рогатого скота на различных линиях культур клеток / И. Г. Каримуллина, В. Г. Гумеров, А. И. Яруллин [и др.] // Инновационные решения актуальных вопросов биобезопасности: сборник материалов Международной научно-практической конференции. – Казань: Издательство Альянс. – 2022. – С. 187-191.
- Колокольцова, Т. Д. Культуры клеток человека и животных: выделение, культивирование, криоконсервация и контроль / Т. Д. Колокольцова, И. Н. Сабурина, А. А. Кубатиев // Патогенез. – 2015. – Т. 13. – № 2. – С. 50-65.
- Осипова, Н. И Роллерная технология культивирования вируса парагриппа-3 (ПГ-3) / Н. И. Осипова // Ветеринария. Реферативный журнал. – 2002. – № 2. – С. 406.
- Самуйленко, А. Я. Оптимизация процесса промышленного культивирования культуры клеток ВНК-21/13-13 для производства вакцин против ящура, болезни ауески и бешенства / А. Я. Самуйленко, Н. В.Мельник, С. А. Гринь [и др.] // Ветеринарный врач. – 2018. – № 1. – С. 24-28.
- Юрков, С. Г. Универсальная роллерная технология культивирования перевиваемых клеток животных / С. Г. Юрков, А. Н. Курносов, С. А. Витина [и др.] // Ветеринария. − 1995. − № 9. − С. 29-34.
- Dill, V. Influence of cell type and cell culture media on the propagation of footand- mouth disease virus with regard to vaccine quality / V. Dill, B. Hoffmann, A. Zimmer [et al.] // Virology Journal. – 2018. – Vol. 15. - № 1. – Р. 46-57.
- Griffiths, B. Scale-up of suspension and anchorage-dependent animal cells / B. Griffiths // Molecular Biotechnology. – 2001. – Vol. 7. – № 3. – Р. 225-238.


