Успешная беременность после сохранения фертильности при опухолевом поражении яичников методом ОТО-IVM
Автор: Лавринович О.Е., Татищева Ю.А., Геркулов Д.А., Сломинская Н.А., Берлев И.В., Яковлева М.Г., Карицкий А.П., Калугина А.С.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 3 т.24, 2025 года.
Бесплатный доступ
Введение. Сохранение фертильности для женщин репродуктивного возраста с опухолевым злокачественным поражением яичников является одной из сложных проблем, т. к. органосохраняющее лечение может повышать риск развития рецидива. Непосредственное вовлечение вместилища всего резерва ооцитов в опухолевый процесс значительно ограничивает возможность реализации наиболее эффективных методов, например, абсолютно противопоказана стимуляция овуляции и криоконсервация коры яичника из-за риска контаминации опухолевыми клетками. Единственно возможным методом сохранения фертильности в таких случаях может быть метод OTO-IVM (Ovarian tissue oocyte in vitro maturation), в основе которого лежит получение незрелых ооцитов из ткани яичника, удаленного при хирургическом лечении, с их последующим дозреванием в условиях in vitro. Описание клинического случая. Представляем случай успешной беременности в результате комплексного междисциплинарного сохранения фертильности. Пациентке, 30 лет, c рецидивом пограничной опухоли в единственном яичнике выполнена операция с сохранением матки и удалением пораженного опухолью яичника. Из удаленного яичника извлечено 22 ооциткумулюсных комплекса. В результате ОТО-IVM получено 12 ооцитов стадии метафаза II, которые были оплодотворены методом интрацитоплазматической инъекции сперматозоида (ИКСИ), получено и криоконсервировано 3 эмбриона на стадии бластоцисты. Пациентке назначена циклическая гормонозаместительная терапия. Через 9 мес один эмбрион разморожен и перенесен в полость матки. В настоящее время констатирована нормально развивающаяся беременность 20 нед. Заключение. Метод ОТО-IVM как метод сохранения фертильности имеет высокую ценность у пациенток со злокачественным поражением яичников, с помощью которого рождение ребенка становится возможным. Необходимо продолжать исследования в совершенствовании метода, определении показаний и противопоказаний для его реализации.
Онкофертильность, сохранение фертильности, созревание ооцитов in vitro, OtO-iVM, опухолевое поражение яичников, овариоэктомия, беременность
Короткий адрес: https://sciup.org/140310584
IDR: 140310584 | УДК: 618.11-006.04-089.87:618.2 | DOI: 10.21294/1814-4861-2025-24-3-172-179
Successful pregnancy after fertility preservation using OTO-IVM method in ovarian cancer
Fertility preservation in women of reproductive age with ovarian cancer is still challenging. The ovarian-sparing surgery may increase the risk of recurrence. The direct involvement of the ovary in the tumor process significantly limits the ability to implement the most effective fertility preservation methods. For example, ovarian stimulation and ovarian cortex cryopreservation are absolutely contraindicated due to the risk of tumor cell contamination. In such cases, the only feasible fertility preservation method may be OTO-IVM (Ovarian Tissue Oocyte In Vitro Maturation), which involves retrieving immature oocytes from ovarian tissue removed during surgery and subsequent in vitro maturation. Clinical Case Description. We present a case of successful pregnancy achieved through comprehensive, multidisciplinary fertility preservation. A 30-year-old patient with a recurrent borderline ovarian tumor in her only remaining ovary underwent surgery with uterine preservation and removal of the affected ovary. From the tumor-involved ovary, 22 cumulus-oocyte complexes were obtained. Following OTO-IVM, 12 metaphase II oocytes were obtained and fertilized via intracytoplasmic sperm injection (ICSI) that resulted in 3 blastocyst-stage embryos, which were cryopreserved. Cyclic hormone replacement therapy was administered to the patient. Nine months later, one embryo was thawed and transferred into the uterine cavity. Currently, an ongoing 20-week pregnancy has been confirmed. Conclusion. The OTO-IVM method holds significant value as a fertility preservation technique for patients with ovarian cancer, making childbirth achievable. Further research is needed to refine the method, optimize protocols, and define clear indications and contraindications for its application.
Текст научной статьи Успешная беременность после сохранения фертильности при опухолевом поражении яичников методом ОТО-IVM
С 2021 г. в ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России ведется клиническое исследование «Оценка эффективности ОТО- IVM как метода сохранения фертильности больных злокачественными новообразованиями репродуктивных органов» (Выписка № 14/129 из протокола № 19 от 03.10.24 Комитета по этике при ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России), посвященное сохранению фертильности пациенток с опухолевым поражением яичников. Единственно возможным методом сохранения фертильности в таких случаях может быть метод OTO-IVM (Ovarian tissue oocyte in vitro maturation), в основе которого лежит получение незрелых ооцитов из ткани яичника, удаленного при хирургическом лечении, с их последующим дозреванием в условиях in vitro [1–4].
Стандартное дозревание in vitro предполагает забор незрелых комплексов «кумулюс-ооцит» из антральных фолликулов яичников, которые не подвергались стимуляции фолликулостимулирующим гормоном или подвергались минимальной стимуляции, с последующим их культивированием вне организма человека. Через 1–2 дня ооциты проходят путь от зародышевого пузырька до стадии метафазы II. Все остальные методы, необходимые для рождения живого ребенка, аналогичны или идентичны обычному экстракорпоральному оплодотворению. Следует отметить, что эффективность получения зрелых ооцитов значительно ниже, чем при классической стимуляции овуляции, и они демонстрируют более низкий потенциал для формирования бластоцист хорошего качества [5]. Однако данный фактор не умаляет значимости метода, когда никакой другой способ сохранения фертильности из собственного биологического материала не доступен. Кроме того, ценность метода ОТО-IVM может быть в сохранении дополнительного материала (ооцитов) при криоконсервации кортекса яичников, что отмечено в отчете Европейского общества репродукции человека и эмбриологии 2021 г. [3].
Научные публикации свидетельствуют о немногочисленных случаях рождения детей у пациенток после выздоровления в результате переносов эмбрионов, полученных из незрелых ооцитов, которые извлекались при криоконсервации коркового слоя яичников [6]. В статье 2023 г. сообщается о 5 живорождениях в мире после OTO-IVM, но только один из них – случай рождения ребенка из ооцита, полученного из пораженного опухолью яичника [7]. Клинический пример в статье 2014 г., где у молодой пациентки, 21 года, со злокачественной опухолью яичника стадии IIIC (микропапиллярная серозная карцинома яичника высокой степени дифференцировки) при овариэктомии были получены незрелые ооциты, часть из них дозрела и была оплодотворена. Полученные эмбрионы были криоконсервированы, а после выздоровления один из них перенесен в полость матки для достижения одноплодной здоровой беременности, приведшей к рождению ребенка [8].
В литературе второй случай родов пациентки, 33 лет, с пограничной опухолью левого яичника в анамнезе представлен публикацией 2024 г., когда при хирургическом лечении из удаленных яичников методом ОТО-IVM получено шесть зрелых ооцитов, которые были оплодотворены методом ИКСИ, и криоконсервировано три эмбриона. Через 3 мес после операции была начата заместительная гормональная терапия и перенесен размороженный эмбрион, что привело к успешной беременности и родам здоровым ребенком путем Кесарева сечения на 36-й нед беременности [9].
Клинический случай
Пациентка, 1994 г.р., наблюдалась у гинеколога по месту жительства (г. Петрозаводск) по поводу первичного бесплодия, гиперпролактинемии, синдрома поликистозных яичников. Планировалось проведение стимуляции овуляции в рамках протокола ЭКО. При контрольном обследовании (УЗИ органов малого таза) выявлено образование правого яичника, размерами 36×27 мм. При МРТ органов малого таза (23.07.21) подтвердилось образование в проекции правого яичника, размерами 28×21×34 мм, а также выявлено образование брюшины в позадиматочном пространстве – 7×7 мм.
Уровень онкомаркера СА–125 (19.06.22): 22 Ед/мл. В республиканском перинатальном центре по месту жительства 18.09.21 выполнено хирургическое лечение в объеме лапароскопии, удаления образования правого яичника, хромо-гидротубация. Гистологическое исследование операционного материала (28.09.21): High-Grade (низкодифференцированная) серозная карцинома. Цитологическое исследование жидкости в малом тазу (18.09.21): выпот с наличием клеток серозной аденокарциномы.
Пациентка самостоятельно обратилась в ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России, где пересмотрены данные обследования, проведенного по месту жительства. Пересмотрен диск МРТ с внутривенным контрастированием (03.10.21), по заключению которого данных за наличие патологических гиперваскулярных образований в полости малого таза не получено. При пересмотре КТ грудной клетки и брюшной полости с внутривенным контрастированием (05.10.21) убедительных данных за наличие вторичных изменений нет. 12.10.21 осуществлен пересмотр готовых цитологических препаратов интраоперационного забора жидкости из малого таза, где обнаружены комплексы клеток аденокарциномы. По данным пересмотра гистологического исследования операционного материала (09.10.21) исключена низкодифференцированная аденокарцинома, установлен диагноз серозной пограничной опухоли яичника. Гистологическое исследование эндометрия (пайпель – биоптат, 9.10.21) не выявило патологических изменений: фрагменты эндометрия пролиферативного типа, без атипии.
На междисциплинарном онкологическом консилиуме (14.10.21) принято решение о повторном хирургическом вмешательстве с целью хирургического стадирования. 29.10.21 выполнена операция в объеме лапароскопической правосторонней аднексэктомии, резекции левого яичника, оментэктомии, мультифокальной биопсии брюшины, иссечении инфильтрата в дугласовом пространстве. Для уточнения объема хирургического вмешательства интраоперационно выполнялось срочное гистологическое исследование, которое подтвердило пограничную серозную опухоль правого яичника, атипическую пролиферативную опухоль левого яичника, что позволило ограничиться органосохраняющим объемом.
По результатам цитологического исследования жидкости из малого таза (1.11.21) обнаружены комплексы и группы атипичных клеток. При иммуноцитохимическом исследовании подтверждено наличие опухолевых аденогенных клеток в асцитической жидкости. Заключительное гистологическое исследование операционного материала (3.11.21): пограничная серозная опухоль, атипическая пролиферативная серозная опухоль яичников с неинвазивными имплантами в брюшине малого таза и параректальной брюшине до 5 мм в наибольшем измерении, яичники с множественными серозными цистаденомами и фолликулярными кистами; правая маточная труба и большой сальник обычного строения. С диагнозом пограничная серозная опухоль правого яичника рT2bN0M0 пациентка выписана из центра.
С целью сохранения фертильности после онкологического консилиума и врачебной комиссии с 13.12.21 по 22.12.24 проведена стимуляция овуляции в протоколе с антагонистами ГнРГ, с заменой триггера финального созревания фолликулов на агонист ГнРГ, с профилактикой транзиторной гиперэстрогении ингибитором ароматазы (Ле- трозол) в дозировке 5 мг в сут, на протяжении всего курса введение гонадотропных препаратов. 24.12.21 выполнена пункция фолликулов: получено 15 ооцитов, оплодотворение методом ЭКО, криокосервированы 8 эмбрионов. По результатам предимплантационного генетического исследования на хромосомные анеуплоидии (ПГТ – А) два эмбриона утилизированы как не пригодные к переносу в полость матки (анеуплоидные). Один эмбрион при расконсервации не разморозился. С 8.08.22 в течение года проведены 3 попытки переноса размороженных эмбрионов в полость матки, беременность не наступила.
Пациентка наблюдалась по месту жительства. Со слов, в апреле 2023 г. выявлено объемное
Б/ B
А/ А
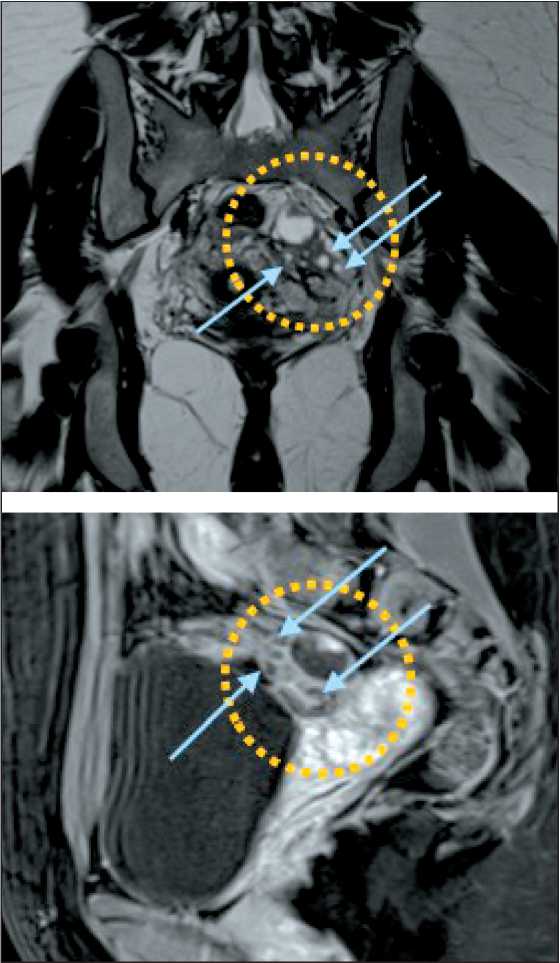
Рис. 1. МРТ органов малого таза с внутривенным контрастированием. Примечания: А – фронтальная проекция;
Б – сагиттальная проекция; желтым кругом выделен яичник, пораженный серозной пограничной опухолью; синими стрелками обозначены антральные фолликулы в яичнике; рисунок выполнен авторами
Fig. 1. MRI image of the pelvis with intravenous contrast. Notes: A – frontal projection; B – sagittal projection; the yellow circle shows the ovary affected by a serous borderline tumor; blue arrows indicate antral follicles in the ovary; created by the authors
Б/ B
А/ А
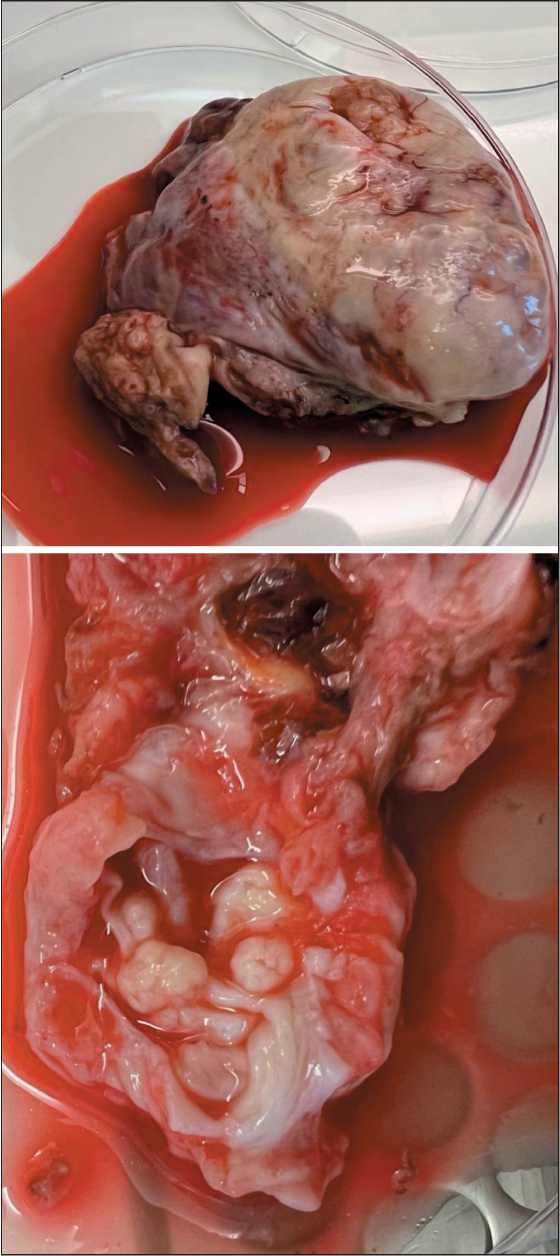
Рис. 2. Яичник, пораженный серозной пограничной опухолью. Примечание: А – вид снаружи; B – вид на разрезе;
рисунок выполнен авторами
Fig. 2. Ovarian serous borderline tumor. Notes: А – exterior view; B – section view; created by the authors
образование левого яичника. Онкологом по месту жительства рекомендовано динамическое наблюдение. При контрольном МРТ органов малого таза (22.09.23): левый яичник 5,4×2,4×3,7 см, с множеством фолликулов, в одном из них, размерами около 1 см с пристеночными разрастаниями по капсуле, активно накапливается контраст. Уровень СА– 125 (20.11.23): 18,7 ед/мл (от 21.04.22 – 3,01 Ед\мл).
Пациентка обратилась в НМИЦ онкологии им. Н.Н. Петрова. По данным МРТ органов малого таза с внутривенным контрастированием (26.12.23): левый яичник, размерами 35×44 мм, с фолликулами по периферии до 8 мм (рис. 1). По задней стенке визуализируется кистозное образование, размерами 23×15 мм, с неравномерно утолщенной капсулой и единичным пристеночным солидным утолщением, размерами 7×5 мм, интенсивно накапливающими контрастный препарат. Правый яичник удален.
При КТ грудной клетки и брюшной полости с внутривенным контрастированием (01.02.24) убедительных данных за наличие вторичных изменений не получено. Таким образом, выдвинуто предположение о рецидиве пограничной серозной опухоли (рT2bN0M0) в единственном правом яичнике. На междисциплинарном онкологическом консилиуме (17.01.24) принято решение о хирургическом лечении с одномоментным сохранением фертильности методом ОТО-IVM, которое реализовано 21.02.24 в объеме лапароскопии, ад-нексэктомии слева. Выполнен интраоперационный забор яичника (рис. 2) для транспортировки в репродуктивную клинику «Скайферт» и реализации метода ОТО-IVM. Яичник транспортировался в среде Flushing Medium (Origio) при температуре 37 °С. В условиях эмбриологической лаборатории из ткани яичника получено 22 ооцит-кумулюсных комплекса, 6 из которых были с признаками атрезии; до стадии МII успешно культивированы 12 ооцитов. Все дозревшие ооциты были оплодотворены спермой полового партнера (супруга) мето-
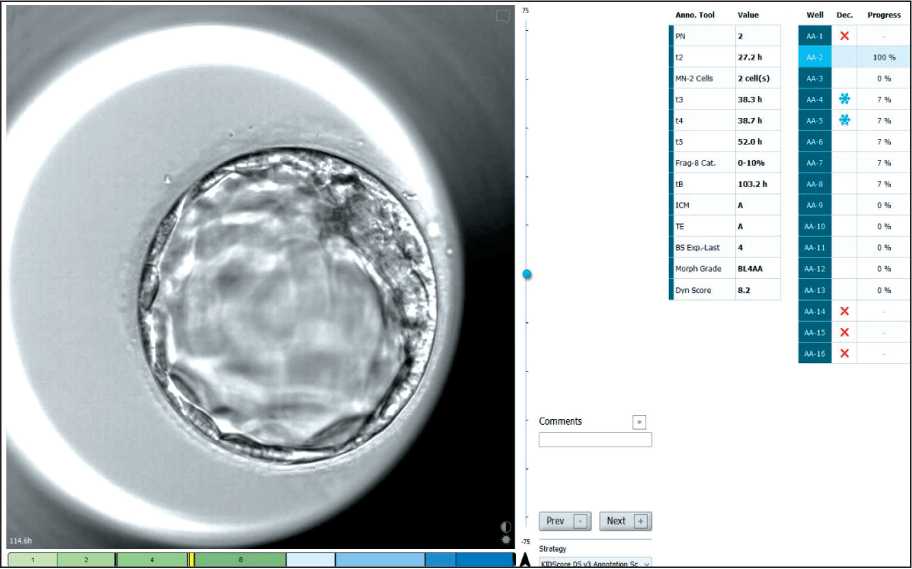
Рис. 3. Эмбрион (бластоциста 4АА) с оценкой морфокинетических параметров до криоконсервации. Примечание: рисунок выполнен авторами
Fig. 3. Embryo (blastocyst 4AA) with morphoki-netical assessment before cryopreservation. Note: created by the authors
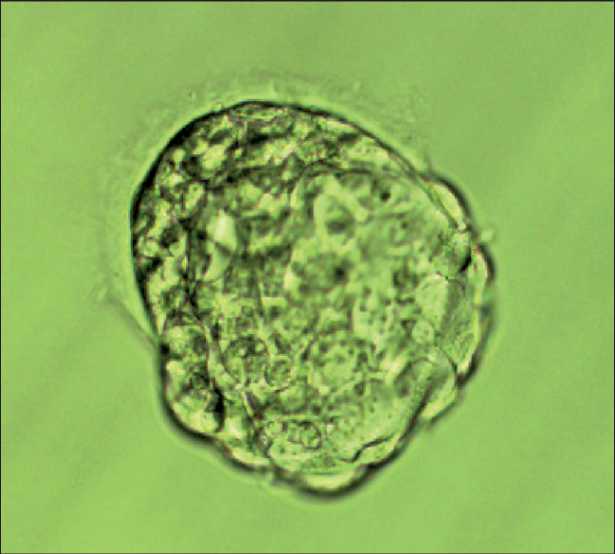
Рис. 4. Размороженный и перенесенный в полость матки эмбрион. Примечание: рисунок выполнен авторами Fig. 4. Embryo thawed and transferred into the uterine cavity.
Note: created by the authors дом ICSI, получено 10 зигот, их культивирование проводилось в time-lapse инкубаторе (EmbryoScope Plus) в одношаговой среде GTL (Vitrolife). На пятый день развития методом витрификации криокон-сервировано 3 эмбриона на стадии бластоциста (BL 4AA, BL4BC, BL2BB) (рис. 3).
Гистологическое исследование (02.03.24) подтвердило наличие рецидива пограничной серозной опухоли в левом яичнике на фоне серозной цистаде-номы (ICD-O code 8442/6). В рекомендациях после выписки пациентке была назначены циклическая гормональная заместительная терапия препаратом «Фемостон 2/10» и динамическое наблюдение у онколога по месту жительства. После очередного обследования и констатации ремиссии заболевания принято решение о возможности переноса эмбриона в полость матки.
С целью подготовки к переносу эмбриона проведена заместительная гормональная терапия (ЗГТ) препаратами эстрогенов (Эстрожель 7,5 мг в сут) и микронизированного прогестерона (Утро- жестан 600 мг в сут, вагинально). Разморозка и перенос эмбриона (рис. 4) в полость матки осуществлены 27.11.24, на 5-е сут приема ми-кронизированного прогестерона, на 18-й день менструального цикла. Толщина эндометрия на момент переноса эмбриона составила 10,2 мм.
Результат анализа крови на ХГЧ (09.12.24) – 807 мМЕ/мл. 24.12.24 проведена ультразвуковая диагностика беременности, плодное яйцо расположено в полости матки, сердцебиение плода визуализировано. 05.11.25 ультразвуковой скрининг на сроке 12 нед и 3 дня. В полости матки один живой плод: КТР – 66 мм, ЧСС – 142 в 1 мин. Заключение: Беременность 12 недель 3 дня. Предлежание хориона. 31.03.25 проведен второй ультразвуковой скрининг на сроке 20 нед и 1 день, заключение которого демонстрирует нормально развивающуюся беременность, соответствующую сроку гестации.


