Увеличение содержания каротиноидов в биомассе Vischeria punctatа Vischer при культивировании в лабораторном биореакторе
Автор: Кузнецова Т.А., Мустафакулов М.Х.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 4 (102) т.86, 2024 года.
Бесплатный доступ
Микроводоросли Vischeria punctata Vischer, штамм IPPAS H-242 (ИФР РАН им. К.А. Тимирязева) культивировали в лабораторном фотобиореакторе, наилучшей средой для выхода биомассы стала среда Болда. Внесение в среду Болда цианокоболамина и тиамина не привели к увеличению выхода биомассы. Для увеличения содержания каротинидов в биомассе микроводорослей было использовано дозированное воздействие различных концентраций перекиси водорода: от 0,1 до 0,3 мл/л суспензии микроводорослей. Одновременно с перекисью водорода в суспензию вносили пиридоксин в концентрации 50 мг/л. Перекись и пиридоксин вносились каждые двое суток при культивировании V. punctata, которое продолжалось 10 суток. Добавки перекиси водорода приводят к снижению продолжительность экспоненциальной фазы роста в вариантах с внесением перекиси водорода 0,1 и 0,2 мл/л на 1 сутки, с внесением перекиси водорода 0,3 мл/л на 2 суток. Также в ответ на стрессовое воздействие отмечено уменьшение средних размеров клеток в популяции. В варианте с концентрацией перекиси водорода 0,3 мл/л происходит снижение популяционной емкости и содержания суммы каротиноидов в воздушно-сухой биомассе. В вариантах с внесением перекиси водорода 0,1 и 0,2 мл/л отмечено увеличение доли каротиноидов в пигментном комплексе по сравнению с контролем на 18,12±0,20 и 18,92±0,14 % соответственно. Наилучшим вариантом эксперимента стало внесение 0,2 мл перекиси водорода на 1 л суспензии микроводорослей, при этом выход биомассы достоверно не отличался от контрольного варианта, содержание суммы каротиноидов возрастает на 23,1 % по сравнению с контролем и достигает 5,97±0,27 мг/г воздушно-сухой биомассы.
Микроводоросли, Vischeria punctata, культивирование, перекись водорода, каротиноиды
Короткий адрес: https://sciup.org/140309670
IDR: 140309670 | УДК: 581.6 | DOI: 10.20914/2310-1202-2024-101-75-83
Increase in carotenoid content in Vischeria punctata Vischer biomass during cultivation in a laboratory bioreactor
Microalgae Vischeria punctata Vischer, strain IPPAS H-242 (K.A. Timiryazev Institute of Physiology and Hydrology of the Russian Academy of Sciences) were cultivated in a laboratory photobioreactor; the best medium for biomass yield was Bold's medium. Addition of cyanocobalamin and thiamine to Bold's medium did not lead to an increase in biomass yield. To increase the carotenide content in the microalgae biomass, dosed exposure to various concentrations of hydrogen peroxide was used: from 0.1 to 0.3 ml/l of microalgae suspension. Pyridoxine at a concentration of 50 mg/l was added to the suspension simultaneously with hydrogen peroxide. Hydrogen peroxide and pyridoxine were added every two days during the cultivation of V. punctata, which lasted for 10 days. Hydrogen peroxide additions lead to a decrease in the duration of the exponential growth phase in the variants with the addition of 0.1 and 0.2 ml/l hydrogen peroxide for 1 day, and with the addition of 0.3 ml/l hydrogen peroxide for 2 days. Also, in response to stress, a decrease in the average cell size in the population was noted. In the variant with a hydrogen peroxide concentration of 0.3 ml/l, there is a decrease in the population capacity and the content of the sum of carotenoids in the air-dry biomass. In the variants with the addition of 0.1 and 0.2 ml/l hydrogen peroxide, an increase in the proportion of carotenoids in the pigment complex was noted compared to the control by 18.12±0.20 and 18.92±0.14%, respectively. The best variant of the experiment was the introduction of 0.2 ml of hydrogen peroxide per 1 liter of microalgae suspension, while the biomass yield did not differ significantly from the control variant, the content of the sum of carotenoids increased by 23.1% compared to the control and reached 5.97±0.11 mg/g of air-dry biomass.
Текст научной статьи Увеличение содержания каротиноидов в биомассе Vischeria punctatа Vischer при культивировании в лабораторном биореакторе
Микроводоросли относятся к важнейшим возобновляемым ресурсам, источникам биологически активных веществ, таких как белок, углеводы, липиды, антиоксиданты, в том числе и каротиноиды [1]. Метаболизм многих штаммов микроводорослей лабилен. В ответ на дозированное
стрессовое воздействие в биомассе микроводорослей накапливаются липиды, углеводы и антиоксиданты. УФ-излучение [2], изменение кислотности среды, снижение температуры культивирования [3] приводит к накоплению каротиноидов.
Основной способ получения каротиноидов в промышленности – химический синтез [4].
This is an open access article distributed under the terms of the Creative Commons Attribution 4.0 International License
Биотехнологическое получение каротиноидов из микроводорослей связано с недостаточным изучением каротиногинеза и факторов позволяющих увеличить содержание каротиноидов в биомассе без уменьшения ее выхода.
Синтез каротиноидов описан в строме хлоропластов и на мембранах тилакоидов [5, 6], а также в цитоплазме микроводорослей [6]. Большое внимание обращено на микроводоросли (например, Chloromonas reticulata Gobi, Dunaliella salina, Haematococcus pluvialis, Scenedesmus almeriensis [7]), накапливающие вторичные каротиноиды вне хлоропластов – нефотосинтетические пигменты, локализованные во внетилакоидных структурах (липидных глобулах) [1]. В стрессовых условиях накопление вторичных каротиноидов связано с накоплением липидов [7,19]. Каротиноиды выполняют важную светособирающую, структурную функцию [8]. Ксантофиллы виолаксантинового цикла в присутствии активных форм кислорода защищают хлорофиллы и липиды от разрушения и обеспечивают устойчивость тилакоидных мембран при высокой интенсивности света [9].
Активные формы кислорода постоянно генерируются в электронно-транспортных цепях митохондрий и хлоропластов [8]. Молекулы Н 2 О 2 не заряжены, имеют низкую реакционную способность, в водных растворах они на расстояниях до 1 мкм. В небольших концентрациях молекулы перекиси являются внутриклеточными мессенджерами, в концентрациях от 1 до 50 мМ они токсичны для клеток [2]. Частью антиоксидантных систем являются ферментативные системы, удаляющие активные формы кислорода (супероксиддисмутаза, каталаза и др.), а также полиеновые соединения, к которым относятся каротиноиды [10,18]. Их антиоксидантная активность определяется наличием двойных связей в молекуле. Антиоксидантная активность каротиноидов in vitro зависит от содержания активных форм кислорода в среде [8].
Vischeria punctata Vischer – пресноводная микроводоросль, обитатель почв [10], неприхотлива при культивировании [11]. Штаммы этой микроводоросли перспективны, так как способны накапливать липиды, незаменимые жирные кислоты [12,20], например эйкозопентоеновую кислоту [11, 13]. Биомасса микроводоросли рассматривается как субстрат для получения биогаза [12]. При культивировании ее на бедных питательными средах эта микроводоросль накапливает экзо- и эндополисахариды [13]. Однако особенности культивирования и метаболизм V. punctata до конца не изучены. Биомасса V. punctata описана как источник β-каротина
Цель работы – определение режима направленного культивирования микроводорослей V. punctata для увеличения содержания каротиноидов в биомассе.
Материалы и методы
Образцы микроводоросли V. Punctate Vischer (штамм IPPAS H-242) была получена из коллекции Балтийского федерального университета им. Иммануила Канта.
Маточную культуру микроводоросли хранили при температуре от 3 до 4 ºС. После шести месяцев хранения маточная культура обновлялась, культивировалась на среде Болда [12] до фазы замедленного роста.
Для культивирования микроводоросли использовали лабораторный биореактор, представляющий собой барботажную колонну объемом 500 мл. Барботирование воздухом в режиме 1,5 л/мин. позволяет перемешивать клеточную суспензию. Определение концентрации клеток при культивировании проводили нефелометрически каждые сутки [5], предварительно суспензию перемешивали. Оптическую плотность определяли спектрофотометром ЮНИКО 1201, при длине волны 750 нм, в кювете сравнения ˗ питательная среда. Для определения оптической плотности каждые сутки отбирали аликвоту (10 мл), до необходимого объема доливали питательную среду. Применение сливно-долиной системы при культивировании микроводорослей позволяет удлинить период экспоненциального роста и увеличить плотность клеток на конец культивирования. Начальная концентрация клеток микроводоросли в питательной среде составляла не более 5 млн кл/мл. Режим освещенности день – 16 часов, ночь – 8 часов, лампа дневного света (ФАР), интенсивность освещенности – 20 кЛк на м2, Т(К) – 400. Культивирование проводили до фазы стабилизации, когда прекращается рост клеток в популяции микроводорослей. Удельную скорость роста находили по формуле:
Ц = ln ( x2 /x1 )/( t 2 - t 1 ) , (1)
где х 1 и х 2 – концентрация клеток, млн клеток на мл в момент времени t 1 и t 2 , соответственно.
Полученную при культивировании суспензию микроводорослей отстаивали в течение двух суток. После отделения питательной среды, сконцентрированную биомассу микроводорослей центрифугировали в режиме – 6000 об/мин в течение 5 минут. Надосадочную жидкость декантировали. Осадок высушивали на воздухе в тёмном месте при Т от 20 до 25 °С до постоянного веса. Хранили воздушно-сухую биомассу в закрытых стерильных ёмкостях при температуре 4–5 °С.
Экстракцию фотосинтетических пигментов проводили 96%-ным этанолом при ультразвуковом облучении на приборе «WiseClean WUC-A06H». Навеску воздушно-сухой биомассы 0,025 г. заливали 10 мл 96%-ного этанола (ГОСТ 5962–2013) и облучали на ультразвуковой ванне «WiseClean WUC-A06H» в режиме 35 кГц, при температуре 40 °С в течение 30 минут. Экстракт отделяли от биомассы центрифугированием в режиме 3500 об/мин в течение 5 минут на приборе СМ-6МТ. Содержание фракций фотосинтетических пигментов в этанольных экстрактах определяли спектрофотометрическим методом [14], определяли оптическую плотность при длинах волн 470 нм (сумма каротиноидов), 649 нм (хлорофилл b), 664 нм (хлорофилл а).
Для оценки состояния популяции клеток при культивировании в разных режимах проводили микроскопрование прижизненных препаратов при увеличении в 640 раз (микроскоп МикМед-6). Микрофотографии делали цифровой камерой IS-500 при использовании компьютерной программы МС-foto. Анализировали не менее 10 полей зрения в каждом варианте, измеряли не менее 50 клеток с помощью программы Le-venhuk. Пересчет в микрометры проводили с помощью коэффициента пересчета, для которого проводили измерения объект-микрометра (ОМП, 0,01 мм, ГОСТ 7513–55).
Полученные результаты статистически обрабатывались: находили среднее значение и ошибку средней. Достоверность отличий определяли, пользуясь критерием Стьюдента.
Результаты
Подбор оптимальной питательной среды для наращивания биомассы V. punctata. В известных базах данных по микроскопическим водорослям рекомендовано для культивирования V. punctata среды Прата и Болда (ВВМ 3N) [11] и модифицированы среда Болда (ВВМ 3N + V) [10], которая отличается наличием витаминов – цианокобаламина и тиамин гидрохлорида. Среда Болда и ее модифицированный вариант по сравнению со средой Прата, богаты нитратами, дополнительно включают соли цинка, кобальта и молиб- дена. Для определения оптимальной среды культивирования был проведен опыт с использованием трех рекомендованных сред (рисунок 1).
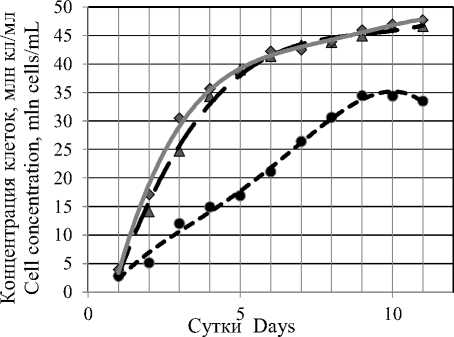
▲ Среда Прата ♦ BBM 3N+V • BBM 3N
Рисунок 1. Кривые культивирования Vischeria punctata в различных питательных средах
Figure 1. Cultivation curves of Vischeria punctata in different nutrient media
Лаг-фаза в вариантах не превышала суток, что характеризует высокую метаболическую активность популяции микроводоросли в маточной культуре. Максимальный скорость роста в среде Болда и ее модифицированном варианте наблюдали в первые 6 суток культивирования, далее она снижалась и к 9 ˗ 10 суткам наступала фаза стабилизации. Концентрация клеток в суспензии достигала 47,0 ± 4,5 млн кл/мл, при этом существенных различий в росте популяции V. punctata в среде Болда и ее модифицированном варианте не наблюдалось (таблица 1).
Среда Прата оказалась менее продуктивной, прирост биомассы наблюдался до 10 суток культивирования, при этом концентрация клеток в суспензии достигала 35,0 ± 3,0 млн кл/мл. На 11 сутки культивирования начинается фаза истощения.
Значение рН в питательных средах находилось в пределах 4,7–5,0. При культивировании V. punctata в течение 10–11 суток происходило увеличение значений рН до 9,88 в среде Прата, до 10,27 и в среде Болда и 10,02 в модифицированной среде Болда, что связано с усвоением нитрат-ионов из среды. Защелачивание среды способствует флокуляции клеток, при этом их метаболическая активность снижается, рост популяции замедляется.
Выход воздушно-сухой биомассы достигает 2,32 ± 0,21 и 2,26 ± 0,11 г/л (среда ВВМ 3N и ВВМ 3N + V соответственно), что выше, чем в среде Прата (1,15 ± 0,20 г/л).
Таблица 1.
Выход воздушно-сухой биомассы после культивирования Vischeria punctata в рекомендованных средах
Table 1.
Yield of air-dried biomass after cultivation of Vischeria punctata in recommended media
|
Питательная среда Nutrient medium |
Удельная скорость роста в экспоненциальную фазу, μ Specific growth rate in exponential phase, μ |
Популяционная емкость, К, млн кл/мл Population capacity, K, mln cl/mL |
рН на конец культивирования pH at the end of cultivation |
Выход биомассы, г/л Biomass yield, g / l |
|
Среда Прата |
0,279 |
33,49 |
9,88 |
1,15 |
|
ВВМ 3N |
0,543 |
46,60 |
10,27 |
2,32 |
|
ВВМ 3N + V |
0,442 |
47,69 |
10,02 |
2,26 |
Таким образом, наиболее эффективной для наращивания биомассы V. punctata оказалась среда ВВМ3N, добавка витаминов не имела существенного значения для накопления биомассы.
Исследование влияния добавки пиридоксина и различных концентраций перекиси водорода на показатели культивирования V. punctata. Дозированное внесение перекиси водорода и пиридоксина в питательную среду Болда проводили в первые сутки культивирования V. punctata, и каждые двое суток до конца культивирования, при этом суспензию микро-водорослей хорошо перемешивали. Перекись водорода в вариантах вносили в концентрациях от 0,1 до 0,3 мл/л суспензии микроводорослей. Совместно с перекисью в питательную среду вносили пиридоксин в концентрации 50 мг/л суспензии микроводорослей среды во всех вариантах (таблица 2). В контрольный вариант перекись и пиридоксин не вносили. Остальные условия культивирования (режим освещенности, температура) были такими же, как и в предыдущем эксперименте.
Таблица 2.
Схема эксперимента (базовая среда Болда)
Table 2.
Experimental design (Bold's base environment)
|
Вариант Option |
V питательной среды, мл V of nutrient medium, ml |
V H 2 O 2 , мл на 500 мл V H 2 O 2 , ml per 500 ml |
М пиридоксина, мг на 500 мл M pyridoxine, mg per 500 ml |
|
контроль control |
500 |
0 |
0 |
|
2 |
500 |
0,05 |
25 |
|
3 |
500 |
0,10 |
25 |
|
4 |
500 |
0,15 |
25 |
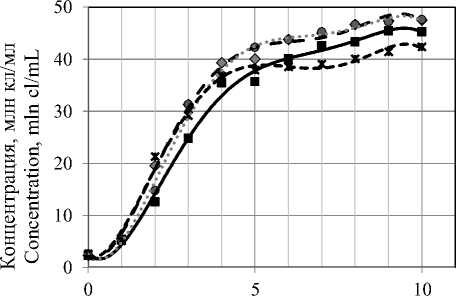
Продолжительность лаг-фазы в экспериментальных вариантах и в контроле не превышала суток. Экспоненциальная фаза роста в контрольном варианте на шестые сутки переходила в фазу замедленного роста (при концентрации 35,68 млн кл/мл). В вариантах с внесением перекиси водорода 0,1 и 0,2 мл/л суспензии микроводорослей экспоненциальная фаза завершалась на пятые сутки культивирования (при концентрации 39,31 и 36,86 млн кл/мл соответственно). В варианте со снесением перекиси водорода 0,3 мл/л суспензии микроводорослей экспоненциальная фаза завершалась на четвертые сутки культивирования (при концентрации 29,13 млн кл/мл) (рисунок 2).
Продолжительность культивирования V. punctata составляла 10 суток, при этом максимальная концентрация клеток достигала в вариантах с внесением перекиси водорода 0,1 и 0,2 мл/л (47,47 и 47,58 млн кл/мл соответственно). В варианте с добавлением перекиси водорода 0,3 мл/л суспензии микроводорослей концентрация клеток достигала 42,34 млн кл/мл, что ниже значений в контрольном варианте.
Сутки Days
V Н2О2, мл/л: ■ контроль (0) ♦0,1 о 0,2 ж 0,3
Рисунок 2. Кривые культивирования суспензий водорослей в среде (ВВM3N) с добавлением перекиси водорода разной концентрации
Figure 2. Curves of cultivation of algae suspensions in a medium (BBM3N) with the addition of hydrogen peroxide of different concentrations
В фазу стабилизации оценивали состояние популяции микроводорослей по микроскопической картине прижизненных неокрашенных препаратов. Наиболее информативным показателем, характеризующим средний размер клеток в популяции, стала площадь проекции клеток (таблица 3). При увеличении объема вносимой перекиси водорода площадь проекции уменьшается пропорционально количеству вносимой добавки.
В вариантах с внесением перекиси водорода 0,1 и 0,2 мл/л (варианты 2 и 3) отмечена тенденция к увеличению популяционной емкости по сравнению с контролем, что связано со стимулирующим влиянием фактора роста пиридоксина, увеличивался выход воздушно-сухой биомассы.
В варианте 4 происходит снижение популяционной емкости, что расцениваем как следствие неблагоприятного влияния наивысшей концентрации вносимой перекиси водорода (0,15 мл на 500 мл) на ростовые характеристики популяции микроводоросли.
Содержание пигментов в биомассе V. punctata , полученной при влиянии добавок пиридоксина и различных концентраций перекиси водорода. Спектрофотометрическим методом определяли содержание фракций пигментного комплекса (хлорофилла а, хлорофилла б и суммы каротиноидов) и их соотношения (таблица 4).
Таблица 3.
Выход воздушно-сухой биомассы после культивирования микроводоросли Vischeria punctata при добавлении перекиси водорода и пиридоксина
Table 3.
Yield of air-dried biomass after cultivation of microalgae Vischeria punctata with the addition of hydrogen peroxide and pyridoxine
|
Вариант | Option |
Удельная скорость роста в экспоненциальную фазу, μ Specific growth rate in exponential phase, μ |
Популяционная емкость, К, млн кл/мл Population capacity, K, million cells / ml |
Площадь проекции клеток, мкм2 Projection area of cells, µm2 |
Выход биомассы, г/л Biomass yield, g/l |
|
Контроль | control |
0,549 |
45,42 |
15,54 ± 0,84 |
2,32 |
|
2 |
0,572 |
47,47 |
15,58 ± 1,02* |
2,52 |
|
3 |
0,556 |
47,58 |
14,69 ± 1,11 |
2,66 |
|
4 |
0,667 |
42,34 |
14,46 ± 0,90 |
2,30 |
Примечание: ± доверительный интервал; *достоверные отличия с вероятностью 95%.
Note: ± confidence interval; * significant differences with a probability of 95%.
Таблица 4.
Сводная таблица содержания пигментов в биомассе в различных вариантах эксперимента
Table 4.
Summary table of pigment content in biomass in different experimental variants
|
Содержание пигментов, мг/г сухой биомассы The pigment content, mg/g dry biomass |
Образцы биомассы, полученные в различных условиях культивирования Biomass samples obtained under various cultivation conditions |
|||
|
Контроль Control |
Концентрация Н 2 О 2 мл/л суспензии V. punctata Concentration of H 2 O 2 ml/l of V. punctata suspension |
|||
|
0,1 |
0,2 |
0,3 |
||
|
Хлорофилл а | Chlorophyll a |
16,17 ± 0,69 |
18,35 ± 1,1** |
17,50 ± 0,76* |
17,73 ± 0,81* |
|
Хлорофилл б | Chlorophyll b |
7,04 ± 0,54 |
8,09 ± 0,588** |
8,09 ± 0,54* |
8,61 ± 0,39** |
|
Сумма каротиноидов | Sum of carotenoids |
4,85 ± 0,08 |
5,84 ± 0,29** |
5,97 ± 0,27** |
4,36 ± 0,29* |
|
Сумма пигментов | Pigment amount |
28,06 ± 1,24 |
32,28 ± 1,79** |
31,56 ± 1,47** |
30,70 ± 0, 1, 27* |
|
Доля каротиноидов от суммы пигментов, % The proportion of carotenoids from the amount of pigments, % |
17,32 ± 0,59 |
18,12 ± 0,49* |
18,92 ± 0,34** |
14,20 ± 0,539** |
|
Соотношение хлорофиллов а/б The ratio of chlorophyll a/b |
2,30 ± 0,12 |
2,27 ± 0,12 |
2,17 ± 0,10 |
2,06 ± 0,10* |
|
Хл (а + б)/Кар | Ch(a + b)/car |
4,78 ± 0,20 |
4,52 ± 0,15 |
4,29 ± 0,10 |
6,04 ± 0,22* |
Примечание: ± доверительный интервал; • достоверные отличия с вероятностью 95%, ** – достоверные отличия с вероятностью 99%
Note: ± confidence interval; • significant differences with a probability of 95%, ** significant differences with a probability of 99%
По результатам эксперимента было определено достоверное увеличение содержания суммы фотосинтезирующих пигментов в биомассе микроводорослей в вариантах с дозированным внесением перекиси водорода и пиридоксина, что связано с активирующим влиянием пиридоксина. Самая большая прибавка содержания суммы пигментов (на 15,0% по сравнению с контролем) отмечена в варианте с минимальной концентрацией вносимой перекиси 0,1 мл/л суспензии микроводорослей. Увеличение добавки перекиси снижает нарастание содержания пигментов: в варианте с добавкой 0,2 мл/л суспензии – на 12,5%, в варианте с добавкой 0,3 мл/л суспензии – на 9,4%.
Также отмечаем, что с увеличением доли вносимой перекиси происходит снижения содержания фракции хлорофилла а и увеличение содержания хлорофилла б, что связано с окислением хлорофилла а. Эта закономерность отражена в изменении отношения фракций хлорофиллов (таблица 4).
В вариантах с концентрацией вносимой перекиси 0,1 и 0,2 мл/л достоверно увеличивается содержание суммы каротиноидов по сравнению с контролем, на 20,4 и 23,1% соответственно. В этих вариантах проявился адаптационный потенциал популяции V. punctata . В варианте с внесением перекиси водорода 0,3 мл/л суспензии микроводорослей адаптационные возможности популяции микроводорослей недостаточны для преодоления стрессового воздействия. В этом варианте мы видим значимое уменьшение содержания суммы каротиноидов на 10,1% по сравнению с контролем.
В вариантах происходит изменение содержания различных видов пигментов, поэтому мы определили относительную величину: долю каротиноидов от суммы фотосинтезирующих пигментов. В вариантах с добавлением перекиси в концентрациях 0,1 и 0,2 мл/л происходит достоверное увеличение доли каротиноидов в пигментном комплексе по сравнению с контролем на 4,6 и 9,2% соответственно. А в варианте с внесением перекиси 0,3 мл/л доля каротиноидов существенно снизилась, на 18,0%, что предположительно связано с высокой стрессовой нагрузкой на антиоксидантные системы микроводорослей.
Обсуждение
Известно, что в хлоропластах образуются активные формы кислорода (АФК), в том числе и перекись водорода, которые при определенных условиях негативно влияют на мембраны тилакоидов [16]. Перекись водорода способна вызывать широкий спектр повреждений, в том числе связанных с перекисным окислением липидов (ПОЛ) [2, 3]. Перекись водорода также способна к окислению сульфгидрильных групп белков в клетках, эта характеристика может объяснять ингибирующее воздействие перекиси на ферменты цикла Кельвина [17].
Важное значение для осуществления фотосинтеза имеет как общее содержание фотосинтезирующих пигментов, так и соотношение различных видов пигментов. Внесение перекиси водорода в суспензию микроводорослей при культивировании в концентрациях от 0,1 до 0,3 мл/л совместно с пиридоксином (25 мг/л) один раз в двое суток, не приводит к уменьшению содержания суммы пигментов, но приводит к существенному изменению их соотношения, что характеризует значимое влияние на метаболизм фотосинтезирующих пигментов.
У высших растений в стрессовых условиях снижение показателя отношения суммы хлорофиллов к сумме каротиноидов в пигментном комплексе «Ch(a + b)/car» является следствием ПОЛ, которое сопровождается накоплением в фотосинтезирующих тканях малонового диальдегида (МДА) [16]. В нашем исследовании этот показатель снижается в вариантах с внесением перекиси водорода 0,1 и 0,2 мл/л по сравнению с контролем, однако учитывая отсутствие снижения суммы пигментов, фракций хлорофиллов и высокую интенсивность нарастания биомассы при культивировании, мы можем говорить о компенсированном стрессе.
В варианте с внесением 0,3 мл/л перекиси водорода происходит снижение содержания суммы каротиноидов в биомассе, что приводит к увеличению соотношения «Ch(a + b) / car», учитывая сниженные ростовые характеристики, мы характеризуем состояние этой популяции как стрессовое без оптимальной его компенсации.
Заключение
По результатам исследования можно сделать следующие выводы:
Наилучшее нарастание биомассы V. punctata (IPPAS H-242) отмечено в среде Болда. Среда Прада менее продуктивна и скорее подходит для сохранения культуры при холодильном хранении. Добавки витаминов в модифицированной среде Болда не привели к увеличению выхода биомассы V. punctata при культивировании.
Внесение перекиси водорода в концентрациях от 0,1 до 0,3 мл/л и 50 мг/л пиридоксина каждые двое суток в течение всего периода культивирования привело к уменьшению продолжительности экспоненциальной фазы роста. В контроле она длилась до 6 суток, в вариантах с внесением перекиси водорода 0,1 и 0,2 мл/л она укорачивается до 5 суток, а в варианте с внесением 0,3 мл/л перекиси водорода она длится до 4 суток. Выход биомассы и популяционная емкость в вариантах с внесением перекиси водорода 0,1 и 0,2 мл/л увеличивается по сравнению с контролем.
Анализ микроскопической картины показал, что в вариантах с внесением перекиси водорода наблюдается тенденция к уменьшению средних размеров клеток в популяции пропорционально доле вносимой перекиси.
Влияние добавки перекиси водорода разной концентрации в сочетании с пиридоксином не привело к уменьшению суммарного содержания фотосинтезирующих пигментов, однако отразилось на соотношении различных видов пиментов в исследуемом комплексе. Перекись водорода способствует окислению хлорофилла а, что отразилось в уменьшении соотношения хлорофилла а к хлорофиллу б. В вариантах с внесением перекиси водорода 0,1 и 0,2 мл/л отмечено увеличение доли каротиноидов в пигментном комплексе по сравнению с контролем на 18,12 ± 0,20 и 18,92 ± 0,14% соответственно. Усиленный каротиногенез отражает компенсаторные реакции на дозированное стрессовое воздействие, которое связано с ПОЛ. В варианте с внесением перекиси водорода 0,3 мл/л содержание каротиноидов снижается по сравнению с контрольным вариантом, что характеризует некомпенсированное стрессовое состояние популяции микроводорослей.
Максимальное содержание каротиноидов отмечено в варианте с внесением перекиси водорода 0,2 мл/л и составляет 5,97 ± 0,27 мг на г воздушносухой биомассы микроводоросли, что достоверно выше этого показателя в контроле на 41,3%.
Рекомендованный способ направленного культивирования V. punctata (штамм IPPAS H-242) позволит получить биомассу с увеличенным содержанием каротиноидов, без уменьшения выхода биомассы при культивировании. Полученную биомассу можно использовать для получения не только каротиноидов, но и других ценных биоактивных соединений для применения в пищевой, косметической и фармацевтической промышленности.


