Варианты дренирования верхних мочевых путей после лапароскопической пиелопластики у детей
Автор: Рудин Ю.Э., Марухненко Д.В., Лагутин Г.В.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Детская урология
Статья в выпуске: 2, 2017 года.
Бесплатный доступ
Введение. В научных работах, посвященных лапароскопической пиелопластике у детей при лечении гидронефроза, указывается на трудности дренирования почки в послеоперационном периоде и связанные с этим осложнения. Цель исследования показать варианты временного отведения мочи после лапароскопической пиелопластики у детей в зависимости от степени гидронефроза и возраста. Материалы и методы. В детском уроандрологическом отделении НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина в 2010- 2016 гг. оперировано 98 детей (62 мальчика и 49 девочек) с гидронефрозом в возрасте от 9 мес. до 17 лет (средний возраст составил 3,48 года). 96 пациентов оперированы лапароскопическим доступом, двое детей - ретроперитонеоскопически. Выполнялась пластика лоханочно-мочеточникового сегмента по методу Anderson-Hynes, у двух пациентов она сочеталась с литоэкстракцией, 5 пациентам выполнен антевазальный пиело-пиелоанастомоз. Длительность операции колебалась от 90 до 370 мин (155 ±15,2 мин). В зависимости от способа дренирования пациенты распределились следующим образом: внутренний стент установлен 72 пациентам, стент-пиелостома - 9 (детям 10-24мес), внутренний стент+нефростома - 15, нефростома - 2 больным. 65 детям дренажи были установлены антеградно, 7 пациентам младшего возраст - ретроградно. Результаты. Среди интраоперационных осложнений отмечено кровотечение из брюшной стенки в области установки троакара у 1 (1%) пациента и конверсия у 1 (1%) ранее трижды оперированного пациента. В зависимости от способа дренирования почки были отмечены следующие осложнения. При установке JJ стента: мочевой затек отмечен у 4 (4,1%) детей с гидронефрозом 4 ст., нарушение функции дренажа со значительным расширением чашечно-лоханочной системы и острым пиелонефритом - у 2 (2%) пациентов, рефлюкс по стенту - у 1 (1%) пациента, нарушение функции стент-пиелостомы - у 1 (1%) пациента, самостоятельное ее отхождение - 1 (1%) пациент, выпадение нефростомы - у 1 (1%) ребенка. Длительность послеоперационного дренирования в среднем составила 34,6±2,4 дня. Однако при сужении предпузырного отдела мочеточника и гидронефрозе 4 ст. стент удаляли через 6-7недель. Хороший эффект лечения без осложнений, получен у 88 (89,7%) больных в результате одной операции. Успешный результат лапароскопической пиелопластики удалось достичь у 93 (94,9%) пациентов после первой операции лапароскопической пластики ЛМС и у 100% больных. После повторной операции. Заключение. Детям младенческого и младшего возраста (10-24 мес) при выполнении эндовидеохирургической пиелопластики предпочтительно использование стент-пиелостомы. Больным с гидронефрозом 3-4 ст. со значительным расширением ЧЛС и снижением функции почки целесообразно применение двойного дренирования - JJстент + нефростома или пиелостома. Бездренажные методики эндовидеохирургической пластики ЛМС не имеют показаний к широкому применению, особенно у детей младшего возраста. Оптимальный метод послеоперационного дренирования почки после лапароскопической пиелопластики позволяет улучшить результаты оперативного лечения и снизить частоту послеоперационных осложнений.
Гидронефроз, дренирование верхних мочевыводящих путей, лапароскопическая пиелопластика, дети
Короткий адрес: https://sciup.org/142188186
IDR: 142188186
Variants for upper urinary tract drainage after laparoscopic pyeloplasty in children
Introduction. Scientific papers, which deal with laparoscopic pyeloplasty in children with hydronephrosis, pay attention to the difficulties of renal drainage during the postoperative period and the associated complications. The aim of this study is to demonstrate the variants of temporary urine diversion in children after laparoscopic pyeloplasty, depending on the degree of hydronephrosis and patient’s age. Materials and methods. 98 children (62 males and 49 females), aged from 9 months to 17 years (mean age was 3.48 years) underwent surgery in the pediatric uroandrological department of N. Lopatkin Research Institute of Urology and Interventional Radiology (Moscow, Russia) during the period of 2010-2016. 96 patients received surgery with laparoscopic access; two patients underwent retroperitoneoscopic surgery. Surgery of the pyeloureteral segment was performed according to Anderson-Hynes method; in two patients, the operation was combined with lithoextraction. 5 patients underwent antevasal pyelo-pyelo anastomosis. The duration of the surgery varied from 90 to 370 min (mean 155±15.2 min). According to the way of drainage, the patients were distributed as follows: 72 patients had internal stenting, 9 patients (aged 10-24 months) received internal stenting combined with nephrostomy, nephrostomy was performed in 2 patients. 65 patients had antegrade drainage; 7 infants had retrograde drainage. Results. Among intraoperative complications, one patient (1%) had bleeding from the abdominal wall, where a trocar was placed. In addition, one patient (1%), who previously underwent three surgical interventions, had conversion. Depending on the type of renal drainage, the following complications were recorded. Among those with the JJ stent, urinous infiltration was found in 4 patients (4.1%) with grade IV hydronephrosis, two patients (2%) had impairment of drainage function combined with the dilation of the pelvicalyceal system and acute pyelonephritis, one patient (1%) had reflux, one had impaired function of pyelostomy stenting, one had its withdrawal, and one child (1%) had a nephrostomy loss. The mean duration of post-operative drainage was 34.6±2.4 days. However, stent withdrawal was performed 6-7 weeks after the surgery in case of 4 grade hydronephrosis and constriction of the prevesical ureter. A good outcome of treatment, without complications, was in 88 patients (89.7%), who had one surgery. We managed to perform successful laparoscopic pyeloplasty in 93 patients (94.9%) after the first surgery of the pyeloureteral segment. The second surgical intervention brought successful results in 100% of the patients. Conclusion. It is preferable to perform internal stenting combined with nephrostomy for treating babies (aged 10-24 months), who undergo endovideosurgical pyeloplasty. For patients with grades III-IV hydronephrosis, who have significant dilation of the pelvicalyceal system and impairment of renal function, it is advisable to apply double drainage: the JJ stent combined with nephrostomy or pyelostomy. Non-drainage methods of endovideosurgical plasty of the pelvicalyceal system are not recommended for wide application, especially in babies. The optimal method of post-operative renal drainage after laparoscopic pyeloplasty helps to increase the results of surgical treatment and reduce the incidence of post-operative complications.
Текст научной статьи Варианты дренирования верхних мочевых путей после лапароскопической пиелопластики у детей
а сегодняшний день «золотым стандартом» для коррекции проходимости лоханочно-мочеточникового сегмента у детей остается расчленяющая пластика лоханочно-мочеточ никового сегмента (ЛМС), предложенная J. Anderson и W. Hynes в 1949 году [1], которая по прошествии времени доказала свою надежность и высокий процент хороших результатов (более 90%) [2-13]. До конца XX века данная методика операции выполнялась из открытого доступа. Однако в конце двадцатого столетия появились работы о возможности выполнения данной операции эндовидеохирургическим трансперитонеальным доступом. Так, в 1995 г. С. Peters и соавт. сообщили о первой выполненной лапароскопической пиелопластике (ЛП) у ребенка [14].
В первых сериях наблюдений указывалось на длительное время операции, что связывалось с неопытностью хирургов в использовании лапароскопического доступа, особенно в наложении швов, с несовершенством оптики [15]. Улучшение технической оснащенности операционных, накопление опыта хирургами и активное знакомство с техникой интракорпорального на- ложения швов позволили улучшить результаты лапароскопической пиелопластики, которые стали сопоставимы с результатами открытых операций [16-19].
Однако результат оперативного лечения гидронефроза зависит не только от оперативного доступа, метода коррекции проходимости ЛМС, опыта хирурга, исходного функционального состояния мочевых путей. Важную роль играет обеспечение адекватного дренирования мочевых путей в послеоперационном периоде.
Существуют работы, посвященные сравнению дренажной и бездренажной пиелопластики [2022]. Сравниваются варианты дренирования пиелостомой, нефросто-мой и JJ стентом, положительные и отрицательные стороны каждого метода.
Обсуждаются преимущества и недостатки антеградной и ретроградной установки внутреннего стента, возможные осложнения дилятации дистального отдела мочеточника при ретроградном дренировании стентами у детей младенческого возраста [23].
Таким образом, на сегодняшний день остается открытым вопрос не только необходимости дренирования верхних мочевых путей после эндовидеохирургического варианта пиелопластики, но и окончательно не определен оптимальный вариант отведения мочи из почки после подобных операций.
В данной работе мы представляем наш опыт использования различных вариантов дренирования мочевыводящих путей после лапароскопической пиелопластики у детей в зависимости от степени гидронефроза, уровня снижения функции почки и возраста ребенка.
МАТЕРИАЛЫ И МЕТОДЫ
В период с 2010 по 2016 г. на базе детского уроандрологического отделения НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИРЦ» Минздрава России оперировано 98 детей (62 мальчика и 36 девочек) с гидронефрозом в возрасте от 9 мес. до 17 лет, средний возраст составил 3,48 года.
На дооперационном этапе всем больным проводилось стандартное урологическое обследование, включавшее в себя ультразвуковое исследование (УЗИ) почек и мочевыводящих путей с доплеровским картированием, экскре- торную урографию, цистографию и статическую нефросцинтиграфию для решения вопроса о необходимости хирургического вмешательства. Для исключения функциональной обструкции, по показаниям, выполнялось УЗИ с лазиксной нагрузкой и ретроградная уретеропиелогра-фия.
Для оценки степени гидронефроза в своей работе мы использовали международную классификацию Onen 2007 года [24]:
Гидронефроз 1 ст. – расширение почечной лоханки;
Гидронефроз 2 ст. – расширение почечной лоханки и чашечек;
Гидронефроз 3 ст. – расширение лоханки и чашечек и истончение паренхимы до ½.;
Гидронефроз 4 ст. – расширение лоханки и чашечек с истончением паренхимы более ½.
Критерием оценки функционального состояния почек являлась степень дефицита очищения почки по данным нефросцинтиграфии: I стадия – отсутствие нарушения функции или дефицит очищения не более 25%; II стадия – дефицит очищения 26 – 50 %; III стадия – дефицит очищения 51 – 75 %; IV стадия – более 75%, вплоть до афункциональ-ной кривой. Определение функционального состояния почек является неотъемлемой частью обследования, так как позволяет определить объем оперативного лечения и определить прогноз лечения.
Распределение больных в зависимости от степени снижения функции почек представлено в таблице 1.
У семи больных при обследовании данные ультразвукового ис-
Таблица 1. Распределение больных в зависимости от степени снижения функции почки по данным динамической нефросцинтиграфии
|
Степень гидронефроза и нарушения функции почки |
Нарушения функции нет |
Снижение функции на 0-25% |
Снижение функции на 26-50% |
Снижение функции на 51-75% |
Снижение функции на >75% |
ВСЕГО |
|
1-2 ст. |
21 |
6 |
0 |
0 |
0 |
27 |
|
2-3 ст. |
0 |
22 |
14 |
0 |
0 |
36 |
|
3-4 ст. |
0 |
7 |
15 |
6 |
7 |
35 |
|
Итого: |
21 |
35 |
29 |
6 |
7 |
98 |
следования соответствовали 4 ст. гидронефроза (выраженная дилятация чашечно-лоханочной системы (ЧЛС), с истончением паренхимы), имелось значительное нарушение паренхиматозного кровотока и снижение функции почки более, чем на 75%. Этим пациентам предварительно выполнена пункционная нефростомия с целью оценки резервных возможностей органа. Через один месяц у трех детей младенческого возраста и двух детей 14 и 15 лет отмечено улучшение функции почки (на 25% и более) на фоне сокращения размеров ее коллекторной системы и улучшения почечного кровотока. Этим пациентам выполнена органосохраняющая операция – лапароскопическая пиелопластика. Двум детям дренирование почки не помогло значимо улучшить функцию паренхимы, в связи, с чем проведена нефрэктомия.
Показаниями к операции служили отрицательная динамика размеров ЧЛС почки в течение года, признаки снижения функции почки и нарушения уродинамики по данным статической и динамической нефросцинтиграфии, истончение паренхимы почки, обострения пиелонефрита или эпизоды лейкоциту-рии, боли в животе.
В сомнительных случаях, при гидронефрозе 1-2 степени, для уточнения функционального или органического характера обструкции 15 детям выполнено ультразвуковое исследование почек с лазиксом (фармакопроба). Сохранение расширения лоханки и чашечек более 30% от исходного, спустя 2 часа после введения лазикса считалось признаками обструкции. Больным с подозрением на пересекающий сосуд все исследование проводили строго в положении стоя. Данный подход обеспечил выявление перемежающегося гидронефроза у 5 больных, у которых признаки обструкции возникали только в вертикальном положении тела при смещении почки вниз.
Подавляющее большинство пациентов (96 детей) оперированы лапароскопическим доступом. Двум больным операция проведена ретро-перитонеоскопически, однако, из-за ограниченного рабочего пространства, данный доступ не нашел в нашей клинике широкого распространения. Методом выбора была расчленяющая пластика лоханочно-мочеточникового сегмента по методу Anderson-Hynes (93 пациента), которая выполнялась антева-зально при наличии добавочного сосуда. У двух пациентов с гидронефрозом и мочекаменной болезнью (МКБ) данная операция сочеталась с литоэкстракцией. 5 пациентам выполнен антевазальный пиело-пиелоанастомоз, так как признаков стриктуры в зоне ЛМС выявлено не было, а причиной нарушения оттока мочи являлся добавочный сосуд.
ОПЕРАТИВНАЯ ТЕХНИКА
Причиной обструкции у 76 пациентов (77,6%) была сегментарная дисплазия стенки мочеточника и у 22 детей (22,4%) выявлен абберант-ный (пересекающий) сосуд. Больной укладывался на операционном столе в положение на боку, с поворотом в ¾. При использовании трансперитонеального доступа первый 5-мм троакар для оптики устанавливали в области пупка. После создания пневмоперито-неума под контролем зрения вводили рабочие троакары 3 мм и 5 мм. Детям 1-7 лет операцию выполняли двумя 3-мм инструментами.
Рассекали париетальную брюшину и смещали толстую кишку медиально. Лоханку и мочеточник выделяли в объеме достаточном, для формирования анастомоза без натяжения. Через брюшную стенку накладывали лигатуру, фиксирующую лоханку в стабильном положении. После пересечения лоханки выше зоны сужения производилась спатуляция мочеточника до здоровых тканей на протяжении 2-3 см. Анастомоз формировали непрерывным швом Monocril 6/0. После формирования задней стенки анастомоза устанавливался интубирующий дренаж JJ стент или стент-пиелостома. Следующим этапом проводилось ушивание передней стенки анастомоза. Производилось ушивание дефекта брюшины. Операция заканчивалась установкой страхового дренажа в брюшную полость и уретрального катетера, которые удалялись на вторые – третьи сутки при неосложненном течении послеоперационного периода.
МЕТОДЫ ДРЕНИРОВАНИЯ
Были использованы разные способы дренирования почки. Основным вариантом дренирования была установка внутреннего «JJ» стента 72 пациентам. В зависимости от возраста ребенка применяли стенты различных размеров и длины: 4 Сн/15 см (10-24 мес.), 4 Сн/20 см (2-6 лет), 4,7 Сн/22 см (6-10 лет), 4,7 Сн/25 см (10-13 лет), 6 Сн/25 см (13-17 лет). Важно отметить, что у детей 10-24 месяцев и моложе, не всегда удается провести стент 4 Сн, поэтому целесообразно иметь стенты меньшего диаметра (3 Сн). Однако в нашем арсенале подобных дренажей не было.
Установка дренажа проводилась антеградным способом, после формирования задней губы анастомоза. Через канал одного из инструментов, либо при помощи пункционной иглы через прокол на коже в поясничной области заводили в мочеточник струну-проводник, по которой устанавливали внутренний стент. Однако у 16 (61,5%) из 26 детей в возрасте 10-24 мес. при антеградном способе установки стента встречено непреодолимое препятствие в зоне везико-уретераль-ного соустья. В связи с чем 7 (43,8%) из 16 больных были перемещены в литотомическое положение, выполнена цистоскопия с дилятацией устья мочеточниковыми бужами и ретроградная установка стента. Данная процедура с перемещением больного и повторным созданием стерильной зоны потребовала около 50-80 мин. Одному больному (14,3%) установить ретроградно стент JJ 4Сн не удалось, операция завершена путем наложения пункционной пиелостомы, что увеличило время операции еще на 40 мин. Основные эпизоды удлинения времени операции были связаны не с формированием уретеропиелоа-настомоза (среднее время 40 мин), а с выполнением нестандартных методов отведения мочи.
В дальнейшем мы изменили подход к дренированию почки у детей младшего (10-24 мес.) возраста. В случае возникновения затруднения проведения стента минимального (4 Cн) размера у 9 из 16 детей (56,2%), у которых отмечено препятствие в предпузырном отделе мочеточника, отведение мочи осуществляли стент-пиелостомой. Мы не пытались устанавливать стент ретроградно и бужировать устье мочеточника. Считаем дилятацию устья мочеточника бужами опасной манипуляцией у детей младшего возраста из-за угрозы развития рубцового сужения дистального отдела мочеточника. Данное осложнение мы наблюдали у одного (14,3%) ребенка из 7 больных с бужированием устья, стеноз возник через два месяца после операции. Этому ребенку проведена реимплантация мочеточника по Коэну с хорошим результатом.
Стент-пиелостома представляет собой трубку 6 Сн с отверстиями, проходящую через зону анастомоза в проксимальный отдел мочеточника, трубка имеет полный завиток в лоханке и далее уже без отверстий выходит на кожу. Установка стент-пиелостомы проводилась следующим образом: чрескож-но в поясничной области вводили пункционную иглу через мышцы в лоханку. По игле заводили металлический проводник в мочеточник. Далее по принципу Сельдингера вводили стент-пиелостому по проводнику таким образом, чтобы уре-теральная часть дренажа прошла через зону анастомоза в проксимальный отдел мочеточника, а полный завиток трубки разместился в лоханке. Дренажную трубку фиксировали к коже узловыми швами.
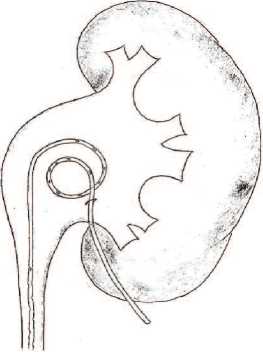
Рис.1. Схема положения стент-пиелостомы в лоханке. Короткий участок стента с отверстиями в мочеточнике, завиток в лоханке, часть стента без отверстий выходит через лоханку на кожу
Схема положения стент-пиело-стомы представлена на рисунке 1.
Больным с гидронефрозом 4 ст. (13 пациентов) с выраженным расширением коллекторной системы почки, c истончением паренхимы и снижением функции, помимо JJ стента, который не мог обеспечить полноценного дренирования почки, устанавливали нефростому. Двум из пяти пациентов, которым выполнен пиело-пиелоанастомоз, проведено дренирование нефростомой без стента. Всего нефростому использовали у 17 (17,3%) больных.
Нефростому устанавливали после формирования задней губы уре-теропиелоанастомоза, проводили длинную пункционную иглу снаружи внутрь под контролем зрения через мышцы поясничной области, паренхиму, среднюю чашечку почки в лоханку. По игле заводили металлический проводник, по которому бужами расширяли пункционный ход до размера нефростомического дренажа. Трубку фиксировали к коже капроновыми лигатурами.
РЕЗУЛЬТАТЫ
Результаты оперативного лечения оценивались по следующим параметрам: длительность операции, сроки госпитализации; осложнения, разрешившиеся при консервативном лечении и потребовавшие повторной операции или манипуляции под наркозом; степень расширения лоханки и чашечек; длительность дренирования верхних мочевых путей.
Отдаленные результаты оценены в сроки от 6 мес. до 6 лет.
Успешным результатом лечения гидронефроза считали исчезновение жалоб, отсутствие конверсии, повторных операций и манипуляций, уменьшение размеров лоханки и чашечек, улучшение или стабилизация функции почек.
Длительность лапароскопической пиелопластики варьировала от 90 до 370 мин, в среднем – 155 ± 15,2 мин. Наиболее продолжительная операция была в случае невозможности антеградного и ретроградного проведения стента у ребенка младенческого возраста, которому в результате была установлена нефростома. Много времени было потрачено на укладку больного для выполнения цистоскопии, неэффективные попытки бужирования мочеточника, ретроградное стентирование и возвращение пациента в первоначальное положение «на боку». Исходно отсутствие в арсенале хирурга стентов оптимального возрастного размера 3Сн для детей младшей возрастной группы и активные попытки провести струну большего диаметра приводили к травматизации и отеку предпузыр-ного сегмента мочеточника. На сегодняшний день нами принята за стандарт тактика, при которой неудачная попытка антеградного проведения стента через уретеровези-кальный сегмент считается поводом для прекращения дальнейших попыток установки стента, включая ретроградное бужирование устья мочеточника, в пользу использования стент-пиелостомы.
Послеоперационный койко-день после лапароскопической пиелопластики составил 4-12 дней, среднее количество койко-дней – 7,5 ± 0,6 дня.
Среди интраоперационных осложнений отмечено кровотечение из брюшной стенки в области установки троакара у 1 (1%) пациента, которое остановлено глубоким прошиванием тканей с захватом сосуда. У 1 (1%) пациента, с подковообразной почкой, трижды оперированного ранее, потребовалась конверсия из-за сложностей идентификации лоханки в грубых рубцах.
В послеоперационном периоде, в зависимости от способа временного отведения мочи, были отмечены осложнения, представленные в таблице 2.
Мочевой затек в результате не герметичности пиелоуретерального анастомоза наблюдали у 4 детей (4,1%) с гидронефрозом 3-4 ст., что потребовало установки пункционной нефростомы. Причиной данного осложнения считаем неадекватное дренирова- ние почки у пациентов с выраженным расширением лоханки и чашечек, был установлен только JJ стент 4 Ch, который был обтурирован сгустком крови. Именно эти осложнения заставили нас более активно использовать нефростому у больных с гидронефрозом 4 ст. Мочевой затек удалось устранить, дренировав почку нефросто-мой, однако у двух из этих больных в отдаленном послеоперационном периоде возникло сужение зоны анастомоза, потребовавшее повторной операции (эндопиелотомия и лапароскопическая пластика ЛМС).
У двух пациентов с JJ стентами отмечена неадекватная функция дренажа, что сопровождалось значительным расширением ЧЛС и обострением пиелонефрита, что потребовало установки пункционной нефростомы. Данные осложнения не сопровождались мочевым затеком и признаками стеноза уретеропиелоанастомоза.
В 2 (2%) случаях отмечено самостоятельное отхождение дренажей. У одного ребенка потеря нефро-стомического дренажа в раннем послеоперационном периоде потребовала повторной пункционной нефростомии. У одного пациента через 2 недели после операции потеря стента-пиелостомы сопровождалась временным расширением ЧЛС, однако повторного дренирования не требовалось. Причиной осложнений считаем недостаточно надежную фиксацию дренажной трубки к коже и ненадлежащий надзор родителей за ребенком дома.
Рефлюкс по стенту с атакой пиелонефрита отмечен у 1 (1%) пациента в возрасте 11 мес., что потребовало повторной установки уретрального катетера и коррекции антибактериальной терапии.
Таблица 2. Частота осложнений в зависимости от метода дренирования почки
|
Способ |
Осложнения |
|||||
|
дренирования почки |
Мочевой затек n (%) |
Нарушение функции дренажа (обструкция) n (%) |
Потеря дренажа n (%) |
Рефлюкс по дренажу n (%) |
Стеноз устья мочеточника |
Всего |
|
JJ стент (72) |
4 (4,1%) |
2 (2%) |
– |
1 (1%) |
1 (1%) |
8 (8,2%) |
|
Стент-пиелостома (9) |
– |
– |
1 (1%) |
– |
– |
1 (1 %) |
|
Нефростома (2) |
– |
– |
1 |
– |
– |
1 (1 %) |
|
JJ cтент+нефростома (15) |
– |
– |
– |
– |
– |
– |
|
Итого: 98 |
4 (4,1%) |
2 (2%) |
2 (1%) |
1 (1%) |
1 (1%) |
10 (10,2%) |
Длительность послеоперационного дренирования зоны анастомоза составила около 5 недель, в среднем 34,6±2,4 дня. Однако при сужении предпузырного отдела мочеточника и гидронефрозе 4 ст. стент удаляли через 6-7 недель.
Удаление нефростомы проводили через 4-6 недель после операции, а при использовании двойного дренирования – после удаления внутреннего стента. Нефростому удаляли после поэтапного ее пережатия, направленного на постепенное включение моторики лоханки, на фоне послеоперационного отека анастомоза. Перекрытие дренажа проводили с обязательным введением антисептика в лоханку для предупреждения обострения пиелонефрита. Мы использовали 1% раствор диоксидина 5 мл, который вводили в лоханку по нефростоме. Нефростому пережимали поэтапно с постепенным увеличением интервала времени: 2-4-8-12-24 часа в сутки. Открывая пережатую нефростому, измеряли объем остаточной мочи в ЧЛС, уменьшение которого свидетельствовало о восстановлении уродинамики и улучшении проходимости по анастомозу. По данным УЗИ оценивали динамику сокращения размеров ЧЛС, в отдельных случаях выполняли антеградную пиелоурете-рографию, которая позволяла рентгенологически подтвердить проходимость через зону анастомоза.
Наибольшее число осложнений возникло у детей с внутренним дренированием JJ стентом 8 из 10.
В отдаленные сроки после лапароскопической пиелопластики 4 (4%) пациентам в связи со стенозом зоны анастомоза потребовалась повторная операция в связи с увеличением размеров ЧЛС и рецидивирующим течением пиелонефрита. 2 (2%) пациентам выполнена эндо-пиелотомия с хорошим результатом. 2 (2%) детям проведена повторная лапароскопическая пиелопластика с положительным эффектом. У 1(1%) пациента после лапароскопической пиелопластики, не- смотря на восстановленный пассаж мочи, потребовалось выполнение нефрэктомии в связи с дальнейшим снижением функции органа. Мы считаем, что выполнение реконструктивно-пластической операции у больного с высоким дефицитом функции почки (79%), было тактической ошибкой.
Хороший эффект лечения без осложнений, получен у 88 (89,7%) больных в результате одной операции. Успешный результат лапароскопической пиелопластики удалось достигнуть у 93 (94,9%) пациентов после первой операции лапароскопической пластики ЛМС, после повторной операции – у 100% больных.
ОБСУЖДЕНИЕ
Лапароскопическая пиелопластика постепенно становится наиболее распространенным методом лечения обструкции пиелоурете-рального сегмента у детей, с эффективностью сопоставимой с результатами открытых операций, а частота осложнений снижается с 36% до 2% [2-4,6,7,9,11,25]. Известны преимущества лапароскопической пиелопластики: хорошая визуализация анатомических структур за счет оптического увеличения, локальное выделение пиелоурете-рального сегмента, возможности прецизионного наложения швов, достаточное рабочее пространство для выполнения пиелоуретероана-стомоза, хороший косметический эффект, короткий послеоперационный период и быстрое восстановление физической активности.
В литературе можно встретить данные авторов о дренажной и без-дренажной пиелопластике. В исследовании K. Smith и соавт. из 52 пациентов, которым установлен внутренний стент, осложнения развились у 6 (12%) пациентов, они включали инфекцию мочевых путей (3 детей), временную обструкцию (3 детей). Из 65 пациентов, которым не проводилось стентирование, осложнения развились у 10 (15%)
детей: длительное подтекание мочи по страховому дренажу (3 детей), уринома (3 пациента), непроходимость анастомоза (3 пациента) и инфекция мочевыводящих путей (1 случай) [23].
Обсуждая вариант бездренаж-ного способа пиелопластики эндовидеохирургическим доступом, считаем, что для его использования существуют довольно узкие показания. Это начальные стадии гидронефроза 2 ст. (без значимого расширения лоханки и чашечек), широкий герметичный анастомоз при пересекающем сосуде у детей старше 6-8 лет, не склонных к выраженному отеку тканей лоханки и мочеточника. По нашему мнению, при бездренажной пиелопластике очень велика опасность обидных мелких осложнений, которые могут иметь очень серьезные последствия. Речь идет о кровяном сгустке в лоханке, минимальной негерметичности анастомоза, отеке анастомоза. Эти состояния при адекватном дренировании почки не приведут к осложнениям, либо их число будет гораздо меньшим. Имея 15-летний опыт открытых бездренажных пиелопластик, мы считаем их широкое использование не целесообразным [20]. Уверены, что преимущества бездренажных методик не столь убедительны для активного применения.
Проводя анализ дренажных методик пластики ЛМС, отметим, что, хотя описанная J. Anderson и W. Hynes пиелопластика была выполнена без использования стента [1], большинство детских урологов выступают за использование внутреннего и/или наружного дренирования, что обеспечивает поддержание правильного положения и «шинирование» зоны анастомоза, профилактику послеоперационной обструкции и стабильное отведение мочи. Наиболее распространенным вариантом дренирования является установка внутреннего JJ стента, также используется мочеточниковый сплинт катетер (стент-пиелостома) и нефростомиче- ские дренажные трубки, но каждый из вариантов отведения мочи имеет свои достоинства и недостатки.
Оценивая эффективность дренирования JJ стентом, ряд авторов указывают на сложности проведения внутреннего стента как при антеградной, так и при ретроградной его установке [21,23,26-28] и относительно высокую (до 12%) частоту осложнений [21], особенно, развитие стриктуры уретеровезикального соустья [29].
Исследование C. Zoeller и соавт. указывает на невозможность проведения double J стента у 9 из 48 пациентов [30]. В сочетании с другими осложнениями, такими как дислокация стента, инфекция мочевых путей, или окклюзия катетера, установка double J стента привела к 35% осложнений по сравнению с 13% в группе с трансренальным стентированием. У 4 (8,3%) пациентов, которым установлен double J стент, потребовалась повторная пиелопластика.
R. Maheshwari при выполнении 74 пиелопластик, с антеградной установкой внутреннего стента сообщил о 13 (17,5%) случаях затруднения проведения дренажа, что потребовало его ретроградной установки. Стоит отметить, что и ретроградный метод установки дренажа не является безопасным, осложнения возникают с частотой до 7% [27].
К недостаткам внутреннего стента авторы относят необходимость его удаления под наркозом [30]. К наиболее частым осложнениям дренирования внутренним стентом относятся инфекции мочевых путей [30-32] и миграция стента [33,34]. Минусом дренирования почки JJ стентом и стент-пиелосто-мой служит отсутствие возможности объективной оценки проходимости через зону анастомоза. Другой особенностью дренирования внутренним стентом и стент-пиелостомой является малый диаметр трубки и дренажных отверстий, что создает риск обтурации дренажа и, как следствие, возникновение мочевого за- тека, стеноза анастомоза и обострению пиелонефрита.
По нашему мнению, дренирование JJ стентом позволяет достигнуть хорошего результата при наличии полного спектра размеров стентов, требующихся ребенку в зависимости от возраста. При отсутствии необходимых дренажей малого диаметра (3 Сн), стоит отказаться от попыток использования JJ стента в пользу стента-пиелостомы или нефростомы.
В исследовании B. VanderBrink и соавт. проведен анализ 59 пиелопластик с установкой KISS катетера (Kidney Internal Splint/Stent), (аналог стент-пиелостомы) у 57 больных. Средний возраст пациентов составил 23 месяца. При данном методе дренирования не выявлено подтекания мочи через зону анастомоза. Непреднамеренное удаление KISS катетера не произошло ни у одного пациента. Послеоперационные эпизоды лихорадки и инфекции мочевых путей развились у двух пациентов без миграции стента [29].
Использование наружных дренажей также имеет свои недостатки. Так при установке наружных дренажей повышается риск инфекции, пациент ощущает дискомфорт в месте выхода дренажа, подтекание мочи по свищу после удаления дренажа. Но наиболее значимым является повреждение почечной паренхимы и развитие кровотечения при установке нефростомы. Такие случаи описаны в исследовании G. Sibley [33]. У 4 пациентов с внешними стентами отмечено значительное кровоизлияние, которое потребовало переливания крови после установки дренажа через почку. Это осложнение также было отмечено G. Ninan, однако переливания крови больному не потребовалось [11]. Другим потенциальным осложнением наружных дренажей является проблема подтекания мочи (> 24 ч) в месте удаления наружного стента или нефростомы. Это произошло у 13 (19%) из 67 пациентов с нефростомиче- ской трубкой Cummings и 3 (20%) из 15 пациентов с другими наружными дренажами [35].
Таким образом, преимущества внутреннего дренирования заключаются в возможности длительного пассажа мочи без контакта дренажа с внешней средой, что при правильной установке стента не приводит к выраженной социальной дезадаптации больного и снижает риск воспалительных осложнений [36]. Однако наряду с достоинствами внутреннего дренирования, есть и недостатки. Так, часто мерой при использовании внутреннего JJ стента требуется установка уретрального катетера в мочевой пузырь с целью профилактики рефлюкса мочи по стенту и необходимость в последующей цистоскопии для удаления стента, которая может привести к таким осложнениям как орхоэпидидимит, простатит, стриктура уретры [37,38].
С другой стороны, наружные методы дренирования верхних мочевых путей обеспечивают более адекватное отведение мочи и позволяют визуально контролировать количество выделяемой мочи, а их удаление не требует эндоскопического вмешательства. Однако применение наружного метода дренирования верхних мочевых путей сопряжено с их дополнительной травматизацией при самой установке дренажа, кроме того наружные дренажи имеют связь с окружающей средой, что повышает вероятность инфицирования мочевых путей, а также требуют тщательного контроля за фиксацией дренажа, что очень проблематично, особенно у детей младшего возраста [39].
Таким образом, выбор оптимального способа послеоперационного дренирования почки после лапароскопической пиелопластики в зависимости от возраста ребенка, степени расширения чашечно-лоханочной системы и снижения функции почки позволяет минимизировать частоту осложнений, уменьшить время оперативного вмешательства и что важно для ребенка, сократить длительность наркоза.
ВЫВОДЫ
-
1. Детям младенческого и младшего возраста (10-24 мес.) при выполнении эндовидеохирургической пиелопластики предпочтительно использование стент-пиелостомы.
-
2. Больным с гидронефрозом 3-4 ст. со значительным расширением ЧЛС и снижением функции почки целесообразно применение двойного дренирования JJ стент + нефростома или пиелостома.
-
3. Бездренажные методики эн-
- довидеохирургической пластики ЛМС не имеют показаний к широкому применению, особенно у детей младшего возраста. Целесообразно их ограниченное использование из-за высокого риска серьезных осложнений.
Резюме:
Введение. В научных работах, посвященных лапароскопической пиелопластике у детей при лечении гидронефроза, указывается на трудности дренирования почки в послеоперационном периоде и связанные с этим осложнения. Цель исследования показать варианты временного отведения мочи после лапароскопической пиелопластики у детей в зависимости от степени гидронефроза и возраста.
Материалы и методы. В детском уроандрологическом отделении НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина в 2010- 2016 гг. оперировано 98 детей (62 мальчика и 49 девочек) с гидронефрозом в возрасте от 9 мес. до 17 лет (средний возраст составил 3,48 года).
96 пациентов оперированы лапароскопическим доступом, двое детей – ретроперитонеоскопически. Выполнялась пластика лоханочно-мочеточникового сегмента по методу Anderson-Hynes, у двух пациентов она сочеталась с литоэкстракцией, 5 пациентам выполнен антевазальный пиело-пиелоанастомоз.
Длительность операции колебалась от 90 до 370 мин (155 ±15,2 мин). В зависимости от способа дренирования пациенты распределились следующим образом: внутренний стент установлен 72 пациентам, стент-пиелостома – 9 (детям 10-24мес), внутренний стент+нефростома – 15, нефростома – 2 больным. 65 детям дренажи были установлены антеградно, 7 пациентам младшего возраст – ретроградно.
Результаты. Среди интраоперационных осложнений отмечено кровотечение из брюшной стенки в области установки троакара у 1 (1%) пациента и конверсия у 1 (1%) ранее трижды оперированного пациента.
В зависимости от способа дренирования почки были отмечены следующие осложнения. При установке JJ стента: мочевой затек отмечен у 4 (4,1%) детей с гидронефрозом 4 ст., нарушение функции дренажа со значительным расширением чашечно-лоханочной системы и острым пиелонефритом – у 2 (2%) пациентов, рефлюкс по стенту – у 1 (1%) пациента, нарушение функции стент-пиелостомы – у 1 (1%) пациента, самостоятельное ее отхождение – 1 (1%) пациент, выпадение нефростомы – у 1 (1%) ребенка.
Длительность послеоперационного дренирования в среднем составила 34,6±2,4 дня. Однако при сужении предпузырного отдела мочеточника и гидронефрозе 4 ст. стент удаляли через 6-7недель.
Хороший эффект лечения без осложнений, получен у 88 (89,7%) больных в результате одной операции. Успешный результат лапароскопической пиелопластики удалось достичь у 93 (94,9%) пациентов после первой операции лапароскопической пластики ЛМС и у 100% больных. После повторной операции.
Заключение. Детям младенческого и младшего возраста (10-24 мес) при выполнении эндовидеохирургической пиелопластики предпочтительно использование стент-пиелостомы. Больным с гидронефрозом 3-4 ст. со значительным расширением ЧЛС и снижением функции почки целесообразно применение двойного дренирования – JJстент + нефростома или пиелостома. Бездренажные методики эндовидеохирургической пластики ЛМС не имеют показаний к широкому применению, особенно у детей младшего возраста. Оптимальный метод послеоперационного дренирования почки после лапароскопической пиелопластики позволяет улучшить результаты оперативного лечения и снизить частоту послеоперационных осложнений.
Список литературы Варианты дренирования верхних мочевых путей после лапароскопической пиелопластики у детей
- Anderson JC, Hynes W Retrocaval ureter: a case diagnosed preoperatively and treated successfully by a plastic operation. Br J Urol 1949;21(3):209-14.
- Bonnard A, Fouquet V, Carricaburu E, Aigrain Y, El-Ghoneimi A. Retroperitoneal laparoscopic versus open pyeloplasty in children. J Urol 2005;173: 1710-3 DOI: 10.1097/01.ju.0000154169.74458.32
- Yee DS, Shanberg AM, Duel BP, Rodriguez E, Rajpoot D. Initial comparison of robotic-assisted laparoscopic versus open pyeloplasty in children.//Urology 2006;67(3):599-602 DOI: 10.1016/j.urology.2005.09.021
- Lee RS, Retik AB, Borer JG, Peters CA. Pediatric robot assisted laparoscopic dismembered pyeloplasty: comparison with a cohort of open surgery.//J Urol 2006;175(2):683-7 DOI: 10.1016/S0022-5347(05)00183-7
- Chacko JK, Koyle AAA, Mingin GC, Furness PD 3rd. The minimally invasive open pyeloplasty. J Pediatr Urol 2006;2(4):368-72. Epub 2006 Jun 22 DOI: 10.1016/j.jpurol.2006.05.001
- Piedrahita YK, Palmer JS. In one-day hospitalization after open pyeloplasty possible and safe? Urology 2006;67(1):181-4 DOI: 10.1016/j.urology.2005.07.044
- Врублевский С.Г., Шмыров О.С., Врублевская Е.Н., Кулаев А.В., Лазишвили М.Н., Корочкин М.В. Эндовидеохирургия гидронефроза у детей. Техника. Дренирование. Осложнения. Сборник тезисов V Юбилейной Всероссийской школы по детской урологии-андрологии. 2016. C. 41-42.
- Piaggio LA, Franc-Guimond J, Noh PH, Wehry M, Figueroa ТЕ, Barthold J, et al. Transperitoneal laparoscopic pyeloplasty for primary ureteropelvic junction obstruction in infants and children: comparison with open surgery. J Urol 2007;178(4 Pt 2):1579-83 DOI: 10.1016/j.juro.2007.03.159
- Braga LHP, Lorenzo AJ, Farhat WA, Bagli DJ, Khoury AE, Pippi Salle JL. Outcome analysis and cost comparison between externalized pyeloureteral and standard stents in 470 consecutive open pyeloplasties. J Urol 2008;180(4 Suppl):1693-8 DOI: 10.1016/j.juro.2008.05.084
- Рудин Ю.Э., Марухненко Д.В., Арустамов Л.Д., Лагутин Г.В. Эндовидеохирургия при лечении обструкции пиелоуретерального сегмента у детей. Экспериментальная и клиническая урология 2014;(4):110-115.
- Ninan GK, Sinha C, Patel R, Marri R. Dismembered pyeloplasty using double J stent in infants and children. Pediatr Surg Int 2009;25(2):191-4 DOI: 10.1007/s00383-008-2313-7
- Коварский С.Л., Захаров А.И., Агеева Н.А., Соттаева З.З., Текотов А.Н., Склярова Т.А., Струянский К.А. Опыт применения неразобщающей пиелопластики при гидронефрозе у детей. Сборник тезисов V Юбилейной Всероссийской школы по детской урологии-андрологии. 2016. C. 58-59.
- Бондаренко С.Г., Абрамов Г.Г. Лапароскопическая пиелопластика у детей грудного возраста. Детская хирургия 2013;(6):7-10.
- Peters CA1, Schlussel RN, Retik AB. Pediatric laparoscopic dismembered pyeloplasty. J Urol 1995;153(6):1962-5.
- Schuessler WW, Grune MT, Tecuanhuey LV, Preminger GM. Laparoscopic dismembered pyeloplasty. J Urol 1993;150(6):1795-9. PMID: 8230507
- Eden C, Gianduzzo T, Chang C, Thiruchelvam N, Jones A. Extraperitoneal laparoscopic pyeloplasty for primary and secondary ureteropelvic junction obstruction. J Urol. 2004;172(6 Pt 1):2308-11.
- Inagaki T, Rha KH, Ong AM, Kavoussi LR, Jarrett TW Laparoscopic pyeloplasty: current status. BJUInt. 2005;95(Suppl 2):102-5 DOI: 10.1111/j.1464-410X.2005.05208.x
- Jarrett TW, Chan DY, Charambura TC, Fugita O, Kavoussi LR. Laparoscopic pyeloplasty: The first 100 cases. J Urol 2002;167(3):1253-6.
- Moon D.A, El-Shazly M.A, Chang C.M, Gianduzzo T.R, Eden C.G. Laparoscopic pyeloplasty: Evolution of a new gold standard. Urology 2006;67(5):932-6. DOI: 10.1016/j.urology.2005.11.024
- Рудин Ю.Э., Осипова А.И., Кузнецова Е.В. Оптимальные методы дренирования мочевыводящих путей после пластики прилоханочного отдела мочеточника у детей с гидронефрозом. Детская хирургия. 2000;(5):16 -19.
- Vijayanand D, Hasan T, Rix D, Soomro N. Laparoscopic transperitoneal disemembered pyeloplasty for ureteropelvic junction obstruction. J Endourol 2006;20(12):1050-3 DOI: 10.1089/end.2006.20.1050
- Chandrasekharam VV. Is retrograde stenting more reliable than antegrade stenting for pyeloplasty in infants and children? Urology 2005;66(6):1301-4 DOI: 10.1016/j.urology.2005.06.132
- Smith KE, Holmes N, Lieb JI, Mandell J, Baskin LS, Kogan BA, Walker RD 3rd. Stented versus nonstented pediatric pyeloplasty: a modern series and review of the literature. J Urol 2002;168(3):1127-30 DOI: 10.1097/01.ju.0000026415.22233.d7
- Onen A. Treatment and outcome of prenatally detected newborn hydronephrosis. J Pediatr Urol 2007;3(6):469-76 DOI: 10.1016/j.jpurol.2007.05.002
- Elmalik K, Chowdhury MM, Capps SNJ. Ureteric stents in pyeloplasty: a help or a hindrance? J Pediatr Urol 2008;4(4):275-9 DOI: 10.1016/j.jpurol.2008.01.205
- Zachary J. Liss, Trevor M. Olsen, Brian A. Roelof, George F. Steinhardt Duration of urinary leakage after open non-stented dismembered pyeloplasty in pediatric patients J Pediatr Urol 2013;9(5):613-6 DOI: 10.1016/j.jpurol.2012.06.002
- Maheshwari R., Ansari M.S. Laparoscopic pyeloplasty in pediatric patients: the SGPGI experience. Indian J Urol 2010;26(1):36-40 DOI: 10.4103/0970-1591.60441
- Салихар Ш.И. Выбор метода временного отведения мочи при реконструктивнопластических операциях на верхних мочевых путях у детей: дис. кан. мед. наук. М. 2010. 155 c.
- VanderBrink BA, Cary C, Cain MP. Kidney Internal Splint/Stent (KISS) Catheter Revisited for Pediatric Pyeloplasty. Urology 2009;74(4):894-6 DOI: 10.1016/j.urology.2009.04.092
- Zoeller C, Lacher M, Ure B, Petersen C, Kuebler JF. Double J or transrenal transanastomotic stent in laparoscopic pyeloplasty in infants and children: a comparative study and our technique. J Laparoendosc Adv Surg Tech A 2014;24(3):205-9 DOI: 10.1089/lap.2013.0338
- Ahmed S, Crankson S. Non-intubeted pyeloplasty for pelviureteric junction obstruction in children. Pediatr Surg Int 1997;12(5-6):389-92. PMID: 9244107.
- Reed MJ, Williams MPL. Open pyeloplasty in children: experience with an improved stenting technique. Urol Int 2003;71(2):201-3. DOI: 71847.
- Sibley GNA, Graham MD, Smith ML. Improving splingtage techniques in pyeloplasty. Br J Urol 1987;60(6):489-91.
- Woo HH, Farnsworth RH. Dysmember pyeloplasty in infants under the age of 12 months. Br J Urol 1996;77(3):449-51.
- Zaidi Z, Mouriquand PDE. The use of a multipurpose stent in children. Br J Urol 1997;80(5):802-5.
- Richter S, Ringel A, Shalev M, Nissenkorn I. The indwelling ureteric stent: a 'friendly' procedure with unfriendly high morbidity. BJU 2000;85(4):408-11. PMID: 10691815
- Мартов А.Г. Рентген-эндоскопические методы диагностики и лечения заболеваний почек и верхних мочевых путей (суправезикальная эндоурология): дис.. д-ра мед. наук. М., 1993. 76 с.
- Мартов А.Г, Зенков С.С., Чепуров А.К., Мазо Е.Б., Покровский С.К. Опасности и осложнения внутреннего дренирования верхних мочевых путей. Урология и нефрология 1995;(1):29-31.
- Combe M, Gelet A, Abdelrahim A. Lopez JG, Dawahra M, Martin X, et al. Ureteropelvic invagination procedure for endopyelotomy (Gelet technique): review of 51 consecutive cases. J Endourol 1996;10(2):153-7 DOI: 10.1089/end.1996.10.153


