Видеолапароскопические операции при гематологических заболеваниях
Автор: Мумладзе Р.Б., Васильев И.T., Багателия З.А., Эминов М.З., Гоголашвили Д.Г., Якомаскин В.Н., Унанян М.К.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 6 (40), 2014 года.
Бесплатный доступ
В статье рассмотрены возможности видеолапароскопической спленэктомии (ВЛСЭ) у больных с различными заболеваниями системы крови. Изучена безопасность метода в условиях нарушенных гемостаза, иммунитета и спленомегалии. Доказана высокая эффективность ВЛСЭ у больных с заболеваниями системы крови и поражением селезенки.
Селезенка, болезни крови, спленомегалия, гемостаз, спленэктомия, видеолапароскопическая спленэктомия
Короткий адрес: https://sciup.org/142211192
IDR: 142211192 | УДК: 616.15;
Текст научной статьи Видеолапароскопические операции при гематологических заболеваниях
Для определения возможностей видеолапароскопиче-ской спленэктомии (ВЛСЭ) в гематологической практике, изучения безопасности метода в условиях нарушенных гемостаза и иммунитета проведено исследование за период с 2008 по 2013 гг. с участием 87 больных в возрасте от 16 до 73 лет с различными заболеваниями системы крови. Заболевания сопровождались спленомегалией у 43 больных. Метод ВЛСЭ был реализован у 87 больных, из них 76 больным операция была завершена лапароскопическим путем. В 12 случаях в связи с анатомическими особенностями селезенки операция была закончена открытым способом удаления селезенки.
Средняя продолжительность ВЛСЭ составила 120,5±11,6 мин. Операционная кровопотеря – в среднем 250 мл. Летальных исходов не было.
В результате проведенного исследования доказана высокая эффективность ВЛСЭ у больных с заболеваниями системы крови с поражением селезенки.
Частым показанием к спленэктомии являются гематологические заболевания, протекающие с поражением селезенки. Лапароскопические спленэктомии начали применять в хирургической практике с 1992 г. [1, 5]. В дальнейшем использованию метода способствовала малая травматичность операции, что особенно важно при нарушении гемостаза, низкая частота осложнений, быстрая послеоперационная реабилитация больных. На сегодняшний день лапароскопическая спленэктомия признана «золотым стандартом» хирургического лечения больных гематологического профиля. Селезенка легко ранима и хорошо кровоснабжается. Так же известно, что отличительной чертой хирургической анатомии селезенки является значительная вариабельность размера органа, строения его связачного аппарата, ангиоархитектоники. Преимущество ВЛСЭ перед традиционной заключается в малой травматичности вмешательства, которое достигается за счет отсутствия больших разрезов брюшной стенки, выполнения всех этапов операции под постоянным зрительным контролем, без выведения селезенки в операционную рану и повреждения смежных органов, низкой частоте осложнений, быстрой послеоперационной реабилитации больных. Хирургическое вмешательство у таких пациентов зачастую сопряжено с высоким риском интра- и послеоперационных осложнений, так как больные с заболеваниями системы крови, как правило, с тяжелыми расстройствами гемостаза и иммунитета. В частности, длительная терапия глюкокортикоидами при аутоиммунных заболеваниях приводит к снижению резистентности к инфекциям, повышенной «хрупкости» тканей, замедлению репаративных процессов [7, 12]. Интраоперационные и послеоперационные осложнения возникают в 13–37%, летальный исход достигает 12% [9, 11].
Показанием к спленэктомии при гематологических заболеваниях являются также абдоминальный болевой синдром, вызванный периспленитом, спленомегалией, компрессией и дисфункцией органов брюшной полости, инфаркты селезенки, блуждающие селезенки.
Показания в гематологии к хирургическому удалению селезенки могут быть плановыми и экстренными. К экстренным относятся разрыв или угрожающий разрыв селезенки (у больных с тромбоцитопенической пурпурой при угрозе кровоизлияния или кровотечения, при гемобластозах в случае разрыва селезенки). Показаниями к плановой спленэктомии являются: аутоиммунная гемолитическая анемия, идиопатическая тромбоцитопеническая пурпура, микросфероцитоз, талласемия, протекающие со спленомегалией и явлениями гиперспленизма, а также неэффективность специфической, в том числе гемотрансфузионной терапии.
Анализ отечественной и зарубежной литературы показывает, что ВЛСЭ является ответственной и сложной операцией. Многочисленные исследования доказали выполнимость и безопасность операции в стандартных условиях – при отсутствии спленомегалии и уровне тромбоцитов выше критического. Однако сама методика ВЛСЭ не унифицирована. Существует несколько модификаций операции, различающихся доступом, последовательностью мобилизации, способом извлечения селезенки и отношением к дренированию. Необходимость совершенствования методики послужило основанием для выполнения данного исследования.
Материалы и методы
Большая часть больных находилась на базе ГКБ им. С.П. Боткина в гематологических отделениях, где проводи- лось комплексное обследование, которое включало в себя стернальную пункцию и иммунофенотипирование с последующей верификацией диагноза и коррекцией сопутствующих заболеваний. В случае неэффективности глюкокортикостероидной или иной заместительной терапии больные переводились в хирургическое отделение для планового оперативного лечения. Наш опыт лапароскопической спленэктомии насчитывает 87 наблюдений за период с 2008 по 2014 гг., проводимых в ГКБ им. С.П. Боткина. Возраст пациентов варьировал от 16 до 72 лет. Из общего числа больных мужчин было 28 (22,4%), женщин 59 (77,6%).
Основным показанием к операции явились заболевания, не поддающиеся консервативному лечению, с частыми или постоянными обострениями. Из 87 больных у 42 пациентов – идиопатическая тромбоцитопеническая пурпура, у 23 – аутоиммунная гемолитическая анемия, у 12 – аутоиммунная цитопения, у 10 больных – лимфома селезенки.
У 8 больных со спленомегалией оперативное вмешательство носило срочный характер, поскольку на фоне имеющегося гематологического заболевания был диагностирован спонтанный разрыв селезенки.
Подготовка больных к лапароскопической спленэктомии у больных гематологического профиля проводилось по стандартной и общепринятой в нашей клинике схеме. Главное внимание обращалось на те исследования, которые позволяют оценить размеры и структуру селезенки, вариант ее кровоснабжения, взаимоотношение хвоста поджелудочной железы и ворот селезенки, наличие добавочных селезенок и увеличенных внутрибрюшных или забрюшинных лимфатических узлов, состояние печени и других органов брюшной полости. Специальные исследования включали УЗИ органов брюшной полости с прицельным осмотром селезенки в импульсном и дуплексных режимах, КТ, радиоизотопное исследование, эндоскопические исследования верхних отделов ЖКТ. Кроме того, больным проводились общие клинические исследования – общий и биохимический анализы крови, определение уровня глюкозы, коагулограмма, электрокардиограмма, рентгенография органов грудной клетки. Компьютерная томография, позволившая детализировать архитектонику сосудов ворот селезенки и диагностировать диффузные и очаговые изменения селезенки, проводилась с ангиоконтрастированием селезеночных сосудов у 49 больных.
При обследовании у пациентов были выявлены сопутствующие заболевания, требующие хирургического лечения, что и было выполнено симультантно. В 9 случаях это была лапароскопическая холецистэктомия по поводу ЖКБ, у 1 больной симультантно проведено оперативное вмешательство по поводу миомы матки.
В среднем размер селезенки составил 16,46±3,34 × 12,55±1,92 см. При этом выраженность спленомегалии не служила противопоказанием для выполнения операции лапароскопическим путем (рис. 1).
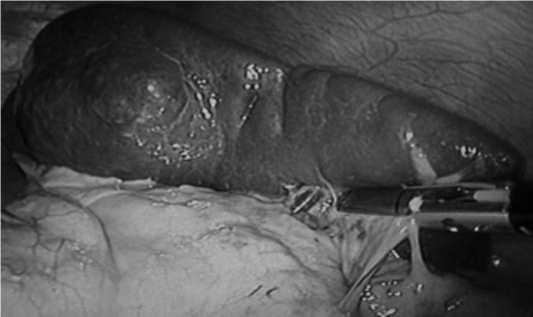
Рис. 1. Мобилизация нижнего полюса селезенки при гиперспленизме
Техника выполнения лапароскопической спленэктомии.
Первоначальное положение больного на на спине. После наложения пневмоперитонеума, введения инструментов и ревизии органов брюшной полости положение пациента менялось – больной поворачивался на бок. Головной конец операционного стола приподнимают на 15–20 градусов.
Пациент укладывается в правое латеральное боковое положение, несколько наклоняется в дорсальном направлении под углом 45 градусов к операционному столу. Операционный стол сгибается для увеличения расстояния между нижними ребрами и подвздошным гребнем. Три 12-мм троакара вводят спереди вдоль левого края реберной дуги.
Для тщательного исследования брюшной полости используется 45-градусный лапароскоп. Далее переходят непосредственно к спленэктомии. Селезеночный изгиб мобилизуют путем рассечения селезеночно-ободочной связки с переходом на желудочно-ободочную и желудочноселезеночную связки. При дисекции могут встречаться множественные ветви желудочно-сальниковых сосудов, идущие к нижнему полюсу селезенки, которые осторожно пересекаются. Остатки пересеченных связок можно использовать для отведения селезенки. Латеральные и задние связки селезенки вначале сохраняют – так будет удобнее держать селезенку, подвешенной к латеральной или задней стенке живота. Далее пересекается селезеночно-почечная связка для формирования «селезеночного тента» и улучшения визуализации и доступа к селезеночным сосудам.
Выбор доступа к сосудистой ножке зависит от индивидуальной анатомии селезеночных сосудов (пучкового или магистрального типа строения слезеночной артерии). Ножку подвергают диссекции и визуализируют спереди и сзади в зависимости от индивидуальной анатомии и строения. Проведение диссекции может помочь «перебрасыванию» селезенки поочередно вперед и назад. Необходимо определить место окончания хвоста поджелудочной железы, чтобы избежать повреждения или рассечения ее паренхимы.
При мобилизации селезенки и пересечении сосудов ворот селезенки нами используется аппарат LigaSure. Крупные сосуды для надежного гемостаза дополнительно перед пересечение клипируются. После этого пересекаются селезеночнодиафрагмальная связка и ткани, прикрепляющие селезенку сзади.
Удаленную селезенку помещают медиальнее операционного поля с помощью атравматического зажима, который не вызывает разрыва хрупкого органа. Осматриваются сосуды ворот, хвоста поджелудочной железы и большая кривизна желудка, чтобы убедится в адекватности гемостаза, выявить признаки повреждений и добавочную ткань селезенки. Проводится санация верхнего квадранта живота и дренирование левого поддиафрагмального пространства силиконовым дренажем на сутки. Через 12-миллиметровый порт вводят пластиковый эндоскопический мешок для извлечения удаленного органв и осторожно помещают в него селезенку. Отверстие мешка закрывают с помощью проти-вотяги за его шнурки. Край мешка с селезенкой выводят через отверстие 12-мм порта, которое при необходимости расширяется. На этом этапе селезенку обычно подвергают морцелляции с помощью окончательного зажима, после чего достают образец. Необходимо выполнить морцелля-цию осторожно, чтобы избежать попадания фрагментов селезенки в брюшную полость как рядом с отверстием мешка, так и при разрыве мешка, так как это может привести к спленозу (рис. 2–5). Рана зашивается послойно. Затем зашиваются троакарные раны.
Результаты и обсуждение
Причиной конверсии у 8 больных (10,3%) являлись большие размеры селезенки, достигающие 20,0 см и более, что явилось причиной интраоперационного кровотечения в объеме 1000 мл вследствие технических сложностей при
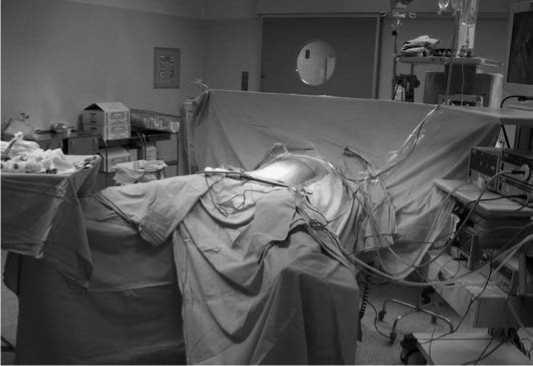
Рис. 2. Положение больного
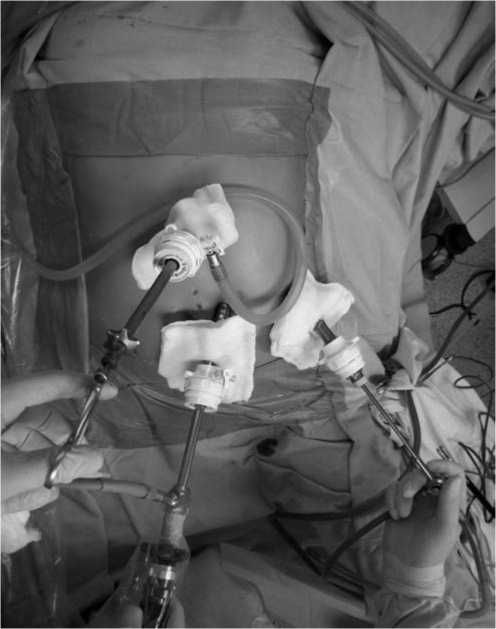
Рис. 3. Положение троакаров
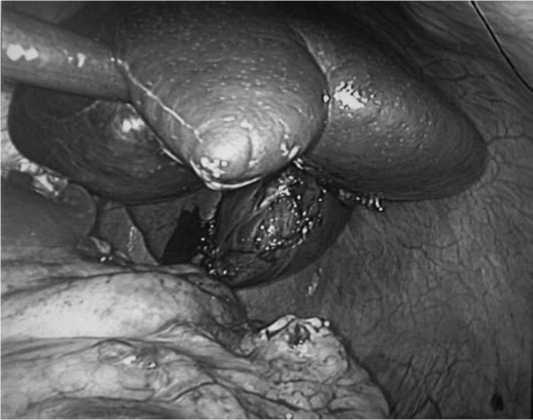
Рис. 4. Удаленная селезенка мобилизации селезенки из-за ее больших размеров. Других интраоперационных осложнений не было. Продолжительность операции составила в среднем 123,5±17,6 минут.
В послеоперационном периоде у 1 (3,7%) больного было отмечено скопление жидкости в левом поддиафрагмальном
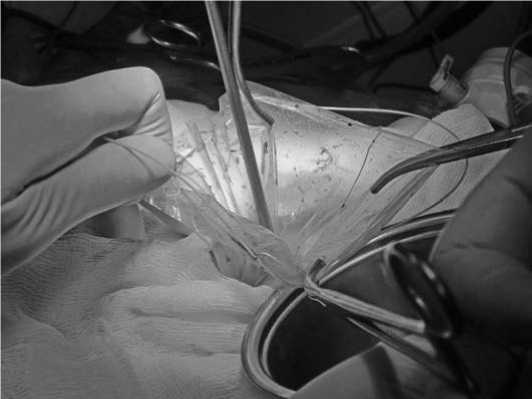
Рис. 5. Марцелляция селезенки пространстве около 150 мл с последующим инфицированием. Выполнено чрекожное дренирование под контролем ультразвука на фоне проводимой антибактериальной терапии. Была отмечена положительная динамика, нормализация температуры.
Продолжительность послеоперационного периода составила 4,5±1,2 койко-дня.
На наш взгляд, использование при пересечении связок и сосудов ножки аппарата LigaSure обеспечивает надежный гемостаз. Однако следует отметить, что такие дополнительные методы гемостаза, как клипирование или перевязка сосудов ворот селезенки эндоскопической петлей при диаметре сосуда более 4–5 мм обеспечивают более надежный и устойчивый гемостаз, что исключает такое грозное осложнение, как послеоперационное кровотечение.
ВЛСЭ позволяет снизить развитие интраоперационных и осложнений раннего послеоперационного периода. Исследования, указанные выше, позволяют прогнозировать возможные интраоперационные осложнения, связанные со спленомегалией. Исходя из нашего опыта, одним из параметров безопасного выполнения ВЛСЭ является длина селезенки до 20 см.
Активное участие в предоперационной подготовке гематолога совместно с хирургами позволяет более полноценно подготовить к операции данную категорию больных и свести к минимуму возможные осложнения во время ВЛСЭ, как и осложнения в послеоперационно периоде.
Выводы
-
1. ВЛСЭ является безопасной и эффективной процедурой, позволяющей успешно применять ее как в плановой, так и в неотложной хирургии.
-
2. Наряду с традиционными преимуществами ВЛСЭ позволяет существенно снизить уровень инфекционных и
- геморрагических послеоперационных осложнений, присущих больным с гематологическими и аутоиммунными заболеваниями.
-
3. Использование аппарата «LigaSure» позволяет осуществить надежный гемостаз сосудов диаметром до 7 мм и снизить риск развития послеоперационных кровотечений.
-
4. ВЛСЭ позволяет сократить сроки пребывания в стационаре и добиться лучших результатов лечения больных с гематологическими заболеваниями.
Список литературы Видеолапароскопические операции при гематологических заболеваниях
- Балалыкин А.С. Эндоскопическая абдоминальная хирургия. М.: ИМАпресс, 1996.
- Емельянов С.И., Матвеев Н.Л., Феденко В.В. Лапароскопическая Хирургия: Прошлое и настоящее//Эндоскопическая хирургия. 1995. №1. С. 5-8.
- Емельянов С.И. Эндоскопическая хирургия -новые задачи и направления научного поиска//Эндоскопическая хирургия. 1997. № 2. С. 54-55.
- Винд Г.Дж. Прикладная лапароскопическая анатомия: брюшная полость и малый таз. М.: Мед. лит., 1999. 384 с.
- Луцевич О.Э., Гордеев С.А., Прохоров Ю.А., Бронштейн А.С. Лапароскопическая хирургия паренхиматозных органов брюшной полости // Тезисы докладов 2 Всероссийского съезда по эндоскопической хирургии // Эндоскопическая хирургия. 1999.
- Силаев М.А., Карагулян С.Р., Шавлохов В.С., Точенов А.В., Гржимоловский А.В., Пантелеев И.В., Веревкина Н.А. Данишян К.И. Удаление селезенки при спленомегалии у гематологических больных//Хирургия. Журнал им.Н.И.Пирогова. 2012. № 8. С. 55-59.
- Пучков К.В., Мартынов М.М., Гаусман Б.Я., Курышкин А.В., Горевой А.А. Открытая или лапароскопическая спленэктомия?//Эндоскопическая хирургия. 1997. Т.3, № 1. С. 22-26.
- Пучков К.В., Гаусман Б.Я., Мартынов М.М. Лапароскопическая спленэктомия: преимущества и технические аспекты//Эндоскопическая хирургия. 1997. Т.3, №1. С. 90.
- Пучков К.В., Иванов В.В., Кувшинов А.С. Новые возможности в лапароскопической хирургии селезенки//8-ой Моск. Междун. конгр. по эндоскопической хирургии. М.: РНЦХ РАМН, 2004. С. 282-284.
- Пучков К.В. Эндовидеохирургические вмешательства на селезенки: избранные лекции по эндовидеохирургии/под редакцией В.Ф.Федорова. Спб.: ООО фирма «КОСТА», 2004. 216 с.
- Backus C.L., Park A.E., Metthews B.D., Heliford B.T. Minilaparoscopic splenectomy//J. Laparoendosc. Adv. Surg.Tech. A. 2000. Vol. 10(5). P. 259-262.
- Delaitre B., Maignein B. Laparoscopic splenectomy//Br. J. Surg. Vol. 79. P. 1334.
- Espert J.J., Targarona E.M., Bombuy E. Evaluation of risk of splenosis during laparoscopic spleneectomy in rat model//World J. Surg. 2001.Vol. 25(7). P. 882-885.
- Carr J.A., Shurafa M., Valenovich V. Surgical indications in idiopatic splenomegaly//Arch. Surg. 2002. Vol. 137(1). P. 64-68.


