Видовая принадлежность и серогрупповая вариабельность стрептококков, выделяемых от свиней в Краснодарском крае
Автор: Толстова Е.А., Агольцов В.А., Черных О.Ю., Семиволос А.М., Падило Л.П., Попова О.М.
Статья в выпуске: 3 т.255, 2023 года.
Бесплатный доступ
Использование комплексной лабораторной диагностики, включающей в себя бактериологический, серологический, биохимический и биологический методы исследований при стрептококкозе свиней позволили определить виды, серогрупповую принадлежность и патогенность стрептококков, циркулирующих у свиней в Краснодарском крае. При исследовании патматериала от свиней (свиноматок; носовые смывы, трупы поросят) были выделены S. pneumonia, S. zooepidemicus, S. faecalis и впервые S. uberis. При определении серогрупповой принадлежности стрептококков в реакции преципитации установили, что в основном среди свиней Краснодарского края циркулируют патогенные варианты серологических групп: B, G, I, R.
Стрептококкоз свиней, виды стрептококков, лабораторная диагностика
Короткий адрес: https://sciup.org/142238923
IDR: 142238923 | УДК: 619.615.33.616.24-002.636.4 | DOI: 10.31588/2413_4201_1883_2_255_329
Species and serogroup variability of streptococci isolated from pigs in the Krasnodar territory
The use of a complex laboratory diagnosis, which includes bacteriological, serological, biochemical and biological research methods for the streptococci of pigs, made it possible to determine the species, serogroup membership and pathogenicity of streptococci circulating in pigs in the Krasnodar Territory. In the study of pigs (sows; nasal lavages, corpses of piglets), S. pneumoniae, S. zooepidemicus, S. faecalis and, for the first time, S. uberis were isolated. When determining the serogroup membership of streptococci in the precipitation reaction, it was found that pathogenic variants circulate mainly in pigs of the Krasnodar Territory: B, G, I, R.
Текст научной статьи Видовая принадлежность и серогрупповая вариабельность стрептококков, выделяемых от свиней в Краснодарском крае
Стрептококкоз свиней представляет собой, как самостоятельное заболевание, так и возникающий на фоне целого ряда инфекционных патологий, который может вызывать тяжелые поражения, в виде менингита, артрита, бронхопневмоний и других патоморфологических изменений [3, 4, 5].
Первой стадией патогенного процесса, является прикрепление и колонизация на слизистой оболочке или на эпителиальных поверхностях хозяина. Второй этап – инвазия в более глубокие ткани и внеклеточная транслокация бактерий в кровяное русло, либо свободно находящихся в циркуляции, либо прикрепленных к поверхности моноцитов. Если S. pneumonia, S. uberis, S. faecalis, S. Zooepidemicus, присутствующие в крови, не вызывают септицемию со смертельным исходом, то стрептококкоз может перейти в третью стадию, включающую проникновение в органы хозяина, в основном путем преодоления гематоэнцефалического барьера, чтобы получить доступ к центральной нервной системе (ЦНС) и вызывать менингит. Четвертая стадия – воспаление, которое имеет связующую роль в патогенезе как системных инфекций, так и инфекций ЦНС. Патоген может индуцировать перепроизводство провоспалительных цитокинов, вызывающих септический шок, или привлечение и активацию различных популяций лейкоцитов, вызывая острое воспаление ЦНС [4, 5, 6].
На всех стадиях патогенного процесса S. pneumonia, S. uberis, S. faecalis , S. zooepidemicus взаимодействует со многими типами иммунокомпетентных клеток хозяина, такими как полиморфноядерные лейкоциты, мононуклеарные макрофаги, лимфоциты, дендритные клетки и микроглия, используя ряд универсальных факторов вирулентности для уклонения от врожденной и адаптивной иммунной защиты хозяина, и для преодоления экологического стресса [7, 8, 9].
Частота встречаемости, тяжесть клинических проявлений стрептококкоза свиней, а также распространенность видов стрептококков, устойчивых к антимикробным агентам, несмотря на проводимую интенсивную антибактериальную терапию, определяют необходимость постоянного мониторинга возбудителей и расширения исследований по повешению эффективности лечения и специфической профилактики стрептококкоза свиней в Краснодарском крае. [7,8,10].
Целью проведения исследований явилась необходимость дифференциации видовой принадлежности и серогрупповой вариабельности стрептококков, выделяемых от свиней и их патогенность.
Материал и методы исследований.
Исследования проводились на базе
Кропоткинской краевой ветеринарной лаборатории. Были применены микроскопические, культуральные и биологические методы исследований. Материалом для лабораторных исследований служили: влагалищные смывы от заболевших свиноматок, смывы из носовых ходов и трупы поросят в возрасте от 1 до 4 месяцев, павших от стрептококкоза. Для определения видов стрептококков использовали СТРЕПТОтест 16, предназначенный для биохимической идентификации стрептококков. Данный набор позволяет проводить до 60-ти определений по 16-ти биохимическим тестам с возможностью визуальной и автоматизированной оценки результатов биохимических реакций по идентификационной таблице. Для установления серогрупповой принадлежности стрептококков использовали стрептококковые групповые преципитирующие сыворотки ФГБУ ВГНКИ. Определение патогенности стрептококков проводили на трех белых беспородных мышах 15-16 г. Для заражения использовали 18-часовые культуры стрептококков. Культуру в объеме 0,5 мл вводили внутрибрюшинно.
Результат исследований.
Возбудители болезни относятся к роду Streptococcus, который включает более 20 серологических групп стрептококков, различающихся антигенными свойствами.
Кроме стрептококков от животных часто выделяли другие грамположительные кокки. Для первичной дифференциации использовали характерные признаки в соответствии с рекомендациями (Таблица 1).
Результаты, полученные при проведении лабораторных диагностических исследований патматериала, поступавшего в Кропоткинскую краевую ветеринарную лабораторию за последние четыре года (с 2019 по 2022гг.), свидетельствуют о высокой частоте обнаружения стрептококков (Таблица 2).
Таблица 1 – Отличительные особенности родов семейства Streptococcaceae
|
Наименование рода |
Характерные признаки |
|
Streptococcus |
Клетки делятся в одной плоскости. Глюкозу ферментируют до образования молочной кислоты без выделения углекислого газа |
|
Leuconostoc |
Клетки делятся в одной плоскости. Глюкозу ферментируют с образованием углекислого газа |
|
Pediococcus |
Клетки делятся в двух плоскостях, образуя тетрады. Глюкозу ферментируют до образования молочной кислоты без выделения углекислого газа. |
|
Aerococcus |
Клетки делятся в двух плоскостях, образуя тетрады. Глюкозу ферментируют до образования молочной кислоты без выделения углекислого газа. |
|
Gemella |
Клетки делятся в одной плоскости. По Граму окрашиваются негативно. |
Таблица 2 – Статистические данные по стрептококкозу свиней в Краснодарском крае за 2019-2022гг
|
Год |
Количество проб патматериала |
Проведено исследований |
Получено положительных результатов |
||
|
Микроскопических |
Бактериологических |
Биологических |
|||
|
2019 |
33 |
33 |
13 |
4 |
14 |
|
2020 |
36 |
36 |
36 |
9 |
12 |
|
2021 |
40 |
40 |
40 |
8 |
15 |
|
2022 |
15 |
15 |
15 |
5 |
3 |
Высевы из патологического материала делали пастеровской пипеткой в мясо-пептонный бульон с 1 % глюкозы и 10 % инактивированной нормальной сывороткой лошади и на мясо-пептонный агар с 1 % глюкозы и 5-10 % дефебринированной крови барана. Посевы инкубировали в термостате при 37 °С в течение 19 часов. На глюкозо- кровяном агаре стрептококки росли в виде мелких, прозрачных и слегка мутноватых колоний, которые были окружены зоной гемолиза.
S. pneumonia - круглые, плоские, полупрозрачные колонии, диаметром 0,50,8 мкм. Иногда встречались мукойдные колонии – они были более крупные, слизистой консистенции. На сывороточноглюкозном бульоне росли с равномерным помутнением среды с образованием осадка (Рисунок 1).
-
S. uberis - на кровяном агаре формировал колонии: крупные, блестящие, вязкие, с неровными краями, прозрачные,
матовые, мелкие, диаметром 0,1-0,2 мм. На сывороточно-глюкозном бульоне росли с равномерным помутнением.
-
S. zooepidemicus – образовывал мелкие колонии, блестящие, вязкие, в виде капли воды, серые, диаметром 0,1-0,3 мм.
-
S. faecalis – колонии округлой формы, с ровными краями, диаметр 1,52 мм, с красноватым оттенком (Рисунок 2). При выделении стрептококков серологической группы Д определяли разновидность энтерококков. Для этого использовали среду с теллуритом калия или энтерококковую дифференциальнодиагностическую среду.
Культура S. faecalis устойчива к теллуриту калия (0,07 %) и хорошо растет на плотной среде в его присутствии, образуя колонии черного цвета. На дифференциально-диагностической среде через 15 ч роста колонии S. faecalis приобретают вишнево-красный цвет.
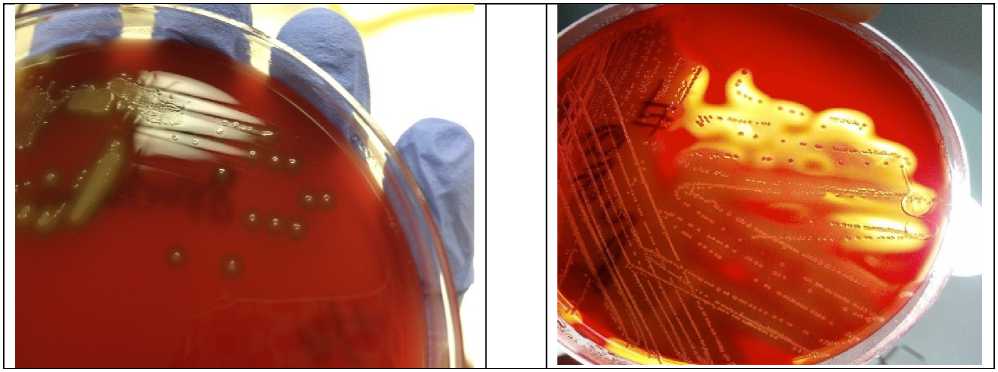
Рисунок 1 – S. pneumonia
Рисунок 2 – S. faecalis
Таблица 3 – Виды стрептококков, выделенные от свиней в Краснодарском крае за 2019- 2022гг
|
Год |
Район |
Исследовано проб |
Исследуемый материал |
Вид и частота выделения стрептококков |
|
2019 |
Усть-Лабинский |
3 |
Смывы из влагалища свиноматок |
S. uberis 3 |
|
г. Краснодар |
8 |
Смывы из влагалища свиноматок, трупы поросят, носовые смывы |
S. pneumonia 4, S. uberis 2, S. faecalis 2 |
|
|
Новопокровский |
3 |
Смывы из влагалища свиноматок, носовые смывы |
S. uberis 2, S. pneumonia 1 |
|
|
2020 |
Выселковский |
6 |
Носовые смывы |
S. pneumonia 6 |
|
г. Краснодар |
6 |
Смывы из влагалища свиноматок |
S. uberis 6 |
|
|
2021 |
г. Краснодар |
15 |
Носовые смывы, трупы поросят |
S. pneumonia 13 S. zooepidemicus2 |
|
2022 |
г. Краснодар |
3 |
Носовые смывы, трупы поросят |
S. uberis 1, S. pneumonia 2 |
Таблица 4 – Идентификационная таблица СТРЕПТОтест 16
|
Показатель |
Ряд1 |
STREPTOtest 16 |
s 9 s s И s |
|||||||||||||||||
|
Ряд 2 |
||||||||||||||||||||
|
Серогруп па |
s щ к |
pi >н Рн |
Н Рн > |
H |
G |
F |
E |
D |
C |
B |
A |
H |
G |
F |
E |
D |
C |
B |
A |
|
|
(Z) ж |
p. < H— |
Pi о |
< |
о < |
Щ Pi |
i |
Pi c |
Щ Pi H |
< H- |
< Pi |
i |
p: 2 |
m C^ |
|||||||
|
A |
+ |
+ |
– |
– |
+ |
+ |
(–) |
– |
– |
+ |
– |
– |
– |
+ |
+ |
– |
– |
– |
– |
S.pyogenes |
|
B |
(+) |
– |
+ |
+ |
+ |
+ |
d |
– |
– |
+ |
– |
– |
– |
(+) |
d |
– |
– |
– |
(+) |
S.agalactiae |
|
C |
– |
– |
– |
– |
+ |
+ |
+ |
– |
– |
+ |
– |
– |
d |
+ |
+ |
– |
– |
– |
+ |
S.dysgalactiae |
|
C |
+ |
– |
– |
– |
+ |
+ |
+ |
– |
– |
+ |
– |
– |
– |
– |
– |
– |
– |
– |
– |
S.equi subsp. equi |
|
C |
+ |
– |
– |
– |
+ |
+ |
+ |
– |
(–) |
+ |
– |
– |
+ |
– |
+ |
– |
– |
– |
(+) |
S.equi subsp. zooepidemicus |
|
C |
+ |
– |
– |
– |
+ |
+ |
(+) |
– |
(–) |
+ |
– |
– |
– |
+ |
d |
– |
– |
– |
+ |
S.equisimilis |
|
G |
+ |
– |
– |
– |
+ |
+ |
(–) |
d |
d |
+ |
– |
– |
– |
(–) |
(+) |
– |
– |
– |
+ |
S.group G |
|
L |
+ |
– |
– |
d |
+ |
+ |
+ |
– |
– |
+ |
– |
– |
– |
+ |
(+) |
– |
– |
– |
+ |
S.group L |
|
E, P, U, V |
+ |
– |
+ |
+ |
+ |
+ |
+ |
d |
+ |
+ |
– |
+ |
(+) |
+ |
d |
– |
– |
– |
(+) |
S.porcinus |
|
R, S, RS, T |
– |
d |
– |
– |
– |
+ |
+ |
(+) |
(+) |
+ |
– |
– |
– |
+ |
+ |
d |
d |
– |
– |
S.suis |
|
F, C, (G, A) |
d |
– |
+ |
– |
+ |
+ |
– |
d |
+ |
+ |
– |
(–) |
– |
+ |
(+) |
d |
– |
(–) |
– |
S.anginosus |
|
F (C, G) |
d |
– |
+ |
– |
+ |
+ |
– |
– |
– |
+ |
– |
– |
– |
(+) |
(–) |
– |
– |
d |
– |
S.constellatus |
|
F, C (G) |
d |
– |
+ |
– |
+ |
+ |
– |
– |
+ |
+ |
– |
– |
– |
+ |
+ |
– |
– |
– |
– |
S.intermedius |
|
– |
– |
+ |
– |
– |
+ |
– |
(+) |
+ |
– |
– |
+ |
+ |
+ |
+ |
(+) |
(+) |
+ |
– |
S.mutan s“group” |
|
|
– |
– |
+ |
– |
d |
+ |
– |
– |
+ |
– |
d |
– |
– |
d |
d |
(+) |
d |
– |
– |
S.salivarius |
|
|
– |
– |
+ |
– |
– |
+ |
– |
– |
d |
– |
+ |
– |
– |
– |
(+) |
– |
– |
– |
– |
S.vestibularis |
|
|
D |
– |
– |
+ |
– |
– |
+ |
– |
d |
+ |
– |
– |
+ |
– |
+ |
+ |
+ |
(+) |
d |
– |
S.bovis I |
|
D |
– |
– |
+ |
– |
– |
+ |
– |
+ |
+ |
– |
– |
– |
– |
(–) |
+ |
+ |
d |
(+) |
– |
S.bovis II/1 |
|
D |
– |
– |
+ |
– |
– |
+ |
d |
(+) |
+ |
– |
– |
– |
– |
+ |
+ |
d |
(–) |
d |
– |
S.bovis II/2 |
|
D |
– |
– |
+ |
– |
– |
+ |
– |
– |
+ |
– |
– |
(–) |
– |
(–) |
d |
(–) |
(–) |
d |
– |
S.equinus |
|
E |
– |
(–) |
+ |
+ |
d |
+ |
+ |
(–) |
+ |
+ |
– |
+ |
+ |
+ |
+ |
(–) |
+ |
– |
+ |
S. uberis |
|
E |
– |
(–) |
+ |
d |
d |
+ |
(–) |
(–) |
+ |
+ |
– |
+ |
+ |
+ |
+ |
(–) |
(–) |
– |
(+) |
S.parauberis |
|
– |
(–) |
– |
+ |
d |
+ |
d |
– |
– |
(–) |
– |
d |
– |
(+) |
(+) |
– |
– |
– |
(–) |
S.acidominimus |
|
|
– |
(–) |
– |
– |
– |
+ |
– |
(+) |
(–) |
d |
– |
– |
– |
+ |
+ |
(+) |
d |
– |
– |
S.pneumoniae |
|
|
– |
– |
– |
– |
d |
+ |
– |
d |
– |
+ |
– |
– |
(–) |
– |
+ |
d |
– |
d |
– |
S.mitis 2 |
|
|
– |
– |
– |
– |
d |
+ |
– |
d |
– |
– |
– |
– |
– |
(–) |
+ |
d |
– |
d |
– |
S.oralis / mitis 1 |
|
|
– |
– |
– |
– |
– |
+ |
– |
d |
+ |
+ |
– |
– |
(–) |
(+) |
+ |
d |
(+) |
d |
– |
S.sanguis esl+ |
|
|
– |
– |
– |
– |
– |
+ |
– |
+ |
– |
+ |
– |
– |
– |
(+) |
+ |
– |
(+) |
– |
– |
S.sanguis esl– |
|
|
– |
– |
– |
– |
+ |
+ |
– |
d |
+ |
+ |
– |
– |
– |
+ |
(+) |
d |
(+) |
d |
– |
S.gordonii |
|
|
– |
d |
(–) |
(+) |
– |
– |
(–) |
d |
(+) |
– |
– |
d |
(–) |
+ |
(+) |
d |
(–) |
– |
d |
Aerococcus viridans |
|
Пояснения:
|
+ = положительная реакция |
d = вариабельная реакция |
– =отрицательная реакция |
|
-+) = большей частью положительная реакция |
( – ) = большей частью отрицательная реакция |
|
|
HEM = β-гемолиз |
PYR = пирролидонилариламидаза (ПИРАтест) |
VPT = ацетон (VPtest) |
Примечание: для зеленящих стрептококков в случае неоднозначной идентификации можно проводить идентификацию до:
S. salivarius group = S. salivarius, S. vestibularis; S. milleri group = S. anginosus, S.
constellatus, S. intermedius; S. sanguis group = S. sanguis, S. gordonii; S. mitis group = S. mitis, S. oralis; (RUOFF, K. L. 1995. Streptococcus, p. 299–307. In: P.R. Murray et al. (ed.), Manual of Clinical Microbiology, 6th ed. ASM, Washington
Streptococcus uberis является экологическим патогеном, ассоциированным с субклиническим и клиническим маститом, как у лактирующих, так и у нелактирующих коров, который может сохраняться в вымени и вызывать хроническую инфекцию в молочной железе [1, 7, 10].
Эталонный штамм S. uberis 0140J является условно-патогенным микроорганизмом, который может адаптироваться к различным экологическим нишам благодаря своей питательной гибкости. Этот вездесущий микроорганизм был выделен из кожи, губ и миндалин коров, в полости рта, рубце, прямой кишке и дыхательных путях, на коже сосков и каналах, а также в инфицированном вымени и фекалиях [2, 3, 10]. S. uberis также может быть выделен из окружающей коровы среды в виде отработанного молока, воды для очистки, подстилки для пастбищ и амбаров. Все это является основным источником инфекции. Коровы выделяют S. uberis со своими фекалиями через слизистые оболочки пищеварительного тракта, что может объяснить широкое распространение и поддержание этого патогена в молоке. Участки рядом с доильным залом богаты органическими веществами (фекалиями, молоком), которые могут попадать на вымя. Когда сосковые каналы открыты, фекальное загрязнение вымени может способствовать проникновению микроорганизмов [3, 10, 12].
Более того, патоген распространяется в слизистых оболочках полости рта и губ при облизывании шерсти и эпидермиса других коров. S. uberis может сохраняться в результате фекальноорального цикла передачи. До сих пор роль микробиоты молочной железы крупного рогатого скота во взаимодействии хозяин– патоген была плохо изучена, и в основном во время инфекционного процесса. У здоровых лактирующих коров исследовали микробный состав и разнообразие из фекалий, молока и лейкоцитов крови [3, 10, 11]. Для определения видовой принадлежности проведены биохимические исследования выделенных культур стрептококков. Продуцирование сероводорода, аммиака и индола определяли с использованием индикаторных бумажек при инкубации стрептококков в МПБ с добавлением 0,2 % глюкозы.
Для определения сахаролитических свойств стрептококков, исследуемые культуры засеяли на специальные питательные среды Гисса. Использовали питательные среды с 12 углеводами и спиртами: раффиноза, ксилоза, сахароза, галактоза, мальтоза, декстроза, глюкоза, маннит, дульцит, лактоза, арабиноза, инулин. Результаты видовой принадлежности стрептококков представлены в таблице 3.
Для идентификации видового состава стрептококков применяли таблицу СТРЕПТОтест 16 (Таблица 4).
Таблица 5 – Результаты постановки реакции преципитации со стрептококками
|
Серологическая группа стрептококков |
Патматериал |
Частоты выделений, % |
|
B |
Смывы из влагалища свиноматок |
17 |
|
C |
- |
- |
|
E |
- |
- |
|
G |
Смывы из влагалища свиноматок; Носовые смывы, трупы поросят |
58 |
|
D |
- |
- |
|
I |
Носовые смывы, трупы поросят |
15 |
|
R |
Носовые смывы, трупы поросят |
10 |
|
S |
- |
- |
Серогрупповую принадлежность стрептококков определяли в реакции преципитации в капиллярах, с преципитирующей сывороткой, по методике ФГБУ ВГНКИ (Таблица 5).
Определение патогенности стрептококков проводили на трех белых беспородных мышах массой 15-16 г. для каждой установленной серогруппы стрептококков. Для заражения использовали 18-часовые культуры стрептококков. Культуру в объеме 0,5 мл вводили внутрибрюшинно. Культуру признают патогенной при гибели не менее двух мышей.
При заражении патогенной культурой стрептококков мыши погибали в течение 1-2 суток (Таблица 6).
Таблица 6 – Результаты постановки биопробы различными серологическими группами стрептококков на белых мышах
|
Серологическая группа |
Гибель мышей, сутки |
Микроскопия мазка печени мышей по Граму |
|
|
1 сутки |
2 сутки |
||
|
B |
- |
+ |
+ |
|
G |
+ |
- |
+ |
|
I |
+ |
- |
+ |
|
R |
- |
+ |
+ |
Из органов павших мышей готовили мазки, окрашивали по Граму, микроскопировали под иммерсионной системой при увеличении х 100.
Заключение. Использование комплексной лабораторной диагностики, включающей в себя бактериологический, серологический, биохимический и биологический методы исследований при стрептококкозе свиней позволили определить виды, серогрупповую принадлежность и патогенность стрептококков, циркулирующих у свиней в Краснодарском крае. Кроме того, впервые в значительном количестве проб патматериала удалось выявить от свиней S. uberis, ранее не являющийся эпизоотически значимым видом стрептококков , который ранее считался причиной маститов у крупного рогатого скота.
Резюме
Использование комплексной лабораторной диагностики, включающей в себя бактериологический, серологический, биохимический и биологический методы исследований при стрептококкозе свиней позволили определить виды, серогрупповую принадлежность и патогенность стрептококков, циркулирующих у свиней в Краснодарском крае. При исследовании патматериала от свиней (свиноматок; носовые смывы, трупы поросят) были выделены S. pneumonia, S. zooepidemicus, S. faecalis и впервые S. uberis . При определении серогрупповой принадлежности стрептококков в реакции преципитации установили, что в основном среди свиней Краснодарского края циркулируют патогенные варианты серологических групп: B, G, I, R.
Список литературы Видовая принадлежность и серогрупповая вариабельность стрептококков, выделяемых от свиней в Краснодарском крае
- Панин, А. Н. Методика и условия постановки реакции коагглютинации для определения серогрупповой принадлежности стрептококков / А.Н. Панин, В. К. Астафьева // Всесоюзная научная конференция: Совершенствование методов государственного контроля ветеринарных препаратов – 1991. – С.168-170.
- Рыжакина, Е. А. Лабораторная диагностика стрептококковых инфекций животных: Методические указания / Е. А. Рыжакина // Вологда – Молочное: Вологодская ГМХА – 2016. – 19 с.
- Терехов, П. Ю. Стрептококкозы свиней / П. Ю. Терехов, А. В. Капустин // Труды Всероссийского НИИ экспериментальной ветеринарии им. Я.Р. Коваленко – 2019. – С. 27-34.
- Толстова, Е. А. Особенности диагностики и терапии стрептококкоза свиней, осложненного РРСС на племенной ферме / Е. А. Толстова, В. А. Агольцов, Л. П. Падило // Научная жизнь – 2022. – Том 17. – Выпуск 1 – С. 157-166.
- Толстова, Е. А. Особенности диагностики и терапии стрептококкоза свиней на племенной ферме / Е. А. Толстова, В. А. Агольцов, О. М. Попова // Проблемы и пути развития ветеринарной и зоотехнической наук Международная научно-практическая конференция обучающихся, аспирантов и молодых ученых, посвященная памяти Колесова А.М. // Саратовский источник – 2022. – С.123-130.
- Толстова, Е. А. Диагностика, терапия и специфическая профилактика стрептококкоза свиней, осложненного пастереллезом и микоплазмом / Е. А. Толстова, М. М. Лигидова, Л. П. Падило, А. М. Семиволос, В. А. Агольцов // Аграрный научный журнал – 2022. – №1 – С.71-75.
- Шевченко, А. А. Рекомендации по лабораторной диагностике стафилококкозов и стрептококкозов животных / А. А. Шевченко, О. Ю. Черных, В. Н. Шевкопляс, Л. В. Шевченко // Краснодар: КубГАУ – 2008. – 31с.
- Эпизоотология с микробиологией: учебник для вузов / А. С. Алиев, Ю. Ю. Данко, И. Д. Ещенко [и др.] – Санкт-Петербург: Лань, 2022. – 432с. – ISBN 978-5-507-44161-7.
- Amaro, R. Development and characterization of a new swine model of invasive pneumococcal pneumonia / R. Amaro, G. Li Bassi, A. Motos, L. Fernandez-Barat // Lab Anim (NY). – 2021 – Nov;50(11) – P. 327-335.
- Fessia, A. S. Potential factors involved in the early pathogenesis of Streptococcus uberis mastitis: a review / A. S. Fessia, L. M. Odierno // Folia Microbiol (Praha). – 2021 – Aug; 66(4) – P. 509-523.
- Costa, M. O. Streptococcus equi subsp. zooepidemicus infection of pigs leads to shedding in faeces and a carrier state / M. O. Costa, J. C. S. Harding, Y. Huang, R. Nosach // Transbound Emerg Dis. – 2022 – Sep;69(5) – P.1503-1509
- Chen, X. Genetic characterization of Streptococcus equi subspecies zooepidemicus associated with high swine mortality in the United States / X. Chen, N. Resende-De-Macedo, P. Sitthicharoenchai, O. Sahin [et al.] // Transbound Emerg Dis. – 2020 – Nov. 67(6) – P. 2797-2808.


