Видовой состав возбудителей настоящей мучнистой росы тыквенных культур
Автор: Слетова Мария Евгеньевна
Журнал: Овощи России @vegetables
Рубрика: Агрохимия, агропочвоведение, защита и карантин растений
Статья в выпуске: 4 (66), 2022 года.
Бесплатный доступ
При возделывании тыквенных культур в большинстве сельскохозяйственных регионов мира одним из наиболее агрессивных заболеваний является настоящая мучнистая роса, поражение растений при которой при оптимальных для возбудителя почвенно-климатических условиях достигает 100%. В открытом и защищённом грунте среди выращиваемых представителей семейства Cucurbitaceae, наибольшее распространение и вредоносность оказывают виды: Podosphaera xanthii (Sphaerotheca fuliginea (Schlecht ex Fr.) Poll) и Erysiphe cichoracearum f. sp. cucurbitacearum (DC ex Merat) (Golovinomyces cichoracearum). В регионах, где присутствуют оба фитопатогена, могут встречаться смешанные инфекции, затрудняющие идентификацию, а, соответственно и дальнейшие мероприятия по защите растений. Возбудители настоящей мучнистой росы тыквенных культур имеют различные требования к температуре и влажности. В течение вегетационного периода может наблюдаться смена видового состава при изменении условий, например, с наступлением нового сезона. По биологическим характеристикам S. fuliginea и E. cichoracearum относятся к облигатным биотрофным патогенам, неспособным к самостоятельному существованию без живой фотосинтезирующей ткани, кроме зимующей (половой) стадии телеоморфы в виде шаровидных кпейстотеций. В этой стадии возбудителей несложно дифференцировать по особенностям морфологии клейстотеций. При анализе растительного материала бахчевых невооружённым взглядом оба вида вызывают схожие симптомы поражения, однако методом микроскопии эти организмы можно различить по комплексу морфологических характеристик. Таксономически значимыми признаками являются: расположение мицелия, образование конидий (единичное или цепочечное), наличие или отсутствие заметных фиброзиновых телец, особенности аппрессория, размер и форма конидий, а также положение и тип их ростковых трубок. Работами российских и зарубежных учёных показана возможность определять виды и физиологические расы патогенов с помощью косвенного метода: реакции на растения - дифференциаторы. На сегодняшний день известно около 30 физиологических рас возбудителя P. xanthii и 2 расы E. cichoracearum. Однако данный метод не всегда коррелирует с методами молекулярного анализа. Определение видового состава возбудителей мучнистой росы, является отравной точкой для разработки дальнейшей стратегии возделывания тыквенных культур и в селекционной работе на устойчивость к данному заболеванию.
Podosphaera xanthii, sphaerotheca fuliginea, erysiphe cichoracearum, golovinomyces cichoracearum, возбудители настоящей мучнистой росы тыквенных культур
Короткий адрес: https://sciup.org/140295695
IDR: 140295695 | УДК: 635.64:632.482.11 | DOI: 10.18619/2072-9146-2022-4-91-97
Species composition and identification of pathogens of real powdery mildew of pumpkin crops
When cultivating pumpkin crops in most agricultural regions of the world, one of the most aggressive diseases is real powdery mildew, the damage of plants in which, under optimal soil and climatic conditions for the pathogen, reaches 100%. In the open and protected ground, among the cultivated representatives of the Cucurbitaceae family, the most widespread and harmful are the species Sphaerotheca fuliginea (Schlecht ex Fr.) Poll and Erysiphe cichoracearum f. sp. cucurbitacearum (DC ex Merat). In regions where both phytopathogens are present, mixed infections may occur, making identification difficult, and, accordingly, further plant protection measures. The pathogens of this powdery mildew of pumpkin crops have different requirements for temperature and humidity. During the growing season, there may be a change in species composition when conditions change, for example, when a new season begins. Symptoms of the disease in the form of a white or yellowish powdery plaque in the form of rounded spots (mainly on the leaves) can manifest themselves at all stages of plant development, the susceptibility of which increases by the beginning of fruiting. According to biological characteristics, S. fuliginea and E. cichoracearum are obligate biotrophic pathogens, unable to exist independently without living photosynthetic tissue, except for the wintering (sexual) stage of teleomorphs in the form of globular kleistothecia. At this stage, it is not difficult to differentiate pathogens by the morphology of kleistothecium. When analyzing the plant material of melons with the naked eye, S. fuliginea and E. cichoracearum cause similar symptoms of damage, but by microscopy these organisms can be distinguished by a complex of morphological characteristics. Taxonomically significant features are: the location of the mycelium, the formation of conidia (single or chain), the presence or absence of noticeable fibrosin bodies, the features of the appressoria, the size and shape of the conidia, as well as the position and type of their sprout tubes. The works of Russian and foreign scientists have shown the possibility of determining the types and physiological races of pathogens using an indirect method: reactions to differentiator plants. To date, about 30 physiological races of the pathogen Podosphaera xanthii (Sphaerotheca fuliginea) and 2 races of E. cichoracearum are known. However, this method does not always correlate with the methods of molecular analysis. Determination of the species composition of powdery mildew pathogens is a starting point for the development of a further strategy for the cultivation of pumpkin crops and in breeding work for resistance to this disease.
Текст научной статьи Видовой состав возбудителей настоящей мучнистой росы тыквенных культур
В озбудители настоящей мучнистой росы тыквенных культур участвуют в конкурентной борьбе за урожай с человеком с самого начала возделывания представителей семейства Cucurbitaceae. Имея потенциально высокую агрессивность и вирулентность, эти патогенные грибы обнаруживают не только механизмы преодоления устойчивости растений, но и поразительную лёгкость к быстрому развитию устойчивых к фунгицидам рас. Их эволюционный потенциал позволяет поражать ценные для возделывания тыквенные культуры на большинстве континентов как в условиях открытого, так и защищённого грунта. Кроме того, растения, ослабленные воздействием паразита, становятся более восприимчивыми к другим грибным, бактериальным и вирусным заболеваниям [1].
Приоритетным, с точки зрения безопасного в пищевом отношении, способом борьбы с заболеванием является создание устойчивых сортов и гибридов востребованных тыквенных культур [2, 3].
Так, например, на сегодняшний момент среди требований, предъявляемых к гибридам огурца, особенно выращиваемых в условиях светокультуры является устойчивость к данному возбудителю. По данным Курепина А.В. и др. снижение урожайности при поражении настоящей мучнистой росой в зимне-весенних оборотах достигает в среднем 35% [4, 5]. Потери же от настоящей мучнистой росы в мире по разным оценкам в зависимости от почвенно-климатических условий, вирулентности и агрессивности расы патогена и восприимчивости выращиваемых культур достигают 20-100% [6].
Необходимость применения научно обоснованных мер защиты возделываемых культур предполагает знание жизненного цикла фитопатогена, особенностей его биологии и распространения, причин угасания и возобновления эпифи-тотии, а также динамики инфекционного процесса, которые базируются на точной и своевременной диагностике возбудителя.
Прошлое столетие ознаменовалось применением новых методов в сельском хозяйстве и науке – методов молекулярной диагностики, способствующих прорыву в разных областях науки и открывающих новые возможности в исследованиях. Однако научный взгляд на полученные результаты, например, в области геносистематики, находится в процессе формирования. На этапе мониторинга, а также при интерпретации результата, применяются классические методы микроскопирования и идентификации по морфологическим признакам, с учётом знания экобиологических нюансов и морфологии потенциального возбудителя [7, 8].
Возбудители настоящей мучнистой росы семейства Cucurbitaceae
Экономически значимыми в России и за рубежом, вызывающими заболевания в открытом и защищённом грунте среди возделываемых представителей семейства Cucurbitaceae , являются виды Sphaerotheca fuliginea ( Schlecht ex Fr. ) Poll и Erysiphe cichoracearum ( DC ex Merat ) [9, 10, 11, 12]. Указанные выше возбудители могут вызывать поражения растений как индивидуально, так и совокупно, затрудняя при этом идентификацию, а, соответственно и дальнейшую тактику мероприятий по защите [13]. В условиях теплиц чаще всего наибольший вред приносит Sphaerotheca fuliginea ( Podosphaera xanthii ).
Согласно современным представлениям возбудители настоящей мучнистой росы относится к царству Fungi отделу
Ascomycota; подотделу Pezizomycotina; классу Leotiomycetes; порядку Erysiphales cемейству Erysiphaceae родам Sphaerotheca и Erisiphe [14]. Таким образом, оба патогена принадлежат к семейству Erysiphaceae, насчитывающем порядка 16 родов и около 650 видов [15].
В засушливых регионах Азии паразитирует ещё один вид возбудителя настоящей мучнистой росы тыквенных – Leveillula taurica f. cucurbitacearum Gol. В Российской Федерации, как правило, этот фитопатоген обнаруживается в южных регионах [16].
К сожалению, в научных публикациях, описывающих номенклатуру возбудителей настоящей мучнистой росы тыквенных культур как в нашей стране, так и за рубежом, встречаются противоречия и до сих пор нет единой позиции мирового научного сообщества. Этот факт, в свою очередь, осложняет интерпретацию и сравнение результатов разных исследований. Так, характерной особенностью в России является не редкое использование наименования грибов по кониди-альной стадии – анаморфе, а в зарубежной практике доминирует по телеоморфе. [17]. В работах одних исследователей возбудитель настоящей мучнистой росы обозначается как Sphaerotheca fuliginea Schleccht. ex Fr. Poll. [18] в других тот же самый фитопатоген носит названия Podosphaera xanthii или Podosphaera fusca [7, 19, 20], а также встречаются упоминания о Sphaerotheca cucurbitae [21, 22].
Другой возбудитель мучнистой росы бахчевых, отличающийся морфологическими и биологическими характеристиками, упоминается в литературе как Erysiphe cichoracearum [23] или описывается как Golovinomyces cichoracearum и Erysiphe orontii[19].
Разногласия в обозначениях возбудителей затрудняют работу по анализу научной информации и её применении в практике. Поэтому предпринятые специалистами в области систематики и другими учёными усилия для единой позиции привели к тому, что на сегодняшний момент предпочтительное наименование в литературе Podosphaera xanthii ( Sphaerotheca fuliginea или Podosphaera fusca ), а также Erysiphe cichoracearum (Golovinomyces cichoracearum или Erysiphe orontii)[24].
Требования к температуре и влажности
Возбудители настоящей мучнистой росы тыквенных культур, обитающие в разных регионах, имеют различные требования к температуре и влажности. Наблюдения американских учёных, проведённые в 1964 году, при развитии эпифитотии на дыне в Калифорнии показали, что конидии выделенного изолята P. xanthii развиваются при влажности свыше 65% и температуре 9…34°С (оптимальная температура составила 21…22°С) [25].
В России исследования, проведённые на культурах арбуза и дыни Соколовым Ю.В., выявили менее теплолюбивых паразитических представителей этого вида. Оптимальными температурными условиями для развития рас S. fuliginea ( P. xanthii ), характерными для почвенно-климатического региона Астрахани, были 15…21°С [26].
Работами других исследователей показано, что для данного вида фитопатогена сочетание повышенной влажности с более прохладными условиями (≥65%, ≤15°С) создавало условия для более низкой споруляции, но способствовало повышению агрессивности наблюдаемых рас. В то же время на фоне жаркой сухой погоды споры были многочисленны, но проявляли слабую патогенность. В среднем, по их данным, инкубационный период в естественных условиях от момента заражения до появления симптомов может длиться от 5 до 11 суток [27].
Для другого возбудителя настоящей мучнистой росы тыквенных культур – E. cichoracearum благоприятной температурой в условиях Калифорнии является 15…30°С (оптимальная – 25°С) и влажность ниже 50% [25]. В астраханском регионе благоприятные для роста и развития местного фитопатогена температурные условия составили 21…27°С и инкубационный период 5 суток [26].
Для диагностики и прогнозирования потенциальной эпи-фитотии важно учитывать то, что в начале заражения может преобладать более холодостойкие представители, но с повышением температуры воздуха в патокомплексе может нарастать новая популяция. В связи с этим, на одной территории может наблюдаться изменения преобладающей расы или вида фитопатогенов в открытом и защищённом грунте [13, 17].
В то же время наблюдения в разных регионах мира показывают, что на отдельных культурах может встречаться только один вид возбудителя [28].
В регионах, где присутствуют оба фитопатогена, могут встречаться смешанные инфекции, а также может наблюдаться смена видового состава при изменении условий, например, при наступлении нового сезона [29].
Особенности биологии
По биологическим характеристикам P. xanthii и E. cichoracearum относятся к облигатным биотрофным патогенам, неспособным к самостоятельному существованию без живой фотосинтезирующей ткани, кроме стадии телеомор-фы виде шаровидных клейстотеций [30]. Благодаря данным свойствам, эти грибы не могут культивироваться на искусственных средах и требуют поддержания в «зелёном конвейере» для роста и спорообразования [31, 32].
По способу взаимодействия с растениями эти грибы проявляют свойства эктопаразитов, которые растут на поверхности живой ткани, получая питательные вещества из клеток эпидермиса хозяина через специализированные структуры, называемые гаусториями. К растению – донору питательных веществ фитопатоген крепится с помощью специализированных выростов гиф – апрессориев.
При мониторинге посевов патогена выдаёт характерный мучнистый белый или желтоватый налёт на поверхности растения. Прежде всего, он покрывает листья как с верхней, так и с нижней стороны, но может встречаться спороношение на стеблях и плодах. Развитие болезни часто начинается с нижнего яруса листьев. Симптомы в виде округлых пятен могут проявляться на всех стадиях развития растения, однако восприимчивость повышается к началу плодоношения [33].
В жизненном цикле представителей аскомицетов присутствуют половая стадия – телеоморфа и конидиальная – ана-морфа. В стадии телеоморфы (зимующая стадия) оба вида возбудителя настоящей мучнистой росы хорошо идентифицировать по морфологии клейстотеций (плодовое тело с асками). Однако клейстотеции начинают формироваться к концу вегетации тыквенных. Сигналом к их возникновению служит наступление похолодания. Стимулирует этот процесс разница между ночной и дневной температурой свыше 10°С. Клейстотеции P. xanthii и E. cichoracearum достаточно хорошо различимы при микроскопировании, однако бывают случаи, когда их сложно обнаружить на растительных остатках, что затрудняет своевременную идентификацию [34]. Для ранней диагностики этот способ не подходит.

Рис. 1. Мучнистая роса на огурце в условиях теплицы Московской области
Fig. 1. Powdery mildew of cucumber in a greenhouse of the Moscow region

Рис. 2. Симптомы мучнистой росы на кабачках в условиях Московской области
Fig. 2. Symptoms of powdery mildew on courgette in the conditions of the Moscow region
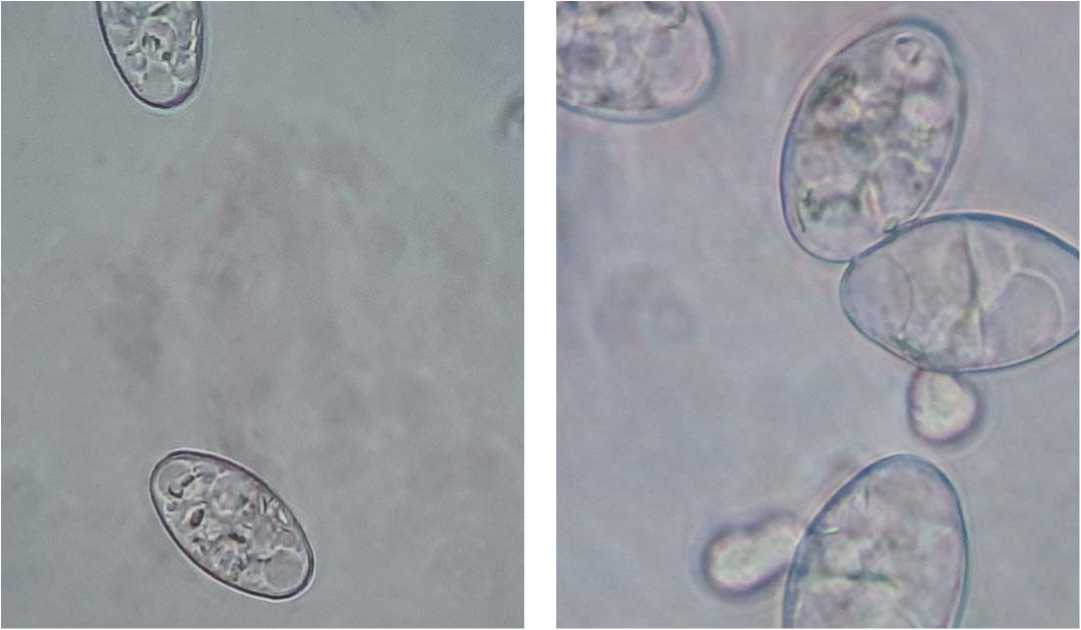
Рис. 3. Возбудитель мучнистой росы огурца Podosphaera xanthii с фиброзиновыми тельцами Fig. 3. The causative agent of powdery mildew of cucumber Podosphaera xanthii with fibrosin bodies
Рис. 4. Прорастание ростковой трубки Podosphaera xanthii в лабораторных условиях Fig. 4. Germination of the germ tube Podosphaera xanthii in laboratory conditions
В период роста и плодоношения тыквенных культур паразитические грибы находятся в конидиальной стадии (анамор-фы). В этой стадии благодаря конидиям, прикреплённым к конидиеносцам, поражённое растение имеет узнаваемый специфический талькообразный налет. В течение благоприятного для развития периода заражение осуществляется конидиями, которые очень мобильны. Они легко открепляются от конидиеносцов и способны преодолевать большие расстояния с потоками воздуха. При попадании на восприимчивое растение начинается рост ростковой трубки, которая преобразуется в ростковую гифу.
По способу прорастания ростковой трубки в лабораторных условиях и другим признакам проводят первичную идентификацию. Для этого свежесобранные споры помещают на предметное стекло в капле стерильной воды и помещают в оптимальные условия для данного вида.
В целом же, при анализе невооружённым глазом растительного материала, Podosphaera xanthii и Erysiphe cichoracearum вызывают почти идентичные симптомы поражения на тыквенных культурах, однако методом микроскопии эти организмы можно различить по комплексу морфологических характеристик [35].
Дифференциация по морфологическим признакам
Характеризуя видовую принадлежность представителей семейства Erysiphaceae, оперируют особенностями половой стадии - телеоморфы. В этой стадии формируется плодовое тело – клейстотеций, линейные размеры которого, а также особенности мицелиальных придатков и количество сумок со спорами (асков) являются таксономически важными характеристиками. Однако клейстотеции в почвенно-климатических условиях могут формироваться в конце вегетации при наступлении похолодания. Поэтому в течение вегетационного периода материал для исследования – конидиеносцы с конидиями. Тем не менее, конидиальная стадия представляет достаточное разнообразие морфологических признаков. Виды могут быть точно идентифицированы, если используется комбинация из нескольких морфологических признаков. Таксономически значимыми признаками являются: расположение мицелия, образование конидий (единичное или цепочечное), наличие или отсутствие заметных фиброзиновых телец, особенности аппрессория, размер и форма конидий, а также положение и тип их ростковых трубок [36].
Оба возбудителя настоящей мучнистой росы имеют тонкостенный мицелий с внутренней дифференциацией перегородками. Сами конидии практически не имеют окраски, достаточно прямые и гибкие. Для диагностики важно то, что зрелые конидии Podosphaera xanthii имеют различимые в световом микроскопе фиброзиновые тела, которые отсутствуют у вида у Erysiphe cichoracearum [37, 38]. Этот признак всегда используют при обнаружении симптомов заболевания в новом географическом регионе. Например, в Бразилии обнаружение мучнистой росы на Lagerstroemiaindica в 2004 году при отсутствии фиброзиновых телец позволило отнести исследуемый вид к Erysiphe australiana [39].
Упомянутые структуры обладают стержнеобразными формами, линейные размеры которых, варьируют от 2 до 8 мкм в диаметре. Фиброзиновые тельца возможно наблюдать, используя световую микроскопию при добавлении к свежесобранным конидиям 3%-ный водный раствор КОН. Назначение этих образований остаётся неясным, однако это не препятствует использовать их в качестве таксономически значимой характеристики [40, 41].
Таксономическая ценность строения и формы конидий остаётся предметом дискуссии, однако может быть использована в качестве дополнительной характеристики. У вида P.
Таблица 1. Морфологические особенности возбудителей настоящей мучнистой росы огурца [*43], [**26] Table 1. Morphological features of pathogens of powdery mildew of cucumbers
В таблице 1 предоставлены результаты исследований, проведённых учёными в северной части Украины и на юге России.
Будучи биотрофами, возбудители настоящей мучнистой росы находятся в тесном взаимодействии с растением – хозяином и сильно подвержены влиянию почвенно-климатических факторов. Поэтому в зависимости от региона обитания их линейные размеры могут варьировать. В Астраханском регионе, где потери урожая от заболевания на культуре арбуза могут достигать 15-26% длина конидий E. cichoracearum составляет 31,88±0,14 мкм и ширина – 16,98±0,08 мкм, при этом индекс составил 1,91±0,01. В этих же условиях размеры конидий P. xanthii : длина – 32,09±0,12, ширина – 19,37±0,08 мкм и индекс – 1,68±0,01 [26].
Использование растений – дифференциаторов для определения видов и рас возбудителей
Работами российских и зарубежных учёных показана возможность определять виды и физиологические расы патогенов с помощью косвенного метода: реакции на растения – дифференциаторы. На сегодняшний день известно около 30 физиологических рас возбудителя P. xanthii и 2 расы E. cichoracearum [44, 45].
Сообщение о первой расе настоящей мучнистой росы на дыне относится к 1925 году в США. Уже в 1938 году устойчивость первого коммерческого сорта дыни PMR 45 была успешно преодолена появлением второй расы патогена. В дальнейшем в Индии, Израиле, Чехии были обнаружены новые расы 3 и 4 [46]. Бардин и его коллеги в 1997 году предложили дифференциальный набор из сортов дынь, включающий сорта с известной реакцией на идентифицированные расы мучнистой росы [47]. Однако новые расы по-прежнему обнаруживаются, расширяя набор дифференциаторов. Благодаря сдвигам в популяциях, которые возникают как вследствие смены сезонов, климата, перемещения по географическим зонам или при появлении нового растения – хозяина этот процесс будет продолжатся.
Однако следует отметить, что поскольку агрессивность и вирулентность возбудителя мучнистой росы находится в тесной взаимосвязи с факторами окружающей среды в том числе: с температурой, влажностью, интенсивностью и продолжительностью освещения, питанием растения, наличи-ем/отсутствием дополнительного стрессора и фазой его раз- вития; то этиже факторы будут определять надёжность и точность идентификации расы патогена. Также важно отметить, что результаты биологических тестов могут не коррелировать с методами молекулярной диагностики [48].
В селекционной работе с тыквенными культурами используют некоторые дифференциаторы, представленные в таблице (2) [49]:
Таблица 2. Виды и сорта – дифференциаторы для определения расы возбудителя мучнистой росы тыквенных культур Table 2. Differentiators for determining the race of the pumpkin powdery mildew pathogen
№
Раса настоящей мучнистой росы
Растение - дифференциатор
|
1 |
А |
C. sativus cv. Marketer |
|
2 |
В1 |
C. melo Védrantais |
|
3 |
В2 |
C. melo PMR 45 |
|
4 |
С |
C. pepo cv. Diamant F1 |
|
5 |
Сm |
C. maxima cv. Goliáš |
|
6 |
D |
C. lanatus cv. Sugar Baby |
Иногда применяют косвенный метод определения вида возбудителя мучнистой росытыквенных при заражении арбуза. Считается, что эта культура поражается только видом E. cichoracearum . Однако работой Соколова Ю.В. показано, что агрессивные изоляты P. xanthii могут заражать арбуз. Также исследования российского ученого показали возможность заражения местными биотипами E. cichoracearum растений астры Aster dumosus L., мака Papaver somniferum L.; P. xanthii –фасоли Faseolus vulgaris L. и папайи Carica papaya L., что позволяет рекомендовать их в качестве дифференциаторов [26].
Применение молекулярных методов
Начиная с 90-х годов прошлого столетия, для идентификации патогенов сельскохозяйственных культур интенсивно внедряют методы молекулярного анализа. Анализ нуклеотидных последовательностей генов или участков ДНК/РНК, позволяет проследить филогенетические связи, выявитьу растения – хозяина экспрессию конкретных генов, отвечающих за синтез веществ защитной функции и другое. Благодаря тому, чтоданные методы достаточно специфичны и чувствительны, диагностиказаболеваний на их основес «работающими» протоколами позволяет достаточно точно проводить идентификацию, изучать генетическую изменчивость рас, находить новые виды, совершенствовать номенклатуру близкородственных патогенов[50]. Несмотря на применение новых под- ходов к решению научных задач, классические методы, не теряют своей актуальности, поскольку только в комплексе позволяют получать достоверные результаты, устраняя недостатки каждого метода, используемого отдельно.
Работой японских учёных в 1998 году показана возможность определять видовую принадлежность возбудителей настоящей росы молекулярными методами как на конидиаль-ной стадии, так и в стадии телеоморфы. Разработанный и улучшенный ими протокол, включающий экстракцию ДНК с помощью метода Chelex, две амплификации с набором праймеров и очистку ДНК электрофорезом, позволил анализировать последовательности ядерной рДНК патогенов мучнистой росы, используя не большое количество исследуемого материала. [51].
Периодические эпифитотии мучнистой росы на тыквенных культурах во всём мире стимулируют разработку новых стратегий получения качественной и безопасной в пищевом отношении продукции. Преодоление барьеров устойчивости ранее не поражающихся растений, усиление агрессивности и вирулентности рас патогена, появление устойчивых к фунгицидам популяций – ставят вопрос о детальном изучении эколого-биологических, морфологических и др. особенностей возбудителей, их видовой и расовой идентификации в каждом географическом регионе выращивания.
Определение видового и расового состава патокомплекса, его динамика в ареале возделывания овощной культуры необходимы как для адекватного и своевременного применения биологических и химических средств защиты, так и для решения задач селекции на устойчивость к преобладающим агрессивным и вирулентным представителям. При создании местных, устойчивых к настоящей мучнистой росе сортов и гибридов тыквенных культур необходимо проводить иммунологическую оценку на искусственном и естественном инфекционных фонах на всех этапах, начиная с исходного материала, обладающего комплексом хозяйственно-ценных признаков.
Этот аспект сохраняет актуальность при продвижении коммерческих селекционных достижений, устойчивых к возбудителям настоящей мучнистой росы, поскольку растения, выращенные в одних почвенно-климатических условиях, могут быть не устойчивы к патогенам в другой зоне, где преобладают другие виды или расы.
В заключение хочется отметить, что стандартизация номенклатуры и подходов к изучению возбудителей настоящей мучнистой росы на мировом уровне благоприятно скажется на развитии и обмене научного и практического опыта и, как следствие, правильном планировании и реализации мероприятий по предотвращению эпифитотий и получению урожая высокого качества.
Об авторе:
Maria E. Sletova – Cand. Sci. (Agriculture),
Researcher at the Laboratory of Immunity and Plant Protection, ,
Список литературы Видовой состав возбудителей настоящей мучнистой росы тыквенных культур
- McCreight, J. D. Melon-powdery mildew interactions reveal variation in melon cultigens and Podosphaera xanthii races 1 and 2. Journal of the American Society for Horticultural Science. 2006;(131):59-65.
- Коротцева И.Б., Кушнерёва В.П. Особенности выращивания сортов огурца селекции ВНИИССОК в открытом грунте Нечерноземной зоны РФ. Овощи России. 2009;(2):43-45. https://doi.org/10.18619/2072-9146-2009-2-43-45
- Kuzuya M., Hosoya K., Yashiro K., Tomita K., Ezura H. Powdery mildew (Sphaerotheca fuliginea) resistance in melon is selectable at the haploid level. Journal of Experimental Botany, 2003;54(384):1069-1074. https://doi.org/10.1093/jxb/erg100
- Курепин А.В., Першин А.Ф., Шевкунов В.Н. «Световая цена» урожая огурца в зимне-весенних оборотах теплиц. Овощи России. 2021;(2):34- 38. https://doi.org/10.18619/2072-9146-2021-2-34-38
- Король В.Г. Гибриды огурца, рекомендуемые для выращивания в защищенном грунте в условиях искусственного освещения. Овощи России. 2021;(5):32-38. https://doi.org/10.18619/2072-9146-2021-5-32-38
- El-Naggar M.A., El-Deeb M.H., Seham S. Ragab. Applied approach for controlling powdery mildew disease of cucumber under plastic houses. Pak. J. Agril. Eng. Vet. Sci. 2012;(28):54-64.
- Meeboon J., Takamatsu S. Notes on powdery mildews (Erysiphales) in Japan: III. Golovinomyces and Podosphaera. The Mycological Society of Japan. 2014. https://doi.org/10.1016/j.myc.2014.07.002
- Takamatsu S., Heluta V., Havrylenko M., Divarangkoon R. Four powdery mildew species with catenate conidia infect Galium: molecular and morphological evidence. Mycological Research. 2009;113(1):117-129. https://doi.org/10.1016/j.myc.2014.07.002
- Гладышко С.Н., Кушнерева В.П., Корганова Н.Н. Исходный материал для селекции огурца с групповой устойчивостью к болезням. Селекция и семеноводство овощных культур. 2002;(37):60-64.
- Кушнерёва В.П. Создание исходных партенокарпических форм огурца, устойчивых к мучнистой росе: дис. канд. с.-х. наук. М., 1982.
- Портянкин А.Е., Шевкунов В.Н. Особенности развития мучнистой росы огурца в защищенном грунте. Состояние и проблемы научного обеспечения овощеводства защищенного грунта (материалы Международной научной конференции). М., 2003. С.75-76.
- Чистякова Л.А., Бирюкова Н.К. Оценка селекционных линий огурца на устойчивость к пероноспорозу и мучнистой росе. Гавриш. 2012;(1):38-41.
- Николаев А.Н. Мучнистая роса тыквенных культур в Молдове. Аграрная наука. 2019;(3):96-101. https://doi.org/10.32634/0869-8155-2019-326-3-96-101
- https://www.mycobank.org/page/Simple names search
- Braun U., Cook R.T.A., Inman A.J., Shin H.D. The Taxonomy of the Powdery Mildew Fungi. in: The Powdery mildews: A Comprehensive Treatise. 2002;(1):13-55.
- Соколов Ю.В. Новый вид для Астраханской области возбудителя мучнистой росы, паразитирующего на тыквенных культурах. Сборник статей молодых ученых и аспирантов НИИОХ. М.,1977. Вып.8. С.31.
- Lebeda, A., Kristkova, E., Sedlakova, B., McCreight, J. D., and Coffey, M. D. 2008. New concept for determination and denomination of pathotypes and races of cucurbit powdery mildew. 125-134 In: Cucurbitaceae 2008. Proceedings of the IXth EUCARPIA meeting on genetics and breeding of cucurbitaceae, Avignon, France, 21-24 May 2008. Institut National de la Recherche Agronomique (INRA).
- Paul Michel Molot, Hervé Lecoq. Les oïdiums des Cucurbitacées. I. - Données bibliographiques.Travaux préliminaires. Agronomie, EDP Sciences. 1986;6(4):355-362. hal-00884885
- del Pino D., Olalla L., Perez-Garcia A., Rivera M. E., Garcia S., Moreno R., de Vicente A., Tores J.A. Occurrence of races and pathotypes of cucurbit powdery mildew in southeastern Spain. Phytoparasitica. 2002;(30):459-466.
- López-Ruiz F. J., Pérez-García A., Fernández-Ortuño D., Romero D., García E., de Vicente A., Brown J.K., Torés J.A. Sensitivities to DMI fungicides in populations of Podosphaera fusca in southcentral Spain. Pest Management Science. 2010;(66):801-808.
- Morishita M., Sugiyama K., Saito T., Sakata Y. Powdery mildew resistance in cucumber. Jarq - Jpn. Agric. Res. Q. 2003;(37):7-14.
- Haramoto M., Hamamura H., Sano S., Felsenstein F.G., Otani H. Sensitivity monitoring of powdery mildew pathogens to cyflufenamid and the evaluation of resistance risk. J. Pestic. Sci. 2006;(31(:397-404.
- Bertrand F., Pitrat A. Screening of a muskmelon germplasm for susceptibility to 5 pathotypes of powdery mildew. 1989. 140-142 р. In: Proceedings of Cucurbitaceae: Evaluation and Enhancement of Cucurbit Germplasm ARS/USDA.
- Cohen R., Burger Y., Katzir N. Phytopathology/Mycology R. Phytoparasitica 2004;32(2):174-183.
- Yarwood C. E., Gardner M. W. Unreported powdery mildews. Plant Dis. Reptr. 1964;(48):310.
- Соколов Ю.В. Разработка и усовершенствование методики селекции арбуза и дыни на устойчивость к мучнистой росе. Астрахань, 2007.
- Bashi E., Aust H.J. Quality of spores produced in cucumber powdery mildew compensated for their quantity. Journal of Plant Diseases and Protection. 1980;(87):594-599.
- Endo T., El Guilli M., Farih A., Tantaoui A. Identification of powdery mildew fungus on Moroccan cucurbitaceous plants Al Awamia. 2012. 125-126 р.
- Lebeda A. The genera and species spectrum of cucumber powdery mildew in Czechoslovakia. Phytopath. Z. 1983;(108):71-79.
- McGrath, M. T. Powdery mildew of cucurbits. Cooperative Extension, Cornell University. Online publication. PP 732.30, 1997.
- Alvarez B.y., Torés J.A. In vitro growth of Sphaerotheca fuliginea (Schlecht. ex Fr.). Effect of different carbon sources on its development. Bol. San. Veg. Plagas. 1997;23(2):283-288.
- Bertrand F., Pitrat A. Screening of a muskmelon germplasm for susceptibility to 5 pathotypes of powdery mildew. 1989. 140-142 р.In: Proceedings of Cucurbitaceae: Evaluation and Enhancement of Cucurbit Germplasm ARS/USDA.
- Lebeda A., Sedlakova B. Screening for Resistance to Cucurbit Powdery Mildew (Golovinomyces cichoracearum, Podosphaera xanthii). Pages 295- 307 in: Mass Screening Techniques for Selection Crops Resistant to Disease, 2010. vol. 1. M. Miranda and M. M. Spencer, eds. International Atomic Energy Agency (FAO), Vienna.
- McCreight J.D. Notes on the change of the causal species of cucurbit powdery mildew in the U.S. Cucurbit Genet. Coop. Rpt. 2004;(27):8-23.
- Cook R.T.A., Inman A.J., Billings C. Identification and classification of powdery mildew anamorphs using light and scanning electron microscopy and host range data. Mycol. Res. 1997;(101):975-1002.
- Hans J. Boesewinkel The morphology of the imperfect states of powdery mildews (Erysiphaceae). The botanical review. 1980;(46):167-224.
- Пидопличко Н.М. Грибы паразиты культурных растений. Киев. Т. 1. 1977. 296 с.
- Сокирко В.П., Горьковенко В.С., Зазимко М.И. Фитопатогенные грибы (морфология и систематика). Краснодар: КубГАУ, 2014. 178 с.
- Liberato J.R., Barreto R.W. New Disease Reports Anamorphic Erysiphe australiana causing powdery mildew on Lagerstroemia indica in Brazil Departamento de Fitopatologia, Universidade Federal de Viçosa, CEP 36570-000, Viçosa, MG, Brazil *rbarreto@ufv.br Accepted: 28 Jun 2004.
- Braun U., Cook R.T.A., Inman A.J., Shin H.D. The Taxonomy of the Powdery Mildew Fungi. in: The Powdery mildews: A Comprehensive Treatise, 2002;(1):13-55.
- Belanger R.R., Bushnell W.R., Dik A.J., Carver T.L.W., eds. American Phytopathological Society Press, Saint Paul, MN.
- Cook R.T.A., Braun U. Conidial germination patterns in powdery mildews. Mycological Research. 2009;113(5):616-636. https://doi.org/10.1016/j.mycres.2009.01.010
- Tomason Y., Gibson P.T. Fungal characteristics and varietal reactions of powdery mildew species on cucurbits in the steppes of Ukraine. Agronomy Research. 2006;(4):549-562.
- Lebeda A., Kristkova E., Sedlakova B., Coffey M.D., McCreight J.D. Gaps and perspectives of pathotype and race determination in Golovinomyces cichoracearum and Podosphaera xanthii. Mycoscience. 2011;(52):159-164.
- Дютин К.Е., Соколов Ю.В. Определение видов мучнистой росы тыквенных культур по конидиальной стадии. Сборник научных трудов ВНИИОБ.-Астрахань, 1978. Вып.7. С.11-14.
- Jahn M., Manger H.M., McCreight J.D. Breeding cucurbit crops for powdery mildew resistance, in: Belanger, R.R., Bushnell, W.R., Dik, A.J. and Carver, L.W. [Eds.] The Powdery Mildews, A Comprehensive Treatise. APS Press, St. Paul, MN, USA. 2002. pp. 239-248.
- Bardin M., Nicot P.C., Normand P., Lemaire J.M. Virulence variation and DNA polymorphism in Sphaerothecafuliginea, causal agent of powdery mildew of cucurbits. Eur. J. Plant Pathol. 1997;(103):545-554.
- Cohen R., Burger Y., Katzir N. Monitoring Physiological Races of Podosphaera xanthii (syn. Sphaerothecafuliginea), the Causal Agent of Powdery Mildew in Cucurbits: Factors Affecting Race Identification and the Importance for Research and Commerce, PHYTOPATHOLOGY/MYCOLOGY R. Cohen et al. Phytoparasitica. 2004;32(2):174-183.
- Bertrand, F. 1991. Les oïdiums des Cucurbitacées. Thèse Université Paris - Sud - Orsay. Spécialité “Phytopathologie”, 225.
- Чесноков Ю.В., Косолапов В.М. Генетические ресурсы растений и ускорение селекционного процесса. Москва: ООО «Угрешская типография», 2016. 172 с.
- Takamatsu S., Hirata T. Nucleotide Diversity Of Rdna Internal Transcribed Spacers Extracted From Conidia And Cleistothecia Of Several Powdery Mildew Fungi. Mycoscience. 37(3). https://doi.org/10.1007/BF02461299
- Chen W.Y., Tsay J.G. Differentiation of two powdery mildews of sunflower (Helianthus annuus) by a PCR-mediated method based on ITS sequences. European journal of plant pathology. 2008;121(1):1-8. https://doi.org/10.1007/s10658-007-9234-5


