Виртуальный раскрой неостворки с учетом анизотропии при операции по неокуспидизации аортального клапана
Автор: Ватузова А.В., Легкий А.А., Калмыкова П.Ю., Колотова А.А., Саитов Д.Р., Саламатова В.Ю., Федотова П.А., Шкарбан С.Б.
Журнал: Российский журнал биомеханики @journal-biomech
Статья в выпуске: 1 т.30, 2026 года.
Бесплатный доступ
Операция Озаки – передовая методика реконструкции аортального клапана, ключевым этапом которой является выкраивание новых индивидуальных створок из аутоперикарда пациента по стандартным шаблонам. Однако избыточный размер клапана повышает риск развития осложнений, поэтому требуется функционально полноценная створка минимального размера, обеспечивающая адекватное смыкание. Цель данного исследования – изучение влияния анизотропии механических свойств материала створки на функцию клапана для оптимизации шаблона. Исследование проводится методом конечных элементов на модели симметричного трёхстворчатого аортального клапана. Моделирование включает виртуальное размещение неостворок и расчёт диастолического состояния нового клапана в мембранном приближении. Рассматривались три потенциала для описания биомеханики клапана. Оценивались величины провисания, площади, высоты и длины коаптации. Результаты выявили оптимальные направления анизотропии для шаблона D = 24 при разных потенциалах: 45–53° для первого, 39–48° для второго и 2–43° для третьего. При правильной ориентации меньший шаблон, например, D = 18, обеспечивает лучшие характеристики и повышает эффективность. Таким образом, учет направления волокон ткани позволяет уменьшить геометрический размер створки без ухудшения её замыкательной способности, что открывает перспективы к созданию более эффективных протоколов.
Аортальный клапан, операция Озаки, неокуспидизация, анизотропия, коаптация, математическое моделирование, мембранная модель, гиперупругая модель, конечно-элементная модель
Короткий адрес: https://sciup.org/146283273
IDR: 146283273 | УДК: 531/534: [57+61] | DOI: 10.15593/RZhBiomeh/2026.1.02
Virtual cutting of new cups for aortic valve neocuspidization with consideration of material anisotropy
The Ozaki procedure is a modern technique for aortic valve reconstruction using the patient's autologous pericardium. The key step involves cutting new cusps (leaflets) using templates based on patient-specific anatomical landmarks. However, excessively large cusps can lead to serious complications, including coronary artery ostial obstruction and thrombosis. Minimizing risks requires creating a minimal yet functional leaflet that ensures effective coaptation. The aim of this study is to investigate the influence of the material properties of the cusp on valve function in order to optimize the neocuspidization template. The study employs finite element analysis of a symmetrical tricuspid valve model. The simulation involves the virtual placement of the neocusps and the calculation of their diastolic state using a membrane formulation. Three potentials were considered to describe the valve biomechanics. Parameters such as billowing, area, height, and length of coaptation are evaluated. The results revealed optimal anisotropy directions for the D = 24 template with different potentials: 45°–53° for the first, 39°–48° for the second and 2°–43° for the third. With proper orientation, a smaller template, such as D = 18, provides better characteristics and improves efficiency. The results indicate that accounting for the fiber direction enables a reduction in the geometric size of the leaflet without compromising its coaptation capacity, opening prospects for creating protocols that are more effective.
Текст научной статьи Виртуальный раскрой неостворки с учетом анизотропии при операции по неокуспидизации аортального клапана
RUSSIAN JOURNAL OF BIOMECHANICS
Аортальный клапан – клапан сердца, расположенный между левым желудочком и корнем аорты [1]. Он обеспечивает однонаправленное течение крови из сердца в аорту, предотвращая ее обратный ток в левый желудочек, и в норме состоит из трех аортальных створок. Заболевания аортального клапана, в частности кальцинирующий аортальный стеноз, становятся существенной проблемой для глобального здравоохранения. В 2021 г. в мире зарегистрировано около 13,3 млн случаев кальцинирующей болезни аортального клапана с наибольшей распространенностью в возрасте 90–94 лет [2]. С 1990 по 2019 г. распространенность кальцинирующей болезни аортального клапана выросла более чем на 150 %, преимущественно из-за старения населения [3; 4].
Аортальный стеноз поражает около 3,7–4,7 % пациентов старше 65 лет, и ожидается удвоение заболеваемости в следующие 50 лет [5]. Смертность в течение пяти лет неоперированных пациентов с умеренным и тяжелым аортальным стенозом составляет 56 % и 67 % соответственно [6]. Несмотря на успехи в лечении, бремя заболеваний аортального клапана растет, что требует улучшения профилактики, ранней диагностики и доступности хирургических вмешательств [2–4].
Единственным эффективным методом лечения аортального стеноза является протезирование клапана, выполняемое открытым или транскатетерным способом. «Золотым стандартом» остается хирургическое вмешательство на открытом сердце, хотя у пациентов с умеренным и низким риском осложнений широкое применение находит транскатетерное протезирование (ТИАК) [7].
Операция Озаки – это хирургический метод реконструкции аортального клапана, при котором пораженные створки аортального клапана заменяются новыми, изготовленными из собственного перикарда пациента (аутоперикарда) [8–12; 13]. Этот подход, также называемый неокуспидизацией аортального клапана, направлен на восстановление нормальной функции клапанах [14; 15]. Одним из достоинств операции Озаки является отсутствие таких осложнений, связанных с использованием искусственных протезов клапанов, как необходимость пожизненной антикоагулянтной терапии или ограниченный срок службы [9–11; 16–18].
Процедура показала многообещающие краткосрочные и среднесрочные результаты, включая отличные гемодинамические показатели неоклапана, низкую частоту ранних осложнений и отсутствие необходимости в повторной операции [9–12; 19–21], и считается перспективной альтернативой традиционной замене клапана [10; 11]. Однако 26
долгосрочная эффективность и результаты, особенно у молодых пациентов и детей, все еще изучаются [9; 22; 23].
В ходе операции Озаки из перикарда пациента формируются новые створки аортального клапана. Для этого сначала перикард предварительно химически обрабатывается, а затем новые створки вырезаются из ткани по шаблонам, размер которых определяется на основе замеров аортального кольца и межкомиссуральных расстояний для каждого пациента [24; 25]. Эта методика, стандартизированная с помощью специализированных инструментов, обеспечивает анатомическое соответствие неоклапана индивидуальным характеристикам пациента [17; 24; 25].
Одним из недостатков операции Озаки является избыточность новых створок, что означает, что реконструированные створки могут быть чрезмерно высокими или большими. Согласно обзору клинических данных [26], использование неостворок большого размера сопряжено с риском преходящего перекрытия устьев коронарных артерий, что может потребовать реоперации [27–29]. Данный риск также возникает при проведении ТИАК при структурном износе неоклапана, реконструированного по методике Озаки, когда крупные неостворки могут быть прижаты стентом, перекрывая устья венечных артерий [17; 30–32].
Другим серьёзным осложнением из-за избыточности размера створки является тромбоз чаши створки, выявляемый, по данным [33], у 12,5 % пациентов и способный приводить к таким последствиям, как транзиторная ишемическая атака [34]. Вероятность тромбоза возрастает из-за увеличенной площади тромбогенной поверхности, что усугубляется большими размерами неостворок [35; 36]. В отличие от них, стандартные биологические протезы, размер створок которых приближен к нативным, в большинстве случаев не подвержены тромбозу. При этом исследования показывают, что тщательный подбор размера неостворки и корректировка её шаблона для операции Озаки позволяет добиться отличных долгосрочных результатов с низкой частотой повторных операций и осложнений [17; 32]. Таким образом, для минимизации указанных рисков размер неостворок целесообразно выбирать минимально возможным, но достаточным для обеспечения адекватной коаптации неоклапана [37].
В рамках данного исследования мы хотим изучить влияние анизотропии материала створки на выбор размера шаблона типа Озаки, а именно возможность уменьшения размеров створки при сохранении или улучшении функциональных характеристик клапана. Оцениваемые параметры нашего исследования включают: площадь коаптации, центральную высоту коаптации, длину коаптации и степень биллоуинга
(провисания) неоклапана [26], где под коаптацией понимается область смыкания (соприкосновения) створок аортального клапана [17; 37; 38].
Исследования по влиянию анизотропии механических свойств материала створки на коаптационные характеристики неоклапана единичны, насколько известно авторам. В работе [39] было получено, что, хотя анизотропия материала створок не оказывает существенного влияния на общие характеристики коаптации, она может влиять на диастолическую конфигурацию неоклапана, потенциально влияя на качество смыкания створок при его закрытии [37]. Однако в работе [39] рассматривались только пять случаев возможных направлений волокон. В рамках данной работы мы хотим провести более подробный и систематический анализ влияния угла направления волокон (анизотропии) на функциональность нового клапана [25; 37]. Согласно результатам работы [40], анизотропия механических свойств створки клапана важна для максимизации её радиального растяжения и площади коаптации, причем для достижения оптимальной коаптации, особенно при физиологических давлениях, требуется определённая степень анизотропии, аналогичная той, что наблюдается у нативных клапанов. Таким образом, анизотропия может играть существенную роль в выборе размера неостворки и оптимальной функции клапана [21; 41]. В процедуре Озаки используется аутоперикард, фиксированный глутаральдегидом. Эта фиксация приводит к распрямлению изначально волнистых пучков коллагеновых и эластичных волокон согласно [42], что может влиять на анизотропные свойства ткани [43–45]. Однако данных о механических свойствах этой ткани нет из-за отсутствия достаточного количества образцов и стандартизованного протокола исследований. Нет единого мнения об изотропии/анизотропии [16; 46; 47] и изменении механических свойств после химической обработки (жестче/мягче) [48; 49].
Поэтому изучение влияния упругих свойств материала створок из аутоперикарда на характеристики коаптации становится актуальным при разработке математической модели для процедуры неокуспидизации [18; 50].
Как было отмечено выше, целью данного исследования является проведение детального и систематического анализа влияния анизотропии (угла направления волокон) на функциональные характеристики нового клапана, с возможностью уменьшения размера шаблона неостворок за счет их раскройки с учетом анизотропии.
Для упрощения численных экспериментов рассматривается задача реконструирования симметричного трехстворчатого клапана в упрощенной постановке. Для виртуального размещения неостворок и нахождения диастолического (закрытого) состояния неоклапана используется конечно-элементная технология, описанная в работах [20; 21; 39; 41; 51]. Основные этапы моделирования закрытого состояния неоклапана, результаты численных экспериментов описаны и их обсуждение описаны далее.
Материалы и методы
Исследование влияния анизотропии материала на коаптацию створок проводилось путём моделирования диастолического состояния аортального клапана.
Построение геометрии
Размер шаблонов неостворок типа Озаки может варьироваться (см. рис. 1, а ) и подбирается с помощью интраоперационных измерений межкомиссуриальных расстояний [52]. Предлагается параметризация шаблона типа Озаки с помощью четырех параметров: L , H , H , R , изменяя которые можно получить различные размеры шаблона (см. рис. 1, б ).

а
Рис. 1. Шаблон неостворок типа Озаки: а – пример трафарета с шаблонами разных размеров, нумерация
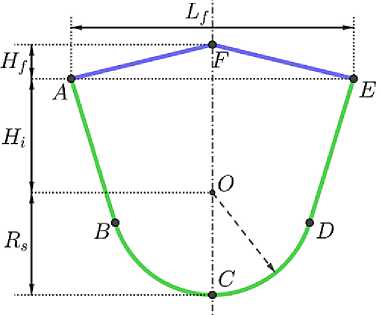
б
имеет тип D = 13, ..., 35, б – параметризация шаблона
а б
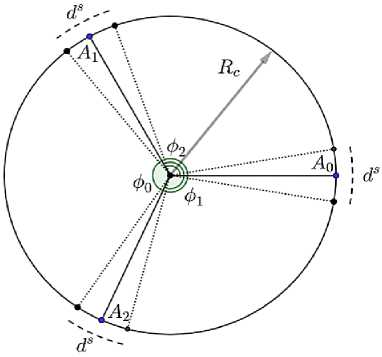
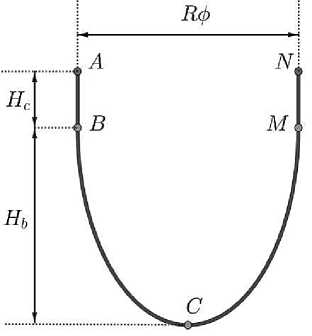
Рис. 2. Схематическое изображение структуры и закрепления створок к корню аорты: а – разделение кореня аорты на три равные части, к которым пришиваются три створки одинаковой формы ( A 0 , A 1 , A 2 – точки соприкосновения неостворок (точки комиссуры) неоклапана), б – линия пришивания неостворок к корню аорты
В данной работе мы будем рассматривать формирование симметричного трехстворчатого неоклапана, при этом корень аорты представим в виде прямого круглого цилиндра радиуса R c (см. рис. 2, а ). Ширина «пришиваемых» к корню аорты створок фиксирована и равна L f = 2 R c . Для дальнейшего анализа и расчетов диаметр корня аорты зафиксирован и равен 24 мм, что соответствует шаблону Озаки номер D = 24.
неостворки рассматривается в мембранной постановке.
Кинематика неостворки
Деформация мембраны описывается деформацией её срединной поверхности. Пусть положение материальных точек отсчетной конфигурации Qo е R3 задается как X = X ^ + X 2e2 + Х 3 ( Хг , X 2) е3 , где
Позиционирование геометрии
Линия
полуэллипс
пришивания
с
представляла собой параметрами
e , e , e обозначают базисные векторы некоторой фиксированной декартовой системы координат. Тогда соответствующие ковариантные G и
2 п
H, = 12 мм, R, = — R - d , b , Ф з с ,
расширенный двумя
отрезками длины Hc = 1,5
мм (см. рис. 2, б ).
Расстояние между соседними линиями пришивания d s было равно 1 мм.
Новая плоская створка размещается в корень согласно алгоритму, предложенному и подробно описанному в работе [53]. Этот алгоритм учитывает особенности пришивания во время операции по неокуспидизации и воспроизводит позицию (начальное положение) вшиваемой неостворки.
Математическая постановка
Используя симметрию клапана, задачу определения его диастолического состояния можно свести к моделированию деформации одного лепестка, а влияние двух остальных учесть с помощью контактных плоскостей. Задача квазистатического равновесия под действием диастолического давления для клапана решается методом конечных элементов, изложенным в [39; 51], при этом деформация
контравариантые G i базисные вектора и нормаль к
Qo определяются как
G а
^Х G“= — дXа , дХ ,
G 1 X G 2
= IG 1 X G 2 II
а = 1,2;
Деформация срединной поверхности – это
взаимно однозначное отображение x = x ( X ) , и
положение материальных точек актуальной деформированной конфигурации Q, е R 3 определяется как x = Х 3 = 1 X i ( X 1 , X 2) e; .
Соответствующие ковариантные g и контравариантые g i базисные векторы и нормаль к Q( имеют вид:
d x а a x а
, g = , дXа dx
а = 1,2;
n =
g 1 X g 2
II g 1 X g 2 II
Используемые в работе потенциалы для моделирования аортального клапана и значения их параметров
|
Вид потенциала |
Параметры |
|
W = c10 ( e C “ 1 ( 1 3 D - 3 )- 1 ) + a_ f e k ( 1 4 D - 1 ) - 1 ] \ ' 2 k 2 3 7 |
C10 = 1,21 кПа C 01 = 7,99 k = 24,23 кПа k2 = 57,62 |
|
W = ц ( 1 3 D - 3 ) + c0 f e c 1 ( ' 3 D-^ + c 2 ( ' 4 D - 1 ) 2 - 1 ] |
ц = 1,18 кПа c 0 = 55,04 c = 8,08 c = 54,00 |
|
W 3 = C 1 ( 1 13 D - 3 ) + a~b f e b ( 1 4 D - 1 ) 2 - 1 ] |
C = 19,59 кПа a = 12,94 кПа b = 77,79 |
Градиент деформации мембраны как трехмерной структуры имеет вид [54; 55]:
F = F2 j +X n ® N , FM = У ga ® G a , Z = —, (3)
2 d 2 d / ea a=1 H где F – поверхностный градиент деформации, который описывает деформацию срединной поверхности мембраны, параметр Z характеризует изменение толщины вследствие деформации, h – толщина мембраны в актуальной конфигурации, H – толщина мембраны в отсчетной конфигурации, ® обозначает тензорное произведение.
Определим инварианты I , J поверхностного правого тензора деформаций Коши – Грина C2d = F2dF2d = E2^=! ga,pG“ ® Ge следующим образом:
1 1 = tr ( C 2 d ) = E g ap G “P , J = det F d = 4 det C d , (4)
a,p= 1
где g a₽ = ( g a , g ₽ ) , G “₽ = ( G “ , G ₽ ) - компоненты
S = 2 W
d C
[56]. Упругий потенциал также называется функцией плотности энергии деформации W (C).
Пусть материал мембраны представляет собой анизотропный гиперупругий материал, а именно изотропную матрицу с одним выделенным семейством волокон, лежащим в плоскости срединной поверхности мембраны f = f 'G3 + f 2G2 . Для плоской развертки створки семейство волокон характеризуется вектором f = cos 0 e3 + sin 0 e2 + 0 e3 (см. рис. 3).
Определим 1 3 D = f - ( Cf ) и 14 = f - ( CMf ) , где a • b обозначает скалярное произведение векторов a и b . Поскольку волокна лежат в срединной плоскости, то 1 4 D = f - ( Cf ) = f - ( C 2 d f ) = 1 4 .
В работе рассматривается три потенциала, предложенные для створки нативного аортального клапана, и параметры потенциалов получены подгонкой к одним и тем же экспериментальным кривым [57] (см. табл.).
Учитывая связь между поверхностными и метрических тензоров.
Материал неостворки считается несжимаемым материалом, в этом случае можно получить следующие соотношения [54; 55]:
1 13 D = 1 1 + J у 1 2 D = J 2 + 1 1 J л (5)
где:
1 3 D = tr C , 1 33D = ( ( tr C ) 2 - tr C 2 ) / 2,
1 33 D = det C = 1, C = F T F = C2 rf+X 2 N ® N .
Определяющие соотношения
Предполагается, что мембрана является гиперупругим материалом. Это означает, что существует упругий потенциал W ( C ) такой, что второй тензор напряжений Пиолы – Кирхгофа
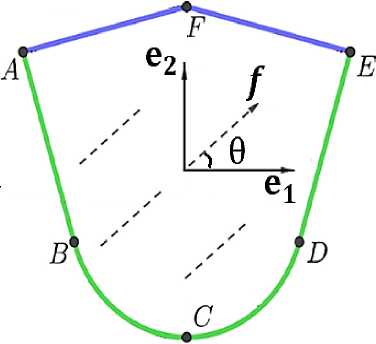
Рис. 3. Шаблон с выделенным семейством волокон, характеризующимся вектором f
3 D - 2
трехмерными инвариантами | = | + J ,
1 3 D = J 2 + I J - 2 , 1 3 D = I 4, упругий потенциал
W = W (C) можно переписать как функцию поверхностных инвариант W = W (I, J, I4).
Компоненты второго тензора напряжений Пиолы – Кирхгофа для несжимаемого материала в мембранном приближении могут быть записаны как функции только поверхностной части правого тензора Коши – Грина [54; 55]:
S = £ s “e G и® G p , s ав = 2 W . (7)
а,Р= 1 d g иР
Численное решение
Для нахождения диастолического состояния аортального клапана используется метод конечных элементов, подробно описанный в работах [39; 51]. Cтворка клапана представляется триангулированной срединной поверхностью, задача равновесия которого под действием приложенных сил сводится к численному решению системы нелинейных алгебраических уравнений относительно новых положений узлов расчетной сетки. Равновесие подразумевает, что в каждом узле расчетной сетки с индексом i выполняется равенство:
F p + F s + F ! = 0 , (8)
где Fi , Fi и Fi – сила диастолического давления ps c крови, сила упругости и контактная сила, которая возникает при соприкосновении с контактными поверхностями. Для избежания проблем стагнации невязки и критерия остановки при решении стационарной задачи, в работе используется динамическая формулировка, предложенная в [58]. Время проведения расчетов берется в 35 мс.
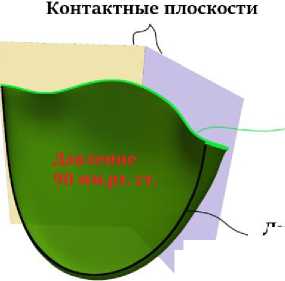
Благодаря симметрии клапана задача сводится к моделированию деформации одного лепестка, заменив другие контактными плоскостями. К пришитой створке приложено диастолическое давление в 90 мм рт. ст., при этом линия пришивания (прикрепления неостворки к аорте) является жестко фиксированной. Граничные условия схематично обозначены на рис. 5. Контактные силы вычисляются методом, предложенным в [39].
Наличие экспоненциальных членов в формуле для каждого потенциала приводит к нефизично большим значениям напряжений, особенно на этапе пришивания клапана. Для того чтобы этого избежать и сделать расчеты более робастными, экспоненциальные члены в потенциалах искусственно ограничиваются сверху, начиная с некоторого момента примерно соответствующего удлинению на 20 %.
Анализируемые коаптационные характеристики
В работе находятся и анализируются следующие характеристики: площадь коаптации, центральная коаптация ( cH ), длина коаптации ( lH ) и провисание ( bH ) (см. рис. 4).
Длина центральной коаптации ( сH , мм) – расстояние от высшей точки соприкосновения трёх
Свободный край
Рис. 5. Схематичное представление граничных условий при решении задачи нахождения диастолического состояния аортального клапана
Линия пришивания (фиксированная граница)
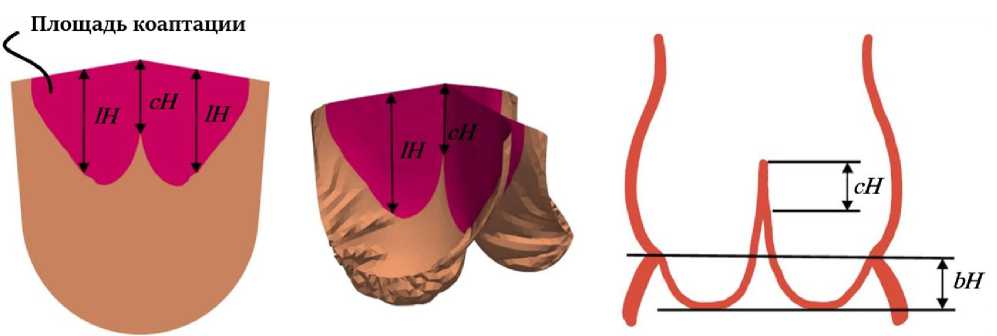
Рис. 4. Схематичное представление оцениваемых характеристик, где площадь коаптации – область, выделенная красным цветом на створках, cH – длина центральной коаптации, lH – длина коаптации, bH – величина провисания (биллоунга)
a
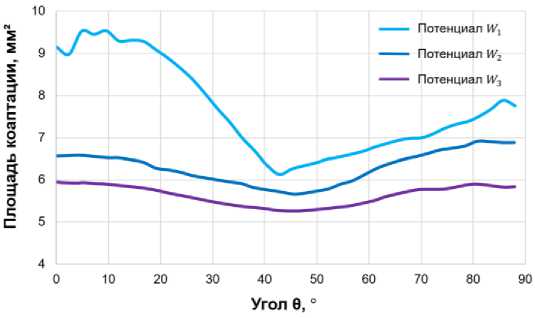
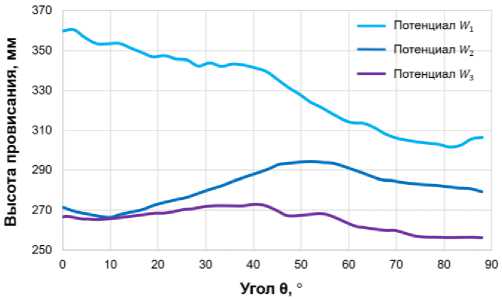
Рис. 6. Величины площади коаптации и провисания в зависимости от угла анизотропии 0 : а - площадь коаптации, б - высота провисания для рассмотренных потенциалов
б
створок клапана до низшей точки относительно плоскости, проходящей через самые нижние точки линий прикрепления всех трёх створок. Величина центральной коаптации характеризует, насколько хорошо створки закроются и не будет ли обратного тока крови.
Длина коаптации ( IH , мм) - расстояние, которое измеряется от середины свободного края контакта двух створок вертикально вниз (перпендикулярно свободному краю) с помощью эхокардиографии.
Провисание створки ( bH , мм) - расстояние от низшей точки прикреплённого края створки до плоскости, содержащей низшие точки всех трех створок.
Результаты
В качестве первого набора виртуальных экспериментов для шаблона типа Озаки D = 24, исследуются направления анизотропии 0 , при которых площадь коаптации будет максимальной и провисание минимальным.
На рис. 6 а, б показаны результаты для первого потенциала W , и, согласно полученным результатам, видно, что оптимальные направления анизотропии лежат в интервале от 45° до 53°.
Оптимальные углы для второго потенциала 0 , отраженные также на рис. 6а, б лежат в интервале от 39° до 48°, но, в отличие от первого потенциала, второй имеет меньшую площадь коаптации и меньшее провисание. Это связано с более «жестким» механическим поведением материала под действием давления. Негладкость в графике связана с численными сложностями из-за механического поведения, описываемого потенциалом W .
Несогласованное включение и выключение ограничений на нефизичный рост напряжений на отдельных треугольных элементах сетки, а также возможность неединственности решения вместе с использованием решателя с большим шагом по времени могло приводить к получению различных решений контактной задачи и, следовательно, наблюдаемой негладкости на графике для W . Этот вопрос требует отдельного изучения и в рамках данной работы не рассматривается, поскольку нас далее интересовал потенциал W , который лучше других вариантов описывает экспериментальные кривые для нативной створки из рассматриваемых трех потенциалов [57].
Также рассмотрим полученные значения площади коаптации и биллоуинга (провисания) для различных углов 0 для третьего потенциала. В отличие от двух предыдущих случаев, он обладает наибольшей площадью коаптации и наибольшим провисанием. Это связано с тем, что поведение потенциала описывает более «мягкий» ответ материала под действием давления. Для третьего потенциала W оптимальная зона углов это от 2° до 43°, что значительно отличается от предыдущих значений. Может, это связано с тем, что потенциал W плохо описывает нелинейное поведение материала в направлении перпендикулярном направлению волокон при увеличении деформации [57].
Для дальнейшего анализа влияния угла анизотропии в исследование включаются более значимые клинические характеристики, такие как высота центральной коаптации и длина коаптации (см. рис. 4) при разных размерах вшиваемых шаблонов. При этом для дальнейших численных экспериментов используется только первый потенциал W . Как было отмечено в работе [57], данный потенциал лучше всего описывает экспериментальные данные для двухосного растяжения створки аортального клапана и является наиболее робастным в наших численных экспериментах.
На рис. 7 приведены результаты для различных размеров шаблонов и угла анизотропии θ . Согласно
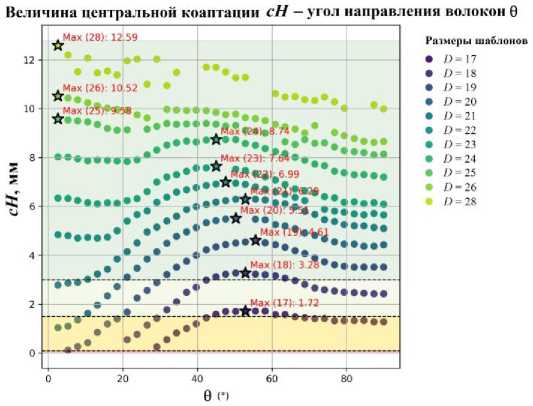
Оптимальные значения (> 3 мм)
Допустимые значения (1,5—3 мм)
Малоподходящие значения (0,1 -1,5 мм)
Недопустимые значения (< 0,1 мм)
Рис. 7. Величина центральной коаптации cH при разных размерах шаблона и углах направления волокон θ
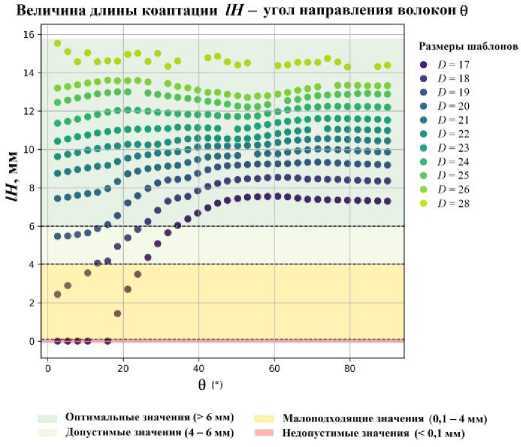
Рис. 8. Величина длины коаптации IH при разных размерах шаблона и углах направления волокон 0 (потенциал W )
(потенциал W )
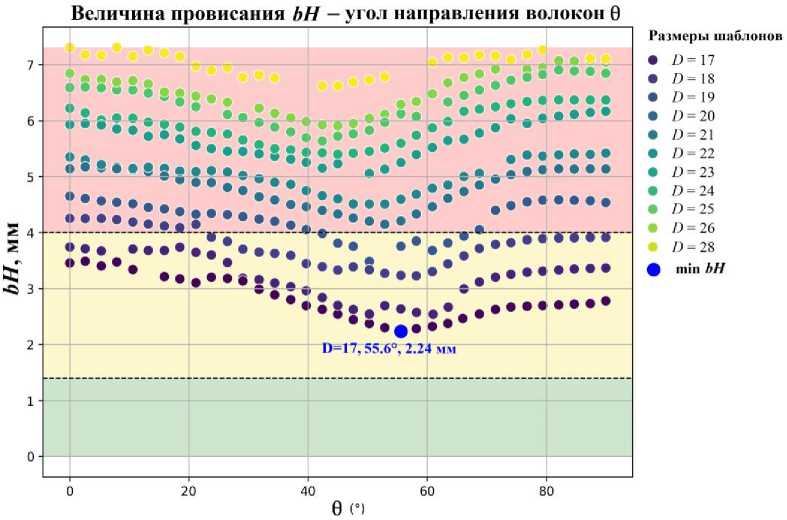
Оптимальные значения (0— 1,4 мм)
Допустимые значения (1,5 — 4 мм)
Недопустимые значения (> 4 мм)
Рис. 9. Величина провисания bH при разных размерах шаблона и углах направления волокон 0 (потенциал W )
полученным результатам, при любом направлении анизотропии высота центральной коаптации cH остаётся в оптимальном диапазоне для шаблона Озаки D = 24. Однако при выборе некоторых направлений угла анизотропии мы можем использовать меньший размер шаблона. Например, при 53˚ величина центральной коаптации для 18-го размера шаблона ( D = 18) находится в оптимальной зоне.
Величины длины коаптации lH для различных размеров шаблонов и угла 0 показаны на рис. 8. Согласно полученным результатам, при угле 0 >30° все варианты разных размеров шаблона оказались в оптимальной зоне.
На рис. 9 показаны результаты для провисания bH , согласно которым ни один размер шаблона не соответствует оптимальному значению, однако при определенном направлении анизотропии некоторые размеры шаблонов попадают в область приемлемых
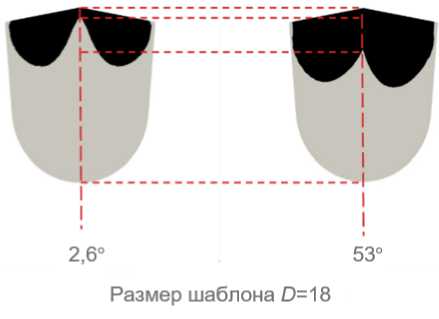
Рис. 10. Зависимость величины центральной коаптации от угла направления волокон 0 для размера шаблона D = 18 (потенциал W )
значений. В частности, минимальное провисание будет при 0 ~ 56° для шаблонов размером D = 17 и D = 18.
Согласно результатам (см. рис. 7-9), при определенном угле анизотропии меньший размер шаблона обеспечивает оптимальные значения рассмотренных характеристик неоклапана. В частности, для корня аорты 24 мм почти оптимальным будет шаблон D = 18 при 0 ® 53°. Таким образом, учет направления анизотропии при раскрое новых створок может помочь уменьшить избыточный размер шаблона и добиться оптимальных значений коаптации (см. рис. 10). Отметим, что предложенные диапазоны параметров замыкательной функции аортального клапана на рис. 7-9 определены в ходе консультаций с кардиохирургами и требуют дальнейшего систематического исследования. Тем не менее это не снижает ценности проведённой работы и полученных результатов.
Обсуждение
Влияние анизотропных упругих свойств материала створок на размер зоны коаптации изучено недостаточно [39; 59]. Данное исследование направлено на изучение влияния анизотропии материала створки, определяемой направлением волокон, на замыкательную функцию нового аортального клапана. В качестве анализируемых параметров выбираются имеющие клиническое значение площадь коаптации, центральная высота коаптации, длина коаптации и степень провисания неоклапана.
Для описания механического поведения неостворки аортального клапана используются три потенциала, ранее предложенные для описания нативной створки. Согласно полученным результатам, коаптационные характеристики крайне чувствительны к выбору гиперупругой модели, несмотря на то что параметры всех моделей были подобраны по одинаковым экспериментальным кривым двухосного растяжения. Это подчеркивает важность проведения экспериментальных исследований мягких тканей при различных режимах деформирования для построения корректных моделей механики материала.
Согласно полученным результатам (см. рис. 6-10), направление анизотропии качественно влияет на коаптационные характеристики, особенно для шаблонов малых размеров. Увеличение угла 0 от 0° до 53° приводит к росту центральной коаптации (см. рис. 7, 10) и площади коаптации для потенциалов W и W 2 (см. рис. 6 а, б ). Это качественно согласуется с данными работы [60], где для нативной свиной створки увеличение угла с 0° до 35° приводило к росту площади смыкания на ~20 мм2 (15 %) и центральной высоты смыкания на ~1 мм (40 %). Отметим, что в [59] рассматривается симметричная относительно вертикали ориентация коллагеновых волокон, в отличие от используемого нами однородного случая. Однако вид гиперупругого потенциала и точные размеры шаблона в указанной работе не приведены, что затрудняет воспроизведение и количественное сравнение результатов.
В работе [39] сделан вывод о слабом влиянии направления анизотропии на коаптацию, что может быть связано с использованием больших створок по протоколу Озаки. Наши результаты (см. рис. 7-9) согласуются с этим: влияние анизотропии становится менее выраженным с увеличением размера шаблона.
Кроме того, наши результаты демонстрируют, что учет ориентации вырезаемого шаблона относительно направления волокон ткани позволяет использовать шаблон типа Озаки меньшего размера, при этом обеспечивая величину коаптации и провисания в заданных пределах. Например, для аорты диаметром 24 мм вместо шаблона D = 24, рекомендуемого методикой Озаки, можно использовать шаблон D = 18 при ориентации волокон под углом примерно в 53°.
Таким образом, сравнение с протоколом Озаки показывает, что оптимальные размеры шаблона могут быть меньше рекомендуемых. Однако для уточнения клинических рекомендаций требуются дальнейшие исследования.
Ограничение исследования
Работа имеет ряд ограничений. Во-первых, использованная мембранная модель не учитывает изгибную жёсткость, что может приводить к завышению оценки коаптации. Во-вторых, в настоящее время отсутствует адекватное определяющее соотношение для описания механических свойств обработанного перикарда, а также отработанный протокол его обработки для задания заданной анизотропии. Считается, что для тканеинженерных клапанов требуется сопоставимая с нативными структурами анизотропия [40]. При этом ориентация коллагеновых волокон в нативных створках крайне неоднородна и сложна [59; 60].
Использование обработанного аутоперикарда не позволяет воспроизвести ориентацию волокон, подобно створке нативного клапана, но знание анизотропии материала позволяет оптимизировать


