Влияние адсорбции атомов и молекул кислорода на электронное строение графеновой наноленты
Автор: Шамина Елена Николаевна, Лебедев Николай Геннадьевич
Журнал: Математическая физика и компьютерное моделирование @mpcm-jvolsu
Рубрика: Физика
Статья в выпуске: 4 (41), 2017 года.
Бесплатный доступ
В работе представлены результаты квантово-химических полуэмпирических исследований процессов адсорбции атомов и молекул кислорода на поверхности графеновой наноленты. Расчеты выполнены на основе модели молекулярного кластера c граничными псевдоатомами с использованием полуэмпирических расчетных схем MNDO и PM3. Определены энергетические характеристики процессов адсорбции.
Модель молекулярного кластера, квантовая химия, энергия адсорбции
Короткий адрес: https://sciup.org/14969053
IDR: 14969053 | УДК: 541.138 | DOI: 10.15688/mpcm.jvolsu.2017.4.9
Influence of adsorption of atoms and molecules of oxygen on the electronic structure of graphene nanoribbons
The article presents the results of calculations of the energy characteristics of adsorption of oxygen atoms and molecules on graphene nanoribbons surface. The calculations of electronic structures were carried out by semi-empirical MNDO and PM3 quantum-chemical methods using the molecular cluster model with boundary pseudoatoms. The main geometrical and electronic-energy characteristics of graphene nanoribbons with adsorbed oxygen atoms and molecules were calculated. It is revealed that the changes of the frontier energies Е HOMO and Е LUMO indicate that the properties of nanoribbons depend on the result of adsorption, in particular, on the increase of these systems reactivity. It is also revealed that an oxygen molecule is weakly bound to the GNR surface with low adsorption energy. The configuration where the oxygen atom is located above the center of the С-С bond, or directly above the carbon atoms of the surface of the GNR has a stronger binding between an oxygen and surface.
Текст научной статьи Влияние адсорбции атомов и молекул кислорода на электронное строение графеновой наноленты
DOI:
Графеновые наноленты (ГНЛ) рассматриваются в литературе в качестве перспективного материала для создания таких устройств, как полевые транзисторы, коммутационные устройства, сенсоры и др. Одним из преимуществ их использования является зависимость электронных свойств от характерных размеров наноленты и геометрии краев [7]. Электронные свойства ГНЛ могут быть модифицированы посредством внесения в структуру нанолент дефектов, таких как вакансий [6] или посредством адсорбции атомов или молекул [4; 5; 8].
Ранее в ряде работ был изучен вопрос о зависимости электронных свойств оксидированных углеродных наноструктур от их геометрии и положения адатома. В частности, в работах [2–3] на основе полуэмпирических исследований авторами была показана осциллирующая зависимость энергий адсорбции процессов оксидирования от диаметра и хиральности углеродной нанотрубки. Чередование минимальных и максимальных значений энергий с ростом диаметра трубок позволило определить оптимальные диаметры хиральных УНТ, на которых адсорбция атомарного и молекулярного кислорода реализуется наиболее эффективно в том смысле, что формируется энергетически более устойчивая система. В работе [9] авторами, в рамках теории функционала плотности, был изучен вопрос о зависимости электронных свойств молекулярно окидированного графена от положения адсорбированной молекулы кислорода относительно поверхности. Было показано, что конфигурация, в которой связь O-O параллельна поверхности, характеризуется наибольшим значением энергии адсорбции (особенно над центром шестиугольника), чем та, где связь O-O перпендикулярна поверхности.
В данной работе представлены результаты расчета энергетических характеристик процессов адсорбции атома кислорода и диссоциативной адсорбции молекулы кислорода на поверхности графеновых нанолент типа «arm-chair». Проведено исследование электронных свойств таких структур в зависимости от концентрации атомов на поверхности и их геометрического расположения.
Расчеты электронного строения данных структур выполнены в рамках модели молекулярного кластера с граничными псевдоатомами с использованием квантово-химических полуэмпиричес-ких методов MNDO и PM3 [1]. Модель молекулярного кластера позволяет сравнительно легко описывать структурные дефекты, функциональные группы на поверхности кристаллов и т. д. Это способствует широкому ее применению в большинстве хемосорбционных и каталитических задач.
Выбор модели
В качестве геометрических моделей изучаемых нанолент выбраны кластеры, содержащие 3 шестиатомных цикла (гексагона) по ширине и от 3 до 6 элементарных ячеек (ЭЯ) по длине. Граничные разорванные химические связи замыкались атомами водорода, которые выбирались в качестве граничных псевдоатомов.
В работе рассмотрено три варианта положения атомарного и молекулярного кислорода (рис. 1). Положение адатомов кислорода в одном случае выбрано над центром С–С-связи, так как он является двухвалентным при формировании ионно-ковалентных связей (рис. 1, а ), а в другом случае непосредственно над атомами углерода поверхности наноленты (рис. 1, в ). Положение адсорбирующейся молекулы кислорода выбрано параллельно С–С-связи (рис. 1, б ).
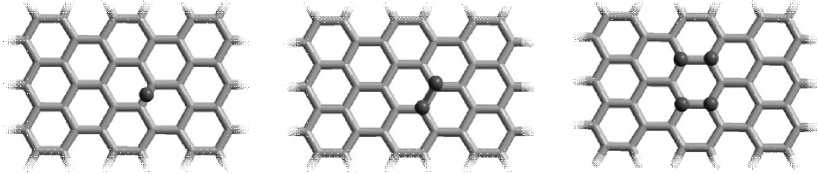
а б в
Рис. 1. Фрагменты структуры графеновой наноленты с указанием положения адсорбирующихся частиц: а – атом кислорода над центром С–С-связи; б – молекула кислорода параллельно С–С-связи;
в – атомы кислорода над атомами углерода
Кроме того, адсорбирующиеся частицы помещались в центральной части наноленты, чтобы уменьшить влияние граничных псевдоатомов.
Обсуждение результатов
Рассчитаны следующие основные электронно-энергетические характеристики: энергии граничных орбиталей Е ВЗМО и Е НВМО; энергия адсорбции Е ад и ширина запрещенной щели Е g и изменение ширины запрещенный зоны Δ Eg , обусловленное адсорбцией.
В результате адсорбции атом кислорода образует две химические связи с соседними атомами углерода, молекула кислорода диссоциирует на атомы, которые образуют по две химической связи с поверхностными активными центрами С, при этом происходит деформация поверхности наноленты так, что атомы углерода смещаются с положений равновесия наружу наноленты. В результате такой деформации связи С–С углеродных гексагонов, над которыми происходило присоединение О2, удлинились по сравнению с невозмущенными значениями в среднем на 9 %.
Анализ результатов показывает, что увеличение длины наноленты приводит к изменению энергетических характеристик процессов оксидирования углеродных нанолент. Величины энер- гий верхней занятой и нижней вакантной МО зависят от длины наноленты: ЕВЗМО монотонно уменьшается, а ЕНВМО – увеличивается (рис. 2). С увеличением длины наноленты разница между энергиями граничных орбиталей убывает, что свидетельствует об увеличении перекрывания между валентной зоной и зоной проводимости и увеличении реакционной способности системы. То есть адсорбированные на поверхности частицы увеличивают сродство ГНЛ к другим атомам или молекулам.
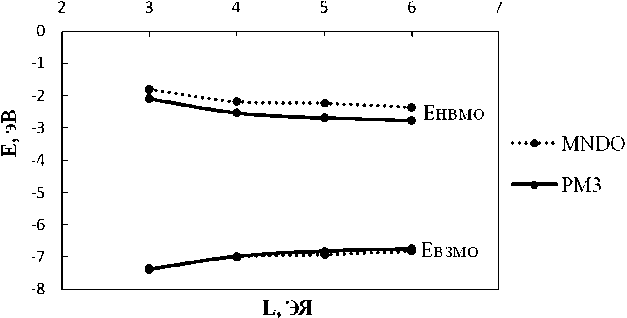
а
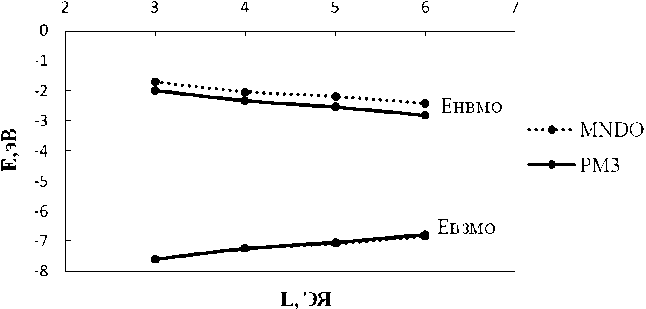
б
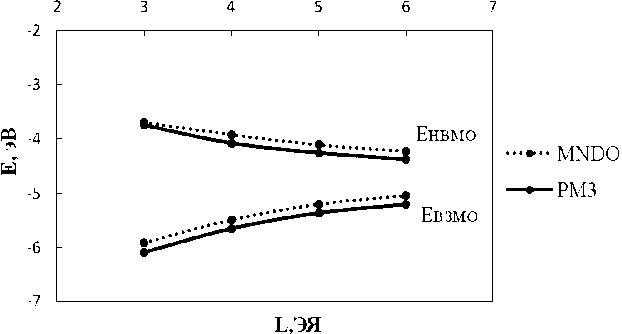
Рис. 2. Энергия граничных орбиталей ГНЛ с адсорбирующимися частицами как функция длины: а – один адатом кислорода; б – молекула кислорода; в – четыре адатома кислорода
Адсорбированные частицы можно рассматривать как дефект структуры – квантовую точку, поляризующую поверхность ленты. Квантовая точка на поверхности создает дополнительные локализованные квантовые состояния электронов, которые могут заполняться электронами системы. Согласно расчетам величина энергии запрещенной щели Еg у ГНЛ с одним атомом кислорода возрастает в пределах ~1,1 ÷ 1,4 эВ (MNDO) и ~0,89 ÷ 1,32 эВ (PM3). При адсорбции молекулы кислорода и ее диссоциации значения величины энергии запрещенной зоны колеблются в пределах значений ~1,05 ÷ 1,68 эВ (MNDO) и ~0,79 ÷ 1,55 эВ (PM3). Величина энергии запрещенной щели Еg у ГНЛ с четырьмя атомами кислорода составляет ~1,21 ÷ 1,67 эВ (MNDO) и ~1,27 ÷ 1,61 эВ (PM3). Полученные данные свидетельствуют о полупроводниковых свойствах изучаемых нанолент.
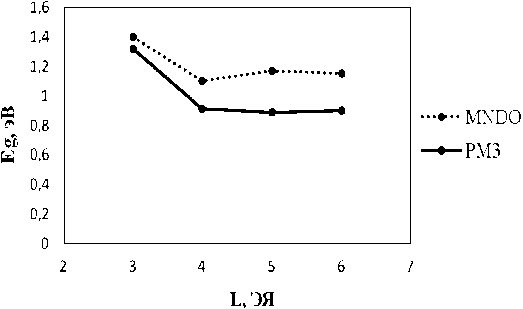
а
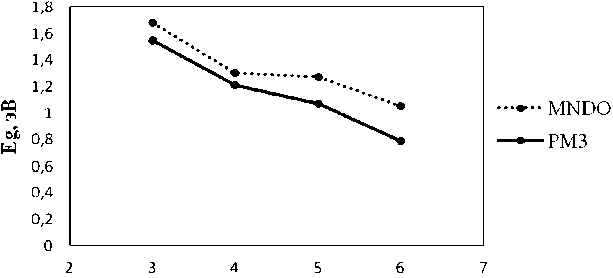
ь,эя
б
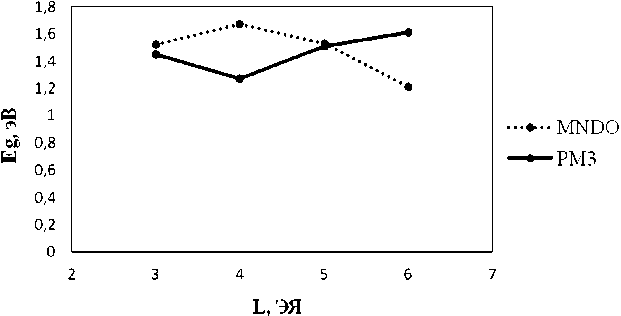
Рис. 3. Энергия запрещенной зоны оксида ГНЛ как функция длины: а – один адатом кислорода; б – молекула кислорода; в – четыре адатома кислорода
Следует заметить, что с увеличением длины наноленты энергия Eg уменьшается (см. рис. 3, а , б ). Это говорит об увеличении «металличности» изучаемой структуры, что соответствует экспериментальным данным: бесконечная графеновая поверхность обладает проводящими свойствами. Однако следует отметить, что при адсорбции четырех атомов кислорода наблюдается отсутствие корреляции численных результатов, полученных разными полуэмпирическими методами (рис. 3, в ). Данное расхождение, на наш взгляд, связано с параметризацией использованных полуэмпири-ческих методов. При этом метод PM3 использует модифицированную формулу для межатомного взаимодействия [1], что приводит к увеличению энергии взаимодействия между молекулами кислорода, адсорбированными на поверхности ГНЛ. Сильная корреляция между молекулами O2 влияет на энергию первого электронного перехода, которая сопоставляется с величиной Eg.
Зависимости энергии химической связи (энергии адсорбции) от длины наноленты пред . ставлены на рисунке 4. Для структуры, содержащей n адсорбированных атомов кислорода, энергия химической связи E ад( n ), приходящаяся на один адсорбированный атом, рассчитывалась следующим образом:
Eад(n) = (Etotal – EGNR – nEO) / n, где Etotal – энергия графеновой наноленты или ее фрагмента (с адсорбированными атомами кислорода на поверхности); EGNR – полная энергия чистой ГНЛ; EО – энергия изолированного атома кислорода.
Кривые на рисунке 4 наглядно демонстрируют, что энергия связывания атома кислорода колеблется около некоторого постоянного значения. При адсорбции одного атома кислорода энергия химической связи составляет в среднем -4,5 эВ в методе MNDO и -3,7 эВ в методе PM3. Отрицательные значения энергии адсорбции указывают на то, что система находится в устойчивом состоянии. При адсорбции четырех атомов кислорода энергия химической связи составляет в среднем -4,2 эВ в методе MNDO и -3,7 эВ в методе PM3.
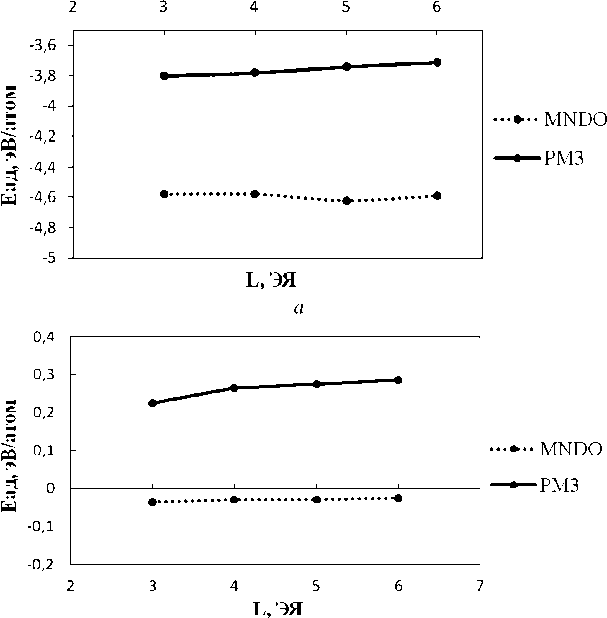
б
Рис. 4. Энергия адсорбции кислорода как функция длины ГНЛ:
а – один адатом кислорода; б – молекула кислорода; в – четыре адатома кислорода (см. также с. 100)
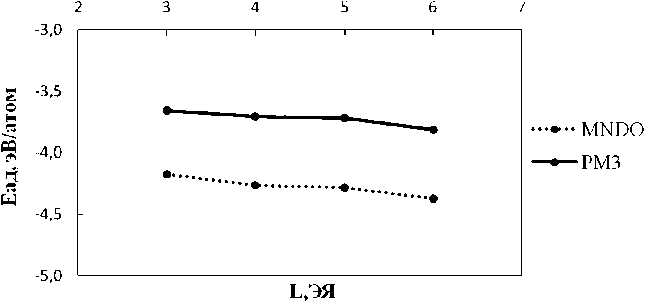
Рис. 4. Окончание
Но при этом наблюдается слабое монотонное убывание величины E ад (рис. 4, в ) с ростом длины ленты, что свидетельствует об увеличении устойчивости образованного оксида ГНЛ и уменьшении влияния границ ленты на процесс адсорбции. При адсорбции молекулы кислорода энергия химической связи составляет в среднем -0,03 эВ в методе MNDO и 0,25 эВ в методе PM3. То есть такое положение молекулы над поверхностью графеновой наноленты является энергетически менее выгодным. Данные результаты хорошо согласуются с аналогичными расчетами с помощью неэмпирических методов [9].
Заключение
На основе модели молекулярного кластера с использованием квантово-химических полу-эмпирических методов MNDO и PM3 изучены электронные свойства графеновых нанолент с адсорбированными атомами и молекулами кислорода. Показана зависимость энергетических характеристик процесса адсорбции от конфигурации адатома и концентрации адатомов. В частности, наибольшая эффективность адсорбции наблюдается в тех случаях, когда адатом кислорода располагается над центром С–С-связи. Поэтому адсорбированные на поверхности ГНЛ молекулы кислорода диссициируют на отдельные адатомы, которые адсорбируются над центрами С–С-связей.
Из анализа результатов расчета следует, что энергия адсорбции адатома кислорода и молекулы кислорода слабо зависит от длины наноленты, а двух молекул кислорода монотонно возрастает с увеличением длины ГНЛ.
Список литературы Влияние адсорбции атомов и молекул кислорода на электронное строение графеновой наноленты
- Степанов, Н. Ф. Квантовая механика и квантовая химия/Н. Ф. Степанов. -М.: Мир, 2001. -519 с.
- Шамина, Е. Н. Влияние хиральности углеродных нанотрубок на диссоциативную адсорбцию молекулярного кислорода на поверхности/Е. Н. Шамина, Н. Г. Лебедев//Журнал физической химии. -2015. -№ 5 (89). -С. 806-811.
- Шамина, Е. Н. Хиральный эффект адсорбции атомарного кислорода на поверхности углеродных нанотрубок/Е. Н. Шамина, Н. Г. Лебедев//Вестник Волгоградского государственного университета. Серия 1, Математика. Физика. -2013. -№ 1 (18). -С. 90-97.
- Electronic, structural, and transport properties of Ni-doped graphene nanoribbons/V. A. Rigo, T. B. Martins, J. R. Antonio da Silva //Phys. Rev. B. -2009. -Vol. 79. -Р. 075435.
- Enhanced half-metallicity in edge-oxidized zigzag graphene nanoribbons/O. Hod, V. Barone, J. Peralta //Nano Lett. -2007. -Vol. 7 (8). -Р. 2295-2299.
- Miller, M. Defect induced distortion of armchair and zigzag graphene and boron nitride nanoribbons/M. Miller, F. J. Owens//Chem. Phys. Lett. -2013. -Vol. 570. -P. 42-45.
- Son, Y. W. Energy Gaps in Graphene Nanoribbons/Y. W. Son, M. L. Cohen, S. G. Louie//Phys. Rev. Lett. -2006. -Vol. 9 (21). -P. 216803-216806.
- Wang, Z. Adsorption of transition metal atoms (Co and Ni) on zigzag graphene nanoribbon/Z. Wang, J. Xiao, M. Li//Appl. Phys. A. -2013. -Vol. 110 (1). -P. 235-239.
- Yu, S. S. Oxidation of Graphene Nanoribbon by Molecular Oxygen/S. S. Yu, W. T. Zheng, J. Qing//IEEE Trans. Nanotechnol. -2008. -Vol. 7 (5). -P. 628-635.


