Влияние антацидных операций на концентрацию гастрина в плазме крови и риск развития злокачественных новообразований толстой кишки
Автор: Корсаков И.Н., Восканян С.Э., Найденов Е.В.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Хирургия
Статья в выпуске: 4 т.11, 2015 года.
Бесплатный доступ
Цель: выявление связи антацидных операций и злокачественных новообразований органов пищеварительной системы. Материал и методы. Исследование проведено на 72 крысах линии Wistar: изучалось влияние стволовой ваготомии, дистальной резекции 2/3 желудка и антрумэктомии на концентрацию гастрина в плазме крови, а также влияние внутрибрюшинного введения азоксиметана на частоту развития злокачественных новообразований толстой кишки. Результаты. Установлено повышение плазменной концентрации гастрина в послеоперационном периоде стволовой ваготомии, установлено некоторое снижение его концентрации после начального пика с дальнейшей стабилизацией. Выявлено снижение концентрации гастрина в результате дистальной резекции желудка до значений, близких к нулю, с последующим незначительным ее повышением и дальнейшей стабилизацией. Определено, что у животных, подвергнутых выполнению стволовой ваготомии в сочетании с индукцией опухолевого роста путем введения химического канцерогена азоксиметана, частота развития новообразований толстой кишки была статистически значимо выше, чем у животных, подвергнутых только введению азоксиметана. Частота развития опухолей у животных, подвергнутых резекции 2/3 желудка, отличалась статистически незначимо от этого параметра у животных контрольной группы. Заключение. Вагусная денервация брюшной полости вызывает значительное стойкое повышение концентрации гастрина в плазме крови. Резекция дистальных отделов желудка вызывает значительное снижение продукции гастрина, сменяющееся незначительным его ростом в отдаленном периоде. Стволовая ваготомия повышает риск развития новообразований брюшной полости у крыс.
Антацидные операции, ваготомия, гастрин, дистальная резекция желудка, злокачественные новообразования
Короткий адрес: https://sciup.org/14918217
IDR: 14918217
Influence of antacids operations at histamine concentration in plasma and the risk of malignancies of the colon
Aim; identify communication between antacid operations and malignant tumors of the digestive system. Material and methods. The study was conducted on the 72 Wistar rats. The effect of the stem vagotomy and resection of the distal 2/3 of the stomach and antrumectomy to the concentration of gastrin in plasma were investigated. The effect of intraperitoneal injection of the azoksimetan on the incidence of malignant tumors of the colon was investigated. Re-sults. Increase of the plasma concentration of the gastrin in the postoperative period after stem vagotomy was found. Reduction of the concentration of the gastrin after distal gastrectomy to values close to zero with slight its rise and subsequent stabilization was found. The incidence of colon tumors in animals after stem vagotomy in conjunction with intraperitoneal injection of the chemical carcinogen azoximetan was higher compared to the animals after isolated injection of the azoximetan. The incidence of tumors in animals after resection of the distal 2/3 of the stomach differed not statistically significant from control animals. Conclusion. Vagal denervation of the abdominal cavity leads for significant increase of the concentration of the histamine of the blood plasma. Resection of the 2/3 distal stomach causes a significant reduction in the production of the gastrin. Truncal vagotomy increases the risk of neoplazms of the peritoneal cavity in the rats.
Текст научной статьи Влияние антацидных операций на концентрацию гастрина в плазме крови и риск развития злокачественных новообразований толстой кишки
Цель: выявление связи антацидных операций и злокачественных новообразований органов пищеварительной системы.
Животные были разбиты на три серии:
серия 1 — изучение влияния подавления желудочной секреции на концентрацию гастрина в плазме крови (29 животных);
группа 1.1 (контрольная) — изучение влияния «ложной» операции на концентрацию гастрина в плазме крови (5 животных);
группа 1.2 — изучение влияния стволовой ваготомии на концентрацию гастрина в плазме крови (8 животных);
серия 2 — адаптация экспериментального способа индукции опухолевого роста для нужд исследования (21 животное);
серия 3 — изучение влияния антацидных операций на выраженность злокачественного роста, индуцированного химическим канцерогеном (23 животных);
группа 3.2 — изучение влияния стволовой ваготомии на выраженность злокачественного роста, инду- цированного внутрибрюшинным введением азоксиметана (12 животных).
Все вмешательства выполнялись под общей анестезией золетилом, доступ к органам верхнего этажа брюшной полости во всех случаях обеспечивался срединной лапаротомией.
Стволовая ваготомия выполнялась путем иссечения участков переднего и заднего стволов блуждающего нерва у пищеводно-желудочного перехода.
Животные контрольной группы были подвергнуты только лапаротомии.
Концентрация гастрина определялась перед выполнением оперативного вмешательства, через 3, 4, 8, 10 и 15 недель после выполнения вмешательства.
Концентрация гастрина в плазме крови определялась методом ИФА с использованием готового набора (USCN Life Science Corp., США) в соответствии с инструкцией производителя набора.
Индукция злокачественных новообразований толстой кишки у животных серии 2 осуществлялась подкожным введением раствора азоксиметана (Sigma-Aldrich Co., США) в дозе 12мг/кг, 8 мг/кг, 6 мг/кг и 4 мг/кг двукратно с интервалом 2 недели или в дозе 10 мг/кг внутрибрюшинно трехкратно. Животные выводились из эксперимента через 16 или 30 недель после первого введения. Наличие новообразований в толстой кишке оценивалось после вскрытия просвета толстой кишки в продольном направлении с использованием пятикратного оптического увеличения.
В серии 3 экспериментов индукция опухолевого роста осуществлялась внутрибрюшинным введением азоксиметана в дозе 10 мг/кг трехкратно. Подавляющее желудочную секрецию вмешательство выполнялось на 7-й день после последнего введения препарата. Животные выводились из эксперимента через 16 недель после первого введения препарата.
Значимость различий между группами оценивалась по χ2 с поправкой Йетса, критерию Вилкоксона для зависимых групп и по U-критерию Манна — Уитни для независимых. Результаты представлены в виде медианы (межквартильный интервал).
Результаты. Лапаротомия в контрольной группе не приводила к значимому изменению плазменной концентрации гастрина.
Исходная концентрация гастрина в плазме крови животных, подвергнутых стволовой ваготомии, составила 155 (127-198) пг/мл. Стволовая ваготомия приводила к значимому (р<0,05 по сравнению с исходным уровнем и по сравнению с контролем) повышению плазменной концентрации гастрина через 4 (до 241 (214-329) пг/мл) и 6 (до 226 (195-312) пг/ мл) недель после выполнении вмешательства, к 10-й неделе исследования концентрация гормона снижалась до 191 (163-254) пг/мл, на 15-й неделе после вмешательства составляя 201 (143-247) пг/мл, не отличалась значимо от предыдущего зарегистрированного значения (рис. 1).
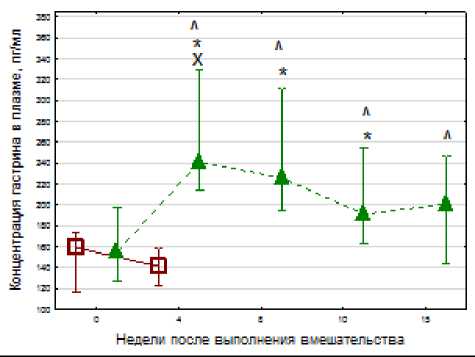
Рис. 1. Динамика концентрации гастрина в плазме крови у животных, подвергнутых стволовой ваготомии: □ — контроль; ▲ — стволовая ваготомия; маркер — медиана; I— межквартильный интервал; * — p< 0,05 по сравнению с предыдущим значением; ^ — p<0,05 по сравнению с исходным значением, критерий Вилкоксона; х — p<0,05 по сравнению с контролем, U-критерий Манна — Уитни
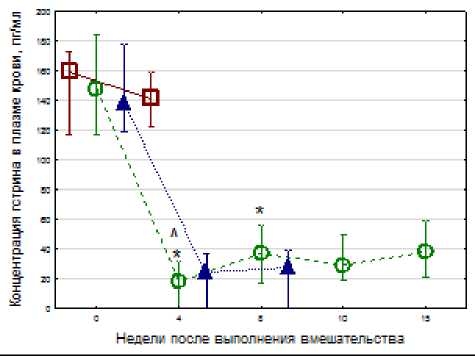
Стволовая ваготомия значимо повышала частоту развития новообразований толстого кишечника у животных, подвергнутых воздействию азоксиметана, по сравнению с группой животных, подвергнутых только введению канцерогена (таблица).
Не выявлено значимых различий в частоте развития новообразований между группами животных, подвергнутых введению азоксиметана и введению
Влияние антацидных операций на активность неопластического процесса, индуцированного химическими канцерогенами
Обсуждение. В исследовании установлено повышение плазменной концентрации гастрина в послеоперационном периоде стволовой ваготомии, выявлено некоторое снижение его концентрации после начального пика с дальнейшей стабилизацией.
Результаты настоящего исследования свидетельствуют о целесообразности проведения дальнейших исследований (когортных или случай — контроль), направленных на изучение влияния ваготомий на риск развития новообразований органов брюшной полости с целью определения целесообразности отнесения больных, перенесших подобные оперативные вмешательства, к соответствующей группе риска.
Результаты исследования позволяют пересмотреть существующее мнение о выполнении ваготомий как об относительно безопасных оперативных вмешательствах.
Выводы:
Список литературы Влияние антацидных операций на концентрацию гастрина в плазме крови и риск развития злокачественных новообразований толстой кишки
- Кузин H.M., Алимов A.H. Селективная проксимальная ваготомия с дуоденопластикой в лечении дуоденальных стенозов у больных язвенной болезнью двенадцатиперстной кишки. Хирургия 1997; (4): 38-43
- Гринберг А.А. Прободная язва. В кн.: Неотложная абдоминальная хирургия (справочное пособие для врачей). М.: Триада-Х, 2000; с. 227-247
- Graham DY, Genta RM. Long-term proton pump inhibitor use and gastrointestinal cancer. Curr Gastroenterol Rep 2008; 10 (6): 543-547
- Jensen RT. Involvement of cholecystokinin/gastrin-related peptides and their receptors in clinical gastrointestinal disorders. Pharmacol Toxicol 2002; 91 (6): 333-350
- Коротько Г.Ф. Желудочное пищеварение. Краснодар, 2007; 256 с.
- Waldum HL, SandvikAK, Brenna Е, Petersen Н. Review Gastrin-histamine sequence in the regulation of gastric acid secretion. Gut 1991; 32 (6): 698-701
- Johnson LR. Physiology of the gastrointestinal tract. : Academic press, 2006; 2004 p.
- Dockray G, Dimaline R, Varro A. Gastrin: old hormone, new functions. Pflugers Arch 2005; 449: 344-355
- Todisco A, Ramamoorthy S, Witham T, et al. Molecular mechanisms for the antiapoptotic action of gastrin. Am J Physiol Gastrointest Liver Physiol 2001; 280 (2): 298-307
- Noble PJ, Wilde G, White MR, et al. Stimulation of gastrin-CCKB receptor promotes migration of gastric AGS cells via multiple paracrine pathways. Am J Physiol Gastrointest Liver Physiol 2003; 284(1): 75-84
- Fourmy D, GigouxV, ReubiJC. Gastrin in gastrointestinal diseases. Gastroenterology 2011; 141 (3): 814-818.


