Влияние факторов риска на непосредственные результаты эндоваскулярной реваскуляризации в сочетании с катетеруправляемым селективным тромболизисом при остром тромбозе периферических артерий у пациентов в острой стадии коронавирусной инфекции COVID-19
Автор: Никольский А.В., Кравчук В.Н., Трофимов Н.А., Мухин А.С., Рыбинский А.Д., Волков Д.В., Петров Д.В., Шарабрин Е.Г., Гришин В.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Сердечно-сосудистая хирургия
Статья в выпуске: 4 (90), 2024 года.
Бесплатный доступ
Введение. Острая ишемия конечности - ургентное состояние, при котором необходима незамедлительная реваскуляризация. Риск осложнений зависит от возраста пациента, причины развития тромбоза артерий конечности, наличия сопутствующей патологии: ИБС, ХБП, дыхательной недостаточности, сахарного диабета, срочности и длительность оперативного лечения.Цель исследования оценка влияния представленных факторов риска на результаты эндоваскулярной реваскуляризации при остром тромбозе у пациентов в острой стадии COVID-19.Материалы и методы. Проанализированы результаты открытого хирургического лечения острой ишемии конечности II класса по Резерфорду у пациентов в острой стадии COVID-19 (71 пациент, I группа) и 50 пациентов без COVID-19 (группа II). Группы сопоставимы по демографическим и клиническим характеристикам.Результаты. Госпитальная летальность составила 36,6 % в I и 10 % во II группе. Большинство летальных исходов в I группе было обусловлено ранними ретромбозами. Факторы риска - ИБС, ХБП, СД и экстренный характер оперативного вмешательства имели большее негативное влияние в I группе на фоне коронавирусной инфекции.Заключение. У пациентов в острой стадии COVID-19 эндоваскулярная реваскуляризация ассоциирована с высоким риском осложнений и летальностью в раннем послеоперационном периоде в сравнении с оперированными пациентами без коронавирусной инфекции. Влияние всех выделенных факторов риска возрастает на фоне COVID-19, статистически значимое повышение отношения шансов развития послеоперационных осложнений выявлено для таких периоперационных факторов риска, как: ИБС, дыхательная недостаточность, сахарный диабет и хроническая болезнь почек, среди интраоперационных факторов значимыми являются экстренный характер операции и длительность оперативного вмешательства.
Covid-19, острая ишемия нижних конечностей, реваскуляризация, катетеруправляемый селективный тромболизис
Короткий адрес: https://sciup.org/142243829
IDR: 142243829 | УДК: 616.13 | DOI: 10.17238/2072-3180-2024-4-84-96
The influence of risk factors on immediate results of endovascular revascularization in combination with catheter-directed selectie thrombolysis in acute trombosis of peripheral arteries in patients with acute COVID-19 infection
Introduction. Acute limb ischemia is an urgent condition in which immediate revascularization is necessary. The risk of complications depends on the age of the patient, the cause of arterial thrombosis of the limb, and the presence of concomitant pathology: Coronary heart disease, CKD, respiratory failure, diabetes mellitus, urgency and duration of surgical treatment.The aim of the study was to assess the impact of the presented risk factors on the results of endovascular revascularization in acute thrombosis in patients in the acute stage of COVID-19.Materials and methods. The results of open surgical treatment of Rutherford class II acute limb ischemia in patients with acute stage COVID-19 (71 patients, group I) and 50 patients without COVID-19 (group II) were analyzed. The groups are comparable in demographic and clinical characteristics.Results. Hospital mortality was 36,6 % in group I and 10 % in group II. The majority of deaths in group I were due to early retrombosis. Risk factors - coronary heart disease, CKD, diabetes and the emergency nature of surgery had a greater negative impact in group I against the background of coronavirus infection.Conclusion. In patients in the acute stage of COVID-19, endovascular revascularization is associated with a high risk of complications and mortality in the early postoperative period compared with operated patients without coronavirus infection. The influence of all identified risk factors increases against the background of COVID-19, a statistically significant increase in the odds ratio of postoperative complications was revealed for such perioperative risk factors as coronary heart disease, respiratory failure, diabetes mellitus and chronic kidney disease, among the intraoperative factors, the emergency nature of the operation and the duration of surgery are significant.
Текст научной статьи Влияние факторов риска на непосредственные результаты эндоваскулярной реваскуляризации в сочетании с катетеруправляемым селективным тромболизисом при остром тромбозе периферических артерий у пациентов в острой стадии коронавирусной инфекции COVID-19
Острая ишемия конечности (ОИК) представляет собой критическое состояние, требующее незамедлительного восстановления кровотока. Это единственный способ сохранить конечность и, в некоторых случаях, спасти жизнь пациента.
Важно, чтобы диагностика и подготовка к хирургическому вмешательству занимали не более 2–2,5 часов [1, 4].
Исследования показали, что на риск осложнений после эндоваскулярной реваскуляризации в раннем послеоперационном периоде влияют следующие факторы: наличие ишемической болезни сердца, хронической болезни почек, дыхательной не- достаточности, сахарного диабета, срочность операции и ее продолжительность свыше 92 минуты [5, 8, 11].
Целью настоящего исследования было оценить влияние факторов риска на непосредственные результаты эндоваскулярной реваскуляризации в сочетании с катетеруправляемым селективным тромболизисом при остром тромбозе периферических артерий у пациентов в острой стадии коронавирусной инфекции СOVID-19.
Материалы и методы
С целью изучения результатов открытого хирургического лечения ОИК II степени по Резерфорду у пациентов в острой стадии COVID-19 проанализированы результаты лечения 71 пациента (I группа), которые были пролечены в период с 14.04.2020 г. по 20.06.2023 г. в клинике ГБУЗ НО «Городская клиническая больница № 5 Нижегородского района г. Нижнего Новгорода» перепрофилированной в специализированный хирургический Ковид-госпиталь, и на базе БУ «Республиканский кардиологический диспансер» г. Чебоксары, перепрофилированного в Ковид-госпиталь со специализированной сердечно-сосудистой хирургической помощью 01.01.2021 г. по 01.03.2022 г. Всем 71 пациенту группы исследования в качестве метода лечения ОИК была выбрана эндоваскулярная реваскуляризация в сочетании с селективным катетеруправляемым тромболизисом.
Контрольную группу составили 50 пациентов (II группа) с ОИК II степени по Резерфорду, оперированных эндоваскулярно (тем же методом) в период с 1.01.2018 г по 14.04.2020 г на тех же клинических базах.
Пациенты сравниваемых групп значимо не отличались по половому и возрастному составу. Возраст пациентов группы исследования составил 72 [66; 80] лет, в контрольной группе – 66 [59;72] лет. Число пациентов старше 75 лет составило 28 человек (23 %), большинство относилось к группе исследования – 15 человек (21 %). Распределение пациентов по полу 59,1 % мужчин в группе исследования и 66,0 % – в контрольной соответственно.
Больные обеих групп были сопоставимы по характеру основного заболевания: локализации острого тромбоза, характеру ОИК и классу ОИК (по Резерфорду). Локализация острого артериального тромбоза у пациентов обеих групп достоверно не отличалась, чаще всего вмешательства выполнялись по поводу поражения артерий нижних конечностей (табл. 1).
Степень проявления клинического течения основного заболевания – ОИК в обеих группах была сопоставима. Пациенты группы исследования чаще поступали в стационар уже со II B классом ОИК по Резерфорду.
Причиной развития острой ишемии конечностей в группе исследования являлись в большей степени тромбозы артерий поливалентной этиологии, тромбоэмболии и атеросклеротическое поражение артерий встречалось в меньшей степени (рис. 1).
При оценке коморбидного фона пациентов контрольной и исследуемой групп, были изучены: ИБС, наличие ДН, СД, ХБП, ФП.
Таблица 1
Распределение больных по локализации ОИК в группах
Table 1
Distribution of patients according to the localization of DEC in groups
|
Локализация тром-боза/Thrombosis localization |
IV группа/ group IV (исследование/ study) n=71 |
II группа/Group II (контроль/control) n=50 |
|
Ишемия нижних ко-нечностей/Ischemia of the lower extremities |
45 (63,3 %) |
41 (82 %) |
|
Подвздошно-бедренный сегмент/Ilio-femoral segment |
8 (11,2 %) |
5 (10 %) |
|
Бедренно-подколен-ный/Femoral-popliteal |
18 (25,3 %) |
16 (32 %) |
|
Берцовые артерии/ Tibial arteries |
19 (26,7 %) |
20 (40 %) |
|
Ишемия верхних конечностей/ Ischemia of the upper extremities |
26 (36,6 %) |
9 (18 %) |
|
Плечевая артерия/ Brachial artery |
14 (19,7 %) |
5 (10 %) |
|
Локтевая и лучевая артерии/Ulnar and radial arteries |
12 (16,9 %) |
4 (8 %) |
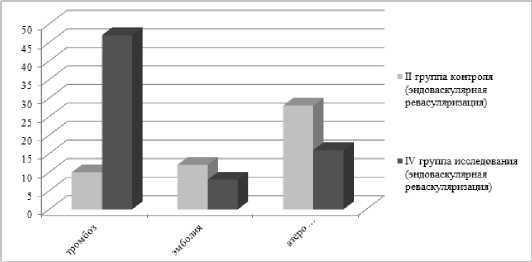
Рис. 1. Распределение больных в группах эндоваскулярной реваскуляризации по генезу развития ОИК
Fig. 1. Distribution of patients in endovascular revascularization groups according to the genesis of the development of DEC
Пациенты исследуемой группы имели ИБС в анамнезе в 52 %, в контрольной группе ИБС встречалась с частотой 68 % p<0,001). Фибрилляция предсердий была в анамнезе у 29 % пациентов группы исследования и у 30 % – пациентов контрольной группы p<0,01). Встречаемость СД в группах была сопоставима: 35 % и 42 % соответственно. В сравниваемых группах пациентов равномерно встречались больные с ХБП (табл. 2).
Таблица 2
Характеристика коморбидного фона пациентов групп эндоваскулярной реваскуляризации
Table 2
Characteristics of the comorbid background of patients with endovascular revascularization groups
|
Показатель/ Indicator |
IV группа/ group IV (исследование/ study) n=71 |
II группа/ Group II (контроль/ control) n=50 |
Уровень значимости/ Significance level, р |
|
ИБС/CHD |
52 % |
68 % |
< 0,326 |
|
СД/ SD |
35 % |
42 % |
< 0,562 |
|
ДН по различным причинам/ DN for various reasons |
66 % |
8 % |
< 0,002 |
|
ХБП/ CKD |
21 % |
18 % |
< 0,134 |
|
ФП / FP |
29 % |
30 % |
< 0,208 |
Достоверные различия были получены для частоты встречаемости в группах пациентов ДН различного генеза. У пациентов группы исследования чаще имела место дыхательная недостаточность на фоне острой стадии коронавирусной инфекции, что негативно влияло на течение основного заболевания (ОИК) в группе исследования. Тяжесть основного заболевания (ОИК) статистически не различалась в группах.
Нами были выделены основные периоперационные факторы риска развития осложнений в группе контроля, для этого пациенты контрольной группы были разделены на подгруппы (а) и (б) на основании наличия или отсутствия у них в раннем послеоперационном периоде осложнений, существенно повлиявших на исход лечения.
Осложнения раннего послеоперационного периода, которые учитывались для формирования подгрупп исследования:
– ретромбоз артерий оперированного сосудистого бассейна, c повторным вмешательством, либо без него,
– необратимый мышечный некроз и ампутация конечности,
– острая сердечная недостаточность,
– дыхательная недостаточность, потребовавшая облигатной кислородотерапии, вспомогательной или продленной ИВЛ,
– острая почечная недостаточность,
– геморрагические осложнения, потребовавшие выполнения гемортансфузии, геморрагические ОНМК,
– инфекционные осложнения.
Указанные осложнения развились у 16 пациентов (32 %) в II группе.
Среди пациентов с осложнениями в подгруппе (а) реже встречались больные с тромбозами периферических артерий верхних конечностей (табл. 1).
Распределение пациентов в подгруппах в зависимости от причины развития острой артериальной недостаточности не различалось (рис. 2).
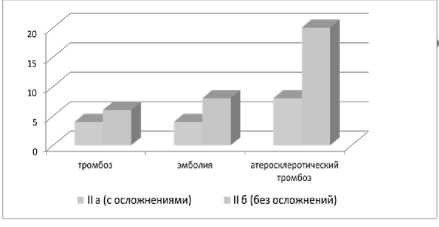
Рис. 2. Распределение больных по генезу развития ОИК во II группе
Fig. 2. Distribution of patients according to the genesis of the development of DEC in group II
В (а) подгруппе II группы закономерно чаще встречались пациенты с исходно более клинически значимым II B классом ОИК по Резерфорду.
Таблица 3
Характеристика предоперационного состояния пациентов II группы
Table 3
Characteristics of the preoperative condition of group II patients
|
Показатель/Indicator |
II а подгруппа/ II a subgroup (с осложнениями/ with complications) n=16 |
II б подгруппа/II b subgroup (без осложне-ний/without complications) n=34 |
|
Возраст, лет /Age, years (Me[Q25;Q75 ]) |
72 [69; 84] |
70 [67; 82] |
|
Женский пол / Female |
6 |
11 |
|
ИБС/ IBS |
75,0 % |
52,9 % |
|
СД/ SD |
50,0 % |
38,2 % |
|
ДН по различным причинам/ DN for various reasons |
12,5 % |
5,8 % |
|
ХБП /CKD |
43,7 % |
5,8 % |
|
ФП /FP |
25,0 % |
32,3 % |
Пациенты, у которых развились осложнения статистически значимо не отличались по возрастному признаку в подгруппах II группы. Половой состав пациентов не имел статистически значимого разделения в когортах пациентов с осложнениями и без (табл. 3).
Во IIа подгруппе большее число больных имело в анамнезе: ИБС, ДН и ХБП, остальная сопутствующая патология равномерно встречалась у пациентов обеих подгрупп II группы (рис. 3).
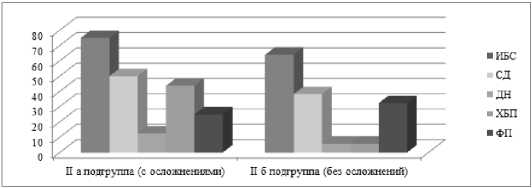
Рис. 3. Коморбидный фон пациентов II группы (эндоваскулярно)
Fig. 3. Comorbid background of group II patients (endovascular)
Перед нами стояла задача выделения наиболее значимых периоперационных и интраоперационных факторов риска развития осложнений, мы сочли возможным проведение анализа в указанных группах. При оценке структуры ранних послеоперационных осложнений обращает на себя внимание преобладание сердечно-сосудистых, которые составили 85 % от всех случаев.
Алгоритм медико-статистической обработки полученных результатов состоял из нескольких этапов. Первоначально была произведена оценка соответствия эмпирического закона распределения количественных переменных теоретическому закону нормального распределения по критерию Шапиро-Уилка. Во всех случаях было установлено его отсутствие. В связи с этим значимость различий средних значений количественных показателей изучалась с использованием U критерия Манна-Уитни.
В первую очередь было произведено сравнения анамнестических данных пациентов и анализ коморбидности в каждой группе.
Факт присутствия в анамнезе сопутствующего заболевания, класс ишемии конечности по Резерфорду, а также возраст пациента и этиология развития острой ишемии рассматривались в дальнейшем анализе в качестве качественных критериев [11].
Возраст оперированных пациентов был представлен в виде качественного критерия с применением шкалы возрастных групп расчета сердечно-сосудистых рисков SCORE2-OP.
Была произведена проверка гипотезы о происхождении групп, сформированных по качественному признаку, из одной и той же популяции, на основе построения таблиц сопряжённости наблюдаемых и ожидаемых частот с применением критерий Хи-квадрат Пирсона (табл. 4).
Из исследуемых качественных признаков во группе II статистическая значимость различий не была установлена для возрастной группы пациентов, этиологии тромбоза и ФП. Пациенты с ранними послеоперационными осложнениями в группе эндоваскулярной реваскуляризации чаще имели в анамнезе ХБП и инсулинпотребный СД. Класс ОИК II B по Резерфорду у этих больных, так же являлся предиктором неблагоприятным событий.
Таблица 4 Оценка связи качественных критериев с развитием ранних послеоперационных осложнений в группе II
Table 4
Assessment of the relationship of qualitative criteria with the development of early postoperative complications in group II
|
Качественные критерии (признаки)/ Qualitative criteria (signs) |
Статистические параметры/ Statistical parameters |
||
|
Критерий χ2 Пирсона/ Pearson ‘s criterion χ2 |
Число степеней свободы/ The number of degrees of freedom, df |
Уровень значимости/ Significance level, р |
|
|
Возраст (75 лет и старше)/ Age (75 years and older) |
0.012229 |
1 |
> 0,057 |
|
ИБС/ IBS |
4.1117 |
1 |
< 0,04 |
|
СД/ SD |
6.911644 |
1 |
< 0,008 |
|
ДН/ DN |
5,4237 |
1 |
< 0,043 |
|
ФП/ FP |
0,017507 |
1 |
> 0,051 |
|
ХБП/ CKD |
10,5701 |
1 |
< 0,001 |
|
Этиология тромбоза/ Etiology of thrombosis |
0,37 |
1 |
> 0,052 |
|
Степень ишемии/ Degree of ischemia |
4,902553 |
1 |
< 0,021 |
Таким образом, обозначенные признаки были выделены, как наиболее информативные для проведения дальнейшей оценки абсолютного риска развития периоперационных осложнений. Для этого был выполнен его расчёт для исследуемых показателей, а также расчет отношения шансов этого риска и 95%-ного доверительного интервала отношения шансов (табл. 5).
Так как во всех случаях 95 %-ный доверительный интервал отношения шансов не содержал 1, различия были признаны статистически значимыми (p < 0,05).
Для всестороннего анализа рисков эндоваскулярного лечения ОИК, необходимо проанализировать не только предоперационные факторы риска развития осложнений, но и выделить наиболее значимые интраоперационные факторы риска для эндоваскулярного метода реваскуляризации.
Анализ интраоперационных критериев развития осложнений во II группе, выявил следующие качественные и количественные признаки:
-
– время операции,
-
– геморрагические осложнения,
-
– экстренная операция.
Таблица 5
Оценка риска развития ранних осложнений в зависимости от различных периоперационных факторов эндоваскулярной реваскуляризации
Table 5
Assessment of the risk of early complications depending on various perioperative factors of endovascular revascularization
|
Предоперци-онные факторы риска/ Preoperative risk factors |
II а |
II б |
Отношение шансов |
95%-ный доверительный интервал отношения шансов |
||
|
абс. |
% |
абс. |
% |
|||
|
ИБС |
14 |
88% |
19 |
56% |
4,9 |
1,95–25,04 |
|
СД |
11 |
69% |
10 |
29% |
5,2 |
1,45–20,01 |
|
ДН |
4 |
25% |
1 |
3% |
11 |
1,11–112,27 |
|
ХБП |
7 |
44% |
2 |
6% |
12,4 |
2,19–73,84 |
|
Степень ишемии |
4 |
25% |
22 |
65% |
0,24 |
0,86–0,79 |
Для эндоваскулярных вмешательств в контрольной группе, качественным критерием являлось экстренное оперативное вмешательство. При оценке временных характеристик вмешательства установлены различия для общей продолжительности операции и объема кровопотери. Следующим этапом был произведен перевод количественных показателей с выявленной статистической значимостью различий в качественные. Для этого произведено построение кривых ошибок (ROC) исследуемых признаков (рис. 5–6).
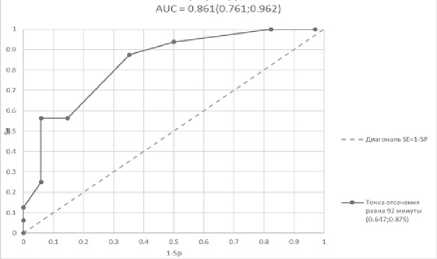
Рис. 5. Кривая ошибок (ROC) исследуемых признаков: время операции в группе II
Fig. 5. Error curve (ROC) of the studied features: operation time in group II
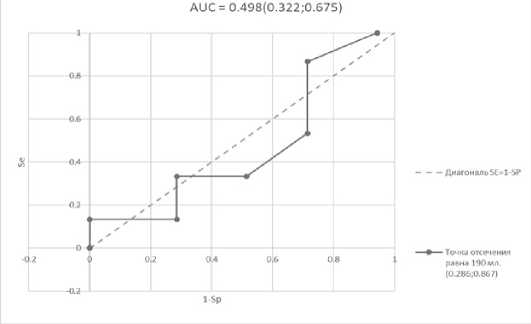
Рис. 6. Кривая ошибок (ROC) исследуемых признаков: кровопотеря в группе II
Fig. 6. Error curve (ROC) of the studied signs: blood loss in group II
Был произведен расчет площади под кривой ошибок для каждой групп, на основании которого была установлена неудовлетворительная характеристика периоперационной кровопотери в качестве прогностической модели развития осложнений (площадь под кривой ошибок менее 0,7). Таким образом, точка разделения была определена для длительности оперативного вмешательства (92 минуты).
Была произведена проверка гипотезы о происхождении групп, сформированных по качественному признаку, из одной и той же популяции, на основе построения таблиц сопряжённости наблюдаемых и ожидаемых частот с применением критерий Хи-квадрат Пирсона, гипотеза была подтверждена для качественных признаков: времени операции и экстренного характера вмешательства.
Выделенные признаки были признаны информативными для проведения дальнейшей оценки абсолютного риска развития осложнений. Для этого был выполнен его расчёт для исследуемых показателей, а также расчет отношения шансов этого риска и 95 %-ного доверительного интервала отношения шансов (табл. 6). Во всех случаях 95 %-ный доверительный интервал отношения шансов не содержал 1, различия были признаны статистически значимыми (p < 0,05).
На основании проведенного медико-статистического анализа, были определены наиболее перспективные направления минимизация рисков эндоваскулярной реваскуляризации у больных с ОИК. В первую очередь они заключаются в снижении травматичности вмешательства за счёт сокращения времени оперативного вмешательства. Лучшие результаты лечения удавалось достичь при плановых и отсроченных вмешательствах в тех ситуациях, когда степень ишемии конечности соответствовала классу II А по Резерфорду, что позволяло провести подготовку пациента к операции, включая инфузионную терапию с целью коррекции электролитных, метаболических и волемических показателей. Значение U-критерия Манна-Уитни позволяет сравнить параметры отношения шансов для каждого из исследуемых факторов риска в контрольной группе.
Таблица 6
Оценка связи качественных критериев с развитием ранних послеоперационных осложнений в группе II
Table 6
Assessment of the relationship of qualitative criteria with the development of early postoperative complications in group II
|
Качественные критерии (признаки)/ Qualitative criteria (signs) |
Статистические параметры /Statistical parameters |
||
|
Критерий χ2 Пирсона/ Pearson’s criterion χ2 |
Число степеней свободы/ Number of degrees of freedom, df |
Уровень значимости /Significance level, р |
|
|
время операции/ operation time |
20,206 |
1 |
< 0,000006 |
|
экстренная операция/ emergency operation |
2,834 |
1 |
< 0,009 |
Было установлено, что наиболее высокие шансы развития осложнений имеют больные, которым операция выполнялась в экстренном порядке по поводу острой ишемии конечности II B класса без предварительной инфузионной терапии и полного протокола дообследования пациента в связи с угрозой развития необратимых ишемических изменений конечности, также прогностической значимостью обладала продолжительность открытой операции более 92 минут (1,52).
Возраст пациента и этиология тромбоза при ОИК не являлись статистически значимыми факторами риска развития послеоперационных осложнений. Среди периоперационных факторов риска значимыми являлись: ИБС (4,9), ХБП (12,4), СД (5,28), ДН (11) и IIB степень ишемии по Резерфорду (0,2).
Статистическую обработку данных проводили с использованием программной среды «R». Количественные показатели представлены в виде медианых и межквартильного интервала (Ме [25 %; 75 %]), качественные — в виде абсолютных и относительных частот. Для сравнения групп применяли U-критерий Манна-Уитни и точный тест Фишера. Различия считали статистически значимыми при p<0,05.
Результаты
В ходе анализа данных 121 пациента с ОИК были получены следующие результаты. Группы пациентов с ОИК в острой стадии новой коронавирусной инфекции и без COVID-19 были сопоставимы по основным демографическим и клиническим характеристикам, за исключением более высокой частоты дыхательной недостаточности у пациентов с COVID-19 (66 % против 8 %, p<0,002). Медиана времени от начала симптомов ОИК до реваскуляризации составила 29 [6; 38] часов без значимых различий между группами (p=0,072).
Качественный и количественный состав интраоперационных факторов риска для обеих групп пациентов не различался, так как, технология выполнения эндоваскулярной реваскуляризации для каждой из групп была стандартной. Интраоперационные факторы риска для открытого метода реваскуляризации при ОИК выделены в исследования и представляют собой: время операции более 92 минут и экстренное вмешательство.
Течение интраоперационного этапа в группах I и II было сходным.
Значимые различия наблюдались в течении послеоперационного периода у пациентов сравниваемых групп (табл. 7).
Таблица 7 Течение раннего послеоперационного периода эндоваскулярной реваскуляризации
Table 7
The course of the early postoperative period of endovascular revascularization
|
Показатель/ Indicator |
I группа (исследования)/ group I (research) n=71 |
II группа (контрольная)/ Group II (control) n=50 |
Уровень значимости/ Significance level, р |
|
Ретромбоз оперированной арте-рии/Thrombosis of the operated artery |
28 (39,4 %) |
8 (16,0 %) |
< 0,018 |
|
Ампутация/ Amputation |
12 (16,9 %) |
6 (12,0 %) |
< 0,027 |
|
ОСН/ acute heart failure |
12 (16,9 %) |
6 (12,0 %) |
< 0,038 |
|
ДН/ respiratory failure |
33 (46,4 %) |
3 (6,0 %) |
< 0,004 |
|
ОПН/acute renal failure |
8 (11,2 %) |
3 (6,0 %) |
< 0,036 |
|
ОНМК/acute cerebrovascular accident |
1 (1,4 %) |
1 (2,0 %) |
< 0,061 |
|
Кровотечения/ Bleeding |
23 (32,3 %) |
7 (14,0 %) |
< 0,012 |
|
Осложненная пункция/ Complicated puncture |
2 (2,8 %) |
2 (4,0 %) |
< 0,054 |
Госпитальная летальность в I группе составила 36,6 % (26 пациентов), в то время как в группе контроля этот показатель был 10 % (5 пациентов). Большая часть летальных исходов в группе исследования была обусловлена развитием ранних ретромбозов оперированного сосудистого бассейна в течении первых суток после хирургического вмешательства, несмотря на проводимую антитромботическую терапию. Повторные оперативные вмешательства демонстрировали различную эффективность в группах: во II группе было выполнено 2 повторных операций, у обоих пациентов это позволило избежать ампутации конечности и выписать из стационара в удовлетворительном состоянии, в IV группе повторно были оперированы четверо пациентов, у всех них развился ретромбоз после повторной операции. Ретромбоз приводил к необратимым изменениям тканей, необходимости выполнения экстренной ампутации конечности. Для пациентов IV группы, находившихся в острой стадии коронавирусной инфекции, ампутация являлась операцией крайне высокого риска. Обширная хирургическая травма при ампутации, общая анестезия с высокой вероятностью перехода на ИВЛ, приводили к 91,6 %-ной госпитальной летальности среди ампутантов в раннем послеоперационном периоде в следствии прогрессирования полиорганной недостаточности.
Пациенты с осложнениями в раннем послеоперационном периоде встречались в 32,0 % (16 пациентов) в контрольной II группе и в 81,7 % (58 пациентов) в группе исследования (IV группа). Частота выполнения ампутаций в группах была сопоставима, несмотря на худшие результаты реваскуляризации в IV группе. Этот факт был обусловлен тяжелым состоянием пациентов группы исследования с развившимися ретромбозами оперированного сосудистого бассейна, 12 пациентов были признаны неоперабельными на момент решения вопроса об ампутации.
Число значимых сердечно-сосудистых осложнений в группах было сопоставимо. ОСН наблюдалась у 12 пациентов (16,9 %) группы IV, в то время как, в группе контроля развилась у 6 пациентов (12,0 %). В группе II, ОСН с развитием ОКС наблюдалась у четырех пациентов: двум больным было выполнено экстренное ЧКВ со стентированием коронарных артерии, летальный исход на фоне ОКС зафиксирован у двух пациентов на фоне реперфузионного синдрома в раннем периоде после реваскуляризации. Два пациента погибли после ампутации на фоне прогрессирующей ОСН.
В IV группе летальные исходы с развитием ОСН наблюдались у трех пациентов после ампутаций, и у одного пациента после повторной операций, одному пациенту с ОКС в послеоперационном периоде была выполнена ЧКВ со стентированием коронарных артерий, он также имели неблагоприятный исход на фоне раннего тромбоза стента и прогрессирования клиники ОСН. У пяти пациентов развитие ОСН происходило на фоне выраженной ДН и приводило к фатальному исходу в послеоперационном периоде. Два пациента с клиникой ОСН были пролечены консерватвино и имели благоприятный исходом заболевания.
ДН значительно чаще наблюдалась в раннем послеоперационном периоде у пациентов IV группы. ДН, потребовавшая различных режимов оксигенотерапии, была отмечена у трех пациентов группы контроля и у 33 пациентов группы исследования. Во II группе дыхательная недостаточность 2 степени развилась в раннем послеоперационном периоде у трех пациентов. В IV группе ДН манифестировала у 33 пациентов. Неблагоприятный исход заболевания наступил у 19 больных: восемь после ампутации конечности, двое после повторных операций по поводу ретромбоза артерий и у десяти больных с прогрессирующей ОИК III класса по Резерфорду.
ОПН манифестировала у трех пациентов контрольной группы, включая одного больного после ампутации конечности с фатальным исходом заболевания. В группе исследования ОПН встречалась у 8 пациентов, четверо из них были с летальным исходом заболевания: 2 пациента после ампутаций, 2 пациента после повторной реваскуляризации. У четырех выживших пациентов ОПН развивалась на фоне исходной ХБП и была скорректирована медикаментозно в раннем послеоперационном периоде.
Частота развития геморрагических осложнений была выше в группе исследования. Течение раннего послеоперационного периода семи пациентов контрольной группы осложнилось гематомами различной локализации: у пяти больных гематомы были межмышечного характера и располагались в области нижних конечностей на бедре или голени, они не потребовали гемотрансфузии, у двоих пациентов гематомы бедра потребовали гемотрансфузионной терапии.
В группе исследования межмышечные гематомы наблюдались у 20 пациентов с благоприятным исходом лечения, ни в одном из случаев не потребовалась гемотрансфузионная терапия. Неблагоприятный исход заболевания зафиксирован у трех пациентов, два из них имели спонтанные гематомы забрюшинного пространства, у обоих пациентов потребовалась трансфузия компонентов крови, оба пациента погибли в раннем послеоперационном периоде на фоне ОСН и прогрессирующей ДН соответственно, еще у одного погибшего пациента развилась гематома предплечья, не потребовавшая гемотрансфузии. У одного пациента после проведенного КТЛ был выявлен ОНМК геморрагического характера, с летальным исходом.
Поскольку качественный профиль периоперационных и интраоперационных факторов риска в группах пациентов не отличался, но наблюдались значительные различия в течении раннего послеоперационного периода, был проведен расчет абсолютного риска развития осложнений и расчет отношения шансов этого риска в группе исследования к 95 %-ному доверительному интервалу отношения шансов. Так как во всех случаях 95 %-ный доверительный интервал отношения шансов не содержал 1, различия были признаны статистически значимыми (p < 0,05).
Для проведения медико-статистического анализа предпе-рационных и интраоперационных факторов риска в I группе были сформированы подгруппы Iа и Iб на основании наличия или отсутствия у пациентов в раннем послеоперационном периоде осложнений, существенно повлиявших на исход лечения (табл. 8).
Таблица 8
Оценка риска развития ранних осложнений в зависимости от периоперационных факторов эндоваскулярной реваскуляризации
Table 8
Assessment of the risk of early complications depending on perioperative factors of endovascular revascularization
|
Предоперационные факторы риска/ Preoperative risk factors |
I а Подгруппа/ I a subgroup |
I б подгруппа/ I b subgroup |
Отношение шансов/ Odds ratio |
95 %-ный доверительный интервал отношения шан-сов/95% confidence interval odds ratio |
||
|
абс. |
% |
абс. |
% |
|||
|
ИБС/CHD |
33 |
57 % |
5 |
38 % |
8,2 |
1,42–36,24 |
|
СД/ SD |
23 |
40 % |
2 |
15 % |
14,4 |
1,20–24,11 |
|
ДН/ DN |
43 |
77 % |
4 |
30 % |
14.7 |
2,26– 105,31 |
|
ХБП/ CKD |
14 |
24 % |
1 |
7 % |
17 |
2,67–90,18 |
|
Степень ишемии/ Degree of ischemia |
46 |
79 % |
6 |
46 % |
0,18 |
0,26–0,79 |
|
Интраоперационные факторы риска / Intraoperative risk factors |
||||||
|
Время операции более 92 минут/ The operation time is more than 92 minutes |
28 |
48 % |
4 |
30 % |
1,7 |
2,23–12,62 |
|
Экстренная операция/ Emergency surgery |
48 |
83 % |
7 |
53 % |
11,1 |
2,88–31,75 |
Влияние известных периоперационных факторов риска было различным в группах сравнения, несмотря на сопоставимый коморбидный фон пациентов и степень тяжести ОИК (табл. 9).
Таблица 9
Сравнительная оценка значимости факторов риска развития ранних осложнений эндоваскулярной реваскуляризации в группах пациентов с новой коронавирусной инфекцией
COVID-19 (группа I) и без нее (группа II)
Table 9
Comparative assessment of the significance of risk factors for the development of early complications of endovascular revascularization in groups of patients with new coronavirus infection COVID-19 (group I) and without it (group II)
|
Предоперационные факторы риска/ Preoperative risk factors |
Отношение шансов II группа/ Odds ratio Group II |
Отношение шансов I группа/ Odds ratio Group I |
|
ИБС/CHD |
4,9 |
8,2 |
|
СД/ SD |
5,2 |
14,4 |
|
ДН/ DN |
11 |
14,7 |
|
ХБП/ CKD |
12,4 |
17 |
|
Степень ишемии/ Degree of ischemia |
0,2 |
0,1 |
|
Интраоперационные факторы риска/ Intraoperative risk factors |
||
|
Время операции более 92 минут/ The operation time is more than 92 minutes |
1,5 |
1,7 |
|
Экстренная операция/ Emergency surgery |
9,1 |
11,1 |
Пациенты с ОИК в острой стадии коронавирусной инфекции имели худший прогноз и тяжелее переносили открытую реваскуляризацию в сравнении с оперированными больными без COVID-19.
Обсуждение
Представленное исследование демонстрирует значительное влияние COVID-19 на исходы эндоваскулярной реваскуляризации при острой ишемии конечностей (ОИК). Госпитальная летальность в группе пациентов с COVID-19 составила 36,6 % по сравнению с 10 % в контрольной группе, что указывает на серьезное ухудшение прогноза при сочетании ОИК и коронавирусной инфекции. Этот результат согласуется с данными других исследований, показывающих повышенный риск тромботических осложнений и смертности у пациентов с COVID-19 (Zhou et al., 2020).
Анализ факторов риска выявил усиление их негативного влияния в группе COVID-19. Отношение шансов для ишемической болезни сердца (ИБС) увеличилось с 4,9 в контрольной группе до 8,2 в группе COVID-19, для сахарного диабета — с 5,2 до 14,4, для дыхательной недостаточности – с 11 до 14,7. Это указывает на синергический эффект COVID-19 и сопутствующих заболеваний, что соответствует наблюдениям Richardson et al. (2020) о повышенной уязвимости пациентов с сопутствующими патологиями. Особого внимания заслуживает высокая частота ретромбозов в группе COVID-19 (39,4 % против 16,0 % в контроле). Это может быть связано с прокоагулянтным состоянием, индуцированным SARS-CoV-2, что подтверждается исследованиями Nishiga et al., 2020. Высокая частота ретромбозов, несмотря на проводимую антитромботическую терапию, указывает на необходимость пересмотра стандартных протоколов антикоагуляции для пациентов с COVID-19. Острая сердечная недостаточность (ОСН) наблюдалась у 16,9 % пациентов в группе COVID-19 по сравнению с 12,0 % в контрольной группе. Это согласуется с данными о прямом кардиотоксическом действии SARS-CoV-2 и системном воспалительном ответе, приводящем к повреждению миокарда (Grasselli et al., 2020). Развитие ОСН в послеоперационном периоде существенно ухудшало прогноз, что подчеркивает важность тщательного мониторинга сердечной функции у пациентов с COVID-19. Дыхательная недостаточность (ДН) была значительно более распространена в группе COVID-19 (46,4 % против 6,0 % в контроле). Это ожидаемо, учитывая первичное поражение легких при COVID-19, высокая частота ДН после сосудистых вмешательств указывает на потенциальное усугубление легочной дисфункции в результате операционного стресса и возможных микроэмболий.
Острая почечная недостаточность (ОПН) также чаще развивалась в группе COVID-19 (11,2 % против 6,0 %). Это может быть связано как с прямым повреждающим действием вируса на почки, так и с системными эффектами тяжелой инфекции, включая гипоперфузию и цитокиновый шторм (Petrikov et al., 2020).
Частота геморрагических осложнений была выше в группе пациентов с острой инфекцией COVID-19 32,3 % относительно 14,0 %. Полученные данные согласуются материалами Nishiga et al., 2020, описывающими прокоагулянтное состояние на фоне острой стадии COVID-19, ассоцииованное с повышенным риском спонтанных кровотечений. Анализ интраоперационных факторов риска показал, что экстренный характер операции имел еще большее значение в группе COVID-19 (ОШ 11,1 против 9,1 в контроле). Это подчеркивает важность своевременной диагностики и лечения ОИК у пациентов с COVID-19, а также необходимость оптимизации предоперационной подготовки в условиях ограниченного времени. Продолжительность операции более 92 минут также была ассоциирована с худшими исходами, хотя разница между группами была менее выражена (ОШ 1,7 в группе COVID-19 против 1,5 в контроле). Это указывает на важность минимизации времени операции и, воз- можно, пересмотра тактики в пользу быстрых, хотя, возможно, менее радикальных вмешательств у пациентов с COVID-19. Особого внимания заслуживает высокая летальность после ампутаций у пациентов с COVID-19 (90,0 %). Это ставит под сомнение целесообразность выполнения высоких ампутаций у этой категории больных и требует поиска альтернативных стратегий лечения критической ишемии.
Полученные данные свидетельствуют о необходимости индивидуализированного подхода к лечению ОИК у пациентов с COVID-19. Учитывая высокий риск ретромбозов, может быть оправдано более агрессивное применение антикоагулянтов в послеоперационном периоде, однако это требует тщательного баланса с риском кровотечений. Osborne et al. (2021) в своем исследовании показали потенциальную пользу раннего назначения аспирина у пациентов с COVID-19, что может быть актуально и для пациентов после сосудистых вмешательств.
Учитывая высокую частоту сердечно-сосудистых осложнений, целесообразно рассмотреть возможность более интенсивного кардиологического мониторинга и поддержки в периопераци-онном периоде. Это может включать расширенное использование эхокардиографии, биомаркеров повреждения миокарда и, возможно, превентивное применение кардиопротективных средств.
Ограничения исследования включают относительно небольшой размер выборки, тем не менее, полученные результаты предоставляют важную информацию для клинической практики и указывают направления для дальнейших исследований.
Заключение
Значимость всех предоперационных факторов риска: ИБС, ХБП, СД и ДН, возрастала для пациентов группы исследования, особенно статистически значимый прирост отношения шансов неблагоприятного прогноза наблюдался для СД и ДН в группе пациентов с коронавирусной инфекцией. Среди интраоперационных факторов у пациентов с ОИК в острой стадии коронавирусной инфекции усиливалось негативное влияние экстренного характера оперативного вмешательства. Таким образом, осложненное течение послеоперационного периода эндоваскулярной реваскуляризации и неблагоприятный исход лечения чаще наблюдался в исследуемой группе пациентов вследствие усиления влияния всех известных периоперационных факторов риска в острой стадии коронавирусной инфекцией.
Список литературы Влияние факторов риска на непосредственные результаты эндоваскулярной реваскуляризации в сочетании с катетеруправляемым селективным тромболизисом при остром тромбозе периферических артерий у пациентов в острой стадии коронавирусной инфекции COVID-19
- Bozzani A., Arici V., Tavazzi G. et al. Acute Thrombosis of Lower Limbs Arteries in the Acute Phase and After Recovery From COVID19. Ann Surg., 2021, № 273(4), рр. e159-e160. DOI: 10.1097/SLA.0000000000004700
- Никольский А.В., Волков Д.В., Федоровцев В.А., Косоногов А.Я., Трофимов Н.А., Косоногов К.А., Пенкнович А.А., Десятникова И.Б., Гаркавцев А.В., Рыбинский А.Д., Ярыгин В.В., Гусев С.В., Трухин К.В. Лечение острых артериальных тромбозов у пациентов с тяжелым течением новой коронавирусной инфекции. Кардиология и сердечно-сосудистая хирургия, 2022. № 15(1). С. 13-18. EDN: BHULNS
- Семьин И.С., Иваненко А.Н., Жарова А.С., Пятков В.А., Бахтин И.Л., Соболев Г.А., Киселев А.Д., Коротких А.В., Казанцев А.Н., Черных К.П. Эндоваскулярная стентовая тромбэктомия у пациентов с оcтрым тромбозом артерий нижних конечностей на фоне COVID-19. Журнал им. Н.В. Склифосовского "Неотложная медицинская помощь", 2023. № 12(1). С. 161-169. EDN: VPIBMC
- Ilonzo N., Judelson D., Al-Jundi W. et al. A review of acute limb ischemia in COVID-positive patients. Semin Vasc Surg., 2021, № 34(2), рр. 8-12. DOI: 10.1053/j.semvascsurg.2021.04.004 EDN: IQMPBF
- Madani M.H., Leung A.N.C., Becker H.C. et al. Aorto-iliac/right leg arterial thrombosis necessitating limb amputation, pulmonary arterial, intracardiac, and ilio-caval venous thrombosis in a 40-year-old with COVID-19. Clin Imaging., 2021, № 75, рр. 1-4. https://doi.org/101016/j.clinimag.2020.12.036. EDN: BULFDZ
- Makhoul K., Shukha Y., Hanna L.A. et al. A case of rapidly progressive upper limb ischemic necrosis in a patient with COVID-19. Int J Infect Dis., 2021, № 106, рр. 401-404. https://doi.org/101016/j.ijid.2021.04.023. EDN: AILQER
- Nishiga M., Wang D. W., Han Y. et al. COVID-19 and cardiovascular disease: from basic mechanisms to clinical perspectives. Nat. Rev. Cardiol., 2020, № 17(9), рр. 543-558. DOI: 10.1038/s41569-020-0413-9 EDN: XOIMJL
- Osborne T. F., Veigulis Z. P., Arreola D. M. et al. Association of mortality and aspirin prescription for COVID-19 patients at the Veterans Health Administration. PLoS One, 2021, vol. 11, № 16(2), рр. E0246825. DOI: 10.1371/journal.pone.0246825 EDN: FHWUNU
- Richardson S., Hirsch J.S., Narasimhan M. et al. Fresenting characteristics, comorbidities, and outcomes among 5700 patients hospitalized with COVID-19 in the New York City area. JAMA, 2020, № 323(20), рр. 2052-2059. DOI: 10.1001/ja-ma.2020.6775 EDN: UVTKVZ
- Шульдяков А.А., Смагина А.Н., Рамазанова К.Х., Ляпина Е.П., Чаббаров Ю.Р., Шешина Н.А., Жук А.А. Патогенетические подходы к коррекции сосудистого звена гомеостаза при COVID-19: обзор. Терапевтический архив, 2023. № 95(11). С. 1004-1008. EDN: PFJFBC


