Влияние гексанового экстракта Serenoa repens на функцию мочевого пузыря при частичной инфравезикальной обструкции
Автор: Сивков Андрей Владимирович, Кирпатовский В.И., Ефремов Г.Д., Голованов С.А., Дрожжева В.В.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Экспериментальная урология
Статья в выпуске: 1 т.16, 2023 года.
Бесплатный доступ
Введение. Традиционно считают, что «мишенью» гексанового экстракта Serenoa repens (HESR) является собственно предстательная железа. Однако, в литературе встречаются данные о том, что терапевтическое действие HESR может осуществляться и на уровне мочевого пузыря. Нами была высказана гипотеза о прямом действии HESR на обструктивный мочевой пузырь, препятствующем развитию его дисфункции. Материал и методы исследования. Исследование проведено на 30 белых беспородных крысах - самках. Инфравезикальную обструкцию (ИВО) моделировали путем наложения лигатуры на предпузырный отдел уретры, в которую предварительно вводили катетер 18G. После удаления катетера формировалось выраженное сужение уретры, затрудняющее отток мочи. Животные были разделены на группы: опытную (n = 10); sham/плацебо (n = 15) и контрольную (n = 5). Со следующего после операции дня, крысам опытной серии ежедневно внутрижелудочно через зонд вводили HESR в виде водно-спиртовой суспензии (27,6 мг/кг), а sham группе - тот же объем 3,5% спиртового раствора. Через 2 недели оценили выживаемость животных, функциональное состояние мочевого пузыря, суточный диурез, биохимические изменения крови и мочи, характеризующие функциональное состояние почек. Функцию мочевого пузыря оценивали по данным инфузионной цистометрии. После обследования животных усыпляли и удаляли мочевой пузырь для определения его массы и гистологического исследования. Результаты исследования. В течение 2 недель после моделирования ИВО в sham группе из-за почечной недостаточности умерло 10 (67%) животных, тогда как в опытной группе - 3 (30%). При обследовании выживших крыс в основной и sham группах выявили резкое переполнение мочевого пузыря. Объем мочевого пузыря оказался большим в опытной группе по сравнению с sham группой (р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Гексановый экстракт, hesr, мочевой пузырь, обструкция, уретра, пермиксон
Короткий адрес: https://sciup.org/142238171
IDR: 142238171 | DOI: 10.29188/2222-8543-2023-16-1-18-28
The effect of the hexanic lipidosterolic extract of Serenoa repens on the bladder function in partial bladder outlet obstruction
Introduction. It is believed that the «target» of the hexane extract of Serenoa repens (HESR) is the prostate gland itself. However, there is evidence in the literature that the therapeutic effect of HESR can be carried out at the level of the bladder. We hypothesized about the direct effect of HESR on the obstructive bladder, preventing the development of its dysfunction. Material and methods. The study was conducted on 30 white mongrel female rats. Bladder outlet obstruction (BOO) was modeled by applying a ligature to the urethra on 18G catheter. The animals were divided into groups: experimental - HESR (n = 10); sham/placebo (n = 15) and control (n = 5). From the day following the operation, rats of the experimental series daily received aqueous alcohol suspension of HESR (27.6 mg/kg) intragastrically through a probe, and the sham group received the same volume of 3.5% alcohol solution. After 2 weeks, the survival rate of the animals, the functional state of the bladder, daily diuresis, biochemical changes in blood and urine characterizing the functional state of the kidneys were evaluated. Bladder function was assessed according to infusion cystometry. After examination, the animals were euthanized and the bladders was removed to determine its mass and histological examination. Results. Within 2 weeks in the sham group 10 (67%) rats died due to renal failure, while in the HESR group - only 3 (30%). An obvious overfilling of the bladder in the main and sham groups was revealed. Bladder volume was larger in the HESR group compared to the sham (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Влияние гексанового экстракта Serenoa repens на функцию мочевого пузыря при частичной инфравезикальной обструкции
Традиционно считают, что «мишенью» гексанового экстракта Serenoa repens (HESR – hexanic extract of Serenoa repens), широко используемого для лечения расстройств мочеиспускания у мужчин с доброкачественной гиперплазией предстательной железы (ДГПЖ) в сочетании с хроническим простатитом, является собственно предстательная железа. Взаимодействие между клетками предстательной железы и HESR реализуется на нескольких уровнях и проявляется ан-тиандрогенным, противовоспалительным и проапоп-тотическим эффектами [1]. Однако в литературе встречаются данные, свидетельствующие, что терапевтическое действие экстракта Serenoa Repens может также осуществляться на уровне мочевого пузыря, но сведения по этому вопросу крайне ограничены [2, 3]. С учетом этого нами была высказана гипотеза о возможности прямого действия HESR (Пермиксон) на об- структивный мочевой пузырь, препятствующего развитию его дисфункции, не опосредованного, но дополняющего влияние препарата на предстательную железу [4]. Для подтверждения этой гипотезы и было предпринято данное исследование.
МАТЕРИАЛ И МЕТОДЫ
Исследование проведено на 30 белых беспородных крысах – самках годовалого возраста массой 330-370 г. Специально были отобраны самки достаточно «пожилого» возраста c соответствующими возрастными изменениями мочевого пузыря, не связанными с предстательной железой. Животные были разделены на группы: опытную (n = 10); sham/плацебо (n = 15) и контрольную/интактные крысы (n = 5).
Инфравезикальную обструкцию (ИВО) моделировали у животных основной и sham групп путем наложения лигатуры на предпузырный отдел уретры, которую предварительно катетеризировали кубиталь ным катетером 18G (диаметр – 1,25 мм), как описано в публикациях [5, 6]. После удаления катетера формиро валось выраженное сужение уретры, затрудняющее отток мочи.
Со следующего после операции дня крысы опыт ной серии ежедневно получали HESR (Пермиксон Pierre Fabre Medicament, Франция) в виде водно-спир товой суспензии в дозе 27,6 мг/кг, которую вводили внутрижелудочно через зонд. Дозу рассчитали, исходя из терапевтической дозы препарата, рекомендованной для человека (320 мг в сутки или 5 мг/кг), с учетом меж видового переноса дозы на основе коэффициента раз личий в площади поверхности тела для мелких лабора торных животных, что составило 30 мг/кг [7]. Непо средственно перед введением животным содержимое капсулы фармакопейного препарата (160 мг препарата) растворяем в 1,6 мл 70% этилового спирта с получе нием маточного раствора с концентрацией 100 мг/мл. В последующем его смешивали с дистиллированной водой в соотношении 1:20. Итоговая концентрация Пермиксона – 5 мг/мл, а спирта – 3,5%. Объем полу ченной суспензии, необходимый для введения, опреде ляли исходя из массы каждой крысы (варьировал в пределах 1,5-1,8 мл). Крысам sham группы ежедневно внутрижелудочно вводили аналогичный объем 3,5% спиртового раствора.
Через 2 недели животных обследовали с определе нием их выживаемости, функционального состояния мочевого пузыря и биохимических изменений крови и мочи, характеризующих функциональное состояние почек. Животных содержали в обменных клетках для определения суточного диуреза, сбора суточной мочи и получения проб для последующего биохимического анализа. Животные всех групп получали стандартный гранулированный корм, рекомендованный для содер жания грызунов.
Функцию мочевого пузыря оценивали по данным инфузионной цистометрии. Мочевой пузырь катетери зировали в области верхушки кубитальным катетером 20G, подсоединенным к инфузионной системе для по степенного его наполнения, и через уретру – катетером 18G для регистрации динамики внутрипузырного дав ления, которую осуществляли на аппаратно-программ ной комплексе («Биола», Россия), с обработкой полу ченных данных компьютерной программой А5 170424 [8]. Рассчитывали следующие показатели: максималь ный объем наполнения мочевого пузыря до начала мо чеиспускания, максимальное внутрипузырное давле ние в начале мочеиспускания, зависимость «объем/дав ление» в течение всего процесса цистометрии,ампли туду спонтанных колебаний внутрипузырного давления в процессе цистометрии.
После завершения функциональных исследований брали пробы крови из нижней полой вены для после дующих биохимических исследований, животных усыпляли и удаляли мочевой пузырь для определения его массы взвешиванием и для гистологического исследования.
Биохимическое исследование проб крови и мочи выполняли на анализаторе «ADVIA-2000 (Siemens) с определением следующих показателей: концентрации мочевины, креатинина, калия, натрия, белка, активность ферментов аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), лактатдегидрогеназы (ЛДГ), щелочной фосфатазы (ЩФ), креатинфосфокиназы (КФК). Из этих данных рассчитывали величину скорости клубочковой фильтрации, канальцевой реабсорбции натрия, суточную экскрецию с мочой метаболитов и ферментов.
Для проведения патоморфологического исследования готовили гистологические срезы по стандартной методике с их окраской гематоксилином и эозином. Для определения морфометрических параметров изображения отцифровывали и загружали в компьютерную программу «HistoScan» (фирма Biovitrum, Россия, Санкт-Петербург). Определяли толщину стенки мочевого пузыря, его отдельных слоев и мышечных пучков, а также площадь очагов склероза мышечной оболочки и выраженность воспалительной реакции по степени распространенности воспалительных инфильтратов. Измерения проводили не менее чем в 10 точках в разных участках препарата (рис. 1).
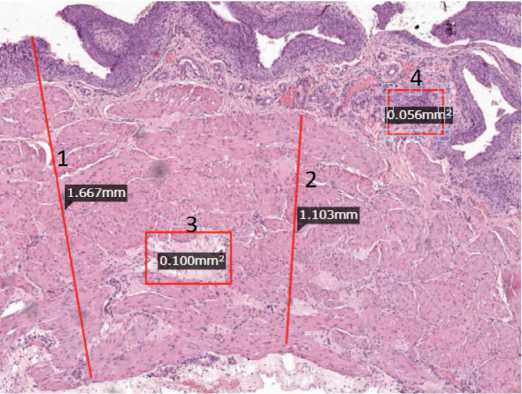
Рис. 1. Пример измерения морфометрических параметров на гистологическом срезе. 1 – общая толщина стенки; 2 – толщина мышечного слоя; 3 – площадь участка склероза; 4 – площадь очага воспалительной инфильтрации Fig. 1. An example of measuring morphometric parameters on a histological section. 1 – total wall thickness; 2 – thickness of the muscle layer; 3 – area of sclerosis; 4 – area of the focus of inflammatory infiltration
Статистическую обработку проводили с исполь зованием программ Excel-2013 и Statistica 6.0 для рас чета средних значений и ошибки средней (М±m) и достоверности различий между группами по критерию Стьюдента для количественных показателей или по критерию χ2 для сравнения качественных параметров. Достоверными считали различия при p <0,05.

РЕЗУЛЬТАТЫ
В течение 2 недель после моделирования ИВО в sham группе умерло 10 из 15 крыс (на 3-и сутки – 6 крыс и на 8-е и 11-е сутки – по 2 крысы), летальность – 67%, тогда как в опытной группе за это время умерло 3 крысы (на 3-и, 5-е и 7-е сутки), летальность – 30%. Причиной гибели животных предположительно явилось развитие почечной недостаточности,так как у этих крыс отмечался резко сниженный диурез (табл. 1), а при аутопсии выявляли гидронефротическую трансформацию почек. Хотя летальность оказалась существенно выше в sham группе, статистический анализ с использованием критерия χ2 выявил лишь пограничные со статистической достоверностью значения (р=0,070), что связано с небольшим числом наблюдений в группах.
При обследовании выживших крыс через 2 недели после моделирования ИВО в основной и sham группах выявили резкое переполнение и перерастяжение мочевого пузыря, тогда как в норме он, как правило, выглядел спавшимся (рис. 2).
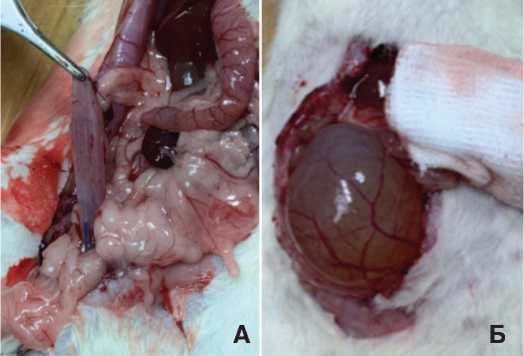
Рис. 2. Внешний вид мочевого пузыря крысы в норме (А) и через 2 недели после моделирования инфравезикальной обструкции (Б)
Fig. 2. The appearance of the bladder of a rat in the norm (A) and 2 weeks after the modeling of infravesical obstruction (B)
При этом объем мочи, определенный в обструктивном мочевом пузыре сразу после вскрытия брюшной полости и катетеризации мочевого пузыря, оказался большим в опытной группе по сравнению с sham группой. Если в sham группе он колебался в диапазоне от 3 до 4,8 мл (в среднем 4,0 ± 0,3 мл), то у крыс опытной серии он варьировал от 3 до 15 мл (в среднем, 8,3±1,6 мл). Различия оказались статистически достоверными ( р <0,05). У интактных крыс емкость мочевого пузыря составляла 0,6-0,8 мл (в среднем 0,7±0,02 мл).
Несмотря на более значительное растяжение мочевого пузыря у крыс, получавших HESR, он сохранял высокую способность эвакуации мочи, о чем свидетельствовали данные суточного диуреза, которые у выживших животных опытной группы составили 10,4±2,6 мл/сутки (от 4 до 25 мл), а в sham группе – всего 7,4±2,1 мл/сутки (от 0,4 до 14 мл). У интактных животных суточный диурез составляет 13,3±1,6 мл/сутки (от 8,5 до 18 мл). При этом в опытной группе лишь у одной из выживших крыс (15%) суточный диурез был ниже минимальных значений, характерных для интактных животных, тогда как в sham группе – у 4 из 5 крыс (80%) диурез был значительно ниже минимального нормального значения, что также свидетельствует о лучшем функциональном состоянии почек крыс основной группы. При статистическом анализе с использованием критерия Стьюдента различия между опытной и sham группами не достигли достоверной значимости (р=0,11), но степень уменьшения диуреза в sham группе по сравнению с интактными животными оказалось статистически значимой (р=0,045), тогда как значения диуреза при терапии HESR и у контрольных животных статистически значимо не различались.Анализ с использованием критерия χ2 выявил статистически значимые различия между числом животных со снижением диуреза ниже минимального значения в норме в опытной и sham группах (р=0,025).
Цистометрия наполнения
Функциональное состояние мочевого пузыря оценивали методом цистометрии наполнения. Такие показатели цистометрии как максимальная функциональная емкость мочевого пузыря и внутрипузырное давление при начале мочеиспускания в опытной и sham группах существенно не различались и составили: 4,9 ± 0,4 мл и 4,4 ± 0,3 мл и 50,2±4,1 и 49,9±5,6 см H 2 O, соответственно. В группе контроля эти параметры, в среднем, составили 0,7±0,02 мл и 28,7±1,4 см H 2 O. Отсутствие различий в значениях внутрипузырного давления при начале мочеиспускания в опытной и sham группах мы связываем с тем, что в эксперименте ИВО была создана суживающей уретру лигатурой и проводимая терапия не могла повлиять на сопротивление уретры, а, следовательно, на то, при каком давлении уретральное сопротивление будет преодолено и начнется мочеиспус-кание.В отношении максимальной функциональной емкости мочевого пузыря следует отметить, что в sham серии этот показатель оказался практически таким же, как и при измерении внутрипузырного объема мочи при первичной катетеризации мочевого пузыря, тогда как в опытной группе значения, полученные при цисто-метрии наполнения, оказались существенно ниже. На наш взгляд эти различия могут свидетельствовать о влиянии терапии HESR на способность обструктивного мочевого пузыря восстанавливать тонус детрузора после его деблокирования и нормализации внутрипу-зырного давления.
При более детальном анализе результатов инфузионной цистометрии выявили существенные различия между группами. В sham группе повышение внутри-пузырного давления возникало практически сразу экспериментальная и клиническая урология № 1 2023 после начала введения физраствора, а его рост сопро вождался иррегулярными колебаниями (рис. 3А), тогда как в основной группе наблюдали более плавный рост давления,без колебаний и с его существенным подъемом при введении более значительного объема физраствора (рис. 3Б).
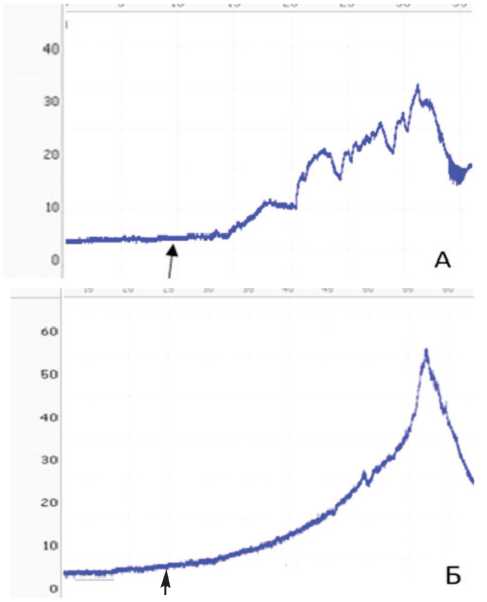
Рис. 3. Результаты цистометрии наполнения. А – Типичный пример динамики внутрипузырного давления при постепенном инфузионном наполнении мочевого пузыря у крысы sham серии. Б – Типичный пример динамики внутрипу-зырного давления при постепенном инфузионном наполнении мочевого пузыря крысы основной группы
Fig. 3. Filling cystometry results. A – A typical example of the dynamics of intravesical pressure during gradual infusion filling of the bladder in a sham series rat. B – A typical example of the dynamics of intravesical pressure during gradual infusion filling of the bladder of the rats of the main group
Динамическое определение зависимости «объем/ давление» выявило более плавный рост этого показа теля в основной группе при введении первых 3 мл физ раствора с последующим ускорением его роста и достижением более высоких значений (рис. 4). Такая
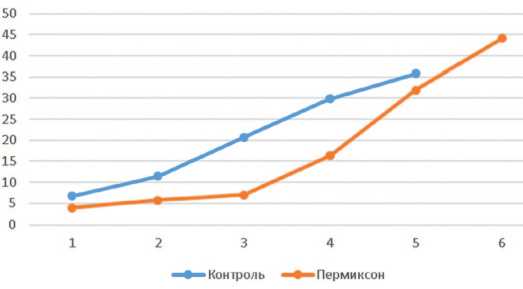
Рис. 4. Сравнительная динамика индекса «объем/давление» в изучаемых группах (ось абсцисс – давление в см H 2 O, ось ординат – объем введенного физраствора в мл)
Fig. 4. Comparative dynamics of the «volume/pressure» index in the studied groups (abscissa axis – pressure in cm H 2 O, ordinate axis – volume of injected saline solution in ml)
динамика близка к изменению этого индекса у крыс с нормальным мочевым пузырем и, по нашему мнению, свидетельствует о лучшем сохранении эластичности (комплаентности) стенки гипертрофированного мочевого пузыря при терапии HESR. Это предположение согласуется с данными о возможности накопления большего объема мочи у крыс, получавших HESR. Более «жесткая» стенка мочевого пузыря ведет к более быстрому достижению критического уровня внутри-пузырного давления, превышающего возможности сфинктера по удержанию мочи (рис. 4).
Как было указано выше, в sham серии при наполнении мочевого пузыря на фоне прогрессивного роста внутрипузырного давления возникали спонтанные колебания давления амплитудой от 4 до 6,9 см H 2 O (в среднем 5,3±0,5 см H 2 O), что можно расценить, как проявление вторичной гиперактивности детрузора, тогда как в основной группе спонтанные колебания давления практически отсутствовали: амплитуда 0-1,6 см H 2 O (в среднем 1,1±0,3 см H 2 O). Статистический анализ выявил достоверные различия по этому показателю ( р <0,01).
Наличие высокоамплитудных спонтанных колебаний внутрипузырного давления в фазу накоплению мочи свидетельствует о формировании детрузорной гиперактивности, часто развивающейся при инфраве-зикальной обструкции. Значительное уменьшение частоты развития и амплитуды спонтанных сокращений детрузора на фоне HESR позволяет сделать заключение о прямом влиянии препарата на гладкомышечные клетки мышечной оболочки мочевого пузыря и/или на механизмы регуляции их сократительной активности (в данном случае на порог возбудимости клеток).
Таким образом, исходя из приведенных данных, можно сделать заключение, что лечение HESR способствует лучшему сохранению функциональных параметров мочевого пузыря, а именно, комплаентности стенки мочевого пузыря, эвакуаторной способности детрузора и препятствует развитию гиперактивности детрузора.
Биохимические исследования
Важной задачей нашего исследования, помимо подтверждения прямого действия HESR на мочевой пузырь, было определение, способствует ли это действие сохранению функции почки, поскольку часто при выраженной ИВО наблюдается развитие почечной недостаточности разной степени тяжести.
Проведенные исследования показали, что терапия HESR способствует сохранению ряда показателей, характеризующих функцию почек, на более близких к норме значениях, чем в sham серии. Хотя при биохимических исследованиях не выявили достоверных различий между группами по уровням креатинина и мочевины крови, но по таким важным параметрам, как суточный диурез, скорость клубочковой фильтрации
и канальцевая реабсорбция натрия, были установлены достоверные различия.
Показано, что в sham опытах диурез снижался почти в 2 раза, тогда как терапия HESR приводила к сохранению диуреза на более близких к норме значе ниях, что, с одной стороны, может быть следствием лучшей сохранности эвакуаторной функции мочевого пузыря, а с другой – сохранности фильтрационной способности почек. Подтверждением значимости по следнего фактора являются данные о достоверно мень шем снижении клиренса креатинина на фоне HESR, по сравнению с sham опытами. Также в меньшей степени ухудшалась канальцевая реабсорбция натрия, как в процентном отношении к объему профильтрованного натрия, так и в абсолютных значениях (табл. 1).
О лучшей сохранности функционального состоя ния почек при терапии HESR крыс c ИВО свидетель ствуют и данные биохимического анализа мочи. В опытах sham серии выявили достоверное снижение концентрации мочевины в моче, а также суточной экс креции мочевины и креатинина с мочой, тогда как в опытной серии все эти показатели не отличались от нормальных значений. То есть, применение HESR пре пятствует существенному ухудшению азотовыдели тельной функции почек при ИВО (табл. 2).
Для оценки выраженности повреждения клеток почек и обструктивного мочевого пузыря (цитолиза), вызванного выраженной ИВО, определяли активность ферментов в крови и моче. В обеих группах выявили повышение активности АСТ, ЛДГ и КФК в крови, тогда как активность АЛТ и ЩФ достоверно не менялась. При этом,если повышение активности АСТ и ЩФ в обеих группах было примерно одинаковым, то в отношении КФК отмечен достоверно более выраженный рост активности фермента в sham группе животных по сравнению с HESR группой (табл. 3).
Этот факт заслуживает особого внимания,по-скольку повышение активности КФК может быть связано с повреждением гладкомышечных клеток детрузора обструктивного мочевого пузыря, а менее значительный рост активности этого фермента в опытной группе отражает лучшую сохранность гладкомышечных клеток детрузора при терапии HESR.
Патоморфологические исследования
При исследовании удаленного мочевого пузыря выявили, что в обеих сериях происходила его значительная гипертрофия, но ее степень оказалась достоверно более выраженной в группе животных, леченых HESR: масса мочевого пузыря возрастала с 96±4 мг в норме до 547±61 мг в sham серии и до 1004±104 мг
Таблица 1. Влияние терапии HESR на показатели функционального состояния почек у крыс с выраженной ИВО
Table 1. The effect of HESR therapy on indicators of the functional state of the kidneys in rats with severe IVO
|
Показатели Indicators |
Норма Norm |
HESR 2 недели HESR 2 weeks |
Sham 2 недели Sham 2 weeks |
|
Концентрация мочевины в крови (ммоль/л) Blood urea concentration (mmol/l) |
8,3±0,3 |
13,9±1,1 |
12,2±2,4 |
|
Концентрация креатинина в крови (мкмоль/л) Blood creatinine concentration (μmol/l) |
60+2 |
126±16 |
101±6 |
|
Суточный диурез (мл) Daily diuresis (ml) |
13,3+0,5 |
10,4+0,8 |
7,4+0,7 * |
|
Клиренс креатинина (мл/мин) Creatinine clearance (ml/min) |
2,92+0,09 |
0,98±0,10 |
0,58 ± 0,06 * |
|
Реабсорбция натрия (%) Sodium reabsorption (%) |
99,5+0,1 |
96,9 ± 0,2 |
93,8 ± 0,3 ** |
|
Абсолютное количество реабсорбированного натрия (мrмоль/ мин) Absolute amount of reabsorbed sodium (mmol/min) |
199+11 |
137 ± 21 |
80 ± 11 * |
Примечание: достоверность различий между опытной и sham группами: * р <0,05, ** р <0,01
Note: significance of differences between the experimental and sham groups: *p<0.05, ** p <0.01
Таблица 2. Параметры биохимического исследования мочи в опытной и контрольной группах
Table 2. Parameters of the biochemical study of urine in the experimental and control groups
|
Показатели Indicators |
Норма Norm |
HESR 2 недели HESR 2 weeks |
Sham 2 недели Sham 2 weeks |
|
Концентрация мочевины в моче (ммоль/л) Urine urea concentration (mmol/l) |
218 ± 26 |
234 ± 10 |
170 ± 21 * |
|
Концентрация креатинина в моче (мкмоль/л) Urine creatinine concentration (μmol/l) |
10,2 ± 1,2 |
10,1 ± 1,1 |
9,4 ± 1,0 |
|
Суточная экскреция мочевины с мочой (ммоль/л) Daily urinary excretion of urea (mmol/l) |
2757 ± 184 |
2882 ± 426 |
1092 ± 218 * |
|
Суточная экскреция креатинина с мочой (мкмоль/л) Daily urinary creatinine excretion (μmol/l) |
135 ± 6 |
131 ± 5 |
78 ± 14 * |
Примечание: достоверность различий между опытной и контрольной группами: * р <0,05
Note: significance of differences between the experimental and control groups: *p<0.05
в HESR серии (различия между опытной и контроль ной группами достоверны при р <0,01).
Более выраженная гипертрофия детрузора в серии с терапией HESR подтвердилась при морфомет рическом исследовании срезов обструктивных моче вых пузырей (табл. 4).
Средняя толщина мышечной стенки мочевого пу зыря в опытной и sham сериях составила 0,801±0,099 и 0,469±0,32 мм ( р <0,001). В опытной серии в большей степени возросла также общая толщина стенки моче вого пузыря, по сравнению с sham: 1,085±0,109 и 0,817±0,011 мм, соответственно ( р <0,05). При этом, со отношение толщины детрузора и толщины всей стенки мочевого пузыря составило 73,3±1,7% и 57,4±3,5%, со ответственно ( р <0,01), что свидетельствует о преобла дающем вкладе гипертрофии детрузора в утолщение стенки обструктивного мочевого пузыря.
Утолщение стенки мочевого пузыря происходило также за счет подслизистого слоя, что было более вы ражено в sham серии опытов: 0,198±0,030 мм по сравне нию с 0,134±0,007 мм при терапии HESR (р<0,05), что связано как с наличием более выраженного отека и вос палительного инфильтрата в этой зоне, а в отдельных препаратах – с развивающимся склерозом (рис. 5А, Б). При этом в половине случаев sham серии выявляли наличие деэпителизированных участков слизистой оболочки (рис. 5В), тогда как в группе HESR участков деэпителизации слизистой мочевого пузыря не выявляли, что может быть связано с развитием более выраженного воспаления в sham экспериментах.
При этом в опытной серии во всех образцах выявляли выраженное расширение сосудов подслизистого слоя (рис. 5Б), тогда как в sham серии гиперемию подслизистого слоя выявили лишь в половине опытов, и она была менее выражена.
Если в опытной группе воспалительную инфильтрацию выявляли только в пределах подслизистого слоя, то в половине случаев sham серии выявляли диффузную инфильтрацию всей стенки мочевого пузыря (рис. 6).
Последствием длительно текущего воспаления становится активация склеротического процесса. Проявления склеротического процесса во всех слоях стенки мочевого пузыря оказались значительно более выра-
Таблица 3. Влияние терапии HESR на активность ферментов в крови и моче
Table 3. Effect of HESR therapy on enzyme activity in blood and urine
|
Показатели Indicators |
Норма Norm |
HESR 2 недели HESR 2 weeks |
Sham 2 недели Sham 2 weeks |
|
Активность ферментов в крови / Enzyme activity in the blood |
|||
|
Активность АСТ в крови (МЕ/л) / AST activity in blood (IU/l) |
68 + 2 |
117 ± 16 |
128 ± 10 |
|
Активность АЛТ в крови (МЕ/л) / ALT activity in blood (IU/l) |
36 + 3 |
23 ± 2 |
31 ± 2 * |
|
Активность ЛДГ в крови (МЕ/л) / LDH activity in blood (IU/L) |
320 + 22 |
1618 ± 223 |
1692 ± 244 |
|
Активность ЩФ в крови (МЕ/л) / ALP activity in blood (IU/l) |
169 + 8 |
240 ± 29 |
202 ± 34 |
|
Активность КФК в крови (МЕ/л) / CPK activity in blood (IU/l) |
198 + 23 |
499 + 31 |
627 + 39 * |
|
Активность ферментов в моче / Enzyme activity in the urine |
|||
|
Активность АСТ в моче (МЕ/л) / AST activity in urine (IU/l) |
1,6 ± 0,7 |
9,2 ± 3,8 |
4,8 ± 2,2 |
|
Активность АЛТ в моче (МЕ/л) / ALT activity in urine (IU/l) |
2,6 ± 1,6 |
7,8 ± 3,7 |
5,5 ± 2,5 |
|
Активность ЛДГ в моче (МЕ/л) / LDH activity in urine (IU/L) |
5,2 ± 0,9 |
5,8 ± 0,9 |
4,8 ± 0,8 |
|
Активность ЩФ в моче (МЕ/л) / ALP activity in urine (IU/l) |
4,8 ± 0,6 |
7,4 ± 5,4 |
13,0 ± 11,3 |
|
Активность КФК в моче (МЕ/л) / CPK activity in urine (IU/l) |
1,4 ± 0,4 |
17,4 ± 10,3 |
2,8 ± 0,9 * |
Примечание: достоверность различий между опытной и контрольной группами: * р <0,05
Note: significance of differences between the experimental and control groups: *p<0.05
Таблица 4. Показатели морфометрии гистологических срезов стенки мочевого пузыря
Table 4. Morphometric parameters of histological sections of the bladder wall
|
Показатели Indicators |
Норма Norm |
HESR 2 недели HESR 2 weeks |
Sham 2 недели Sham 2 weeks |
|
Толщина подслизистого слоя (мм) Submucosal thickness (mm) |
0,109±0,009 |
0,134 ± 0,007* |
0,198 ± 0,030 |
|
Толщина детрузора (мм) Detrusor thickness (mm) |
0,254±0,021 |
0,801 ± 0,099*** |
0,469 ± 0,32 |
|
Толщина стенки мочевого пузыря (мм) Bladder wall thickness (mm) |
0,363±0,015 |
1,085 ± 0,109* |
0,817 ± 0,011 |
|
Отношение толщины детрузора и всей стенки мочевого пузыря (%) The ratio of the thickness of the detrusor and the entire bladder wall (%) |
69,9±1,0 |
73,3 ± 1,7** |
57,4 ± 3,5 |
|
Площадь очагов склероза (мм2) Area of sclerosis foci (mm2) |
0 |
0,026 ± 0,02* |
0,051 ± 0,011 |
Примечание: достоверность различий между опытной и sham группами: * р <0,05, ** р <0,01, *** р <0,001
Note: significance of differences between the experimental and sham groups: *p<0.05, ** p <0.01, *** р <0,001
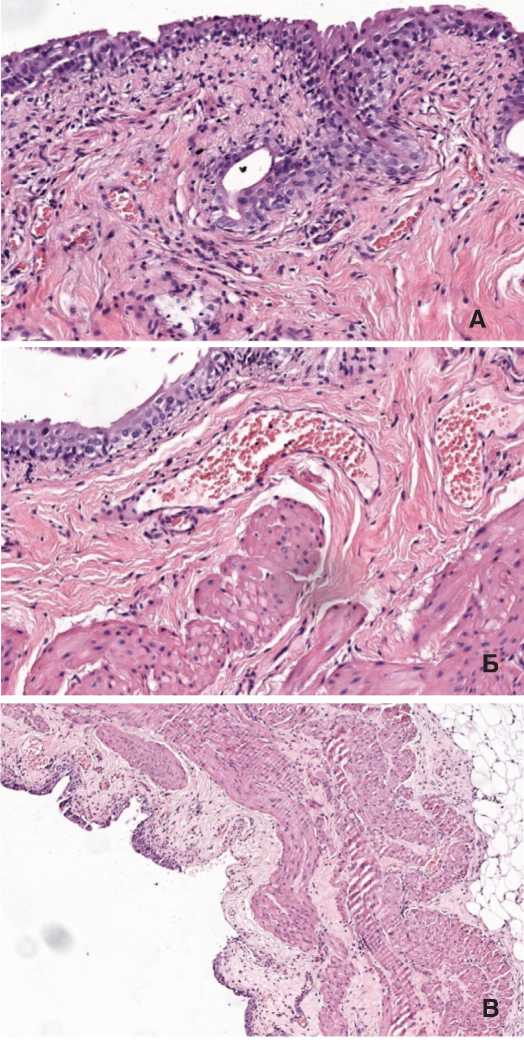
Рис. 5. А – Выраженное утолщение подслизистого слоя с диффузным воспалительным инфильтратом и склерозом в sham группе, окраска гематоксилином и эозином, ув. 200х. Б – умеренный склероз подслизистого слоя с выраженным расширением кровеносных сосудов и минимальной воспалительной реакцией в HESR группе, окраска гематоксилином и эозином, ув. 200х. В – участок деэпителизации слизистой мочевого пузыря, утолщение подслизистого слоя в sham группе, окраска гематоксилином и эозином, ув. 100х
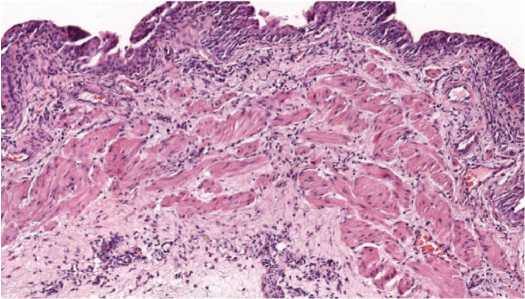
Рис. 6. Выраженный диффузный воспалительный инфильтрат, захватывающий всю стенку мочевого пузыря, sham группа, окраска гематоксилином и эозином, ув. 100х
А
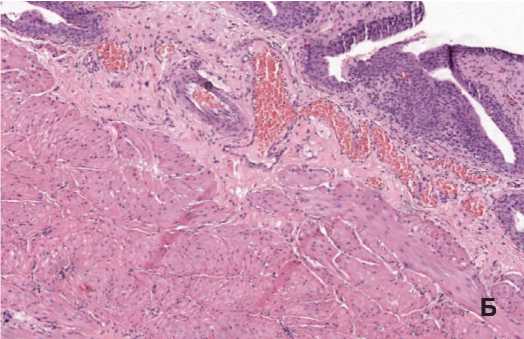
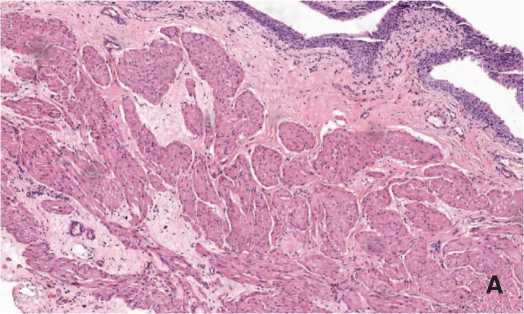
Рис. 7. А – Резко выраженный склероз подслизистого слоя, диффузный пери-мускулярный крупно- и мелкоочаговый склероз мышечной оболочки, sham группа. Б – Умеренно выраженный склероз подслизистого слоя с резким полнокровием сосудов, минимальный склероз мышечной оболочки, HESR группа. Окраска гематоксилином и эозином, ув. 100х.
ОБСУЖДЕНИЕ
жены в sham серии. В этих опытах в мышечной оболочке выявляли как выраженный диффузный перимускуляр-ный склероз (толстые прослойки соединительной ткани, окружающие пучки гладкомышечных клеток), так и локальные очаги склероза разной площади (рис. 7), тогда как в опытной серии площадь склеротических очагов была достоверно ( р <0,05) меньше – 0,026±0,02 по сравнению с 0,051±0,011 мм2 в sham группе (табл. 4).
Большинство исследований демонстрируют, что хроническое воздействие частичной ИВО на мочевой пузырь претерпевает фазы компенсации и декомпенса ции. В компенсированной фазе мышца детрузора уве личивает силу, чтобы преодолеть возросшее сопро тивление. Благодаря увеличению массы мочевого пу зыря, его сократительная функция сохраняется [9].
Типичная гистологическая картина этой фазы – гипертрофия детрузора и существенное увеличение массы мочевого пузыря,что наблюдают и в эксперименте, и у больных ДГПЖ [10].
Электронно-микроскопические исследования показали,что следствием мышечной гипертрофии и гиперплазии при ИВО является увеличение отложения коллагена и потеря парасимпатических нервных окончаний [11]. Это ведет к нестабильному «электрическому статусу» в зоне обструкции и неупорядоченным сокращениям детрузора [12]. Возникшая гиперактивность детрузора характеризуется спонтанными сокращениями, не связанными с мочеиспусканием, с повышенной частотой или без нее и последующим уменьшением объема мочеиспускания и емкости мочевого пузыря. При этом, изменение объема мочеиспускания и емкости мочевого пузыря в значительной степени зависят от продолжительности и тяжести обструкции [13-15]. В декомпенсированной фазе масса мочевого пузыря продолжает какое-то время увеличиваться, но сократимость стенок мочевого пузыря и функция опорожнения ухудшаются. Конец этой фазы характеризуется преобладанием фиброзной ткани в стенке мочевого пузыря,низкой емкостью мочевого пузыря и его плохой податливостью [16].
В экспериментах показано,что через 6 недель экспериментально вызванной умеренной и тяжелой ИВО у крыс, вес мочевого пузыря оказался в 2-2,5 раза больше,по сравнению с контрольной группой [17]. Это сопоставимо с данными C. Liu и соавт об увеличении веса мочевого пузыря крыс после 4х недель выраженной ИВО в 2-2,5 раза [18, 19]. Ранее M. Saito и соавт. доложили, что масса мочевого пузыря после двух недель «жесткой» обструкции выросла более, чем в 4 раза [20]. Результаты настоящего исследования также показали рост веса мочевого пузыря при ИВО, однако они несколько отличаются от приведенных выше данных в сторону большего увеличения веса мочевого пузыря. Если в sham группе такое увеличение превысило средний вес мочевого пузыря контрольной группы в 5,7 раза, что прибли- жается к данным M . Saito и соавт., то в группе HESR – в 10,5 раз.
Проведенные нами гистологические исследования подтвердили развитие гипертрофии мочевого пузыря, статистически достоверно более выраженное в HESR группе: увеличение толщины детрузора и стенки мочевого пузыря. При этом, площадь очагов склероза была значимо больше в sham группе, что свидетельствует о декомпенсации мочевого пузыря.
Таким образом, в настоящем исследовании, в условиях «жесткой» ИВО, наблюдали выраженную гипертрофию детрузора у животных основной группы, что характерно для описанной выше первой стадии патологического процесса – гипертрофии. В то же время, состояние мочевого пузыря у крыс sham группы можно характеризовать, как декомпенсированное. То есть, на значение HESR, вероятно, «затормозило» развитие патологического процесса на этапе гипертрофии – начала фазы декомпенсации, по сравнению с sham груп пой, где наблюдали выраженную декомпенсацию мочевого пузыря.
Цистометрия является традиционным исследовательским подходом для выявления изменений функции мочевого пузыря, в том числе у грызунов [21]. Наиболее широко используемыми животными для таких экспериментов являются крысы из-за относительной простоты технологии цистометрии. На моделях грызунов обычно исследуют следующие цистометрические параметры: объем мочеиспускания, остаточный объем, емкость мочевого пузыря, пороговое давление (давление в мочевом пузыре в начале сокращения детрузора для мочеиспускания), давление мочеиспускания (максимальное давление мочеиспускания), интервал мочеиспускания и исходное давление. Однако, трудно определить их нормальный диапазон [22]. T. Kitta и соавт. представили облик типичных кривых цистометрии наполнения у крыс в норме (sham) и при искусственно вызванной ИВО (рис. 8) [23, 24].
У животных с ИВО, как правило, увеличены: продолжительность цикла мочеиспускания, объем мочеиспускания, остаточный объем мочи и пороговое давле-
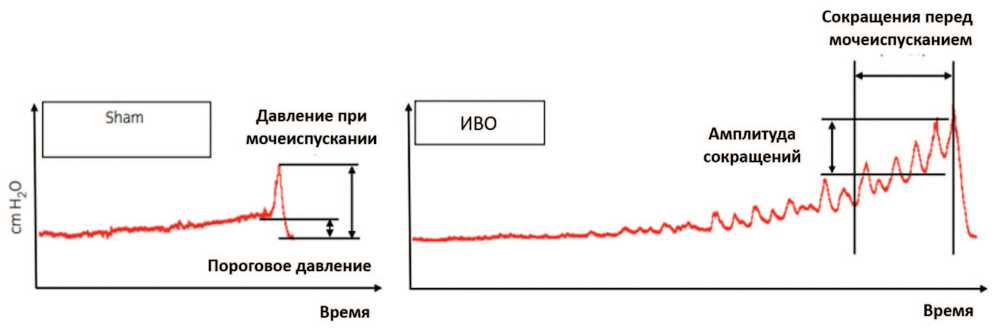
Рис. 8. Типичные цистометрические кривые крыс в норме и при ИВО в модификации [23, 24]
Fig. 8. Typical cystometric curves of normal (sham) and IVO rats in modification [23, 24]
ние, что отражает увеличение емкости и гипертрофию мочевого пузыря. Во время фазы наполнения мочевого пузыря при ИВО наблюдают непроизвольные сокращения детрузора (в некоторых случаях описываемые как сокращения перед мочеиспусканием), сопровождающиеся повышением давления в мочевом пузыре больше 2,0-4,0 см H 2 O [25-28].
В настоящем исследовании результаты инфузионной цистометрии выявили существенные различия между группами. В sham группе повышение внутрипу-зырного давления возникало практически сразу после начала введения физраствора, а его рост сопровождался иррегулярными колебаниями, отражающими возникновение детрузорной гиперактивности (рис. 3А), тогда как в основной группе наблюдали плавный рост давления до более высоких значений без признаков гиперактивности (рис. 3А-Б). При этом, рисунки цистометрических кривых, полученных нами в HESR и sham группах, практически полностью повторяют эталонные варианты, характерные для нормы и ИВО, соответственно (рис. 8). То есть, динамика изменения внутрипузырного давления у крыс, получавших HESR, приближена к таковой у контрольных животных. Кроме того, изменение индекса «объем/давление» в основной группе, по нашему мнению, свидетельствует о лучшем сохранении комплаент-ности стенки гипертрофированного мочевого пузыря при терапии HESR. Это подтверждают данными о большем объеме накопления мочи у крыс, получавших HESR.
Лучшее функциональное состояние мочевого пузыря у животных основной группы способствовало большей сохранности функции почек, что отразилось в достоверно лучших показателях суточного диуреза, клиренса креатинина и реабсорбции натрия.
В настоящем исследовании была выбрана модель тяжелой ИВО для имитации длительно существующей обструкции мочевых путей, приводящей к выраженными нарушениям функции мочевого пузыря и почек. Эксперименты, проведенные на самках крыс, подтвердили высказанную нами ранее гипотезу о возможном прямом действии гексанового экстракта Serenoa repens (Пермиксон) на мочевой пузырь, помимо влияния на предстательную железу. Это подтверждено рядом фактов на фоне применения HESR:
-
• сохранение целостности эпителиальной выстилки слизистой оболочки мочевого пузыря, что предотвращает проникновение мочи в интерстиций под действием повышенного внутрипузырного давления и развитие воспаления в стенке мочевого пузыря;
-
• регуляция процессов гипертрофии, воспаления и склерозирования детрузора на фоне ИВО;
-
• интенсификация кровоснабжения подслизистого слоя мочевого пузыря;
-
• предотвращение развития детрузорной гиперактивности;
-
• улучшение комплаентности и эвакуаторной функции мочевого пузыря.
ЗАКЛЮЧЕНИЕ
Таким образом, исходя из полученных в ходе настоящего исследования,можно сделать заключение, что в условиях тяжелой ИВО на фоне гипертрофии детрузора применение HESR способствует лучшему сохранению функциональных параметров мочевого пузыря, а именно, комплаентности и эвакуаторной способности, также уменьшает степень воспаления и склерозирования стенки мочевого пузыря, препятствует развитию декомпенсации мочевого пузыря и, тем самым, содействует сохранению функции почек. Значительное уменьшение частоты развития и амплитуды спонтанных сокращений детрузора на фоне HESR позволяет сделать заключение о прямом влиянии препарата на гладкомышечные клетки мышечной оболочки мочевого пузыря и/или на механизмы регуляции их сократительной активности.
Механизмы влияния HESR на мочевой пузырь в настоящий момент не ясны. Однако, без сомнения, как и в случае с ДГПЖ, это воздействие носит комплекс ный характер,где противовоспалительное действие HESR имеет первостепенное значение. Рассмотрению этого будут посвящены дополнительные исследования и публикации.
ЛИТЕ РАТУ РА/RE FERENCE S
ЛИТЕРАТУPA/REFERENC ES
Urology 2015;(4):16-21. (In Russian)].
Сведения об авторах:
Сивков А.В. – к.м.н., заместитель директора по научной работе НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия; РИНЦ Author ID 622663;
Кирпатовский В.И. – д.м.н., профессор, гл. научный сотрудник НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИРЦ»
Минздрава России; Москва, Россия; РИНЦ Author ID 604441;
Ефремов Г.Д. – к.м.н., заведующий научно-лабораторным отделом НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия; РИНЦ AuthorID 637962;
Голованов С.А. – д.м.н., руководитель группы клинической лабораторной диагностики научно-лабораторного отдела НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава;
Москва, Россия; РИНЦ AuthorID 636685;
Дрожжева В.В. – старший научный сотрудник научно-лабораторного отдела НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИРЦ» Минздрава России; Москва, Россия; РИНЦ AuthorID 696724
Вклад авторов:
Сивков А.В. – концепция и дизайн исследования, написание текста статьи, 35% Кирпатовский В.И. – экспериментальные исследования, обработка результатов и написание текста, 35%
Ефремов Г.Д. – морфологические исследования, анализ данных, 15%
Голованов С.А. – биохимические исследования, анализ данных, 10%
Дрожжева В.В. – биохимические исследования, анализ данных, 5%
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Финансирование: Исследование проведено при финансовой поддержке ООО «Пьер Фабр».
Статья поступила: 06.01.23
Результаты рецензирования: 08.02.23
Исправления получены: 17.02.23
Принята к публикации: 27.02.23
Information about authors:
Sivkov A.V. – PhD, Deputy Director of N. Lopatkin Scientific Research Instituteof Urology and Interventional Radiology – Branch of theNational Medical ResearchCentre of Radiology of the Ministry of Health of Russian Federation; Moscow, Russia; RSCI Author ID 622663;
Kirpatovskiy V.I. – Dr. Sc., professor, сhiefscientific Researcher of N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology – Branch of theNational Medical Research CentreofRadiology of the Ministry of Health of Russian Federation; Moscow, Russia;
RSCI Author ID 604441;
Efremov G.D. – PhD, head of scientific laboratory department of N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology – Branch of the National Medical Research Centre of Radiology of the Ministry of Health of Russian Federation; Moscow, Russia; RSCI AuthorID 637962;
Golovanov S.A. – Dr. Sc., head of clinical laboratory diagnostic group of scientific laboratory department, N. Lopatkin Scientific Research Institute ofUrology and Interventional Radiology – Branch of the National Medical Research Centre of Radiology of the Ministry of Health of Russian Federation; Moscow, Russia; RSCI AuthorID 636685;
Drozhzheva V.V. – researcher of scientific Laboratory Department of N. Lopatkin Scientific Research Institute of Urology and Interventional Radiology – Branch of the National Medical Research Centre of Radiology of the Ministry of Health of Russian Federation;
Moscow, Russia; RSCI AuthorID 696724
Authors’ contributions:
Sivkov A.V. – concept and design of the study, writing the text of the article, 35% Kirpatovsky V.I. – experimental research, processing of results and writing the text, 35%
Efremov G.D. – morphological studies, data analysis, 15%
Golovanov S.A. – biochemical research, data analysis, 10%
Drozhzheva V.V. – biochemical research, data analysis, 5%
Conflict of interest. The authors declare no conflict of interest.
Financing. The study was funded by Pierre Fabre LLC.
Received: 06.01.23
Peer review: 08.02.23
Corrections received: 17.02.23
Accepted for publication: 27.02.23
Лечение умеренных нарушений мочеиспускания, связанных с доброкачественной гиперплазией предстательной железы у взрослых мужчин
Список литературы Влияние гексанового экстракта Serenoa repens на функцию мочевого пузыря при частичной инфравезикальной обструкции
- Habib FK. Serenoa repens: The scientific basis for the treatment of benign prostatic hyperplasia. Eur Urol Suppl 2009;8(13):887-93. https://doi.org/10.1016/j.eursup.2009.11.005.
- Suzuki M, Oki T, Sugiyama T, Umegaki K, Uchida S, Yamada S. Muscarinic and alpha 1-adrenergic receptor binding characteristics of Saw Palmetto extract in rat lower urinary tract. Urology 2007;69(6):1216-20. https://doi.org/10.1016/j.urology.2007.02.038
- Nasrin S, Masuda E, Kugaya Н, Osano A, Ito Y, Yamada S. Effects of Saw Palmetto extract on urodynamic parameters, bladder muscarinic and purinergic receptors and urinary cytokines in rats with cyclophosphamide-induced cystitis. Low Urin Tract Symptoms 2014;6(1):57-63. https://doi.org/10.1111/luts.12015.
- Сивков А.В. Кирпатовский В.И. Экстракты Serenoa Repens в лечении расстройств мочеиспускания у больных ДГПЖ: дискуссия об эффективности и комплексном механизме действия. Экспериментальная и клиническая урология 2020;(4):96-105. [Sivkov A.V., Kirpatovskiy V.I. Serenoa Repens in the treatment of voiding dysfunction in patients with BPH: discussion of effectiveness and complex mechanism of action. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and Clinical Urology 2020;(4):96-105. (In Russian)]. https://doi.org/10.29188/2222-8543-2020-13-4-96-104.
- Кирпатовский В.И., Кудрявцев Ю.В., Мудрая И.С., Белик С.М., Хромов Р.А. Гетерогенность морфологических и функциональных изменений разных отделов мочевого пузыря крыс при инфравезикальной обструкции мочевых путей. Бюллетень экспериментальной биологии и медицины 2009;147(1):108-12. [Kirpatovskii V.I., Kudryavtsev Yu.V., Mudraya I.S., Belik S.M., Khromov R.A. Heterogeneity of morphological and functional changes in various compartments of rat urinary bladder in infravesical obstruction of the urinary tract. Byulleten' eksperimental'noy biologii i meditsiny = Bulletin of Experimental Biology and Medicine 2009;147(1):108-12. (In Russian)].
- Кирпатовский В.И., Мудрая И.С., Голованов С.А., Дрожжева В.В., Адамян Н.К., Иванов В.П., Фролова Е.В. Протективное действие противоишемической терапии и α-адреноблокаторов на состояние мочевого пузыря при экспериментально вызванной инфравезикальной обструкции. Экспериментальная и клиническая урология 2015;(4):16-21. [Kirpatovskiy V.I., Mudrya I.S., Golovanov S.A., Drozhzheva V.V., Adamyan N.K., Ivanov V.P., Frolova E.V. Protective action of the anti-ischemic therapy with alpha-adrenoblockers on experimental infravesicalthe bladder obstruction. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and Clinical Urology 2015;(4):16-21. (In Russian)].
- Шекунова Е.В., Ковалева М.А., Макарова М.Н., Макаров В.Г. Выбор дозы препарата для доклинического исследования. Межвидовой перенос доз. Ведомости научного центра экспертизы средств медицинского применения 2020;10(1):19-28. [Shekunova E.V., Kovaleva M.A., Makarova M.N., Makarov V.G. Dose selection in preclinical studies: cross-species dose conversion. Vedomosti Naučnogo centra èkspertizy sredstv medicinskogo primeneniâ = Bulletin of the Scientific Centre for Expert Evaluation of Medicinal Products 2020;10(1):19-28. (In Russian)].
- Кирпатовский В.И., Баблумян А.Ю., Голованов С.А., Дрожжева В.В., Адамян Н.К., Мурадян А.А., и др. Влияние противоишемической терапии на восстановление функции мочевого пузыря после острой задержки мочи. Экспериментальная и клиническая урология 2018;(1):28-35. [Kirpatovskiy V.I. Bablamyan A.Yu., Golovanov S.A., Drozhzheva V.V., Adamyan N.K., Muradyan A.A., et al. The influence of anti-ischemic therapy on the recovery of urinary bladder function after acute urinary retention. Eksperimentalnaya i Klinicheskaya urologiya = Experimental and Clinical Urology 2018;(1):28-35. (In Russian)].
- Collado A, Batista E, Gelabert-Mas A, Corominas JM, Arano P, Villavicencio H. Detrusor quantitative morphometry in obstructed males and controls. J Urol 2006;176(6 Pt 1):2722–8.
- Michishita M, Yano K, Kasahara K, Tomita K, Matsuzaki O. Increased expression of 5-HT(2A) and 5-HT(2B) receptors in detrusor muscle after partial bladder outlet obstruction in rats. Biomed Res 2015;36(3):187–94. https://doi.org/10.2220/biomedres.36.187.
- Dixon JS, Gilpin CJ, Gilpin SA, Gosling JA, Brading AF, Speakman MJ. Sequential morphological changes in the pig detrusor in response to chronic partial urethral obstruction. Br J Urol 1989;64(4):385–90. https://doi.org/10.1111/j.1464-410x.1989.tb06048.x.
- Seki N, Karim OM, Mostwin JL. Changes in electrical properties of guinea pig smooth muscle membrane by experimental bladder outflow obstruction. Am J Physiol 1992;262(5 Pt 2):F885–91. https://doi.org/10.1152/ajprenal.1992.262.5.F885.
- Schroder A, Uvelius B, Newgreen D, Andersson K-E. Bladder overactivity in mice after 1 week of outlet obstruction. Mainly afferent dysfunction? J Urol 2003;170(3):1017-21. https://doi.org/10.1097/01.ju.0000070926.39442.4c.
- Malmgren A. Bladder instability and abnormal micturition patterns in rats with infravesical outflow obstruction. Neurourol Urodyn 1987;6(5):371-380. https://doi.org/10.1002/ nau.1930060504.
- Mostwin JL, Karim OM, van Koeveringe G, Brooks E L. The guinea pig as a model of gradual urethral obstruction. J Urol 1991;145(4):854-8. https://doi.org/10.1016/s0022-5347(17)38477-x.
- Gosling JA, Kung LS, Dixon JS, Horan P, Whitbeck C, Levin RM. Correlation between the structure and function of the rabbit urinary bladder following partial outlet obstruction. J Urol 2000;163(4):1349–56.
- Sezginer EK, Yilmaz-Oral D, Lokman U, Nebioglu S, Aktan F, Gur S. Effects of varying degrees of partial bladder outlet obstruction on urinary bladder function of rats: A novel link to inflammation, oxidative stress and hypoxia. Lower Urinary Tract Symptoms 2019;11(2):O193-O201. https://doi.org/10.1111/luts.12211.
- Liu C, Xu H, Fu S, Chen Y, Chen Q, Cai Z, et al. Sulforaphane ameliorates bladder dysfunction through activation of the Nrf2–ARE pathway in a rat model of partial bladder outlet obstruction. Oxid Med Cell Longev 2016;2016:7598294. https://doi.org/10.1155/2016/7598294.
- Shirazi M, Mirkhani H, Monabbati A, Moghtadernejad S, Aminsharifi A. The effect of pentoxifylline on detrusor muscle contractility after partial urethral obstruction in a rat model. Int Urol Nephrol 2015;47(9):1493–7. https://doi.org/10.1007/s11255-015-1049-2.
- Saito M, Wein AJ, Levin RM. Effect of partial outlet obstruction on contractility: comparison between severe and mild obstruction. Neurourol Urodyn 1993;12(6):573–583. https://doi.org/10.1002/nau.1930120610.
- Smith PP, Hurtado E, Smith CP, Boone TB, Somogyi GT. Comparison of cystometric methods in female rats. Neurourol Urodyn 2008;27(4):324–9. https://doi.org/10.1002/nau.20512.
- Andersson KE, Soler R, Fullhase C. Rodent models for urodynamic investigation. Neurourol Urodyn 2011;30(5):636–46. https://doi.org/10.1002/nau.21108.
- Kitta T, Kakizaki H, Tanaka H, Sano H, Furuno T, Mitsui T, et al. An alpha-amino-3- hydroxy-5-methyl4-isoxazolepropionate glutamate-receptor antagonist can inhibit premicturition contractions in rats with bladder outlet obstruction. BJU Int 2007;100(1):181–6. https://doi.org/10.1111/j.1464-410X.2007.06919.x.
- Sawada N, Nomiya M, Hood B, Koslov D, Zarifpour M, Andersson KE. Protective effect of a beta3-adrenoceptor agonist on bladder function in a rat model of chronic bladder ischemia. Eur Urol 2013;64(4):664–71. https://doi.org/10.1016/j.eururo.2013.06.043.
- Levin RM, Saito M, Wein AJ, Packard D, Cohen A, Haugaard N. Effect of partial outlet obstruction on choline acetyltransferase activity in the rat and rabbit. Neurourol Urodyn 1993;12(3):255–61. https://doi.org/10.1002/nau.1930120308.
- Chai TC, Gemalmaz H, Andersson KE, Tuttle JB, Steers WD. Persistently increased voiding frequency despite relief of bladder outlet obstruction. J Urol 1999;161(5):1689–93.
- Tanaka H, Kakizaki H, Shibata T, Ameda K, Koyanagi T. Effects of chronic blockade of Nmethyl-D-aspartate receptors by MK-801 on neuroplasticity of the micturition reflex pathway after partial urethral obstruction in the rat. J Urol 2003;170(4 Pt 1):1427-31. https://doi.org/10.1097/01.ju.0000074713.69589.4a 170: 1427–1431.
- Tanaka H, Kakizaki H, Shibata T, Mitsui T, Koyanagi T. Effect of preemptive treatment of capsaicin or resiniferatoxin on the development of pre-micturition contractions after partial urethral obstruction in the rat. J Urol 2003;170(3):1022-6. https://doi.org/10.1097/01.ju.0000071479.02427.7d.


