Влияние глубины передней камеры на точность расчета оптической силы интраокулярной линзы на глазах с короткой переднезадней осью
Автор: Цыганков Александр Юрьевич, Першин Кирилл Борисович, Пашинова Надежда Фдоровна, Лих Иван Александрович, Ахраров Абдусамад Аристанович
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 4 т.11, 2020 года.
Бесплатный доступ
Обоснование. Расчет оптической силы интраокулярной линзы (ИОЛ) на глазах с короткой переднезадней осью представляет значительные трудности в связи с нестандартными анатомическими параметрами глаза, включая глубину передней камеры. Цель исследования - провести анализ эффективности шести формул для расчета оптической силы ИОЛ в зависимости от глубины передней камеры у пациентов с короткой переднезадней осью. Методы. Всего в исследование вошли 86 пациентов (133 глаза) с короткой переднезадней осью - от 18,54 до 21,98 (20,7 ± 0,9) мм. Группу I (n = 29, 40 глаз) составили пациенты с глубиной передней камеры (anterior chamber depth, ACD) менее 2,5 мм, группу II (n = 30, 49 глаз) - пациенты с ACD от 2,5 до 2,9 мм, группу III (n = 27, 44 глаза) - пациенты с ACD более 2,9 мм. Расчет оптической силы ИОЛ проводили по формуле SRK/T, ретроспективное сравнение - по формулам Hoffer Q, Holladay II, Olsen, Haigis и Barrett Universal II. Результаты. Во всех группах отмечено увеличение некорригированной и максимально корригированной остроты зрения в послеоперационном периоде. В группе I значимых различий при сравнении медианной абсолютной погрешности (MedAE) для шести формул не выявлено (p 0,05). Наименьшая MedAE (0,17) и лучшие значения MNE (-0,01 ± 0,58) показаны для формулы Haigis, в то время как формула SRK/T характеризовалась наибольшей MedAE (0,37). В группе II частота достижения рефракции ±0,25 и ±0,50 дптр для формулы Haigis была значимо выше. Заключение. Для глаз с ACD function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Факоэмульсификация катаракты, короткие глаза, расчет интраокулярной линзы
Короткий адрес: https://sciup.org/143174488
IDR: 143174488 | DOI: 10.17816/clinpract34864
Influence of the anterior chamber depth on the accuracy of the intraocular lens optical power calculation in short eyes
Background. The calculation of the optical strength of the intraocular lens (IOL) in eyes with a short anterior-posterior axis presents significant difficulties due to non-standard anatomical parameters of the eye, including the anterior chamber depth. Aim: determination of the relationship between the anterior chamber depth (ACD) and the accuracy of the IOL optical power calculation in eyes with an axial length of less than 22 mm. Methods. A total of 86 patients (133 eyes) with a short axis - from 18.54 to 21.98 (20.7 ± 0.9) mm, were included in the study. Group I (n = 29, 40 eyes) consisted of patients with ACD of less than 2.5 mm. Group II (n = 30, 49 eyes) included patients with ACD from 2.5 to 2.9 mm Group III (n = 27, 44 eyes) included patients with ACD greater than 2.9 mm. The calculation of the IOL optical power was carried out according to the formula SRK/T, the retrospective comparison was performed according to the Hoffer Q, Holladay II, Olsen, Haigis and Barrett Universal II formulas. Results. In all three groups, there was an increase in UCVA and BCVA in the postoperative period. In group I, there were no significant differences when comparing MedAE for the six formulas (p 0.05). The lowest MedAE (0.17) and the best MNE values (-0.01 ± 0.58) are shown for the Haigis formula, while the SRK/T formula was characterized by the highest MedAE (0.37). In group II, the refractive index ±0.25 and ±0.50 D for the Haigis formula was significantly higher. Conclusion. For eyes with ACD of less than 2.4 mm, none of the formulas showed a significant advantage, while for ACD of 2.4-2.9 mm and higher, the use of the Haigis formula is recommended, and the SRK / T formula showed the worst result. The data obtained dictate the need to review the existing standards for calculating the IOL optical power in patients with short eyes depending on ACD.
Текст научной статьи Влияние глубины передней камеры на точность расчета оптической силы интраокулярной линзы на глазах с короткой переднезадней осью
<линическая’2п20
п эакти ка Том 11 №4
ного положения линзы (effective lens position, ELP) представляется наиболее значимым для предоперационного расчета оптической силы ИОЛ [4].
В связи с использованием AL в качестве одной из переменных в абсолютном большинстве формул для расчета оптической силы ИОЛ, включая формулы третьего и четвертого поколения, биометрия относится к наиболее значимым факторам точности предоперационного планирования. Точность различных формул варьирует в зависимости от ACD, даже при наличии неизменных преломляющей силы роговицы и AL [5]. J. Jeong и соавт. [6] изучали роль биометрических параметров для 91 глаза в дооперационном периоде в точности применения различных формул. Показано, что измерение ACD в дооперационном периоде является ключевым фактором различия формул третьего поколения в сравнении с формулой Haigis. Прогнозирование послеоперационной рефракции на основе ACD было более точным, чем без учета ACD на коротких глазах и глазах с мелкой передней камерой [5]. На сегодняшний день доступны единичные работы, посвященные анализу вклада ACD в точность расчета оптической силы ИОЛ на коротких глазах [7].
Цель исследования — определить взаимосвязь между глубиной передней камеры и точностью расчета оптической ИОЛ на глазах с аксиальной длиной < 22 мм.
МЕТОДЫ
Дизайн исследования
Выполнено проспективное исследование.
Критерии соответствия
Критерии включения: наличие у пациентов показаний к удалению катаракты; аксиальная длина глаза менее 22 мм.
Критерии невключения: наличие осложненной катаракты; необходимость имплантации нестандартных видов интраокулярных линз; аксиальная длина глаза более 22 мм.
Критерии исключения: выявление в ходе хирургического вмешательства сопутствующей патологии глазного дна, влияющей на функциональный исход лечения.
Условия проведения
Исследование проведено на базе офтальмологических клиник «Эксимер» Москвы и Новосибирска, кафедры офтальмологии Ташкентской медицинской академии.
Продолжительность исследования
Исследование проведено в период с января 2017 по декабрь 2018 г.
Описание медицинского вмешательства
Разделение пациентов ( n = 86; 133 глаза) на группы проводили согласно величине ACD. Группу I ( n = 29, 40 глаз) составили пациенты с ACD < 2,5 мм, группу II ( n = 30, 49 глаз) — с ACD от 2,5 до 2,9 мм, группу III ( n = 27, 44 глаза) — с ACD > 2,9 мм.
Всем пациентам проводили как стандартное (авторефрактометрия, тонометрия, визометрия, компьютерная периметрия, биомикроскопия, офтальмоскопия в условиях максимального мидриаза), так и специальное (кератотопография, эхография, ультразвуковая пахиметрия, оптическая когерентная биометрия с определением аксиальной длины глаза, глубины передней камеры и кривизны роговицы, по показаниям — оптическая когерентная томография) офтальмологическое обследование.
Клинико-функциональные параметры пациентов всех групп представлены в табл. 1. Приведены средние значения с учетом стандартного отклонения, а также диапазон минимальных и максимальных значений исследуемых параметров. Статистически значимых различий между группами в дооперационном периоде не выявлено, за исключением факичной глубины передней камеры, что определило разделение пациентов на исследуемые группы.
Операцию факоэмульсификации проводили c использованием микрохирургических систем Stel-laris (Bausch and Lomb, США) и Infinity (Alcon, США) через роговичный височный туннельный разрез длиной 1,8 мм. У пациентов с обратным астигматизмом более 0,75 D с целью его коррекции разрез расширяли до 2,5 мм или до 3,75 мм в зависимости от степени дефекта. Во всех случаях имплантированы различные монофокальные ИОЛ (Alcon, США).
Методы регистрации исходов
Расчет оптической силы ИОЛ проводили по формуле SRK/T, ретроспективное сравнение — по формулам Hoffer Q, Holladay II, Olsen, Haigis и Barrett Universal II. Точность каждой из формул рассчитывали путем сравнения целевого и расчетного сферического эквивалента (spherical equivalent; SE), в идеале равного нулю при вычитании расчетного SE из целевого SE (через 6 мес после хирургического вмешательства). Анализ проводили
Таблица 1
Клинико-функциональные параметры в дооперационном периоде
|
Группа I Группа II Группа III Параметр ( n = 29, ( n = 30, ( n = 27, p 40 глаз) 49 глаз) 44 глаза) |
||||
|
Возраст, лет |
27–83 58,9 ± 13,8 |
27–88 65,1 ± 13,2 |
28–75 51,1 ± 12,2 |
>0,05 |
|
Аксиальная длина глаза, мм |
18,54–21,96 20,55 ± 0,97 |
18,56–21,98 20,67 ± 0,98 |
19,39–21,94 20,81 ± 0,74 |
>0,05 |
|
Факичная глубина передней камеры, мм |
2,05–2,48 2,32 ± 0,12 |
2,53–2,86 2,7 ± 0,09 |
2,90–3,70 3,11 ± 0,20 |
<0,05 |
|
Сферический компонент рефракции, дптр |
-1,5–14,0 3,9 ± 4,7 |
-0,75–11,0 4,7 ± 3,6 |
-1,00–10,0 4,5 ± 4,1 |
>0,05 |
|
Цилиндрический компонент рефракции, дптр |
-1,75–4,5 1,1 ± 1,7 |
-3,0–5,50 0,7 ± 1,9 |
-4,75–3,75 0,4 ± 1,4 |
>0,05 |
|
Ось цилиндра, град. |
0–176 93,0 ± 59,7 |
0–178 91,2 ± 59,4 |
0–180 83,1 ± 55,9 |
>0,05 |
|
Показатели кератометрии: • К 1 |
34,5–47,3 44,1 ± 3,4 |
38,2–48,0 44,4 ± 2,2 |
40,3–47,2 44,1 ± 1,46 |
>0,05 |
|
• К 2 |
35,4–49,0 45,1 ± 3,2 |
41,6–49,1 46,0 ± 1,7 |
43,0–48,7 45,4 ± 1,4 |
>0,05 |
|
Некорригированная острота зрения вдаль |
0,01–0,3 0,12 ± 0,08 |
0,01–0,7 0,1 ± 0,12 |
0,02–0,7 0,15 ± 0,17 |
>0,05 |
|
Максимально корригированная острота зрения вдаль |
0,01–1,0 0,54 ± 0,28 |
0,01–0,9 0,48 ± 0,26 |
0,1–1,0 0,56 ± 0,24 |
>0,05 |
|
Период наблюдения, мес |
6,0–18,0 14,1 ± 2,0 |
7,0–20,0 13,8 ± 1,7 |
6,0–24,0 12,5 ± 2,4 |
>0,05 |
Примечания. Указаны значения min, max, M ± STD. Полужирным шрифтом выделено статистически значимое различие между группами.
с помощью программного обеспечения системы VERION© и открытых данных на сайтах исследуемых формул. Период наблюдения пациентов составил от 6 до 24 (12,7 ± 2,4) мес.
Этическая экспертиза
Получено одобрение от Локального этического комитета офтальмологической клиники «Эксимер» (г. Москва, № 4 от 09.11.2016; г. Новосибирск, № 2 от 11.11.2016) и Ташкентской медицинской академии (№ 118 от 19.04.2017).
Статистический анализ
Статистическая обработка результатов исследования выполнена с использованием приложения Microsoft Excel 2010 и статистической программы Statistica 10.1 (StatSoft, США). Проведен расчет среднего арифметического значения (М), стандартного отклонения от среднего арифметическо- го значения (SD), минимальных (min) и максимальных (max) значений, размаха вариации Rv (разность max-min). Для оценки достоверности полученных результатов при сравнении средних показателей-использовался t-критерий Стьюдента. При сравнении частоты встречаемости признака использовался точный критерий Фишера. Различия между выборками считали достоверными при p < 0,05, доверительный интервал 95%. Отклонение расчетного значения сферического эквивалента от целевого определяли с помощью дисперсионного анализа (ANOVA) и регрессионного анализа, при этом проводили ретроспективное сравнение отклонения сферического эквивалента с помощью различных формул для расчета ИОЛ. Для оценки различий средних погрешностей применяли тест Краскела–Уоллиса (Kruskal–Wallis). Погрешность оценки (estimation error, E) определяли как разницу между фактической послеоперационной SE в тече-
<линическая’2п20 п эакти ка Том 11 №4
ние 6 мес наблюдения и прогнозируемой послеоперационной SE. Абсолютную погрешность (absolute error, AE) определяли как абсолютное значение E. Среднюю числовую погрешность (mean numerical error, MNE), среднюю (mean absolte error, MAE) и медианную (median absolute error, MedAE) абсолютную погрешность рассчитывали для каждой формулы. Отдельно оценивали процент глаз с MNE в пределах ±0,25, ±0,50, ±1,0 и ±2,0 дптр для каждой формулы.
РЕЗУЛЬТАТЫ
Объекты (участники) исследования
Обследованы 86 пациентов (133 глаза) с короткой переднезадней осью — от 18,54 до 21,98 (20,7 ± 0,9) мм, факоэмульсификацией катаракты или удалением прозрачного хрусталика с рефракционной целью и имплантацией ИОЛ. Женщины составили 55,8% ( n = 48), мужчины — 44,2% ( n = 38). Возрастной диапазон варьировал от 27 до 88 (61,0 ± 13,8) лет.
Основные результаты исследования
Во всех группах отмечено увеличение некорри-гированной (НКОЗ) и максимально корригированной (МКОЗ) остроты зрения вдаль в послеоперационном периоде. В группе I показано увеличение
НКОЗ с 0,12 ± 0,08 до 0,57 ± 0,20 ( p < 0,05), а МКОЗ — с 0,54 ± 0,28 до 0,64 ± 0,24 ( p > 0,05). Для группы II отмечена динамика НКОЗ с 0,1 ± 0,12 до 0,56 ± 0,23 ( p < 0,05), МКОЗ — с 0,48 ± 0,26 до 0,65 ± 0,25 ( p > 0,05). В группе III определен рост НКОЗ с 0,15 ± 0,17 до 0,61 ± 0,26 ( p < 0,05), МКОЗ — с 0,56 ± 0,24 до 0,70 ± 0,22 ( p > 0,05). Таким образом, во всех исследуемых группах отмечен статистически значимый рост НКОЗ через 6 мес наблюдения.
Для шести исследуемых формул проведен расчет основных погрешностей (табл. 2). При одинаковых MAE для нескольких формул их эффективность в группе пациентов с короткой передне-задней осью одинакова, несмотря на возможную различную частоту попадания в целевую рефракцию одной из групп с аксиальной длиной глаза менее 22 мм.
В группе I значимых различий при сравнении MedAE для шести формул не выявлено ( p < 0,05). Наибольшие значения MedAE (0,51 и 0,49 соответственно) и меньший диапазон MNE (-0,03 ± 0,89 и -0,01 ± 0,97 соответственно) показаны для формул Haigis и Barrett Universal II.
Отсутствие значимых различий при сравнении MedAE показано и для группы II, однако значения показателя при использовании формулы Haigis, в отличие от группы I, было наименьшим
Таблица 2
Средняя числовая (MNE), средняя абсолютная (MAE) и медианная абсолютная (MedAE) погрешность при использовании формул Hoffer Q, Holladay 2, Haigis, SRK/T, Olsen и Barrett Universal II в исследуемых группах
|
Параметр |
Hoffer Q |
Holladay 2 |
Haigis |
SRK/T |
Olsen |
Barrett Universal II |
|
Группа I (40 глаз) MNE(D) ± SD Диапазон MAE(D) ± SD MedAE |
-0,38 ± 0,61 -2,0–3,28 0,64 ± 0,75 0,39 |
-0,12 ± 1,03 -2,06–2,97 0,68 ± 0,73 0,37 |
-0,03 ± 0,89 -2,09–3,31 0,75 ± 0,71 0,51 |
-0,42 ± 0,98 -2,16–3,20 0,72 ± 0,79 0,43 |
-0,29 ± 0,94 -2,10–3,09 0,68 ± 0,75 0,35 |
-0,01 ± 0,97 -1,81–3,02 0,66 ± 0,69 0,49 |
|
Группа II (49 глаз) MNE(D) ± SD Диапазон MAE(D) ± SD MedAE |
-0,12 ± 0,64 -1,31–2,06 0,58 ± 0,55 0,50 |
-0,02 ± 0,71 -1,24–2,13 0,63 ± 0,48 0,53 |
0,05 ± 0,69 -1,09–1,97 0,58 ± 0,53 0,45 |
-0,14 ± 0,94 -1,36–2,51 0,70 ± 0,51 0,59 |
-0,10 ± 0,81 -1,48–2,05 0,67 ± 0,49 0,56 |
0,21 ± 0,85 -1,34–2,80 0,63 ± 0,66 0,50 |
|
Группа III (44 глаза) MNE(D) ± SD Диапазон MAE(D) ± SD MedAE |
0,10 ± 0,41 -1,29–1,87 0,37 ± 0,45 0,23 |
-0,04 ± 0,55 -1,39–2,06 0,37 ± 0,40 0,22 |
-0,01 ± 0,58 -1,52–1,99 0,40 ± 0,47 0,17 |
0,05 ± 0,61 -1,44–2,16 0,43 ± 0,50 0,37 |
0,21 ± 0,65 -1,20–2,43 0,35 ± 0,49 0,27 |
0,02 ± 0,58 -1,35–2,09 0,48 ± 0,48 0,35 |
Примечание. MNE (D) — средняя числовая погрешность, MAE(D) — средняя абсолютная погрешность, MedAE — медианная абсолютная погрешность. D — диоптрии.
и составило 0,45, а наибольшее — для формул SRK/T и Olsen (0,59 и 0,56 соответственно). Данные формулы характеризовались наибольшим значением MAE (0,70 и 0,67 соответственно), в то время как для других формул MAE была ниже ( p > 0,05). Наименьшее значение MNE показано для формул Haigis (0,05 ± 0,69) и Holladay 2 (-0,02 ± 0,71). Различия MNE для исследуемых формул не были статистически значимыми ( p > 0,05).
В группе III значимых различий при сопоставлении средних значений MedAE не выявлено (р > 0,05). Наименьшая MedAE (0,17) и лучшие значения MNE (-0,01 ± 0,58) показаны для формулы Haigis, в то время как формула SRK/T характеризовалась наибольшей MedAE (0,37).
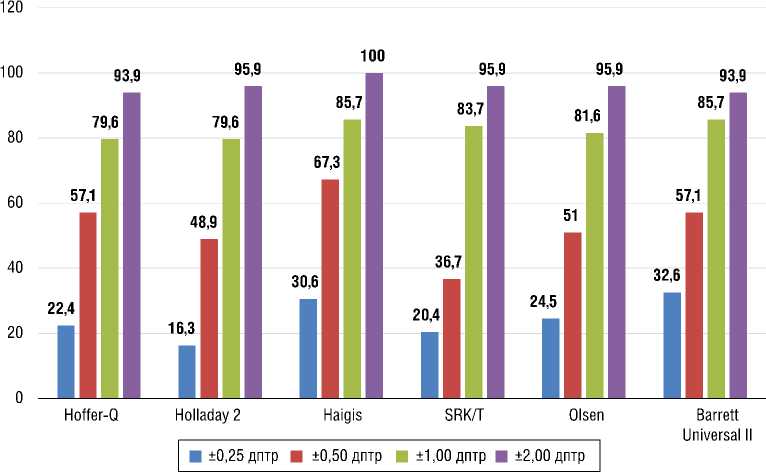
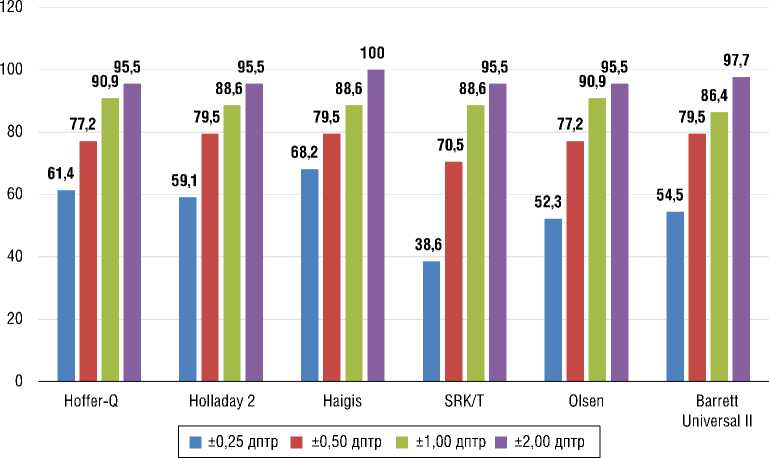
На рис. 1–3 представлен процент глаз с MNE в диапазоне ±0,25, ±0,50, ±1,0 и ±2,0 дптр для каждой формулы по группам. MNE обратно пропорциональна количеству глаз, попавших в целевую рефракцию, т.е. низкое значение MNE соответствует большей частоте попадания в целевую рефракцию.
Результаты были сопоставимы во всех трех группах, за исключением процента достижения рефракции ±0,25 и ±0,50 дптр в группе II, где показано значимое преимущество формулы Haigis.
Рис. 1. Процент глаз с MNE в диапазоне ±0,25, ±0,50, ±1,0 и ±2,0 дптр в группе I ( n = 29, 40 глаз)
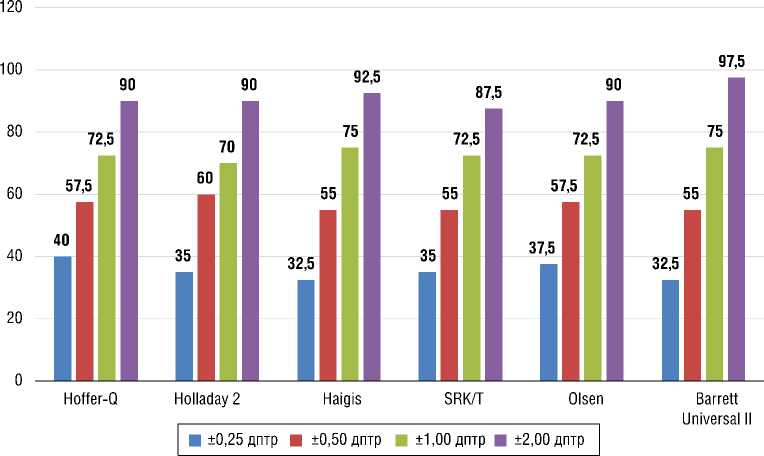
Рис. 2. Процент глаз с MNE в диапазоне ±0,25, ±0,50, ±1,0 и ±2,0 дптр в группе II ( n = 30, 49 глаз)
<линическая’2п20 п эакти ка Том 11 №4
Рис. 3. Процент глаз с MNE в диапазоне ±0,25, ±0,50, ±1,0 и ±2,0 дптр в группе III ( n = 27, 44 глаза)
ОБСУЖДЕНИЕ
Точное измерение ACD играет одну из ключевых ролей в прогнозировании послеоперационной рефракции и определении эффективного положения линзы. Прогностическая точность различных формул для расчета оптической силы ИОЛ зависит не только от AL, но и от ACD [8, 9]. На глазах с короткой аксиальной длиной неверный расчет в измерении ACD приводит к большей ошибке, чем на длинных глазах. В ряде исследований показано влияние ACD в коротких глазах на точность расчетов с использованием формул третьего и четвертого поколений [5, 9], однако данные исследования проводили без учета формул Barrett Universal II и Holladay 2. В настоящей работе изучали шесть наиболее часто используемых формул для расчета оптической силы ИОЛ.
-
Y. Eom и соавт. [5] в группе глаз с ACD < 2,5 мм показали, что формула Haigis ассоциирована с более точным расчетом послеоперационной рефракции. Вместе с тем в работе S. Yang и со-авт. [9], напротив, применение данной формулы приводило к наибольшей ошибке прогнозирования. В нашей работе формулы Haigis и Barrett Universal II были ассоциированы как с наибольшей MedAE, так и меньшим диапазоном MNE, что не позволяет рекомендовать их для использования в данной группе пациентов.
В указанных выше работах [5, 9] в группе глаз с ACD 2,5–2,9 мм ни для одной из исследуемых формул не показано значимого преимущества. В нашей работе наименьшие MAE и MedAE определены для формулы Haigis, что также сопровождалось наиболее высоким процентом попадания в целевую рефракцию ±0,5 дптр. Данная формула представляется наиболее эффективной для пациентов с ACD 2,5–2,9 мм. В то же время наибольшие MAE и MedAE и наименьший процент попадания в целевую рефракцию ±0,5 дптр определен для формулы SRK/T, что свидетельствует о необходимости пересмотра стандартных подходов к расчету оптической силы ИОЛ в данной группе пациентов. Схожие данные получены и в группе с ACD > 2,9 мм, что согласуется с данными литературы [5, 7, 9].
ЗАКЛЮЧЕНИЕ
В работе представлен анализ эффективности шести формул для расчета оптической силы ИОЛ в зависимости от глубины передней камеры у пациентов с короткой переднезадней осью. Для глаз с глубиной передней камеры < 2,4 мм ни одна формула не показала значимого преимущества, в то время как при 2,4–2,9 мм и выше рекомендовано применение формулы Haigis, а формула SRK/T продемонстрировала худший результат. Полученные данные диктуют необходимость пересмотра существующих стандартов расчета оптической силы ИОЛ у пациентов на коротких глазах в зависимости от глубины передней камеры.
ИНФОРМИРОВАННОЕ СОГЛАСИЕ
Пациенты добровольно подписали информированное согласие на участие в исследовании и публикацию персональной медицинской информации в обезличенной форме в журнале «Клиническая практика».
ИСТОЧНИК ФИНАНСИРОВАНИЯ
Исследование не имело спонсорской поддержки и осуществлялось на личные средства авторов.
Список литературы Влияние глубины передней камеры на точность расчета оптической силы интраокулярной линзы на глазах с короткой переднезадней осью
- Gokce SE, Zeiter JH, Weikert MP, et al. Intraocular lens power calculations in short eyes using 7 formulas. J Cataract Refract Surg. 2017; 43(7): 892-897. DOI: 10.1016/j.jcrs.2017.07.004
- Першин К.Б., Пашинова Н.Ф., Цыганков А.Ю., Легких С.Л. Алгоритм выбора формулы для расчета оптической силы ИОЛ при экстремальной миопии // Точка зрения. Восток-Запад. - 2016. - №1. - С. 64-67.
- Olsen T.Calculation of intraocular lens power: a review. ActaOphthalmol Scand. 2007; 85(5): 472-485. DOI: 10.1111/j.1600-0420.2007.00879.x
- Першин К.Б., Пашинова Н.Ф., Цыганков А.Ю., и др. Биометрия при расчете ИОЛ как фактор успешной хирургии катаракты // Катарактальная и рефракционная хирургия. - 2016. - T.16. - №1. - С. 15-22.
- Eom Y, Kang S-Y, Song JS, et al. Comparison of Hoffer Q and Haigis formulae for intraocular lens power calculation according to the anterior chamber depth in short eyes. Am J Ophthalmol. 2014; 157(4): 818-824.e2. DOI: 10.1016/j.ajo.2013.12.017
- Jeong J, Song H, Lee JK, et al.The effect of ocular biometric factors on the accuracy of various IOL power calculation formulas.BMC Ophthalmol. 2017;17(1):62. DOI: 10.1186/s12886-017-0454-y
- Shrivastava AK, Behera P, Kacher R, Kumar B. Effect of anterior chamber depth on predictive accuracy of seven intraocular lens formulas in eyes with axial length less than 22 mm. Clin Ophthalmol. 2019; 13:1579-1586. DOI: 10.2147/OPTH.S217932
- Hoffer KJ, Aramberri J, Haigis W, et al. Protocols for studies of intraocular lens formula accuracy. Am J Ophthalmol. 2015; 160(3): 403-405.e1. DOI: 10.1016/j.ajo.2015.05.029
- Yang S, Whang WJ, Joo CK. Effect of anterior chamber depth on the choice of intraocular lens calculation formula. PLoS One. 2017; 12(12): e0189868. DOI: 10.1371/journal.pone.0189868


