Влияние Helicobacter pylori на дифференцировку Т-регуляторных клеток
Автор: Матвеичев А.В., Талаева М.В., Талаев В.Ю., Неумоина Н.В., Перфилова К.М., Лапаев Д.Г., Мохонова Е.В., Цыганова М.И., Коптелова В.Н., Никитина З.И., Лапин В.А., Мелентьев Д.А.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Медико-биологические аспекты оценки воздействия факторов риска
Статья в выпуске: 1 (17), 2017 года.
Бесплатный доступ
Оценка риска возникновения инфекций, вызываемых грамотрицательной бактерией Helicobacter pylori, является актуальной проблемой для здравоохранения в связи с широтой распространения возбудителя, обширным спектром вызываемых патологий, включающим злокачественные новообразования желудочно-кишечного тракта. Возбудитель склонен к длительному, хроническому персистированию, несмотря на его «хрупкость» и высокую требовательность к условиям культивирования. Проблема персистенции при этом представляет особенный интерес в связи с наличием данных о способности Helicobacter pylori изменять протекание иммунного ответа у инфицированных лиц в сторону благоприятных для себя супрессивных, регуляторных форм иммунных реакций как на уровне желудка, так и на уровне всего организма в целом. Цель работы cостояла в оценке способности Helicobacter pylori стимулировать дифференцировку Т-регуляторных CD4+CD25+FoxP3+клеток человека - основных медиаторов регуляции иммунного ответа - в условиях прямого контакта между бактериями и Т-клетками, без участия наиболее профессиональных антигенпрезентирующих клеток. Объектами исследования являлись клинические изоляты Helicobacter pylori и образцы Т-лимфоцитов лиц, не имевших в анамнезе Helicobacter pylori-инфекции, совместно культивируемые в условиях in vitro. Изменение содержания Т-регуляторных клеток оценивали цитофлюорометрически. Установлено, что при 18-часовом сокультивировании Т-лимфоцитов и Helicobacter pylori в соотношениях от 1: 10 до 1: 50 в культурах повышается содержание Т-регуляторных клеток в среднем в 2,12 раза. Данный эффект не требует наличия в культуре дендритных клеток и, по-видимому, затрагивает Т-лимфоциты, исходно коммитированные в своем развитии в сторону Т-регуляторных клеток. Также, по мнению авторов, влияние на дифференцировку Т-регуляторных клеток является специфическим свойством Helicobacter pylori.
Лимфоциты, т-регуляторные клетки, дифференцировка, костимуляция, антитела, проточная цитофлюорометрия, клеточные культуры
Короткий адрес: https://sciup.org/14237988
IDR: 14237988 | УДК: 616.98: | DOI: 10.21668/health.risk/2017.1.03
Influence exerted by Helicobacter pylori on regulatory T-cells differentiation
Estimating risks of infections induced by gram-negative Helicobacter pylori, is a vital problem for healthcare due to wide spread of the agent and wide range of induced pathologies which include malignant neoplasms in gastrointestinal tract. The agent is prone to long-term chronic persistence despite its "fragility" and its being greatly demanding to culturing conditions. The persistence issue is of special interest here as it is related to data on Helicobacter pylori capability to change immune response in infected people inducing suppressive regulatory immune reactions which are more favorable for the agent, both in stomach and in a whole body. Our research goal was to estimate Helicobacter pylori capability to induce differentiation of regulatory CD4+CD25+FoxP3+ human T-cells as basic mediators of immune response regulation under direct contact between bacteria and T-cells without any participation of most professional antigen-presenting cells. Our research objects were clinical isolates of Helicobacter pylori and T-lymphocytes samples taken from people who didn't have Helicobacter pylori-infection in their case history; isolates and samples were jointly cultivated in vitro. We applied cytofluorometry to estimate changes in regulatory T-cells content. We detected that if T-lymphocytes and Helicobacter pylori were jointly cultivated during 18 hours in ratios from 1:10 to 1:50, regulatory T-cells content in cultures increased 2.12 times on average. This effects doesn't require any dendritic cells in a culture and obviously affects T-lymphocytes which are originally committed to regulatory T-cells in their development. Also, in our opinion, influence exerted on regulatory T-cells differentiation is a specific feature of Helicobacter pylori.
Текст научной статьи Влияние Helicobacter pylori на дифференцировку Т-регуляторных клеток
APC, антитела к FoxP3, меченные PE, все – производства eBioscience, США. Пермеабилизацию мембран, необходимую для мечения FoxP3, производили набором «Foxp3 / Transcription Factor Staining Buffer Set» (eBioscience, США) согласно инструкциям производителя. Анализ осуществляли на цитофлюориметре FacsCalibur (Beckton Dickinson, США). Для статистической обработки данных использовался критерий Ньюмена–Кейлса.
Результаты и их обсуждение. Данные оценки влияния H. pylori на дифференцировку лимфоцитов в сторону Т-рег при отсутствии в культурах дендритных клеток представлены на рис. 1 и 2. Как можно видеть, добавление H. pylori к культуре Т-клеток приводило к достоверному повышению числа Т-регуляторных CD4+CD25+FoxP3+ клеток через 18 часов совместного культивирования (среднее содержание Т-рег в культурах без стимуляции бактериями составляло 6,01 ± 0,72 % от всех CD4+ клеток, при добавлении H. pylori в соотношении 1:10 содержание Т-рег увеличивалось до 15,04 ± 1,97 %, p <0,01).
Содержание клеток в культурах с соотношением лимфоцитов к бактериям 1:20 и 1:50 также было достоверно выше контрольных значений нестимулированных лимфоцитов (12,7 ± 1,53 % для 1:20 и 10,42 ± 1,97 % для 1:50, отличие от контроля достоверно, p <0,01).
В то же время, как можно видеть, в ряду соотношений наблюдалась тенденция к обратной дозовой зависимости. Соотношение 1:10 показало наибольший прирост содержания Т-рег, который понижался при увеличении числа бактерий в культурах. Однако данная тенденция осталась статистически недостоверной. Таким образом, полученные данные свидетельствуют о наличии действия H. pylori на отвечающие Т-лимфоциты, не зависимо от присутствия в культуре наиболее профессиональных антигенпрезентирующих клеток – дендритных, и, по нашему мнению, опосредуемых прямым контактом между бактериями и отвечающими Т-лимфоцитами. В то же время в данных условиях эксперимента не исключена роль присутствующих в культурах B-лимфоцитов, также имеющих антигенпрезентирующие свойства. Для исключения их влияния в дальнейшем будут произведены работы с деплецией B-клеток.
Для проверки значимости костимуляции нами были поставлены дополнительные варианты культур с применением не только бактерий,
FoxP3 PE CD25 APC SSC-H
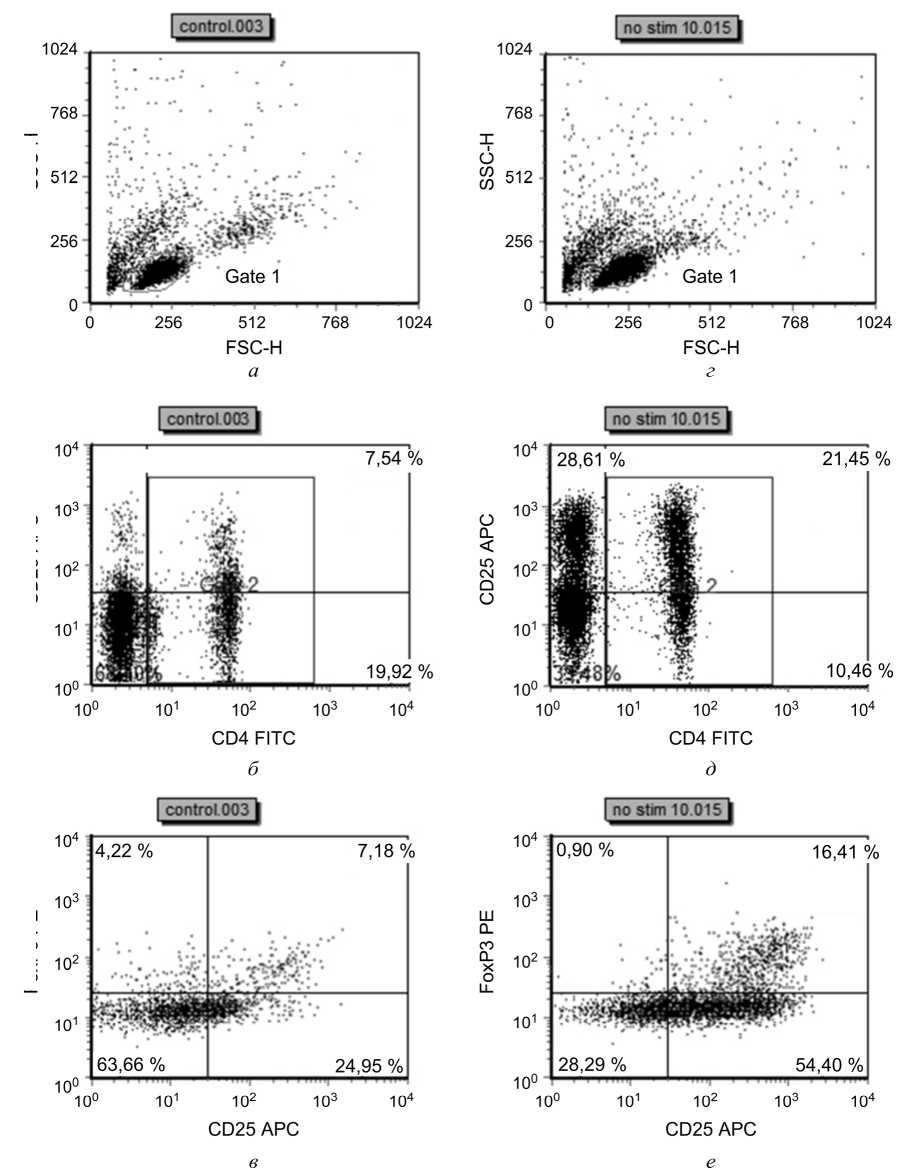
Рис. 1. H. pylori повышает содержание Т-регуляторных клеток при прямом сокультивировании с лимфоцитами: а – в – данные репрезентативного эксперимента, содержание Т-регуляторных клеток в контрольных культурах без H. pylori ( а – распределение клеток по светорассеиванию, б – выделение CD4+CD25+ клеток, в – выделение FoxP3+ Т-регуляторных клеток, оцениваемая популяция находится в верхнем правом квадранте); г – е – данные репрезентативного эксперимента, содержание Т-регуляторных клеток в культурах, росших в присутствии H. pylori ( г – распределение клеток по светорассеиванию, д – выделение CD4+CD25+ клеток, е – выделение FoxP3+ Т-регуляторных клеток, оцениваемая популяция находится в верхнем правом квадранте). Оцениваемые маркеры и регистрируемые параметры указаны по осям, процентное соотношение клеток – в углах квадрантов
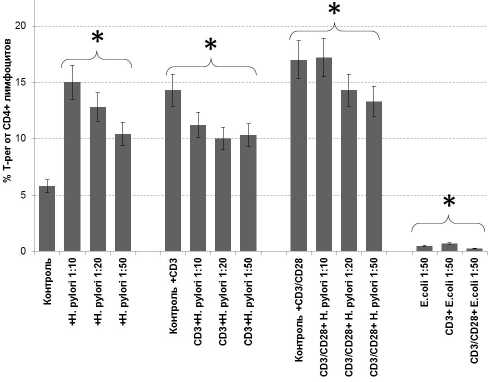
Рис. 2. Влияние H. pylory на дифференцировку Т-регуляторных клеток. Варианты стимуляции обозначены под диаграммой. Контороль – лимфоциты без добавления бактерий и антител;
* достоверные отличия от контрольной культуры, p <0,01
но и стимулирующих антител к CD3 и CD28, предоставляющих Т-клеткам сигнал, подобный стимуляции от АПК. Данные анализа культур с добавлением антител также приведены на рис. 2. Как можно видеть, стимуляция антителами сразу приводила к появлению в культуре достаточно высоких уровней содержания Т-рег (14,0 ± 1,29 % Т-рег для культур с добавлением только CD3 без H. pylori, 16,54 ± 2,13 % для культур с добавлением смеси CD3 и CD28 – модель более полной стимуляции, опять же без добавления H. pylori ). Введение в культуры H. pylori не приводило к увеличению содержания Т-рег (для культур с CD3 содержание Т-рег составляло 11,25 ± 1,06 % для соотношения 1:10, 10,04 ± 1,14 – для соотношения 1:20, 10,28 ± 1,54 % – для соотношения 1:50, достоверных отличий от культуры с CD3 без H. pylori нет; для культур со смесью CD3 и CD28 содержание Т-рег 16,93 ± 3,74 % для соотношения 1:10, 13,95 ± 2,13 % – для соотношения 1:20, 12,82 ± ± 1,28 % – для соотношения 1:50, достоверных отличий от культуры со смесью CD3+CD28 без H. pylori нет). Как и в случае с культурами, стимулированными только H. pylori , наблюдалась тенденция к обратной дозовой зависимости между дозой микроба в культуре и содержанием Т-рег.
Все значения содержания Т-рег в культурах с CD3 и CD3+CD28 достоверно отличались от содержания Т-рег в культурах лимфоцитов без антител и H. pylori (p<0,01) и не отличались от культур, стимулированных H. pylori без антител. Таким образом, H. pylori стимулирует дифференцировку лимфоцитов в сторону Т-рег на уровне активации антителами. Отсутствие повышения числа Т-рег в культурах, стимулированных одновременно H. pylori и антителами, по-видимому, объясняется поликлональным характером активирующего действия антител, которые вызвали дифференцировку всех CD4+ Т-клеток, исходно имевших коммитирование к развитию в сторону Т-рег.
Для проверки специфичности действия H. pylori нами применялись культуры лимфоцитов, стимулированные другим микроорганизмом, обитающим в желудочно-кишечном тракте человека – Escherichia coli (E.coli).
Используемые нами культуры лимфоцитов и E. coli росли как в отсутствии, так и в присутствии антител к CD3 и CD28. Соотношение лимфоцитов и E. coli составляло 1:50. Как можно видеть из рис. 1, E. coli не вызывала созревания Т-рег в культурах и препятствовала стимулирующему действию антител. Таким образом, полученные данные свидетельствуют о том, что стимулирующее дифференцировку Т-рег влияние является свойством именно H. pylori и, по всей видимости, не опосредуется паттернами патогенов (сходными у H. pylori и E.coli – подвижных грамотрицательных микроорганизмов).
Выводы. Оценка способности микроорганизмов модулировать иммунный ответ, в особенности, если подобное модулирование способствует выживанию микроорганизма во внутренней среде хозяина, является актуальной фундаментальной и практической задачей. Понимание данных механизмов, несомненно, может способствовать как прогнозированию возможных рисков, обусловленных микроорганизмом, так и повышению эффективности терапевтических подходов к патологиям, обусловленным данным микроорганизмом. В представленной работе нами показана способность H. pylori оказывать дифференцировочное действие на Т-лимфоциты, направляющее их развитие в сторону Т-регуляторных клеток. При отсутствии в культурах дендритных клеток – популяции иммуно-цитов, процесс, по современным данным, имеет наиболее выраженную способность управлять течением иммунного ответа. В пределах исследуемой группы данное действие наблюдалось при соотношениях микробов и Т-клеток от 1:10 до 1:50, не требовало присутствия в куль- турах АПК или стимулирующих антител. В среднем рост процентного содержания Т-регулятор-ных CD4+CD25+FoxP3+ клеток среди CD4+лим-фоцитов составлял 2,12 раза. По всей видимости, в условиях данного эксперимента воздействие H. pylori затрагивало клетки, исходно коммитированные к развитию в сторону Т-рег, так как поликлональная стимуляция антителами к CD28 и/или CD3 «поглощала» эффект от введения бактерий – культуры, стимулированные только антителами, а также антителами одновременно с H. pylori, статистически не отличались по содержанию Т-рег. Дифференцирующее действие, по всей видимости, являлось специфическим свойством именно H. pylori, так как стимуляция лимфоцитов с помощью другого микроорганизма, способного длительно выживать в условиях ЖКТ – E. coli – не вызывала повышения содержания Т-регуляторных клеток. Таким образом, нами была принципиально продемонстрирована способность H. pylori оказывать влияние на дифференцировку регуляторных Т-клеток, не опосредуемая презентацией микробных антигенов дендритными клетками, но, по всей видимости, зависящая именно от прямого воздействия микроба на Т-клетки. Понимание данного механизма может позволить выделить действующее начало, индуцирующее развитие Т-рег и, таким образом, потенциально являющееся естественным толерогенным фактором, применимым в качестве лекарственного средства.
Список литературы Влияние Helicobacter pylori на дифференцировку Т-регуляторных клеток
- Методы лабораторной диагностики инфекции, обусловленной Helicobacter pylori: пособие для врачей/А.Б. Жебрун, А.В. Сварваль, Р.С. Ферман, Л.Б. Гончарова. -СПб.: ФБУН НИИЭМ имени Пастера, 2014. -60 с.
- Evidence for transepithelial dendritic cells in human H. pylori active gastritis/V. Necchi, R. Manca, V. Ricci, E. Solcia//Helicobacter. -2009. -Vol. 14, №. 3. -P. 208-222.
- Helicobacter pylori induces activation of human peripheral γδ+ T lymphocytes/B. Romi, E. Soldaini, L. Pancotto, F. Castellino, G. Del Giudice, F. Schiavetti//PLoS One. -2011. -Vol. 6, № 4. -P. e19324.
- Helicobacter pylori induces miR-155 in T Cells in a cAMP-Foxp3-dependent manner/L.F Fehri, M. Koch, E. Belogolova, H. Khalil //PLoS One. -2010. -Vol. 5, № 3. -P. e9500.
- Helicobacter pylori infection prevents allergic asthma in mouse models through the induction of regulatory T cells/I.C. Arnold, N. Dehzad, S. Reuter, H Martin //Journal Clin. Invest. -2011. -Vol. 121, № 8. -P. 3088-3093.
- Helicobacter pylori polyclonally activates murine CD4 (+) T cells in the absence of antigen-presenting cells / C. Rosenplänter, F. Sommer, P. Kleemann, A. Belkovets // Eur. J. Immunol. 2007, 37 (7): 1905-1915.
- Human peripheral and gastric lymphocyte responses to Helicobacter pylori NapA and AphC differ in infected and uninfected individuals/H.J. Windle, Y.S. Ang, V. Athie-Morales, R. McManus //Gut. -2005. -Vol. 54, № 1. -P. 25-32.
- Involvement of Toll-like receptors on Helicobacter pylori-induced immunity/R. Käbisch, R. Mejías-Luque, M. Gerhard, C. Prinz//PLoS One. -2014. -Vol. 9, № 8. -P. e104804.
- Mucosal FOXP3-expressing CD4+ CD25high regulatory T cells in Helicobacter pylori-infected patients/A. Lundgren, E. Stromberg, A. Sjoling, C. Lindholm //Infect. Immun. -2005. -Vol. 73, № 1. -P. 523-531.
- Pachathundikandi S.K., Müller A., Backert S. Inflammasome activation by Helicobacter pylori and its Implications for persistence and immunity//Curr. Top. Microbiol. Immunol. -2016. -Vol. 397. -P. 117-131.
- Raghavan S., Quiding-Järbrink M. Immune modulation by regulatory T cells in Helicobacter pylori-associated diseases//Endocr. Metab. Immune. Disord. Drug. Targets. -2012. -Vol. 12, № 1. -P. 71-85.
- Sakaguchi S., Wing K., Yamaguchi T. Dynamics of peripheral tolerance and immune regulation mediated by Treg//Eur. J. Immunol. -2009. -Vol. 39, № 9. -P. 2331-2336.
- Sanchez A.M., Yang Y. The role of natural regulatory T cells in infection//Immunol. Res. -2011. -Vol. 49, № 1-3. -P. 124-134.
- Shiu J., Blanchard T.G. Dendritic cell function in the host response to Helicobacter pylori infection of the gastric mucosa//Pathog. Dis. -2013. -Vol. 67, № 1. -P. 46-53.
- The effect of Helicobacter pylori on asthma and allergy/A. Amedei, G. Codolo, G. Del Prete, M. de Bernard, M.M. D'Elios//Journal Asthma. Allergy. -2010. -Vol. 3. -P. 139-147.
- Whiteside T.L. The role of regulatory T cells in cancer immunology//Immunotargets. Ther. -2015. -Vol. 4. -P. 159-171.


